Комбинированная терапия туберкулеза
Иллюстрации
Показать всеГруппа изобретений относится к области медицины и предназначена для терапии туберкулеза. Применяют соединение формулы (I), (S)-N-[[3-[3-фтор-4-(4-тиоморфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида, или его фармацевтически приемлемой соли в комбинации с по меньшей мере двумя агентами для изготовления лекарственного средства для лечения туберкулеза после того как субъект прошел начальную фазу лечения туберкулеза. Использование заявленной группы изобретений обеспечивает высокий терапевтический эффект при лечении туберкулеза. 3 н. и 7 з.п. ф-лы, 12 табл., 8 пр.
Реферат
Область изобретения
Настоящее изобретение относится к способам лечения туберкулеза, включая разновидности с множественной лекарственной устойчивостью и латентный туберкулез. Более конкретно, настоящее изобретение относится к способу лечения туберкулеза у млекопитающего, при котором указанному млекопитающему, нуждающемуся в этом, вводят эффективное количество соединения формулы (I), (S)-N-[[3-[3-фтор-4-(4-тиоморфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида, или его фармацевтически приемлемой соли в комбинации с по меньшей мере двумя агентами, полезными при лечении туберкулеза. Настоящее изобретение также относится к фармацевтической композиции, содержащей: (1) терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли, (2) терапевтически эффективное количество по меньшей мере одного агента, полезного при лечении туберкулеза, и (3) один или более чем один фармацевтически приемлемый носитель или наполнитель.
Предшествующий уровень техники
Туберкулез (ТБ) приводит к смерти приблизительно 1,6 миллиона человек во всем мире каждый год, что делает его второй основной причиной смерти взрослых после ВИЧ. Каждый год происходит почти 500000 новых случаев ТБ с множественной лекарственной устойчивостью (multidrug-resistant, МЛУ), и недавнее появление ТБ с расширенной лекарственной устойчивостью (extensively drug-resistant, РЛУ-ТБ) предвещает новую эпидемию неизлечимого ТБ. (Смотри Dorman, S.Е. et al., Nat. Med 13:295-298 2007, Zignol, M. et al., J Infect. Dis 194:479-485, 2006.) Необходимы новые лекарственные средства с мощной противотуберкулезной активностью, особенно против неразмножающихся устойчивых организмов, для сокращения продолжительности лечения ТБ и, посредством этого, облегчения глобального внедрения лечения под непосредственным наблюдением. (Смотри O'Brien, R.J. et al., Am. J.Respir. Crit Care Med. 163:1055-1058, 2001.)
В настоящее время лечение туберкулеза, чувствительного к лекарственным средствам, заключается во введении комбинации по меньшей мере следующих лекарственных средств: изониазида, рифампина и пиразинамида. Для эффективного лечения вышеупомянутые лекарственные средства дают пациенту в начальной фазе лечения в течение 8 недель, на протяжении которых данные лекарственные средства используют в комбинации для уничтожения быстроразмножающейся популяции Mycobacterium tuberculosis, а также для предупреждения появления устойчивости к лекарственному средству. После начальной фазы лечения следует продолжение или фаза стерилизации в течение 18 недель, на протяжении которых дают два или более чем два стерилизующих лекарственных средства (например, изониазид и рифампин) для уничтожения периодически делящейся популяции (неразмножающихся устойчивых организмов) Mycobacterium tuberculosis.
В то время как вышеупомянутая комбинация лекарственных средств совместно обеспечивает лечение против чувствительной инфекции Mycobacterium tuberculosis за время от 4 до 6 месяцев, такая комбинированная терапия не всегда является успешной, особенно у пациентов, имеющих штаммы, устойчивые к лекарственным средствам. Большая продолжительность лечения, продолжающегося шесть месяцев, также может приводить к неприятным побочным эффектам. Кроме того, соблюдение схемы и режима лечения при относительно длинном курсе лечения обычно является плохим. Такое несоблюдение схемы и режима лечения может приводить к провалу лечения, приводя к развитию устойчивости к лекарственному средству.
Оксазолидиноны включают класс ингибиторов синтеза белка, которые блокируют трансляцию путем предотвращения образования инициирующего комплекса (относительно механизма, смотри K.Leach et al., Molecular Cell, 26:4, 460-462, 2007). Линезолид (LZD, Zyvox®), единственный продающийся на рынке оксазолидинон, обладает активностью в отношении грамположительных бактерий и в настоящее время одобрен для применения при осложненных инфекциях кожи и кожных структур и внутрибольничной пневмонии (Zyvox® листовка-вкладыш в упаковке). Однако он также является активным против многих видов микобактерий, включая Mycobacterium tuberculosis, для которой его МИК (минимальная ингибирующая концентрация) варьирует от 0,125 до 1 мкг/мл с МИК50 0,5 мкг/мл и МИК90 1 мкг/мл. (Смотри Alcala, L. et al., Antimicrob Agents Chemother 47: 416-417, 2003; Cynamon, M.H., et al., Antimicrob Agents Chemother 43: 1189-1191, 1999; Fattorini, L., et al., Antimicrob Agents Chemother 47: 360-362, 2003). В результате LZD используют в случае отличных от указанных на этикетке показаний для лечения не поддающихся воздействию случаев МЛУ- и РЛУ-ТБ. Несмотря на то что несколько серий случаев говорит о том, что LZD может способствовать успешному превращению культуры мокроты в таких случаях, его отдельная активность у пациентов с ТБ и его точный вклад в комбинированные схемы лечения остается неясным. Эти исследования также демонстрируют то, что продолжительность введения LZD может быть ограничена гематологической и нейрологической токсичностью, которая может возникать при долговременном введении. (Смотри Fortun, J., et al., 56: 180-185, 2005; Park, I.N., et al., Antimicrob Chemother 58: 701-704, 2006; Zignol, M., et al., J Infect. Dis 194: 479-485, 2006.) Следовательно, желательными являются новые оксазолидиноны с более мощной активностью in vivo против Mycobacterium tuberculosis и меньшим риском токсичности при длительном введении.
Ранее были описаны оксазолидиноны с более мощной активностью против Mycobacterium tuberculosis. (Смотри Barbachyn, M.R. et al., J Med Chem. 39: 680-685, 1996; Sood, R., et al., Antimicrob Agents Chemother 49: 4351-4353, 2005.) Противотуберкулезная активность соединения формулы (I), (S)-N-[[3-[3-фтор-4-(4-тиоморфолинил)фенил]-2-оксо-5-оксазолидинил]метил] ацетамида, была впервые описана в 1996. (Смотри Barbachyn, M.R., et al., J Med Chem. 39: 680-685, 1996.) Последующие эксперименты на мышиной модели выявили то, что соединение формулы (I) является более активным, чем LZD, при введении обоих лекарственных средств в дозе 100 мг/кг, но клиническая релевантность этой дозы LZD не была установлена, и активности соединения формулы (I) и LZD не были явно отличными при сравнении в более низких дозах. (Смотри Cynamon, M.H., et al., Antimicrob Agents Chemother 43: 1189-1191, 1999.) Кроме того, несмотря на то что соединение формулы (I), по-видимому, имеет умеренную активность при объединении с рифампином (RIF) в модели острой (ранней) инфекции, соединение формулы (I) не имеет дополнительной активности при объединении с изониазидом (INH). (Cynamon, M.H., et al., Antimicrob Agents Chemother 43: 1189-1191, 1999.) Важнее всего то, что активность соединения формулы (I), одного или в комбинации с RIF или INH, оценивали только на протяжении исходных 4 недель лечения, что является недостаточным для оценки активности соединения или комбинации агентов против неразмножающихся сохраняющихся клеток, которая в свою очередь в конечном счете определяет продолжительность лечения, необходимого для излечения (т.е. предупреждения рецидива после завершения лечения).
Следовательно, существует насущная потребность в разработке более новых схем лечения, которые могут быть использованы для предупреждения, лечения и/или снижения туберкулеза и/или для устранения угрозы появления туберкулеза с множественной лекарственной устойчивостью, или сокращения продолжительности лечения.
Краткое изложение сущности изобретения
Настоящее изобретение относится к способу лечения туберкулеза у млекопитающего, при котором указанному млекопитающему, нуждающемуся в этом, вводят эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли:
в комбинации с по меньшей мере двумя агентами, полезными при лечении туберкулеза.
В одном воплощении указанные по меньшей мере два агента выбраны из группы, состоящей из изониазида, рифампина, рифапентина, рифабутина, пиразинамида, этамбутола, стрептомицина, канамицина, амикацина, моксифлоксацина, гатифлоксацина, левофлоксацина, офлоксацина, ципрофлоксацина, капреомицина, этионамида, циклосерина, пара-аминосалициловой кислоты, тиацетазона, кларитромицина, амоксициллина-клавулановой кислоты, имипенема, меропенема, виомицина, теризидона, клофазимина, ТМС-207, РА-824, ОРС-7683, LL-3858 и SQ-109.
В другом воплощении один из указанных по меньшей мере двух агентов выбран из группы, состоящей из изониазида, рифампина, рифапентина, рифабутина, пиразинамида, моксифлоксацина, гатифлоксацина, левофлоксацина, офлоксацина, ципрофлоксацина, клофазимина и этамбутола.
В еще одном воплощении один из указанных по меньшей мере двух агентов представляет собой пиразинамид.
В еще одном воплощении один из указанных по меньшей мере двух агентов представляет собой рифампин.
В еще одном воплощении один из указанных по меньшей мере двух агентов представляет собой рифапентин.
В еще одном воплощении один из указанных по меньшей мере двух агентов представляет собой РА-824.
В еще одном воплощении один из указанных по меньшей мере двух агентов представляет собой ОРС-67683.
В еще одном воплощении один из указанных по меньшей мере двух агентов представляет собой ТМС-207.
В еще одном воплощении один из указанных по меньшей мере двух агентов выбран из группы, состоящей из моксифлоксацина, гатифлоксацина, левофлоксацина и офлоксацина.
В еще одном воплощении один из указанных по меньшей мере двух агентов представляет собой моксифлоксацин.
В конкретном воплощении указанные по меньшей мере два агента представляют собой пиразинамид и рифампин.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой пиразинамид, рифампин и изониазид.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой пиразинамид и рифапентин.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой пиразинамид, рифапентин и изониазид.
В конкретном воплощении указанные по меньшей мере два агента представляют собой пиразинамид и моксифлоксацин.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой пиразинамид, моксифлоксацин и рифампин.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой пиразинамид, моксифлоксацин и рифапентин.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой РА-824 и пиразинамид.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой РА-824, пиразинамид и агент, выбранный из группы, состоящей из стрептомицина, канамицина, амикацина и капреомицина.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой РА-824 и моксифлоксацин.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой РА-824, моксифлоксацин и агент, выбранный из группы, состоящей из стрептомицина, канамицина, амикацина и капреомицина.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой ОРС-67683 и пиразинамид.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой ОРС-67683, пиразинамид и агент, выбранный из группы, состоящей из стрептомицина, канамицина, амикацина и капреомицина.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой ОРС-67683 и моксифлоксацин.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой ОРС-67683, моксифлоксацин и агент, выбранный из группы, состоящей из стрептомицина, канамицина, амикацина и капреомицина.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой ТМС-207 и пиразинамид.
В еще одном конкретном воплощении указанные по меньшей мере два агента представляют собой ТМС-207, пиразинамид и моксифлоксацин или изониазид.
В еще одном воплощении указанный туберкулез включает активный туберкулез или латентный туберкулез.
В еще одном воплощении указанный активный туберкулез включает чувствительный к лекарственным средствам, устойчивый к одному лекарственному средству, туберкулез с множественной лекарственной устойчивостью (МЛУ) или туберкулез с расширенной лекарственной устойчивостью (РЛУ).
В еще одном воплощении способ по настоящему изобретению позволяет полностью устранить туберкулез, чувствительный к лекарственным средствам, устойчивый к одному лекарственному средству, туберкулез с множественной лекарственной устойчивостью или туберкулез с расширенной лекарственной устойчивостью (РЛУ) по завершении лечения.
В еще одном воплощении указанный туберкулез вызван инфекцией Mycobacterium, выбранной из группы, состоящей из Mycobacterium tuberculosis, Mycobacterium bovis или другого родственного вида микобактерий.
В еще одном воплощении способ по настоящему изобретению предупреждает рецидив инфекции Mycobacterium после завершения лечения.
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли вводят перорально.
В еще одном воплощении каждый из указанных по меньшей мере двух агентов вводят перорально.
В еще одном воплощении указанные по меньшей мере два агента вводят совместно в композиции.
В еще одном воплощении указанные по меньшей мере два агента вводят раздельно.
В еще одном воплощении указанные по меньшей мере два агента вводят совместно, и другой агент, полезный для лечения туберкулеза, вводят отдельно.
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли вводят один раз в сутки (QD) или два раза в сутки (BID).
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли вводят один раз в неделю, дважды в неделю, трижды в неделю или через день.
В одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 10 мг до примерно 2000 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 250 мг до примерно 1000 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 600 мг до примерно 1000 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 25 мг до примерно 1000 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 50 мг до примерно 500 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 100 мг до примерно 500 мг.
Настоящее изобретение также относится к способу лечения туберкулеза у млекопитающего после того, как указанное млекопитающее прошло начальную фазу лечения, при котором указанному млекопитающему, нуждающемуся в этом, вводят эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли:
в комбинации с по меньшей мере одним агентом, полезным при лечении туберкулеза.
В одном воплощении указанный по меньшей мере один агент выбран из группы, состоящей из рифампина, рифапентина, рифабутина, пиразинамида, этамбутола, стрептомицина, канамицина, амикацина, моксифлоксацина, гатифлоксацина, левофлоксацина, офлоксацина, ципрофлоксацина, капреомицина, этионамида, циклосерина, пара-аминосалициловой кислоты, тиацетазона, кларитромицина, амоксициллина-клавулановой кислоты, имипенема, меропенема, клофазимина, виомицина, теризидона, ТМС-207, РА-824, ОРС-7683, LL-3858 и SQ-109.
В еще одном воплощении по меньшей мере один указанный агент выбран из группы, состоящей из рифампина, рифапентина, рифабутина, пиразинамида, моксифлоксацина, гатифлоксацина, левофлоксацина, офлоксацина и этамбутола.
В конкретном воплощении указанный по меньшей мере один агент представляет собой пиразинамид.
В конкретном воплощении указанный по меньшей мере один агент представляет собой рифампин.
В конкретном воплощении указанный по меньшей мере один агент представляет собой рифапентин.
В конкретном воплощении указанный по меньшей мере один агент представляет собой РА-824.
В конкретном воплощении указанный по меньшей мере один агент представляет собой ОРС-7683.
В конкретном воплощении указанный по меньшей мере один агент представляет собой ТМС-207.
В конкретном воплощении указанный по меньшей мере один агент выбран из группы, состоящей из моксифлоксацина, гатифлоксацина, левофлоксацина и офлоксацина.
В конкретном воплощении указанный по меньшей мере один агент представляет собой моксифлоксацин.
В еще одном воплощении указанный туберкулез включает активный туберкулез или латентный туберкулез.
В еще одном воплощении указанный активный туберкулез включает туберкулез, чувствительный к лекарственным средствам, устойчивый к одному лекарственному средству, туберкулез с множественной лекарственной устойчивостью (МЛУ) или туберкулез с расширенной лекарственной устойчивостью (РЛУ).
В еще одном воплощении способ по настоящему изобретению полностью устраняет туберкулез, чувствительный к лекарственным средствам, устойчивый к одному лекарственному средству, туберкулез с множественной лекарственной устойчивостью (МЛУ) и туберкулез с расширенной лекарственной устойчивостью (РЛУ) по завершении лечения.
В еще одном воплощении указанный туберкулез вызван инфекцией Mycobacterium, выбранной из группы, состоящей из Mycobacterium tuberculosis, Mycobacterium bovis или другого родственного вида микобактерий.
В еще одном воплощении способ по настоящему изобретению предупреждает рецидив инфекции Mycobacterium после завершения лечения.
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли вводят перорально.
В еще одном воплощении указанный по меньшей мере один агент вводят перорально.
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли и указанный по меньшей мере один агент вводят совместно в композиции.
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли и указанный по меньшей мере один агент вводят раздельно.
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли вводят один раз в сутки (QD) или два раза в сутки (BID).
В еще одном воплощении соединение формулы (I) и его фармацевтически приемлемые соли вводят один раз в неделю, дважды в неделю, трижды в неделю или через день.
В одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 10 мг до примерно 2000 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 25 мг до примерно 1000 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 50 мг до примерно 500 мг.
В еще одном воплощении соединение формулы (I) или его фармацевтически приемлемую соль вводят в количестве от примерно 100 мг до примерно 500 мг.
Настоящее изобретение также относится к фармацевтической композиции, содержащей:
1) терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли:
2) терапевтически эффективное количество по меньшей мере одного агента, полезного при лечении туберкулеза, и
3) один или более чем один фармацевтически приемлемый носитель или наполнитель.
В еще одном воплощении указанный по меньшей мере один агент выбран из группы, состоящей из изониазида, рифампина, рифапентина, рифабутина, пиразинамида, этамбутола, стрептомицина, канамицина, амикацина, моксифлоксацина, гатифлоксацина, левофлоксацина, офлоксацина, ципрофлоксацина, капреомицина, этионамида, циклосерина, пара-аминосалициловой кислоты, тиацетазона, кларитромицина, клофазимина, амоксициллина-клавулановой кислоты, имипенема, меропенема, виомицина, теризидона, клофазимина, ТМС-207, РА-824, ОРС-7683, LL-3858 и SQ-109.
В еще одном воплощении указанный по меньшей мере один агент выбран из группы, состоящей из изониазида, рифампина, рифапентина, рифабутина, пиразинамида, моксифлоксацина, гатифлоксацина, левофлоксацина, офлоксацина и этамбутола.
В конкретном воплощении указанный по меньшей мере один агент представляет собой пиразинамид.
В конкретном воплощении указанный по меньшей мере один агент представляет собой рифампин.
В конкретном воплощении указанный по меньшей мере один агент представляет собой рифапентин.
В конкретном воплощении указанный по меньшей мере один агент представляет собой изониазид.
В конкретном воплощении указанный по меньшей мере один агент представляет собой РА-824.
В конкретном воплощении указанный по меньшей мере один агент представляет собой ОРС-7683.
В конкретном воплощении указанный по меньшей мере один агент представляет собой ТМС-207.
В конкретном воплощении указанный по меньшей мере один агент выбран из группы, состоящей из моксифлоксацина, гатифлоксацина, левофлоксацина и офлоксацина.
В конкретном воплощении указанный по меньшей мере один агент представляет собой моксифлоксацин.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 10 мг до примерно 2000 мг соединения формулы (I) или его фармацевтически приемлемой соли.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 250 мг до примерно 1000 мг соединения формулы (I) или его фармацевтически приемлемой соли.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 600 мг до примерно 1000 мг соединения формулы (I) или его фармацевтически приемлемой соли.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 25 мг до примерно 1000 мг соединения формулы (I) или его фармацевтически приемлемой соли.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 50 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли.
Кроме того, любой препарат, включая комбинации, приведенные ниже, может содержать от 250 мг до 1000 мг соединения формулы (I) или его фармацевтически приемлемой соли или от 600 мг до 1000 мг соединения формулы (I) или его фармацевтически приемлемой соли.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли и примерно 600 мг рифампина.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли и примерно 300 мг изониазида.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли, примерно 300 мг изониазида и примерно 600 мг рифампина.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли, примерно 300 мг изониазида, примерно 600 мг рифампина и от примерно 20-25 мг/кг до примерно 50-70 мг/кг пиразинамида.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли и от примерно 10-15 мг/кг до примерно 20-30 мг/кг изониазида.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли, от примерно 10-15 мг/кг до примерно 20-30 мг/кг изониазида и от примерно 10 мг/кг до примерно 20 мг/кг рифампина.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 100 мг до примерно 500 мг соединения формулы (I) или его фармацевтически приемлемой соли, от примерно 10-15 мг/кг до примерно 20-30 мг/кг изониазида, от 10 мг/кг до примерно 20 мг/кг рифампина и от примерно 15-30 мг/кг до примерно 50 мг/кг пиразинамида.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 50 мг до примерно 250 мг соединения формулы (I) или его фармацевтически приемлемой соли, примерно 75 мг изониазида, примерно 150 мг рифампина и примерно 400 мг пиразинамида.
В еще одном воплощении данная фармацевтическая композиция содержит от примерно 25 мг до примерно 250 мг соединения формулы (I) или его фармацевтически приемлемой соли и примерно 300 мг рифампина.
Настоящее изобретение также относится к производственному изделию, содержащему упакованную композицию, содержащую:
(а) (1) терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли:
(2) терапевтически эффективное количество по меньшей мере одного агента, полезного при лечении туберкулеза, и
(3) один или более чем один фармацевтически приемлемый носитель или наполнитель;
(б) вкладыш с инструкциями для введения упакованной композиции (а) для лечения туберкулеза; и
(в) контейнер для (а) и (б).
Настоящее изобретение также относится к фармацевтической упаковке для лечения туберкулеза у млекопитающего, которая содержит соединение формулы (I) или его фармацевтически приемлемую соль:
и вкладыш с инструкциями для введения указанной композиции в комбинации с по меньшей мере одним агентом, полезным при лечении туберкулеза.
Эти и другие аспекты, преимущества и отличительные признаки данного изобретения станут очевидными из следующего подробного описания данного изобретения.
Подробное описание изобретения
Настоящее изобретение относится к способу лечения туберкулеза у млекопитающего, при котором указанному млекопитающему вводят эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли:
в комбинации с по меньшей мере двумя агентами, полезными при лечении туберкулеза.
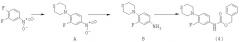
Соединение формулы (I) по данному изобретению, (S)-N-[[3-[3-фтор-4-(4-тиоморфолинил)фенил]-2-оксо-5-оксазолидинил]метил]ацетамида, раскрыто в патенте США №5880118 (включенном сюда во всей его полноте посредством ссылки) в Примере 1. Как описано более подробно ниже, соединение формулы (I) по данному изобретению можно вводить в виде свободного основания или в форме его соли.
Фраза «фармацевтически приемлемая соль(ли)» при использовании здесь, если не указано иначе, включает соли кислотных или основных групп, которые могут присутствовать в соединениях формулы (I).
Например, соединения формулы (I), которые являются основными по природе, способны к образованию целого ряда солей" с разными неорганическими и органическими кислотами. Кислоты, которые можно использовать для получения фармацевтически приемлемых солей присоединения кислоты таких основных соединений, являются кислотами, которые образуют нетоксичные соли присоединения кислоты, т.е. соли, содержащие фармакологически приемлемые анионы, такие как соли гидрохлорид, гидробромид, гидройодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, лактат, салицилат, цитрат, кислый цитрат, тартрат, пантотенат, битартрат, аскорбат, сукцинат, малеат, фумарат, глюконат, глюкуронат, сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, пара-толуолсульфонат и памоат [т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)].
Примеры солей включают соли ацетат, акрилат, бензолсульфонат, бензоат (такой как хлорбензоат, метилбензоат, динитробензоат, гидроксибензоат и метоксибензоат), бикарбонат, бисульфат, бисульфит, битартрат, борат, бромид, бутин-1,4-диоат, кальция эдетат, камсилат, хлорид, капроат, каприлат, цитрат, деканоат, дигидрофосфат, эдетат, эдисилат, эстолат, эзилат, этилсукцинат, формиат, фумарат, глюцептат, глюконат, глутамат, гликолят, гликолиларсанилат, гептаноат, гексин-1,6-диоат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, γ-гидроксибутират, йодид, изобутират, изотионат, лактат, лактобионат, лаурат, малат, малеат, малонат, манделат, мезилат, метафосфат, метансульфонат, метилсульфат, моногидрофосфат, мукат, напсилат, нафталин-1-сульфонат, нафталин-2-сульфонат, нитрат, олеат, оксалат, памоат (эмбонат), пальмитат, пантотенат, фенилацетаты, фенилбутират, фенилпропионат, фталат, фосфат/дифосфат, полигалактуронат, пропансульфонат, пропионат, пропиолат, пирофосфат, пиросульфат, салицилат, стеарат, субацетат, суберат, сукцинат, сульфат, сульфонат, сульфит, таннат, тартрат, теоклат, тозилат, триэтиодод и валерат, но не ограничиваются ими.
Данное изобретение также относится к солям присоединения основания соединений формулы (I). Химические основания, которые можно использовать в качестве реагентов для получения фармацевтически приемлемых основных солей соединений формулы (I), которые являются кислотными по природе, представляют собой основания, которые образуют нетоксичные основные соли с такими соединениями. Такие нетоксичные основные соли включают соли, полученные из таких фармакологически приемлемых катионов, как катионы щелочных металлов (например, калия и натрия), катионы щелочноземельных металлов (например, кальция и магния), соли присоединения аммония или водорастворимого амина, такого как N-метилглюкамин (меглумин), и соли низшего алканоламмония и другие основные соли фармацевтически приемлемых органических аминов, но не ограничиваются ими.
Также могут быть образованы гемисоли кислот и оснований, например, гемисульфат и гемикальциевые соли.
Для обзора подходящих солей, смотри Stahl and Wermuth, Handbook of Pharmaceutical Salts: Properties, Selection, and Use (Wiley-VCH, 2002). Способы получения фармацевтически приемлемых солей соединений формулы (I) по данному изобретению известны специалисту в данной области.
Термины «формула (I)» и «формулы (I) или их фармацевтически приемлемые соли» при использовании здесь определены так, что они включают все формы соединения формулы (I), включая изомеры, кристаллические и некристаллические формы, изоморфы, полиморфы, метаболиты, сольваты, гидраты и их пролекарства.
Термин «сольват» используется здесь для описания нековалентной или легко обратимой комбинации между растворителем и растворенным веществом или диспергентами и дисперсной фазой. Будет понятно, что данный сольват может находиться в форме твердого вещества, суспензии (например, суспензии или дисперсии) или раствора. Неограничивающие примеры растворителей включают этанол, метанол, пропанол, ацетонитрил, диметиловый эфир, диэтиловый эфир, тетрагидрофуран, хлористый метилен и воду. Термин «гидрат» используется, когда указанным растворителем является вода.
Принятой в настоящее время системой классификации органических гидратов является система, которая определяет гидраты с изолированным сайтом или канальные гидраты - смотри K.R.Morris, Polymorphism in Pharmaceutical Solids (Ed. H.G.Brittain, Marcel Dekker, 1995). Гидраты с изолированным сайтом представляют собой гидраты, в которых молекулы воды изолированы от непосредственного контакта друг с другом органическими молекулами, находящимися между ними. В канальных гидратах молекулы воды лежат в каналах кристаллической решетки, где они находятся рядом с другими молекулами воды.
Когда растворитель или вода являются прочно связанными, данный комплекс будет иметь хорошо определенную стехиометрию, независимо от влажности. Однако когда растворитель или вода являются слабо связанными, как в канальных сольватах и гигроскопических соединениях, содержание воды/растворителя будет зависеть от влажности и условий сушки. В таких случаях нестехиометрические количества будут нормой.
Данное изобретение также относится к пролекарствам соединений формулы (I). Таким образом, определенные производные соединений формулы (I), которые сами по себе могут не иметь или иметь слабую фармакологическую активность, при введении в или на организм могут превращаться в соединения формулы (I), имеющие желательную активность, например, путем гидролитического расщепления. Такие производные именуются «пролекарствами». Дополнительную информацию по применению пролекарств можно найти в Pro-drugs as Novel Delivery Systems, Vol.14, ACS Symposium Series (T.Higuchi and W.Stella) и в Bioreversible Carriers in Drug Design, Pergamon Press, 1987 (Ed. E.B.Roche, American Pharmaceutical Association).
Пролекарства согласно данному изобретению можно получить, например, заменой подходящих функциональных групп, присутствующих в соединениях формулы (I), определенными группировками, известными специалистам в данной области как «прогруппировки», как описано, например, у H.Bundgaard в Design of Prodrugs (Elsevier, 1985).
Некоторые неограничивающие примеры пролекарств согласно данному изобретению включают:
(1) где соединение формулы (I) содержит функциональную группу карбоновой кислоты, которая преобразована в подходящую метаболически лабильную группу (сложные эфиры, карбаматы и т.д.) соединения формулы (I);
(2) где соединение формулы (I) содержит спиртовую функциональную группу, которая преобразована в подходящую метаболически лабильную группу (простые эфиры, сложные эфиры, карбаматы, ацетали, кетали и т.д.) соединения формулы (I); и
(3) где соединение формулы (I) содержит первичную или вторичную функциональную аминогруппу или амид, которые преобразованы в подходящую метаболически лабильную группу, например, гидролизуемую группу (амиды, карбаматы, мочевины, фосфонаты, сульфонаты и т.д.) соединения формулы (I).
Дополнительные примеры заменяющих групп согласно вышеупомянутым примерам и примерам других типов пролекарств можно найти в вышеупомянутых ссылках.
Соединения формулы (I) по данному изобретению могут демонстрировать явления таутомерии и структурной изомерии. Например, соединения формулы (I) по данному изобретению могут существовать в нескольких таутомерных формах, включая енольную и имино форму, кето и енамино форму и их геометрические изомеры и смеси. Все такие таутомерные формы включены в пределы объема соединений формулы (I) по данному изобретению. Таутомеры существуют в виде смесей таутомерных наборов в растворе. В твердой форме обычно преобладает один таутомер. Даже несмотря на то, что может быть описан один таутомер, настоящее изобретение включает все таутомеры соединений формулы (I) по данному изобретению.
Настоящее изобретение также включает изотопно-меченые соединения, которые являются идентичными соединениям, перечисленным в формуле (I), приведенной выше, если не считать того, что один или более чем один атом заменен атомом, имеющим отличную атомную массу или массовое число от атомной массы или массового числа, обычно обнаруживаемых в природе. Примеры изотопов, которые могут быть включены в соединения формулы (I), включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2H, 3H, 13C, 14C, 15N, 18O, 17O, 35S и 18F, но не ограничиваются ими. Некоторые изотопно-меченые соединения формулы (I) по данному изобретению, например, соединения, в которые включены радиоактивные изотопы, такие как 3H и 14C, являются полезными в анализах распределения в ткани лекарственного средства и/или субстрата. Тритированные, т.е. 3H, и углерод-14, т.е. 14C, изотопы являются особенно предпочтительными из-за простоты их получения и детектируемости. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2H, может дать определенные терапевтические преимущества, происходящие из-за большей метаболической стабильности, например, увеличенного периода полувыведения in vivo или пониженных требований по дозировке, и, следовательно, может быть предпочтительным в некоторых обстоятельствах. Изотопно-меченые соединения формулы (I) по данному изобретению обычно можно получить путем проведения процедур, раскрытых в Схемах и/или Примерах и Получениях, приведенных ниже, путем замены реагента, не меченого изотопом, изотопно-меченым реагентом.
Соединения формулы (I) по данному изобретению могут демонстрировать полиморфизм. Полиморфы соединений формулы (I) по данному изобретению можно получить кристаллизацией соединения формулы (I) по изобретению при разных условиях. Например, можно использовать разные растворители (включая воду) или разные смеси растворителей для перекристаллизации; кристал