Способ получения хлора из хлороводорода с помощью вольфрамсодержащих соединений
Иллюстрации
Показать всеИзобретение может быть использовано в химической промышленности. Способ получения хлора из хлороводорода с помощью вольфрамсодержащих соединений включает хлорирование триоксида вольфрама хлороводородом при температуре более 1400 К. Образующийся диоксидихлорид вольфрама выделяют из газовой смеси продуктов реакции и окисляют кислородом при температуре менее 900 К для получения хлора. Триоксид вольфрама возвращают на стадию хлорирования. Изобретение позволяет получать хлор из хлороводорода с высокой удельной производительностью без катализаторов. 2 ил., 2 пр.
Реферат
Изобретение относится к области химической технологии неорганических веществ и касается получения хлора.
Для получения хлора из хлороводорода известны способы электролиза водных растворов соляной кислоты (Л.М. Якименко «Производство хлора, каустической соды и неорганических хлорпродуктов». - М.: Химия, 1974, 600 с.). Процессы на аноде зависят от условий проведения электролиза, в частности от концентрации кислоты, температуры, материала анода и др. В промышленных электролизерах обычно используют ~30%-ную соляную кислоту, температура раствора 70-85°С. На производство 1 т Cl2 расходуется примерно 1800-1900 кВт∗ч электроэнергии постоянного тока. При этом попутно производится дополнительный продукт - водород, выделяющийся на катоде.
Известен способ окисления хлороводорода кислородом в водном растворе с использованием электролизера с газодиффузионным катодом на основе допированных азотом углеродных нанотрубок (WO 2009/118162). Недостатком способа является сложность изготовления газодиффузионного катода.
Общими недостатками различных вариантов получения хлора из хлороводорода электролизом являются значительные прямые затраты электрической энергии и невысокая удельная производительность электролизеров.
С 1868 года известен каталитический способ получения хлора, основанный на окислении хлороводорода кислородом воздуха или чистым кислородом - процесс Дикона (Henry Deacon, US Patent 85370). Первоначально катализатором служил хлорид меди. Реакция окисления протекала с приемлемой скоростью при температуре около 450°С, на выходе из конвертора газовая смесь содержала 6-8% хлора. Позднее в качестве катализатора окисления хлороводорода испытывались соединения меди, железа, хрома или композиция на их основе. Оптимальная рабочая температура таких катализаторов лежит выше 350°С, но в этих условиях происходит быстрое улетучивание активных компонентов катализатора и снижение степени конверсии.
Известны различные варианты усовершенствованного способа окисления хлороводорода по Дикону с использованием высокоактивных катализаторов, позволяющих снижать температуру процесса, имеющих меньшую летучесть и сниженную чувствительность к отравлению. Предлагалось применение кислорода вместо воздуха, проведение процесса в псевдоожиженном слое (UK 1192666 (1970); FRG patent 1271083, 1271084 (1968); French patent 1521916 (1968)).
К недостаткам каталитических процессов следует отнести относительно невысокую удельную производительность и необходимость регенерации или замены дорогостоящих катализаторов.
Известен способ получения хлора окислением хлороводорода в проточной реакционной зоне в среде низкотемпературной плазмы под воздействием импульсного электрического разряда (WO 2008/002197 А1). Недостатком способа является трудность поддержания расконтрагированного разряда в плазме электроотрицательного газа при нормальном и повышенном давлениях. Понижение давления газа, когда такой разряд относительно легко осуществим, заметно уменьшает удельную производительность процесса. Затраты электрической энергии плазмохимического способа сопоставимы с электрохимическим.
Известен двухстадийный способ окисления хлороводорода. На первой стадии осуществляется перевод хлороводорода в хлорид железа, на второй - окисление хлорида железа кислородом с выделением хлора (WO 01/64578 А1 (2001)). Недостатками данного способа являются проведение процесса при относительно невысоких температурах (200-450°С) и применение пористых инертных носителей для оксида и хлорида железа, что существенно снижает удельную производительность реактора конверсии хлороводорода. Кроме того, при продувании кислородом пористого носителя происходит унос хлорида железа (III) за счет реакции хлорида железа (II) с выделяющимся хлором.
Известен двухстадийный железоводородный способ конверсии хлороводорода для получения хлора (Кустов А.Д., Тарабанько В.Е., Тарабанько Н.В., Парфенов О.Г. О получении хлора из хлористого водорода // Химия в интересах устойчивого развития, т.18, 2010, с.339-346.; Заявка на патент РФ №2010145938/05(066213), положит. решение от 23.11.2011 г.). На первой стадии при температуре 1000-1200°С твердый оксид железа (III) хлорируется газовой смесью хлороводорода и водорода при объемном соотношении 8:1 и давлении 0,1 МПа. После понижения температуры газовой смеси продуктов реакции до 500-600°С из нее выделяется твердый хлорид железа (II), а смесь избыточного хлороводорода и паров воды поступает на разделение, после которого осушенный газообразный хлороводород возвращается на стадию хлорирования. На второй стадии процесса твердый хлорид железа (II) испаряется при температуре 1000-1200°С и подается в реактор окисления, где смешивается с кислородом. Недостатком данного способа является необходимость использования водорода на стадии хлорирования оксида железа.
Предлагаемое изобретение направлено на повышение производительности и упрощение процесса конверсии хлороводорода для рециклинга хлора за счет исключения использования водорода в исходной реакционной смеси. Поставленная задача решается путем высокотемпературного хлорирования триоксида вольфрама хлороводородом, а затем окисления получаемого диоксидихлорида вольфрама кислородом с выделением хлора. Все химические процессы ведутся при нормальном давлении.
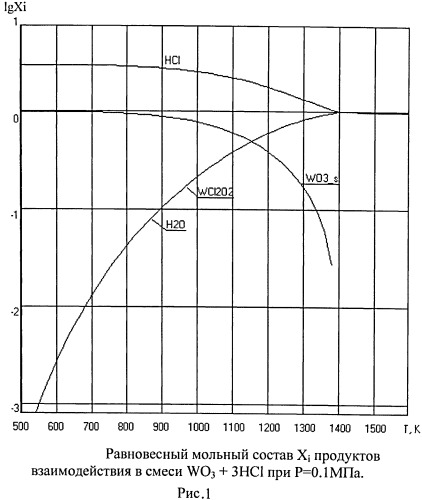
На первой стадии в реактор через дозирующее устройство подается триоксид вольфрама в виде порошка крупностью -0,1 мм, где хлорируется хлороводородом по эндотермической реакции:
WO3+3HCl→WO2Cl2+H2O+HCl, T≥1400 K
Расчеты (рис.1) и лабораторные испытания показали, что реакция идет с выходом, близким к 100%, за время 15-30 минут.
После быстрого понижения температуры газовой смеси продуктов реакции до Т<520К из нее выделяется твердый диоксидихлорид вольфрама, а смесь избыточного хлороводорода и паров воды поступает на разделение (осушку), после которого газообразный хлороводород возвращается на стадию хлорирования. Удельная производительность процесса на стадии хлорирования триоксида вольфрама сопоставима с таковой для оксида железа (III) по связанному хлору и может достигать величины 130 т/(м3∗ч) Cl2.
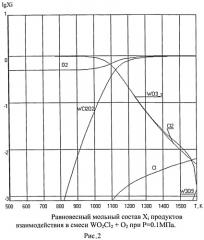
На второй стадии диоксидихлорид вольфрама подается в реактор окисления, где взаимодействует с кислородом по экзотермической реакции с выделением хлора (рис.2):
WO2Cl2+O2→WO3+Cl2+1/2O2, Т≤900 К
Пример 1.
Во вращающуюся обогреваемую трубчатую печь при температуре 1400 К подается порошок триоксида вольфрама со скоростью 0,6 кг/мин. В противотоке при давлении 0,1 МПа в печь подается хлороводород со скоростью 174 дм3/мин. На выходе печи образуются диоксидихлорид вольфрама со скоростью 0,74 кг/мин и газовая смесь хлороводорода и паров воды с отношением 1:1 со скоростью 116 дм3/мин. При температуре 500 К диоксидихлорид вольфрама конденсируется из газовой фазы и транспортируется в дозатор реактора окисления. После отделения воды циркулирующий газообразный хлороводород со скоростью 58 дм3/мин возвращается на вход печи хлорирования.
Пример 2.
Во вращающуюся печь с температурой на входе 500 К из дозатора поступает порошок диоксидихлорида вольфрама со скоростью 0,74 кг/мин и кислород в противотоке со скоростью 29 дм3/мин и давлении 0,1 МПа. При движении вдоль печи температура возрастает до 900 К, диоксидихлорид вольфрама возгоняется и диспропорционирует с образованием высших оксихлоридов, хлоридов, триоксида вольфрама и хлора. В присутствии кислорода конечным продуктом реакции является твердый триоксид вольфрама. На выходе реактора образуется хлор со скоростью 58 дм3/мин и триоксид вольфрама со скоростью 0,6 кг/мин, который возвращается в дозирующее устройство на стадию хлорирования.
Способ получения хлора из хлороводорода с помощью вольфрамсодержащих соединений, включающий хлорирование триоксида вольфрама хлороводородом при температуре более 1400 К, выделение диоксидихлорида вольфрама из газовой смеси продуктов хлорирования, окисление диоксидихлорида вольфрама кислородом с выделением хлора при температуре менее 900 К и возврат триоксида вольфрама на стадию хлорирования.