Способ получения частиц диоксида титана и частица диоксида титана
Иллюстрации
Показать всеИзобретение относится к химической промышленности, в частности к получению диоксида титана путем окисления жидкого тетрахлорида титана. Жидкий тетрахлорид титана вводят в реактор с кислородсодержащим газом по меньшей мере в две стадии. На первой стадии дозируется количество тетрахлорида титана, необходимое для запуска окисления. Количество стадий и распределение количества тетрахлорида титана по стадиями устанавливают в зависимости от адиабатической температуры смеси исходных веществ, рассчитанной для каждой стадии и обеспечивающей спонтанное протекание реакции. Способ обеспечивает равномерное распределение тетрахлорида титана и, следовательно, гомогенные условия протекания реакции, а также сокращение доли грубых частиц в пигменте. 2 н. и 7 з.п. ф-лы, 6 ил., 2 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к получению диоксида титана (TiO2) окислением тетрахлорида титана (ТiCl4), при этом тетрахлорид титана применяется в жидком виде.
Уровень техники
В одном из коммерчески используемых процессов производства частиц пигмента (диоксида титана), так называемом хлоридном процессе, тетрахлорид титана с таким окисляющим газом, как кислород, воздух и т.п., а также с определенными добавками, превращается в трубчатом реакторе в диоксид титана и газообразный хлор:
ТiCl4+О2→TiО2+2 Cl2,
Частицы ТiO2 отделяются затем от газообразного хлора. Как добавки известны АlСl3 - для получения рутильной формы кристаллов, а также водяной пар или щелочные соли - как центры кристаллизации.
На основании высокой энергии активации окисления TiСl4 исходные вещества должны нагреваться настолько сильно, что адиабатическая температура смеси исходных веществ достигает перед наступлением реакции примерно 800°С, чтобы реакция протекала полностью. Реакция окисления сильно экзотермическая, так что после полного адиабатического оборота температура потока продукта выше примерно на 900°С, чем температура исходных веществ. Вплоть до отделения частиц TiO2 от газообразных продуктов реакции с помощью фильтра, эта смесь должна продолжительно охлаждаться на охлаждающем участке, чтобы избежать потерь на фильтре.
Согласно US 3,615,202 кислород и ТiCl4 предварительно нагреваются и вводятся затем для реакции в трубчатый реактор. Так как общая смесь исходных веществ дозируется соответственно в трубчатый реактор, нужно говорить об одностадийном процессе. Также ЕР 0427878 В1 описывает одностадийный процесс, при нагревании кислорода от примерно 1500°С до 1650°С и смешении с примерно 450°С-градусным горячим паром ТiCl4-АlСl3. Ведение процесса энергетически неудовлетворительно в обоих случаях, так как по отношению к 100% подачи энергии для разогрева исходных веществ, после высвобождается примерно 160% тепловой энергии реакции. Затем примерно 210% тепловой энергии должны отводиться из горячего потока продукта на охлаждающем участке. Вместе с тем значительная энтальпия реакции используется не для активации реакции, а передается системе охлаждающей жидкости.
В одностадийном процессе согласно GB 696,618 TiCl4 вводится в реактор коаксиально, а горячий кислородосодержащий газ тангенциально. TiCl4 может подводиться в газообразной или в жидкой форме.
В ЕР 0583063 В1 с целью энергетической оптимизации описывается двухстадийноое введение TiCl4 в реактор. TiCl4 подается в горячий кислородный поток в первом пункте подачи с температурой минимум 450°С и смешанный с АlСl3, а в следующем пункте подачи с температурой 350°С до 400°С и без АlСl3.
Процесс согласно ЕР 0852568 В1 предусматривает дозирование кислорода наряду с TiCl4 также двухстадийно. Тем не менее, задача этого процесса - эффективный контроль среднего размера частиц TiO2 и вместе с тем цветности основных частиц пигмента TiO2. Здесь первоначально вводится в примерно 950°С горячий поток кислорода примерно 400°С горячий пар TiCl4. В следующей зоне реакции образуются частицы TiO2 и происходит увеличение частиц. Во втором пункте подачи подается менее сильно нагретый пар ТiCl4 (примерно 180°С). Кислород вводится во втором пункте подачи с температурой между 25 и 1040°С, причем температура смеси достаточна, чтобы реакция началась.
Многостадийный процесс согласно US 6,387,347 дополнительно должен сокращать образование агломерата. К тому же уже нагретый поток ТiCl4 перед дозировкой в реактор разделяется на 2 части. Первая часть потока окисляется в первой ступени реактора. Вторая часть потока охлаждается через распыление жидкого TiCl4 (снижение перегрева) и, присоединяясь, дозируется в реактор. Снижение перегрева происходит вне реактора, причем температура конденсации общего потока не используется.
US 2007/0172414 A1 раскрывает многостадийный процесс реакции TiCl4 и O2, при котором на первой стадии в реактор вводится газообразный TiCl4, а на второй стадии жидкий TiCl4. Этот процесс делает возможным энергоэкономию и улучшение спектра размера частицы.
Раскрытие изобретения
Цель данного изобретения состоит в том, чтобы сделать процесс получения диоксида титана путем окисления хлорида титана, что делает возможной дальнейшую энергоэкономию в существующих технологиях известных процессов.
В следствие этого, достижение цели состоит в описании способа получения частиц диоксида титана реакцией хлорида титана с кислородосодержащим газом в трубчатом реакторе, чтобы тетрахлорид титана вводился в реактор по меньшей мере в 2 стадии и исключительно в жидкой форме, а также в производстве диоксида титана по этому способу.
Дальнейшие предпочтительные формы изобретения описаны в подпроцессах.
В следствие этого, соответствующий изобретению способ отличается от упомянутых одностадийных или многостадийных хлоридных процессов получения диоксида титана по существующим технологиям тем, что TiCl4 вводится в реактор окисления минимум в 2 стадиях и исключительно в жидкой форме.
При этом весь используемый жидкий ТiCl4 разделяется по количеству на несколько стадий таким образом, что в первой стадии дозируется только небольшое количество, чтобы запустить окисление несмотря на применение жидкой фазы. Необходимая энергия активации предоставляется в первую стадию только через предварительно нагретый кислород. На всех следующих стадиях энергия активации предоставляется предварительно нагретым кислородом и выделенной на предыдущих стадиях энергией энтальпии реакции окисления ТiCl4.
При проведении процесса очень важно то, что реакция затухает не через впрыскивание большого количества жидкого TiCl4 на одной из стадий. Эффективную расчетную точку для того, чтобы реакция спонтанно протекала или угасала, обеспечивает рассчитанная адиабата температуры смеси всех исходных веществ в соответствующей стадии до начала реакции. Опыт показывает, что реакция с адиабатической температурой смеси примерно 740°С протекает полностью. На этом основании специалист может устанавливать количество необходимых стадий и разделение TiCl4 на эти стадии.
Неожиданно соответствующий изобретению хлоридный процесс с чистой жидкой дозировкой TiCl4 может проводиться не только при использовании предварительно нагретого примерно до 1600°С кислорода, но и при использовании предварительно нагретого кислорода до температуры в области 740°С - 1000°С. В последнем случае появляется необходимость дополнительного нагревания кислорода во вспомогательном пламени, к примеру, с толуолом. Дополнительное преимущество второго варианта - это более низкое потребление хлора, которое возникает из-за образования HCl в ходе сгорания толуола.
Краткое описание чертежей
Следующие Фигуры от 1 до 6 служат лучшему пониманию предпочтительных воплощений изобретения:
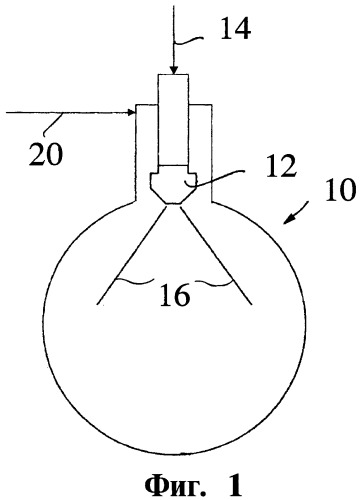
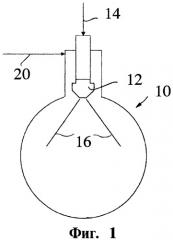
Фиг.1: Схематическое изображение трубчатого реактора с однокомпонентной форсункой, которая направлена параллельно плоскости, перпендикулярной к центральной оси реактора.
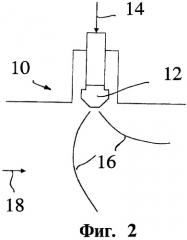
Фиг.2: Вид сбоку реактора по Фиг.1.
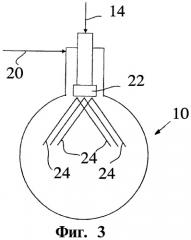
Фиг.3: Схематическое изображение трубчатого реактора с форсункой с несколькими коническими отверстиями.
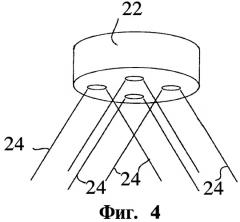
Фиг.4: Увеличенное представление форсунки по Фиг.3.
Фиг.5: Схематическое изображение трубчатого реактора с 3 однокомпонентными соплами, которые направлены радиально в объеме трубчатого реактора и параллельно плоскости, перпендикулярной к центральной оси реактора.
Фиг.6: Схематическое изображение трубчатого реактора с 3 однокомпонентными форсунками, которые направлены тангенциально в объеме трубчатого реактора и параллельно плоскости, перпендикулярной к центральной оси реактора.
Осуществление изобретения
Соответствующий изобретению способ может быть проведен при условиях следующих примеров 1 и 2, при этом настоящее изобретение не ограниченивается этим списком. Сравнительный пример содержит одностадийную дозировку газообразного ТiCl4 согласно технологии (ЕР 0427878 В1):
| Пример 1 | Пример 2 | Сравнение | ||
| Количество стадий | 2 | 5 | 1 | |
| О2-температура | ||||
| перед зоной реакции (°С) | 1650 | 920 | 1650 | |
| Требуется Толуола (кг/ч.) | 110 | 0 | 110 | |
| Потребление Cl из-за | ||||
| образования HCl (кг/ч.) | 340 | 0 | 340 | |
| TiCl4 (т/ч) | 1. Стадия | 9,1 | 1,2 | 24,0 |
| 2. Стадия | 14,9 | 2,9 | - | |
| 3. Стадия | - | 4,3 | - | |
| 4. Стадия | - | 6,5 | - | |
| 5. Стадия | - | 9,1 | - |
Соответствующий изобретению способ предлагает несколько преимуществ по сравнению с дозировкой газообразного TiCl4:
- Энергетические издержки и погрешности оборудования проявляются при испарении ТiCl4.
- При жидкой дозировке на основе высокого импульса впрыскиваемых капель жидкости, TiCl4 может лучше распределяться, и могут создаваться таким образом более гомогенные условия реакции.
При многостадийном процессе смешивания с относительно холодными исходными веществами во второй и последующих стадиях сгорания, адиабатическая температура реакции будет опущенной, так что процесс спекания, т.е. увеличения частицы заканчивается более скоро. Таким образом сокращается доля грубых частиц в пигменте.
Фигуры от 1 до 6 показывают примерные воплощения изобретения. Фиг.1 и Фиг.2 показывают трубчатый реактор (10). Поступление жидкого TiCl4 (14) в трубчатый реактор (10) происходит, к примеру, форсунками (12), которые расположены кольцеобразно в объеме реактора (10). Жидкий TiCl4 (14) распыляется с помощью форсунки (12) в маленькие капли (16), которые испаряются в реакторе (10) без удара о стену реактора (10). Фиг.2 показывает направление (18) потока газа в реакторе (10). Форсунка (12) предпочтительно обдувается эффективно защищающим газом (20), который дополнительно вводится в реактор (10), чтобы предотвращать налипание твердых веществ и тепловое повреждение форсунки (12). Фиг.1 показывает выравнивание форсунки (12) параллельно уровню, перпендикулярному центральной оси реактора (10).
Фиг.3 и Фиг.4 показывают предпочтительное исполнение изобретения, при котором используется форсунка с несколькими коническими отверстиями (22), которая распыляет вводимый жидкий TiCl4 (14) по сравнению с однокомпонентной форсункой (12) в меньшие капли (24). Для другого фоплощения изобретения применяются вместо однокомпонентной форсунки как (12 и 22) 2-компонентные форсунки, при которых одновременно могут вводиться в реактор (10) как жидкий TiCl4, так и газообразная среда. В качестве газообразной среды могут использоваться, к примеру, один или смесь газов из группы азот, аргон, газообразный хлор и кислород.
Фиг.5 показывает воплощение изобретения, при котором форсунки (12) расположены радиально в объеме трубчатого реактора (10) и направлены параллельно плоскости, перпендикулярной центральной оси реактора (10). Жидкий TiCl4 (14) вводится форсунками (12) в реактор (10) и распыляется (26).
Фиг.6 показывает воплощение изобретения, при котором форсунки (12) расположены тангенциально в объеме трубчатого реактора (10) и направлены параллельно плоскости, перпендикулярной центральной оси реактора (10). Жидкий ТiCl4 (14) подается форсунками (12) в реактор (10) и распыляется (28). Через тангенциальное расположение форсунок (12) поток в реакторе (10) переводится во вращение. Таким образом, согласно технологии, принесенные в реактор (10) частицы для чистки лучше распределяются для очистки внутренних стен реактора (10).
Описанные воплощения изобретения представляют только возможные формы изобретения и не нужно понимать их как ограничение изобретения. К примеру, соответствующий изобретению способ опционально охватывает также известную специалистам дозировку в зону реакции 20 добавок для рутилизации (например, АlСl3) и для образования центров кристаллизации (например, щелочные соли). Далее соответствующий изобретению процесс охватывает также воплощения изобретения, при которых кислород дозируется многостадийно.
1. Способ получения частиц диоксида титана, включающий реакцию тетрахлорида титана с кислородосодержащим газом в трубчатом реакторе, отличающийся тем, что тетрахлорид титана вводят в реактор в жидкой форме по меньшей мере в две стадии, при этом на первой стадии вводят количество тетрахлорида титана, необходимое для запуска реакции окисления, а количество необходимых стадий и разделение количества тетрахлорида титана на стадии устанавливают в зависимости от рассчитанной адиабатической температуры смеси исходных веществ на каждой стадии до начала реакции, обеспечивающей ее спонтанное протекание.
2. Способ по п.1, отличающийся тем, что тетрахлорид титана вводят однокомпонентной форсункой, в частности форсункой с группой конических отверстий.
3. Способ по п.1, отличающийся тем, что тетрахлорид титана вводят двухкомпонентными форсунками.
4. Способ по п.3, отличающийся тем, что в нем используют газообразную среду, выбранную из группы газов, включающей азот, аргон, газообразный хлор или смесь из этих газов.
5. Способ по любому из пп.2-4, отличающийся тем, что форсунки обволакивают защитным газом.
6. Способ по любому из пп.2-4, отличающийся тем, что форсунки устанавливают направленными параллельно плоскости, перпендикулярной центральной оси реактора.
7. Способ по п.6, отличающийся тем, что форсунки располагают тангенциально на окружности реактора.
8. Способ по п.1, отличающийся тем, что кислородосодержащий газ предварительно нагревают до температуры примерно 1600°С, предпочтительно до температуры в области примерно 740°С-1000°С.
9. Частица диоксида титана, полученная способом по любому из пп.1-8.