Модифицированная липидом двухцепочечная рнк, обладающая эффектом рнк-интерференции
Иллюстрации
Показать всеИзобретение относится к области молекулярной биологии, генетики и медицины. Предложена модифицированная липидом двухцепочечная РНК, содержащая антисмысловую цепь, имеющую нуклеотидную последовательность, комплементарную целевой последовательности, и смысловую цепь, имеющую нуклеотидную последовательность, комплементарную антисмысловой цепи. Смысловая цепь содержит липид, присоединенный напрямую или через линкер, по меньшей мере к одному из первых шести нуклеотидов 5'-концевой стороны. Данная двухцепочечная РНК способна ингибировать экспрессию гена-мишени. Предложенная РНК обладает высокой нуклеазной устойчивостью, эффективностью внутриклеточного накопления и высоким эффектом РНК-интерференции. Изобретение может быть использовано в медицине для лечения болезней, обусловленных генетическими нарушениями. 4 н. и 8 з.п. ф-лы, 10 ил., 2 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к модифицированной липидом двухцепочечной РНК, способной эффективно ингибировать экспрессию гена-мишени. Более конкретно, настоящее изобретение относится к модифицированной липидом двухцепочечной РНК, которая обладает высокой устойчивостью к нуклеазе, высокой эффективностью внутриклеточного накопления, и вызывает превосходный эффект РНК-интерференции.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Разработка лекарственных средств для эффективного лечения трудноизлечимых заболеваний, таких как рак и СПИД, является важной задачей в области медико-биологических наук. Одним из потенциальных способов решения данной задачи является использования генетических лекарств, воздействующих только на специфические гены. В особенности, в качестве подобного генетического лекарства в последнее время много внимания привлекает к себе способ РНК-интерференции (РНКи), использующий короткую двухцепочечную РНК длиной в 21 нуклеотидное основание (малая интерферирующая РНК: миРНК). Способ РНКи впервые описан Fire et al. в 1998 (смотри непатентный документ 1). Согласно отчету Fire et al., когда гомологичная специфической области гена, функцию которого необходимо ингибировать, двухцепочечная РНК из приблизительно 100 пар оснований доставляется внутрь клеток, она расщепляется под действием дайсера на фрагменты длиной приблизительно от 20 до 25 пар оснований, и затем взаимодействует с множеством белков с образованием комплекса РНК/белок (такой комплекс обозначается как RISC: РНК-индуцированный ингибирующий комплекс), который связывается с гомологичным участком мРНК, синтезированной с гена-мишени, и таким образом значительно ингибирует экспрессию гена. Однако было отмечено, что когда длинная двухцепочечная РНК из приблизительно 30 пар оснований или длиннее доставляется внутрь клеток млекопитающих, индуцируется интерфероновый ответ, являющийся противовирусным ответом, и тем самым вызывается процесс апоптоза. Таким образом, применение способа РНКи в отношении млекопитающих считалось сложным. Затем Tuschl et al. химическим способом синтезировали двухцепочечную РНК длиной в 21 основание, которая имеет выступающие концы на обоих 3'-концах, и отмечено, что когда такая двухцепочечная РНК напрямую доставляется внутрь клеток млекопитающих, двухцепочечная РНК способна специфично к последовательности значительно ингибировать экспрессию гена без развития интерферонового ответа (смотри непатентный документ 2). Tuschl et al. в дальнейшем синтезировали короткие двухцепочечные РНК, состоящие из двухцепочечного фрагмента из 19 пар оснований и выступающего конца(ов) различных протяженностей на 3' или 5'-концах, и изучали их эффекты РНК-интерференции. В итоге, наблюдения показывают, что миРНК длиной в 21 основание, имеющие выступающий конец из 2 оснований на обоих 3'-концах, проявляли очень сильный эффект РНК-интерференции, в то время как другие типы коротких двухцепочечных РНК не демонстрировали значимый эффект РНК-интерференции. Основываясь на данной работе, способ РНК-интерференции с использованием двухцепочечной РНК длиной в 21 основание, имеющей выступающий конец из 2 оснований на обоих 3'-концах, является общеупотребительным. Способ ингибирования экспрессии гена-мишени с использованием короткой двухцепочечной РНК длиной в 21 основание представляет собой способ, обозначаемый в настоящем документе как "миРНК способ", для разграничения его со способом РНКи.
Благодаря тому, что в способе миРНК используют синтетическую РНК, получение и хранение образцов является сравнительно легким; кроме того, могут быть получены очень сильные эффекты. Таким образом, способ миРНК привлекает к себе значительное внимание не только в области медико-биологических наук, но также и в области биотехнологического бизнеса.
Однако данный превосходный способ миРНК также имеет проблему, требующую решения. Как описано выше, миРНК состоит из молекулы РНК, уже разделенной под действием нуклеазы. По сравнению с одноцепочечной РНК, фрагмент двухцепочечной РНК обладает сравнительно высокой устойчивостью к нуклеазе, содержащейся в среде и/или клетке. Однако двухцепочечная РНК, состоящая из 19 пар оснований, почти не производит известные эффекты РНК-интерференции. По существу отмечено, что, будучи доставленной внутрь клеток, содержащая последовательность гена-мишени синтетическая миРНК хотя и производит сильный ингибирующий эффект на экспрессию гена в течение приблизительно от 2 до приблизительно 4 суток, ее эффект РНК-интерференции значительно снижается в дальнейшем и практически полностью исчезает через приблизительно семь суток.
Недавно было показано, что различные химические модифицикации миРНК снабжают синтетические миРНК повышенной эффективностью внутриклеточного накопления и пролонгированными высокоактивными эффектами РНК-интерференции. Например, для повышения устойчивости к экзонуклеазному расщеплению, миРНК модифицируют посредством аминогруппы, тиоловой группы или участка без оснований на конце синтезированной миРНК. Однако отмечено, что большинство терминально модифицированных миРНК длиной в 21 основание обладают значительно сниженными эффектами РНК-интерференции.
Недавно J. Rossi et al. отметили, что двухцепочечная РНК из 27 пар оснований производит эффект РНК-интерференции приблизительно в 100 раз больший, чем двухцепочечная РНК длиной в 21 основание (смотри непатентный документ 3). Это возможно происходит благодаря тому, что после расщепления РНК из 27 пар оснований РНКаза III-подобным ферментом дайсером на миРНК длиной в 21 основание, белковый комплекс RISC распознает миРНК таким образом, что миРНК способно производить эффекты с большой эффективностью.
Как описано выше, благодаря тому, что РНК длиной в 27 оснований может производить превосходные эффекты РНК-интерференции, повышаются ожидания, связанные с использованием такой РНК в качестве генетического лекарства. Однако совершенно неизвестен эффективный технический способ для увеличения эффекта РНК-интерференции РНК длиной в 27 оснований. Кроме того, также неясен технический способ для увеличения эффекта РНК-интерференции двухцепочечной РНК протяженностью короче или длиннее 27 оснований и обладающей эффектом РНК-интерференции.
Двухцепочечные РНК, имеющие эффекты РНК-интерференции, как правило, сконструированы с учетом выступающих концов. Для РНК без выступающих концов (т.е., имеющие тупые концы) также изучались их эффекты РНК-интерференции. Однако результаты указывают на то, что эффекты РНК-интерференции двухцепочечной РНК затупленной на 5'-концевой стороне смысловой цепи практически такие же или ниже, чем эффекты двухцепочечных РНК, имеющих выступающий конец на 5'-концевой стороне смысловой цепи (смотри непатентный документ 4).
Липиды обладают высокой проницаемостью для клеточной мембраны, и признаны практичными для доставки лекарственных средств внутрь клеток. Ожидается, что присоединение таких липидов к двухцепочечной РНК, обладающей эффектом РНК-интерференции, повысит эффективность внутриклеточного накопления и таким образом усилит эффекты РНК-интерференции. Однако, известно, что если липид просто присоединен к двухцепочечной РНК, обладающей эффектом РНК-интерференции, то это резко снижает ее эффект РНК-интерференции. На известном уровне техники все еще необходимо сконструировать модифицированную липидом двухцепочечную РНК, обладающую одновременно превосходным эффектом РНК-интерференции и практическим эффектом, основанным на липиде.
Непатентный документ 1: Fire et al., Nature, 391, 806-811 (1998)
Непатентный документ 2: Tuschl et al., EMBO Journal, 20, 6877-6888 (2001)
Непатентный документ 3: J. Rossi et al., Nature Biotech., 23, 222-226 (2005)
Непатентный документ 4: J. T. Marques et al., Nature Biotech., 24, 559-565 (2005)
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ЗАДАЧА, ПОДЛЕЖАЩАЯ РЕШЕНИЮ ПОСРЕДСТВОМ ИЗОБРЕТЕНИЯ
Предмет настоящего изобретения обеспечивает новую двухцепочечную РНК, имеющую высокую устойчивость к нуклеазе и высокую эффективность внутриклеточного накопления, и способную производить превосходный эффект РНК-интерференции. Другой предмет настоящего изобретения обеспечивает фармацевтическую композицию, содержащую новую двухцепочечную РНК. Дополнительный предмет настоящего изобретения обеспечивает способ ингибирования экспрессии гена-мишени, заключающий в себе введение двухцепочечной РНК внутрь клеток для ингибирования экспрессии гена-мишени.
СРЕДСТВА РЕШЕНИЯ ЗАДАЧИ
Авторы настоящего изобретения проводили многочисленные исследования для получения описанных выше объектов и обнаружили, что, если липид присоединен напрямую или через линкер, по меньшей мере, к одному из первых шести нуклеотидов на 5'-конце смысловой цепи двухцепочечной РНК, содержащей смысловую цепь, имеющую комплементарную целевой последовательности в гене-мишени нуклеотидную последовательность, и антисмысловую цепь, имеющую комплементарную смысловой цепи нуклеотидную последовательность, двухцепочечная РНК способна ингибировать экспрессию гена-мишени, то сконструированная таким образом двухцепочечная РНК обладает высокой нуклеазной устойчивостью и высокой эффективностью внутриклеточного накопления и производит превосходный эффект РНК-интерференции. Настоящее изобретение стало результатом дальнейшего изучения, основанного на данном открытии.
Более конкретно, настоящее изобретение относится к следующей модифицированной липидом двухцепочечной РНК, фармацевтическим композициям, содержащим новую двухцепочечную РНК, способам ингибирования экспрессии гена-мишени и т.д.
Пункт 1. Модифицированная липидом двухцепочечная РНК, содержащая смысловую цепь, имеющую комплементарную целевой последовательности в гене-мишени нуклеотидную последовательность, и антисмысловую цепь, имеющую комплементарную смысловой цепи нуклеотидную последовательность, причем двухцепочечная РНК способна ингибировать экспрессию гена-мишени, и смысловая цепь имеет липид, присоединенный напрямую или через линкер, по меньшей мере, к одному из первых шести нуклеотидов на 5'-конце.
Пункт 2. Модифицированная липидом двухцепочечная РНК по п. 1, тупоконечная на 5'-концевой стороне смысловой цепи, и тупоконечная или имеющая выступающий конец на 3'-концевой стороне смысловой цепи.
Пункт 3. Модифицированная липидом двухцепочечная РНК по п. 1, имеющая выступающие концы одновременно на 5'- и 3'-концевых сторонах смысловой цепи.
Пункт 4. Модифицированная липидом двухцепочечная РНК по любому из пп. 1-3, в которой смысловая цепь состоит из 21-27 нуклеотидов.
Пункт 5. Модифицированная липидом двухцепочечная РНК по п. 2, тупоконечная одновременно на 5'- и 3'-концевых сторонах смысловой цепи, и в которой каждая из смысловой и антисмысловой цепей состоит из 27 нуклеотидов.
Пункт 6. Модифицированная липидом двухцепочечная РНК по п. 2, тупоконечная одновременно на 5'- и 3'-концевых сторонах смысловой цепи, и в которой каждая из смысловой и антисмысловой цепей состоит из 23 нуклеотидов.
Пункт 7. Модифицированная липидом двухцепочечная РНК по п. 2, тупоконечная на 5'-концевой стороне смысловой цепи, причем смысловая цепь, состоит из 25 нуклеотидов, а антисмысловая цепь, состоит из 23 нуклеотидов.
Пункт 8. Модифицированная липидом двухцепочечная РНК по п. 3, в которой каждая из смысловой и антисмысловой цепей состоит из 21 нуклеотида.
Пункт 9. Модифицированная липидом двухцепочечная РНК по любому из пп. 1-8, в которой липид представляет собой жирную кислоту, имеющую от 6 до 50 атомов углерода.
Пункт 10. Модифицированная липидом двухцепочечная РНК по любому из пп. 1-9, в которой липид представляет собой лауриновую кислоту, стеариновую кислоту, миристиновую кислоту или пальмитиновую кислоту.
Пункт 11. Модифицированная липидом двухцепочечная РНК по любому из пп. 1-10, в которой липид присоединен, по меньшей мере, к одному из первых шести нуклеотидов на 5'-конце смысловой цепи через линкер, причем линкер представлен структурной формулой
-NH-(CH2)n1- (L-4),
где n1 представляет собой целое число от 1 до 40.
Пункт 12. Фармацевтическая композиция, содержащая модифицированную липидом двухцепочечную РНК по любому из пп. 1-10 и фармацевтически приемлемую основу.
Пункт 13. Применение модифицированной липидом двухцепочечной РНК по любому из пп. 1-10 для производства фармацевтической композиции с целью ингибирования экспрессии гена-мишени.
Пункт 14. Способ ингибирования экспрессии гена-мишени, включающий введение модифицированной липидом двухцепочечной РНК по любому из пп. 1-10 внутрь клеток для ингибирования экспрессии гена-мишени.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
Модифицированная липидом двухцепочечная РНК по настоящему изобретению модифицирована липидом на 5'-концевой стороне смысловой цепи и вследствие этого производит существенно увеличенный эффект РНК-интерференции. Более конкретно, модифицированная липидом двухцепочечная РНК имеет липид, присоединенный к специфическому участку РНК, и таким образом обладает заметно повышенной устойчивостью к нуклеазе и эффективностью внутриклеточного накопления без ослабления процессинга дайсером или связывания РНК с RISC, и таким образом может значительно способствовать медицинскому применению.
Модифицированная липидом двухцепочечная РНК по настоящему изобретению даже в случае самостоятельного использования обладает превосходной способностью к внутриклеточной доставке. Таким образом, модифицированная липидом двухцепочечная РНК может доставляться внутрь клеток без использования любых известных средств для генетической трансфекции или использования сниженного количества известного средства для генетической трансфекции. Таким образом, модифицированная липидом двухцепочечная РНК по настоящему изобретению способна снижать выраженность цитотоксичности, сопровождающую использование известных средств для генетической трансфекции, тем самым гарантируя высокий уровень безопасности для клинических применений.
Таким образом, экспрессия гена-мишени может более эффективно ингибируется или ослабляться посредством применения фармацевтической композиции по настоящему изобретению или посредством применения способа ингибирования экспрессии гена-мишени по настоящему изобретению.
НАИЛУЧШИЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В данной спецификации "тупой конец" или "тупоконечный" относится к концевой структуре двухцепочечной РНК, в которой основания в концевых участках смысловой цепи и основания в концевых участках антисмысловой цепи, комплементарной смысловой цепи, спарены без образования одиночной цепочки. "Выступающий конец" относится к концевой части нуклеотидной последовательности, в которой находится одиночная цепочка, не формирующая двойную цепочку благодаря отсутствию комплементарных оснований в концевых участках смысловой цепи двухцепочечной РНК или в концевых участках антисмысловой цепи, комплементарной смысловой цепи.
Модифицированная липидом двухцепочечная РНК по изобретению включает смысловую цепь, имеющую нуклеотидную последовательность, комплементарную целевой последовательности в гене-мишени.
Ген-мишень в настоящем документе относится к гену, экспрессию которого необходимо ингибировать посредством эффекта РНК-интерференции. Ген-мишень для модифицированной липидом двухцепочечной РНК по изобретению не определен строго, и его можно выбирать подходящим образом согласно предполагаемому применению модифицированной липидом двухцепочечной РНК.
Целевая последовательность в гене-мишени не определена строго при условии, что экспрессию гена можно ингибировать эффектами РНК-интерференции. Целевую последовательность можно определять подходящим образом согласно известному способу, например, используя поиск NCBI BLAST и т.д. Например, целевая последовательность может являться областью, состоящей из 19-30 оснований, следующих за основаниями "АА" в области экзона, находящегося на расстоянии 50-100 оснований от стартового кодона кодирующей области (ORF) гена-мишени, и содержащая приблизительно 50% GC. В данной области экспериментально показано, что превосходные эффекты РНК-интерференции можно получать при помощи цепочки, комплементарной такой целевой последовательности. Например, целевую последовательность можно определять согласно инструкциям IDT (Integrated DNA Technologies, Inc.; дайсер-субстратный дизайн РНКи). Недавнее сообщение показало, что двухцепочечную РНК, обладающую сильными эффектами РНК-интерференции можно получать посредством конструирования двухцепочечной РНК, которая содержит: (i) пару A/U на 5'-концевой стороне антисмысловой цепи; (ii) пару G/C на 5'-концевой стороне смысловой цепи; и (iii) приблизительно пять пар A/U на 5'-концевой стороне антисмысловой цепи; (iv) и не содержит девять и более пар G/C (Ui-Tei et al., Nucleic Acids Res., 32, 936-948 (2004)).
Если смысловая цепь модифицированной липидом двухцепочечной РНК по изобретению не имеет выступающего конца, то смысловая цепь состоит из нуклеотидной последовательности, комплементарной целевой последовательности. Если смысловая цепь имеет выступающий конец на 5'-конце и/или 3'-конце, то смысловая цепь состоит из нуклеотидной последовательности, имеющей нуклеотидную последовательность, комплементарную целевой последовательности и нуклеотидную последовательность выступающего конца, присоединенную к 5'-концу и/или 3'-концу комплементарной нуклеотидной последовательности.
При условии достижения эффекта РНК-интерференции количество нуклеотидов, составляющих смысловую цепь в модифицированной липидом двухцепочечной РНК по изобретению, не определено строго и может выбираться подходящим образом согласно требуемой структуре двухцепочечной РНК. Количество нуклеотидов обычно составляет от 21 до 27, предпочтительно 21, 23, 25 или 27, и более предпочтительно 21, 23 или 27. Если смысловая цепь не имеет выступающего конца, то количество нуклеотидов, составляющих смысловую цепь, соответствует общему количеству нуклеотидов, составляющих комплементарную целевой нуклеотидную последовательность. Если смысловая цепь имеет выступающий конец, то количество нуклеотидов, составляющих смысловую цепь, соответствует сумме количества нуклеотидов, составляющих выступающий конец, и количества нуклеотидов, составляющих комплементарную целевой нуклеотидную последовательность. Модифицированная липидом двухцепочечная РНК по изобретению включает антисмысловую цепь, имеющую комплементарную смысловой цепи нуклеотидную последовательность.
Если антисмысловая цепь модифицированной липидом двухцепочечной РНК по изобретению не имеет выступающего конца, то антисмысловая цепь состоит из нуклеотидной последовательности, комплементарной части или всем "комплементарным целевой последовательности нуклеотидам" смысловой цепи. Если антисмысловая цепь имеет выступающий конец на 5'-конце и/или 3'-конце, то антисмысловая цепь состоит из: нуклеотидной последовательности, части или всем "комплементарным целевой последовательности нуклеотидам" смысловой цепи; и нуклеотидной последовательности выступающего конца, присоединенного к 5'-концу и/или 3'-концу комплементарной нуклеотидной последовательности антисмысловой цепи. При условии достижения эффекта РНК-нтерференции количество нуклеотидов, составляющих антисмысловую цепь в модифицированной липидом двухцепочечной РНК по изобретению, не определено строго и может выбираться подходящим образом согласно требуемой структуре двухцепочечной РНК. Количество нуклеотидов обычно составляет от 21 до 27, предпочтительно 21, 23, 25 или 27, и более предпочтительно 21, 23 или 27. Если антисмысловая цепь не имеет выступающего конца, то количество нуклеотидов, составляющих антисмысловую цепь, соответствует общему количеству нуклеотидов, составляющих комплементарную целевой последовательности нуклеотидную последовательность. Если антисмысловая цепь имеет выступающий конец, то количество нуклеотидов, составляющих антисмысловую цепь, соответствует сумме количества нуклеотидов, составляющих выступающий конец, и количества нуклеотидов, составляющих комплементарную целевой нуклеотидную последовательность.
Нуклеотиды, составляющие смысловую цепь и антисмысловую цепь модифицированной липидом двухцепочечной РНК по изобретению, в основном представляют собой рибонуклеотиды. Для повышения устойчивости к ферментативному расщеплению последовательность РНК может содержать различные химически модифицированные нуклеотиды, такие как 2'-О-метил-модифицированные нуклеотиды, 2'-F-модифицированные нуклеотиды, LNA (замкнутая нуклеиновая кислота) нуклеотиды, дезоксирибонуклеотиды или т.п. В особенности, если модифицированная липидом двухцепочечная РНК по изобретению имеет выступающий конец, то выступающий конец смысловой цепи и/или антисмысловой РНК может состоять из дезоксирибонуклеотидов. Примеры таких химически модифицированных нуклеотидов включают нуклеотиды с фосфат-модифицированной структурой, такие как фосфотиоат-модифицированная ДНК/РНК и боранофосфат-модифицированная ДНК/РНК; 2'-модифицированные нуклеотиды, такие как 2'-О-Ме-модифицированные РНК и 2'-F-модифицированные РНК; модифицированные нуклеотиды, полученные посредством сшивания сахара молекулы нуклеотида, такие как LNA (замкнутая нуклеиновая кислота) и ENA (2'-O-,4'-C-этилен- соединенные нуклеиновые кислоты); модифицированные нуклеотиды, имеющие различные структуры, такие как ПНК (пептидная нуклеиновая кислота) и морфолиннуклеотид; нуклеотиды с модифицированными основаниями, такие как 5-фторуридин и 5-пропилуридин; и т.п.
Структурно модифицированная липидом двухцепочечная РНК по изобретению не определена строго при условии, что смысловая и антисмысловая цепи гибридизованы в двойную цепь. Например, модифицированная липидом двухцепочечная РНК предпочтительно имеет следующую структуру: структура (A), в которой двухцепочечная РНК тупоконечная (т.е. имеет тупой конец) на 5'-концевой стороне смысловой цепи и тупоконечная или имеет выступающий конец (одноцепочечный фрагмент) на 3'-концевой стороне смысловой цепи; структура (B), в которой двухцепочечная РНК имеет выступающие концы на 5' и 3'- на 5'-концевых сторонах смысловой цепи. Структура, в которой двухцепочечная РНК имеет выступающий конец на 3'-концевой стороне смысловой цепи включает случаи, когда 3'-концевой фрагмент смысловой цепи образует выступающий конец, и случаи, когда 5'-концевой фрагмент антисмысловой цепи образует выступающий конец. Структура, в которой двухцепочечная РНК имеет выступающий конец на 5'-концевой стороне смысловой цепи включает случай, когда 5'-концевой фрагмент смысловой цепи образует выступающий конец, и случай, когда 3'-концевой фрагмент антисмысловой цепи образует выступающий конец.
Для достижения дополнительно усиленного эффекта РНК-интерференции среди двухцепочечных РНК, которые можно использовать для создания модифицированной липидом двухцепочечной РНК по изобретению, особенно предпочтительны двухцепочечные РНК, имеющие структуры с (A-1) по (A-3), представленные ниже, среди имеющих указанную выше структуру (A), и особенно предпочтительны двухцепочечные РНК со структурой (B-1), представленной ниже, среди имеющих указанную выше структуру (B). Структура (A-1), в которой двухцепочечная РНК тупоконечная на обоих 5' и 3'-концах смысловой цепи, и каждая из смысловых и антисмысловых цепей состоит из 27 нуклеотидов; структура (A-2), в которой двухцепочечная РНК тупоконечная на обоих 5' и 3'-концах смысловой цепи, и каждая из смысловых и антисмысловых цепей состоит из 23 нуклеотидов, соответственно; структура (A-3), в которой двухцепочечная РНК тупоконечная на 5'-концевой стороне смысловой цепи, и смысловая цепь состоит из 25 нуклеотидов, и антисмысловая цепь состоит из 23 нуклеотидов; и структура (B-1), в которой двухцепочечная РНК имеет выступающие концы, состоящие каждый из двух нуклеотидов на каждом 3'-конце смысловой цепи и 3'-конце антисмысловой цепи, и каждая из смысловых и антисмысловых цепей состоит из 21 нуклеотида.
Более конкретно, в структурах (A-1) и (A-2) смысловые и антисмысловые цепи гибридизованы без образования выступающих концов. В структуре (A-3) смысловые и антисмысловые цепи гибридизованы таким образом, что двухцепочечная РНК тупоконечная на 5'-конце смысловой цепи, и первые и второй нуклеотиды с 3'-конца смысловой цепи образуют выступающий конец. Структура (B-1) такова, что с первого по 19-й нуклеотиды с 5'-конца смысловой цепи и с третьего по 21-й нуклеотиды с 3'-конца антисмысловой цепи гибридизованы таким образом, что первый и второй нуклеотиды с 3'-конца смысловой цепи и первый и второй нуклеотиды с 3'-конца антисмысловой цепи образуют выступающие концы, соответственно.
Модифицированная липидом двухцепочечная РНК по изобретению имеет, по меньшей мере, один липид, присоединенный, по меньшей мере, к одному из первых шести нуклеотидов с 5'-конца смысловой цепи. Модифицированная липидом двухцепочечная РНК по изобретению не имеет замещающих групп ни в какой другой позиции, кроме 5'-концевого фрагмента смысловой цепи. Более конкретно, замещающие группы не содержатся в иных областях, кроме 5'-концевого фрагмента смысловой и антисмысловой цепи, и эти области состоят из нуклеотидов. Присоединение липида(ов) только к 5'-концевому фрагменту смысловой цепи способно повысить эффективность внутриклеточного накопления и обеспечить исключительно превосходный эффект РНК-интерференции.
Присоединенный к смысловой цепи модифицированной липидом двухцепочечной РНК по изобретению липид не определен строго, и вследствие этого примеры включают простые липиды (сложные эфиры жирных кислот с различными спиртами); сложные липиды, такие как фосфолипиды и гликолипиды; производные липидов, такие как жирные кислоты, высшие спирты, жирорастворимые витамины, стероиды и углеводороды. Для повышения эффективности внутриклеточного накопления и эффекта РНК-интерференции, используемый липид является предпочтительно производным липида, более предпочтительно жирной кислотой, имеющей от 6 до 50 атомов углерода, еще более предпочтительно жирной кислотой, имеющей от 10 до 22 атомов углерода, особенно предпочтительно жирной кислотой, имеющей от 12 до 18 атомов углерода, более конкретно, предпочтительно лауриновой кислотой, стеариновой кислотой, миристиновой кислотой или пальмитиновой кислотой и наиболее предпочтительно пальмитиновой кислотой.
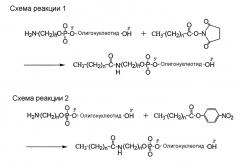
Способ присоединения липида к смысловой цепи для образования модифицированной липидом двухцепочечной РНК по изобретению не определен строго. Липид можно присоединять к смысловой цепи напрямую или через линкер. В настоящем изобретении, линкер, через который липид присоединен к смысловой цепи не является линкером, состоящим из нуклеиновой кислоты. Линкер не определен строго при условии, что посредством него можно соединять липид и смысловую цепь. Например, в качестве линкера можно использовать линкеры, имеющие следующие структуры:
-O-Co-O- (L-1)
-NH-CO-O- (L-2)
-NH-CO-NH- (L-3)
-NH-(CH2)n1- (L-4)
-S-(CH2)n1- (L-5)
-CO-(CH2)n1-CO- (L-6)
-CO-(CH2)n1-NH- (L-7)
-NH-(CH2)n1-NH- (L-8)
-CO-NH-(CH2)n1-NH-CO- (L-9)
-C(=S)-NH-(CH2)n1-NH-CO- (L-10)
-C(=S)-NH-(CH2)n1-NH-C-(=S)- (L-11)
-CO-O-(CH2)n1-0-CO- (L-12)
-C(=S)-O-(CH2)n1-O-CO- (L-13)
-C(=S)-O-(CH2)n1-O-C-(=S)- (L-14)
-CO-NH-(CH2)n1-O-CO- (L-15)
-C(=S)-NH-(CH2)n1-O-CO- (L-16)
-C(=S)-NH-(CH2)n1-O-C-(=S)- (L-17)
-CO-NH-(CH2)n1-O-CO- (L-18)
-C(=S)-NH-(CH2)n1-CO- (L-19)
-C(=S)-O-(CH2)n1-NH-CO- (L-20)
-C(=S)-NH-(CH2)n1-O-C-(=S)- (L-21)
-NH-(CH2CH2O)n2-CH(CH2OH)- (L-22)
-NH-(CH2CH2O)n2-CH2- (L-23)
В указанных выше формулах (L-4)-(L-21), n1- это число от 1 до 40, предпочтительно число от 2 до 20, и более предпочтительно число от 2 до 12.
В указанных выше формулах (L-22) и (L-23), n2 это число от 1 до 20, предпочтительно число от 1 до 10, и более предпочтительно число от 1 до 6.
Линкеры в формулах (L-4)-(L-23) могут связывать смысловую цепь как с правой, так и с левой стороны. Предпочтительно, специфический участок смысловой цепи (или нуклеиновая кислота в конъюгате нуклеиновой кислоты) присоединен с правой стороны к линкерам по формулам (L-4)-(L-23), и липид присоединен к их левой стороне.
Участок присоединения липида к линкеру может выбираться соответствующим образом согласно типам используемых липидов и линкеров. Например, если в качестве липида используется жирная кислота, то ее можно присоединять посредством сложноэфирной связи, амидной связи или подобной связи, образуемой между карбоксильной группой жирной кислоты и линкером. Более конкретно, если в качестве липида используется жирная кислота, то липид предпочтительно присоединен посредством замены -OH карбоксильной группы жирной кислоты линкером.
Линкер выбирают подходящим образом согласно типу присоединяемого липида. Если в качестве липида используется жирная кислота, то предпочтительно использовать линкеры, представленные формулой (L-4).
В дополнение к указанным выше линкерам также применимы другие линкеры. Вследствие этого примеры включают линкеры двойного действия (линкеры, содержащие 2 функциональные группы), такие как N-сукцинимидил-3-(2-пиридилдитио)-пропионат, N-4-малеинимид масляной кислоты, S-(2-пиридилдитио)-цистамин, йодоацетоксисукцинимид, N-(4-малеинимидбутилокси)-сукцинимид, N-[5-(3'-малеинимидпропиламид)-1-карбоксипентил]-иминодиуксусная кислота, N-(5-аминопентил)-иминодиуксусная кислота и т.п. В смысловой цепи, нуклеотид, присоединенный к липиду или к линкеру, используемому для присоединения липида, не определен строго при условии, что это, по меньшей мере, один из первых шести нуклеотидов 5'-конца смысловой цепи, предпочтительно - по меньшей мере, один из первых четырех нуклеотидов 5'-конца, более предпочтительно первый и/или второй нуклеотиды 5'-конца, и особенно предпочтительно нуклеотид на 5'-конце (первый нуклеотид 5'-конца).
Участок присоединения смысловой цепи к липиду или к линкеру, используемому для присоединения липида, не определен строго. Предпочтительно она присоединена посредством замены атома водорода в гидроксильной группе остатка фосфорной кислоты специфического нуклеотида смысловой цепи.
Количество липидов, присоединяемых модифицированной липидом двухцепочечной РНК по изобретению, не определено строго. Например, можно присоединять от одного до трех липидов, предпочтительно один или два липида, и более предпочтительно один липид.
Модифицированную липидом двухцепочечную РНК по изобретению можно получать синтезом смысловой цепи, имеющей дополнительно, по меньшей мере, один присоединенный липид, и антисмысловой цепи соответственно, и гибридизацией смысловой и антисмысловой цепей согласно известным способам. Смысловую цепь, имеющую дополнительно присоединенный липид, также можно получать согласно известным способам синтеза.
Модифицированная двухцепочечная РНК по изобретению может вводиться внутрь клеток для ингибирования или ослабления экспрессии гена-мишени, и таким образом может использоваться в качестве фармацевтического препарата для ингибирования или ослабления экспрессии гена-мишени или композиции для генной терапии, т.е., фармацевтической композиции. Фармацевтическая композиция по изобретению может выпускаться в составе различных лекарственных форм. Примеры лекарственных форм фармацевтической композиции по изобретению включают жидкие препараты, такие как жидкости (такие как сиропы), капли, и инъекционные препараты; твердые препараты, такие как таблетки, пилюли, порошки, гранулы и капсулы (такие как мягкие капсулы); и т.п. Если фармацевтическая композиция по изобретению представляет собой жидкий препарат, то композиция может замораживаться или сохраняться после удаления из него воды посредством лиофилизации и т.д. Лиофилизированные препараты и сухие сиропы и т.д. можно применять в виде растворов после добавления в момент применения дистиллированной воды для инъекций, стерильной воды или т.п. Если фармацевтическая композиция по изобретению представляет собой твердый препарат, то композицию можно использовать в виде раствора после добавления в момент применения дистиллированной воды для инъекций, стерильной воды или т.п.
фармацевтическая композиция может состоять только из модифицированной липидом двухцепочечной РНК, или при необходимости может также содержать приемлемый фармацевтический носитель. Используемый носитель не определен строго при условии, что он не нарушает ингибирующее влияние модифицированной двухцепочечной РНК по изобретению на экспрессию гена-мишени, и может выбираться подходящим образом соответственно дозировке. Примеры возможных носителей включают очищенную воду, водные растворы сахаров, буферы, физиологический раствор, водные растворы полимеров, вода, очищенная от РНКазы, и т.д. Если фармацевтическая композиция по изобретению содержит носитель, то пропорции этих компонентов в композиции не определены строго при условии, что они не нарушают ингибирующее и ослабляющее влияние модифицированной двухцепочечной РНК по изобретению на экспрессию гена-мишени, и могут выбираться подходящим образом соответственно дозировке.
Например, фармацевтическая композиция по изобретению может содержать модифицированную двухцепочечную РНК в количестве от 0,001 до 50, более предпочтительно от 0,01 до 10, и еще более предпочтительно от 0,1 до 1. фармацевтическая композиция по изобретению может содержать носитель в количестве от 50 до 99,999 масс.%, предпочтительно от 90 до 99,99 масс.%, и еще более предпочтительно от 99 до 99,9 масс.% от общей массы композиции.
Ген-мишень и заболевание, в отношении которых применяют фармацевтическую композицию по изобретению, не определены строго. Известна взаимосвязь между геном-мишенью и заболеванием. Тип клетки, внутрь которой вводят фармацевтическую композицию по изобретению, не ограничен. Используемая клетка может быть человеческой или не принадлежащей человеку животной клеткой. Фармацевтическую композицию по изобретению можно использовать in vitro или in vivo.
Количество и способ введения модифицированной липидом двухцепочечной РНК по изобретению внутрь клеток такие же, как в обычном способе миРНК. Например, если фармацевтическая композиция по изобретению используется для введения модифицированной липидом двухцепочечной РНК внутрь клеток in vitro, то можно использовать способ культивирования клеток в присутствии соответствующего количества фармацевтической композиции. Если фармацевтическая композиция по изобретению используется для введения модифицированной липидом двухцепочечной РНК внутрь культивируемых клеток или клеток, выделенных из живого организма in vitro, то модифицированная липидом двухцепочечная РНК по изобретению может вводиться в присутствии сыворотки. Если фармацевтическая композиция по изобретению используется для введения модифицированной липидом двухцепочечной РНК внутрь клеток in vivo, то можно использовать непосредственную инъекцию фармацевтической композиции внутрь ткани; внутривенную, подкожную, мышечную, внутрибрюшинную, внутриглазную, желудочно-кишечную или зубную инъекцию; ингаляционное введение внутрь носовой полости, ротовой полости, легких или т.п.; пероральное введение; трансдермальное введение через кожу; трансмукозальное введение через слизистую ротовой полости, слизистую влагалища, слизистую глаза, слизистую прямой кишки и слизистую матки; и т.п. способы.
Если используется фармацевтическая композиция по изобретению, то вместе с ней может необязательно использоваться известное средство для генетической трансфекции, применяемое для трансфекции миРНК внутрь клеток. Альтернативно, фармацевтическая композиция по изобретению может содержать средство для генетической трансфекции. Модифицированная липидом двухцепочечная РНК, содержащаяся в фармацевтической композиции по изобретению, даже в случае самостоятельного использования имеет превосходную способность к трансфекции клеток. Таким образом, модифицированная липидом двухцепочечная РНК может вводиться внутрь клеток без помощи известного средства для генетической трансфекции, используемого для трансфекции миРНК внутрь клеток, или при помощи сниженного количества средства для генетической трансфекции.
Можно использ