Магнитная наночастица для лечения и/или профилактики рака, на ее основе инфузионный раствор и фармацевтическая композиция
Иллюстрации
Показать всеГруппа изобретений относится к медицине и касается магнитных наночастиц для лечения и/или профилактики рака, выполненных из оксидов железа или чистого железа, содержащего оксидный слой, где по меньшей мере одно терапевтически активное вещество связано с указанными частицами. При этом высвобождение по меньшей мере одного терапевтически активного вещества вызывается или инициируется, или существенно ускоряется переменным магнитным полем. Группа изобретений обеспечивает уменьшение неконтролируемого высвобождения терапевтически активных веществ во время транспортировки наночастиц к раковым клеткам. 3 н. и 10 з.п. ф-лы. 11 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к наночастицам, к которым присоединены терапевтически активные вещества, при этом высвобождение терапевтически активных веществ вызывается, инициируется или существенно усиливается при воздействии переменного магнитного поля.
Уровень техники
Известно, что суперпарамагнитные наночастицы могут использоваться в качестве наполнителей при лечении заболеваний. В данном контексте применяются различные подходы. Одна из известных стратегий, например, основана на так называемой "магнитной доставке лекарств", при которой предпринимаются попытки получить локальное повышение концентрации активного ингредиента посредством магнитного поля (DE 10059151 А, Alexiou). Сходным образом, предпринимаются попытки химически придать частицам свойства нахождения мишени для получения эффекта аккумулирования упомянутых частиц в определенных частях тела (DE 4428851 А1, ЕР 0516252 А2). В патенте WO 98/58673 (INM) описаны многооболочечные частицы для проникновения в опухолевые клетки, где конъюгаты состоят из частицы и активного ингредиента.
Раскрытие изобретения
Целью настоящего изобретения является присоединение к наночастицам терапевтически активных веществ таким образом, что в здоровых тканях не наблюдается заметного высвобождения терапевтически активных соединений, а при проникновении наночастиц в опухолевую ткань или опухолевые клетки может происходить контролируемое высвобождение терапевтически активных соединений.
Указанная цель достигается с помощью наночастиц по пункту 1 формулы изобретения, а также с помощью фармацевтической композиции по пункту 11 и с помощью упомянутых наночастиц по пункту 12.
Другие предпочтительные варианты следуют из зависимых пунктов формулы изобретения, примеров и описания.
Настоящее изобретение относится к наночастицам, в которых терапевтически активные вещества присоединены к упомянутым наночастицам и в которых отделение терапевтически активных веществ от упомянутых наночастиц вызывается, инициируется или существенно усиливается под воздействием переменного магнитного поля. В этом контексте, по меньшей мере одно терапевтически активное вещество высвобождается посредством прямого воздействия переменного магнитного поля или вследствие локального нагрева, вызываемого переменным магнитным полем. Предпочтительно, высвобождение вызывается тем фактом, что термически лабильный линкер между активным ингредиентом, например терапевтически активным веществом и наночастицей расщепляется термически и/или тем, что используемый линкер лабилен по отношению к переменному магнитному полю. Поэтому, настоящее изобретение заключается в связывании терапевтически активного вещества, в частности цитостатика, с наночастицей посредством линкера, который может расщепляться термически и/или посредством магнитного поля.
Наночастицы в соответствии с настоящим изобретением характеризуются тем, что по меньшей мере одно терапевтически активное вещество связано с наночастицей, при этом отделение по меньшей мере одного терапевтически активного вещества от наночастицы вызывается или инициируется или существенно усиливается переменным магнитным полем.
Другими словами, настоящее изобретение относится к наночастицам, в которых по меньшей мере одно терапевтически активное вещество связано ковалентно или ионно, или связано посредством водородных связей, или посредством комплексообразования (комплексная связь), или посредством внедрения, или посредством липофильных взаимодействий через линкер, и этот линкер может расщепляться вследствие термической инициации или инициации электромагнитным или соответственно магнитным полем.
Термически инициируемое расщепление означает, что локальный нагрев в физиологических условиях до температуры более 45°С, предпочтительно более 50°С, достаточен для расщепления линкера. Инициируемое электромагнитным или соответственно магнитным полем расщепление означает, что применение электромагнитного или соответственно магнитного поля при физиологических условиях вызывает расщепление линкера, или только посредством электромагнитного или соответственно магнитного поля, или/и посредством локального уменьшения рН, индуцированного электромагнитным или соответственно магнитным полем.
По меньшей мере одно терапевтически активное вещество, то есть молекулы по меньшей мере одного класса терапевтически активных веществ или один определенный активный ингредиент, предпочтительно связывается посредством ковалентной или преимущественно ковалентной связи и/или достаточно прочной ионной связи, клатратных соединений или комплексообразования (комплексные связи) или соответственно посредством установления достаточного количества водородных связей или гидрофобных взаимодействий таким образом, чтобы с достаточной степенью надежности избежать неконтролируемого высвобождения терапевтически активного вещества. Неконтролируемое выделение означает высвобождение терапевтически активных веществ в здоровых тканях, особенно, высвобождение без активного воздействия переменного магнитного поля.
Такое неконтролируемое высвобождение приводит к высвобождению терапевтически активных веществ в местах, где они могут скорее вызвать нежелательные побочные эффекты нежели терапевтические эффекты, а именно вне раковых тканей или соответственно вне раковых клеток.
Таким образом, терапевтически активные вещества остаются крепко связанными с наночастицами и транспортируются к раковым клеткам вместе с наночастицей. Во время транспортировки наночастиц к раковым тканям высвобождаются количества терапевтически активных веществ от небольших до незначительных. После доставки в раковые клетки терапевтически активные вещества высвобождаются посредством переменного магнитного поля, в частности посредством внешнего переменного магнитного поля или, соответственно, посредством переменного магнитного поля, применяемого извне (импульс).
В данном контексте, "вызванный или инициированный переменным магнитным полем" означает, что высвобождение или соответственно отделение либо непосредственно вызывается переменным магнитным полем либо соответственно импульсами, либо непрямым образом, например активацией или соответственно индуцированием генной экспрессии энзимов или генерацией тепла.
Наночастицы состоят из магнитного материала, предпочтительно ферромагнитного, антиферромагнитного, ферримагнитного, антиферримагнитного или суперпарамагнитного материала, более предпочтительно из оксидов железа, особенно суперпарамагнитных оксидов железа или из чистого железа с оксидным слоем. Такие наночастицы могут нагреваться переменным магнитным полем. Ткань, содержащую такие наночастицы, можно нагреть до температур выше 50°С. Такие высокие температуры могут достигаться благодаря тому, что до 800 пг железа и более может адсорбироваться в форме наночастиц одной раковой клеткой.
Наночастицы предпочтительно состоят из оксидов железа и в частности из магнетита (Fе3О4), магхемита (γ-Fе2О3) или смесей двух указанных оксидов. В целом, предпочтительные наночастицы представлены формулой FeOx, где Х означает число от 1 до 2. Наночастицы предпочтительно имеют диаметр менее 500 нм. Наночастицы предпочтительно имеют средний диаметр 15 нм и лежат в пределах от 1 до 100 нм, особенно предпочтительно, в диапазоне от 10 до 20 нм.
В дополнение к магнитным материалам формулы FeOx, где Х означает число от 1 до 2, в соответствии с настоящим изобретением могут использоваться материалы общей формулы МFе2О4, где М=Со, Ni, Mn, Zn, Cd, Ba или другие ферриты. Более того, могут применяться также кремниевые или полимерные частицы, в которые включены и/или с которыми связаны магнитные материалы, такие как упомянутые в тексте магнитные материалы.
Терапевтически активные вещества присоединяются к описанным наночастицам, в частности, к суперпарамагнитным наночастицам, при этом предпочтительной является ковалентная связь. Выбираемые терапевтически активные вещества включают антипролиферативные, антимиграционные, антиангиогенные,противотромбозные, противовоспалительные,цитостатики, цитотоксические, антикоагуляционные, антибактериальные, антивирусные и/или противогрибковые препараты, где предпочтительными являются антипролиферативные, антимиграционные, антиангиогенные, цитостатические и/или цитотоксические вещества, а также нуклеиновые кислоты, аминокислоты, пептиды, белки, углеводы, жиры, гликопротеины, гликаны или липопротеины имеющие антипролиферативные, антимиграционные, анти-ангиогенные, противотромбозные, противовоспалительные, цитостатические, цитотоксические, антикоагуляционные, антибактериальные, антивирусные и/или противогрибковые свойства. Более того, такие вещества могут также представлять собой радиосенсибилизаторы или сенсибилизаторы или усилители других комбинированных общепринятых способов лечения рака, либо могут содержать такие сенсибилизаторы.
В качестве цитотоксических и/или цитостатических соединений, то есть химических соединений имеющих цитотоксические и/или цитостатические свойства, могут использоваться следующие: алкилирующие агенты, антибиотики с цитостатическими свойствами, антиметаболиты, ингибиторы микроканальцев и ингибиторы топоизомеразы, соединения содержащие платину и другие цитостатики, такие как например аспарагиназа, третиноин, алкалоиды, подофиллотоксины, таксаны и милтефозин®, гормоны, иммуномодуляторы, моноклональные антитела, сигнальные трансдукторы (молекулы для трансдукции сигнала) и цитокины.
Примеры алкилирующих агентов включают, помимо прочих, хлорэтамин, циклофосфамид, трофосфамид, ифосфамид, мелфалан, хлорамбуцил, бусульфан, тиотепа, кармустин, ломустин, дакарбазин, прокарбазин, темозолумид, треосульфан, эстрамустин и нимустин.
Примеры антибиотиков с цитостатическими свойствами включают даунорубицин, доксорубицин (адриамицин), дактиномицин, митомицин С, блеомицин, эпирубицин (4-эпиадриамицин), идарубицин, митоксантрон, амсакрин и актиномицин D.
Метотрексат, 5-фторурацил, 6-тиогуанин, 6-меркаптопурин, флударубин, кладрибин, пентостатин, гемцитабин, цитарабин, азатиоприн, ралтитрексед, капецитабин, цитозин арабинозид, тиогуанин и меркаптопурин можно привести в качестве примеров антиметаболитов (антиметаболических агентов).
Винкристин, винбластин, виндезин, этопозид, а также тенипозид принадлежат, в числе прочих, к классу алкалоидов и подофиллотоксинов. Платиносодержащие соединения также могут использоваться в соответствии с настоящим изобретением. Цисплатин, карбоплатин и оксалиплатин являются примерами платиносодержащих соединений. К ингибиторам микроканальцев относятся, например, такие алкалоиды как алкалоиды барвинка (винкристин, винбластин, виндезин, винорелбин) и паклитаксел (Тахоl®), а также производные паклитаксела. Примеры ингибиторов топоизомеразы включают этопозид, тенипозид, камптотецин, топотекан и иринотекан.
Паклитаксел и доцетаксел являются примерами соединений класса таксанов, а в числе других цитостатических соединений (другие цитостатики) находятся, например, гидроксикарбамид (гидроксимочевина), иматиниб, Miltefosin®, амсакрин, топотекан (ингибитор изомеразы-1), пентостатин, бексаротен, биолимусА9, рапамицин (сиролимус), родомицин D, аметантрон, бендамустин, оксазафосфорин, 5'-деокси-5-фторуридин, 9-аминокамптотецин, производные подофиллотоксина, митоподозид, алкалоиды барвинка, калихеамицины, майтанзиноиды, третиноин и аспарагиназа. Представителями соединений класса моноклональных антител являются, в числе прочих, трастузумаб (также известный как Herceptin®), алемтузумаб (также известный как MabCampath®) и ритуксимаб (также известный как MabThera®).
В соответствии с настоящим изобретением могут также использоваться гормоны, такие как, например, глюкокортикоиды (преднизон), эстрогены (фосфестрол, эстрамустин), LHRH (бусерелин, госерелин, лейпрорелин, трипторелин), флутамид, ципротерона ацетат, тамоксифен, торемифен, аминоглутетимид, форместан, экземестан, летрозол и анастрозол. Среди классов иммуномодуляторов, цитокинов, антител и трансдукторов сигнала присутствуют интерлейкин-2, интерферон-(, эритропоетин, G-CSF, трастузумаб (Herceptin®), ритуксимаб (MabThera®), гефитиниб (Iressa®), ибритумомаб (Zevalin®), левамизол, а также ретиноиды.
Вышеупомянутые соединения предпочтительно связаны с наночастицами ковалентно. Например, вещества могут связываться через гидроксильные группы, аминогруппы, карбонильные группы, тиольные группы или карбоксильные группы, в зависимости от того, какие функциональные группы несет соответствующее вещество. Так, например, доксорубицин может связываться через свои первичные гидроксильные группы в форме сложного эфира; платиновые производные (цисплатин, карбоплатин, оксаплатин, и т.д.) могут присоединяться к аминогруппе посредством нуклеофильного замещения у платины; или паклитаксел может связываться через иминную связь.
Гидроксильные группы предпочтительно связываются в виде сложных эфиров, ацеталей или кеталей; тиогруппы предпочтительно связываются как тиоэфиры, тиоацетали или тиокетали; аминогруппы предпочтительно связываются как амиды и частично в виде иминов (оснований Шиффа) или в качестве уретанов в ходе реакции с изоцианатной группой; карбоксильные группы предпочтительно связываются в качестве сложных эфиров или амидов и карбонильные группы предпочтительно связываются в виде ацеталей или соответственно кеталей.
Приготовление наночастиц без активного ингредиента и без оболочки детально описано в DE 4428851 А. Более того, известна функционализация поверхности наночастиц, так что аминогруппы, гидроксильные группы, карбоксильные группы или карбонильные группы могут образовываться на поверхности наночастиц по известным методикам.
Поэтому настоящее изобретение относится к наночастицам, имеющим множество аминогрупп, гидроксильных групп, карбоксильных групп или карбонильных групп на их поверхностях, и где линкеры связаны с по меньшей мере одной частью из упомянутых функциональных групп посредством иминной связи, аминной связи, сложноэфирной связи, амидной связи или кетальной связи. Кроме того, перечисленные линкеры связывают терапевтически активное вещество ковалентным, ионным, комплексным, липофильным путем или посредством водородных связей.
Отличительной особенностью предпочтительного варианта наночастиц настоящего изобретения является связывание активных компонентов с магнитными наночастицами посредством связей специального типа. Упомянутые связи построены таким образом, что высвобождение активных ингредиентов может стимулироваться внешним магнитным полем (импульсом).
Переменное магнитное поле действует как внешний стимул, который в случае суперпарамагнитных частиц запускает различные процессы релаксации в молекуле. Среди прочих, эти процессы приводят к нагреванию частиц и их окружения. В соответствии с настоящим изобретением, упомянутые процессы, запускаемые переменным магнитным полем, используются для расщепления связи между наночастицей и терапевтически активным веществом или для значительного ускорения процесса расщепления. В данном контексте, скорость расщепления посредством биологических процессов (например энзиматическое расщепление) может сильно ускоряться импульсом, поэтому увеличение концентрации активного ингредиента в месте назначения может достигаться только посредством использования импульса. Сходным образом, связь может быть построена таким образом, что запускается или значительно ускоряется расщепление посредством химических реакций (например гидролиз). Более того, индуцированное магнитным полем нагревание может вызывать расплавление молекулы нуклеиновой кислоты или полипетидной молекулы, используемых в качестве линкера.
Терапевтически активные соединения связываются непосредственно или через линкерные молекулы. Линкерные молекулы предпочтительно связываются с наночастицами или соответствующей наночастицей посредством амидной связи или эфирной связи.
В соответствии с настоящим изобретением возможно также использование в качестве линкеров нуклеиновых кислот (дезоксирибонуклеиновая кислота (ДНК), рибонуклеиновая кислота (РНК)) или полипетидов различной длины. Необходимые молекулы могут производиться либо генетически, либо синтетически. Линкеры могут расщепляться термически индуцируемым, магнитно индуцируемым или кислотно индуцируемым образом при физиологических условиях.
Расщепление линкера означает, что линкер содержит в своем составе по меньшей мере одну связь, которая может расщепляться в физиологических условиях вследствие воздействия тепла, влияния магнитного поля, то есть магнитного импульса или вследствие воздействия кислоты. Вследствие воздействия тепла (предпочтительно по меньшей мере 45°С) и/или влияния магнитного поля и/или вследствие воздействия кислоты вышеуказанная связь должна расщепляться в физиологических условиях по меньшей мере в два раза быстрее, чем в случае отсутствия воздействия. Образование кислоты и локальное понижение рН может, например, вызываться уже мертвыми клетками. Выражение "связь в составе линкера" также включает связь между линкером и наночастицей, а также связь между линкером и терапевтически активным веществом. Кроме того, линкер может состоять из двух или трех линкерных молекул.
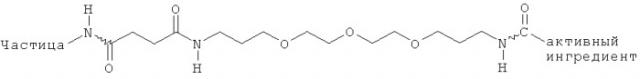
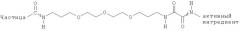
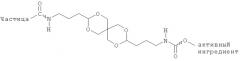
Для обеспечения необходимой способности к расщеплению, линкеры имеют по меньшей мере одну из следующих функциональных групп: -S-S-, -O-Р(=O)(O-)-O-, -СО-СО-, -NH-CO-CO-NH-, -С=N-С, кетали, -CO-NH-N=C-, триоксисиланы (-O-)(-O-)(-O-)Si-C или ацетали.
Например, подходящие линкеры могут иметь следующую форму:
Зигзагообразная линия означает связь между активным ингредиентом и линкером или соответственно, между линкером и наночастицей.
Предпочтительные нуклеиновые кислоты представляют собой конструкции, предпочтительно дважды скрученные конструкции, имеющие температуру плавления в диапазоне от 40 до 60°С. Когда используются дважды скрученные ДНК, РНК или ПНК, одна цепочка содержит группу, способную к связыванию с частицей (например, амино- или карбоксиотная группа, связанная с фосфорамидатной группой). Комплементарная цепочка может, например, содержать активный компонент, который также связан посредством ковалентной связи. Вследствие основного попарногосвязывания между цепочками, активный компонент также связывается с частицей. Высвобождение активного компонента возможно только в случае расплавления двойной спирали вследствие генерации тепла в переменном магнитном поле. В этом процессе отдельные цепочки разделяются, и активный компонент отщепляется от частицы. И температура плавления, и разрушение линкера могут контролироваться выбором соответствующих гомо-гибридов или гетеро-гибридов из ДНК-ДНК, ДНК-РНК, ДНК-ПНК, РНК-РНК, РНК-ПНКили ПНК-ПНК.
Предпочтительными полипептидами являются такие молекулы, которые имеют тенденцию к формированию определенных гомо-димеров или гетеро-димеров, особенно посредством водородных связей (такие как, например, между иммуноглобулиновыми доменами) или посредством гидрофобных взаимодействий (как например, в так называемых лейциновых зипперах). В оговоренных случаях тоже используются такие пары с температурой плавления в диапазоне от 40 до 60°С, которые поэтому в физиологических условиях присутствуют преимущественно в спаренном состоянии, но которые не распадаются на свои мономеры при терапевтически достижимых температурах. Для указанных целей один связующий член ковалентно связан с наночастицей, а второй ковалентно связан с терапевтически активным веществом. Когда связь между двумя пептидными цепочками ослабляется, наночастицы отделяются и терапевтически активные вещества, которые впоследствии, возможно только вследствие расщепления такого как энзиматическое расщепление, присутствуют в свободно диффундирующей форме.
Сходным образом, в соответствующем линкере могут использоваться взаимодействия между полипептидом и нуклеиновой кислотой. Для достижения указанной цели, с наночастицами связываются полипептиды, взаимодействующие с нуклеиновыми кислотами нековалентным образом и способные к связыванию с нуклеиновыми кислотами. Указанные взаимодействия также могут ослабляться под воздействием тепла, так что связывающая нуклеиновая кислота высвобождается вдополнение ксвязанной эффекторной молекуле. Иногда даже выделяющаяся нуклеиновая кислота сама может играть роль эффекторной молекулы (например, siRNA, антисмысловая ДНК, и т.д.). Подходящими нуклеиновыми кислотами, связывающими полипептиды, могут быть в частности цинковые пальцы, имеющие длину от 20 до 50 аминокислот, но также могут использоваться часто повторяющиеся элементы типа "спираль-поворот-спираль" ДНК-связывающих доменов или SSB-белки для связывания ДНК (маленький протеин, имеющий ДНК-связывающий домен размером около 100 аминокислот), или соответственно "РНК-распознающий элемент" (RRM или соответственно RNP-1) одноцепочечных РНК-связывающих протеинов (насчитывает около 90 аминокислот), или "связующий элемент двухцепочечных РНК" (DRBM) двухцепочечных РНК-связывающих протеинов (насчитывает около 65 аминокислот).
Другой вариант осуществления изобретения заключается в использовании в линкерной системе связи низкомолекулярных лигандов нуклеиновых кислот (аптамеров) или соответственно протеинов. В общем, могут использоваться все молекулы, например путем продуцирования антител против так называемого "гаптена" (например, часто используются антитела против динитрофенола, тринитрофенола, дигоксигенина, дигоксина, биотина). В частности, могут применяться связующие участки биомолекул, таких как коэнзимы (например коэнзим А, АТР, GTP, FAD, NADH, NADPH, биотин, фолиевая кислота, пиридоксал фосфат, и т.д.), субстраты (например, связывающий сайт глутатиона глутатион-3-трансферазы GST, состоящий из 73 аминокислот) или гормоны (например, гормон-связывающий домен ядерного гормонального рецептора андрогенов, эстрогенов, ретиноевая кислота, тироксина, витамина D3, насчитывающий от 218 до 252 аминокислот). Одно из наиболее часто использующихся взаимодействий и одновременно самое сильное из известных нековалентное связывание - это связывание биотина с авидином или соответственно стрептавидином. Вследствие высокой связующей способности, возможно предпочтительно использовать модифицированные аналоги авидина или соответственно биотина (например, дестиобиотин или иминобиотин) с менее сильными связями, для обеспечения плавления в технически достижимом интервале температур. Во всех случаях имеет смысл связывать микромолекулярный лиганд с эффекторной молекулой и связывать макромолекулярный лиганд с наночастицей; однако, обратный порядок также может быть более выгодным, в зависимости от выбора лиганда.
В этом предпочтительном варианте рассматриваются только связывающие способы, посредством которых образуется связь между наночастицей и активным компонентом, где указанная связь достаточно устойчива при "нормальных" физиологических условиях, но значительно менее устойчива, когда используются условия импульса в соответствии с настоящим изобретением. Механизм высвобождения сам по себе и также тип связи зависят от мишени (например, опухоль в случае раковых заболеваний) и должны быть вариабельны посредством обычных способов химического связывания. Сходным образом, выделение может происходить внутриклеточно (например, в клетках опухоли) или внеклеточно. Произведенные в соответствии с настоящим изобретением наночастицы отличаются от известных носителей активных компонентов тем, что эффективность может быть достигнута только посредством активации в переменном магнитном поле, в то время как без указанного импульса активный компонент остается по большей части в неактивном состоянии.
В соответствии с настоящим изобретением, конъюгаты наночастицы и активного компонента предпочтительно основаны на железосодержащих магнитных ядрах; упомянутые ядра окружены одним или более коллоидными оболочками или покрытиями, которые позволяют активным ингредиентам связываться с ними через функциональные группы. Ядро предпочтительно состоит из магнетита или магемита. Главная функция таких оболочек состоит в обеспечении коллоидного распределения в водной среде и в защите наночастиц от агломерации. В принципе, частицы с несколькими оболочками, как описано в WO 98/58673, представляют собой подходящую основу для конъюгатов наночастицы с активным компонентом, которые могут быть активированы, поскольку биологическое поведение таких частиц можно адаптировать посредством покрытия полимерами и поскольку активные компоненты можно связать с функциональными группами первичной оболочки.
Активные компоненты можно связывать с первичными оболочками с использованием различных методов. В случае если ядро частицы стабилизировано аминосиланами или оболочкой или соответственно несущим аминогруппы покрытием, активные компоненты можно, например, связать с аминогруппой, расположенной близко к поверхности. В этом контексте, связывание можно провести через, например, сукцинимидиловые эфиры, сульфосукцинимидиловые эфиры, изотиоцианаты, триазинилхлориды, сульфонилхлориды, тетрафторфениловые эфиры или через альдегидные группы. Для этой цели, активный компонент должен быть способен к связыванию с такими группами химическим способом. Если активный компонент не может быть непосредственно связан с использованием упомянутых способов, можно использовать линкерную молекулу. Указанный "линкер" соединяет активный компонент с функциональными группами защитной оболочки и таким образом увеличивает вариабельность в плане различных возможностей соединения. Поэтому предпочтительным является использование линкера, содержащего группу, которая является термолабильной, электромагнитно-лабильной, фотолабильной, кислотно-лабильной, интеркалирована или может интеркалироваться или расщепляться посредством энзиматического расщепления. Более того, механизм высвобождения может также контролироваться посредством линкера. Так, линкер также может вводить группы, позволяющие отсоединить активный компонент.Подходящие группы включают, например, расщепляемые ацетали, сложные эфиры, гидразоннные или иминные группы. Сходным образом, пептидные последовательности могут использоваться как линкеры, в которых активный компонент выделяется только после энзиматического расщепления или вследствие расплавления нековалентной связи. Более того, ДНК, РНК и ПНК молекулы могут использоваться предпочтительно в качестве двухцепочечных линкеров, где высвобождение происходит вследствие термически индуцируемого разрушения двойной цепочки.
В соответствии с настоящим изобретением, могут использоваться только такие линкеры, которые не претерпевают никакого расщепления при нормальных физиологических условиях или скорость такого расщепления очень мала. Например, линкерные молекулы могут быть построены таким образом, что даже если высвобождение в целевой зоне возможно (например, энзиматическое расщепление в клетках опухоли), то указанное высвобождение настолько медленно при нормальных условиях, что достижение терапевтической концентрации активного компонента невозможно. Расщепление линкерной молекулы или соответственно расщепление линкерной молекулы с достаточно большой скоростью является исключительно следствием импульса переменного магнитного поля извне, приводящее к активации активного компонента. Предпочтительно эта цель достигается вследствие того факта, что конформация, допускающая энзиматическое расщепление линкера, возникает только когда происходит термически индуцируемое разрушение двойной цепочки нуклеиновых кислот или соответственно множественных цепочек, или альтернативно расщепление пептидных димеров или соответственно пептидных олигомеров.
Частицы, стабилизированные различными функциональными группами (например, карбокси, эпокси, альдегидными), могут обрабатываться теми же способами, что и частицы, стабилизированные аминосиланами. Определяющим при выборе способа связывания является то, что высвобождение должно происходить только при указанных выше условиях. Сходным об разом, активный компонент может связываться с ал коксисиланом, который был функционализирован посредством вышеупомянутых групп (смотри пример 1), где на следующей стадии упомянутый конъюгат связывается с защитной оболочкой частиц, которые уже были стабилизированы силанами. Связывание не ограничивается только ковалентными связями. Всоответствии с настоящим изобретением, возможно также создавать ионные взаимодействия с достаточной устойчивостью.
Дополнительное покрытие (например, полимерами) конъюгатов наночастиц с активным компонентом, который может быть активирован как описано в патенте WO 98/58673, также возможно и может использоваться для улучшения биологических свойств конъюгатов наночастиц с активным компонентом. Сходным образом, могут связываться другие молекулы, придающие всей конструкции способность находить мишень (например, поликлональные антитела, моноклональные антитела, гуманизированные антитела, антитела человека, химерные антитела, рекомбинантные антитела, биспецифичные антитела, фрагменты антител, аптамеры, фрагменты Fab, фрагменты Fc, пептиды, пептидомиметики, гап-меры, рибозимы, CpG олигомеры, ДНК-зимы, рибо-переключатели или липиды). Для достижения этой цели, дополнительные модификации не должны оказывать влияние на процесс высвобождения (который может активироваться) активного компонента в целевой зоне.
Таким образом, различные молекулы, имеющие до 500 углеродных атомов или от 10 до 30 пар оснований, предпочтительно 15-25 пар оснований или 10-30 аминокислот, предпочтительно от 15 до 25 аминокислот, могут выполнять роль линкеров, при условии что линкер содержит группу, которая может расщепляться термически, фотохимически или энзиматически, кислотно-лабильную группу или любую другую группу, которую можно легко отщепить. Поэтому связь в составе линкерной молекулы и/или связь между линкером и активным компонентом и/или связь между линкером и поверхностью наночастицы должна быть легко расщепляема непосредственно под воздействием переменного магнитного поля или расщепляема опосредованно. Опосоредованное расщепление означает, что энзимы, такие как пептидазы, эстеразы или гидролазы, переходят в возбужденное состояние в районе мишени, например в раковых клетках, например посредством переменного магнитного поля или что их активность или действие увеличивается и упомянутые энзимы получают способность к вышеупомянутому расщеплению. Кроме того, опосредованное расщепление может происходить когда используются магнитные наночастицы, если эти частицы нагреваются переменным магнитным полем, что приводит к расщеплению термически лабильных связей. Также стоит рассмотреть увеличение рН в целевой зоне под воздействием переменного магнитного поля и последующее расщепление кислотно-лабильных связей в составе линкерной молекулы.
Сложноэфирная группа и амидная или соответственно пептидная группа входят в число энзиматически расщепляемых групп в составе линкерной молекулы или непосредственно около нее. Группы, которые могут расщепляться термически или посредством кислоты, включают например фосфатные группы, тиофосфатные группы, сульфатные группы, фосфамидные группы, карбаматные группы или иминные группы.
Активный компонент необязательно должен быть ковалентно связан с линкером; вместо этого он также может быть связан ионно или через водородные связи, или может присутствовать в интеркалированной или комплексной форме.
Более того, можно также связать активные компоненты с поверхностью наночастиц адсорбционно и покрыть их барьерным слоем, так чтобы с большой степенью вероятности предотвратить высвобождение активного компонента до тех пор пока барьерный слой модифицируется, в частности разрушается, под воздействием переменного магнитного поля таким образом, что становится возможным выделение активного компонента.
В другом предпочтительном варианте, наночастицы, соответствующие настоящему изобретению окружены или соответственно покрыты одной или более оболочками или покрытиями. Упомянутые оболочки или покрытия могут иметь одну или более функций и могут выступать в роли защитной оболочки, барьерного слоя или клеточно-селективного покрытия.
В случае если связь терапевтически активного вещества с наночастицей слабая, например в случае нековалентной, ионной, адсорбционной, липофильной и/или ван-дер-Ваальсовой связи и/или присоединения посредством водородных связей, защитная оболочка или барьерное покрытие могут предотвращать выделение терапевтически активных веществ до тех пор, пока наночастицы не достигнут своего места назначения. Внешний слой, несущий клеточно-специфичные функциональности, может наноситься на защитную оболочку или барьерное покрытие вместо указанных защитных оболочек или барьерных покрытий или как дополнительный слой к этим защитным оболочкам или барьерному покрытию.
Указанное клеточно-специфическое покрытие увеличивает сродство наночастиц к определенным клеткам, например к определенным бактериальным клеткам или к определенным раковым клеткам; вследствие этого, оно служит целям клеточной дискриминации. Такие клеточно-специфичные наночастицы предпочтительно аккумулируются в клетках, к которым у них имеется повышенное сродство благодаря функционализированной поверхности; вследствие этого, такие наночастицы становятся опухоле-специфичными. Благодаря такой технологии, можно разработать специфичные к опухолям наночастицы, например для определенных видов рака.
Кроме того, наночастицы также можно стабилизировать коллоидной защитной оболочкой, защищающей наночастицы от агломерации. Предпочтительно, такие защитные оболочки или покрытия обеспечиваются аминогруппами или карбоксильными группами. Для таких защитных оболочек или соответственно покрытий могут использоваться биологические, синтетические или полусинтетические полимеры. Для получения барьерного слоя обычно используются полимеры, предпочтительно биостабильные полимеры, например полимеры которые весьма устойчивы к биологической деградации. Для образования клеточно-специфических оболочек или соответственнопокрытийпредпочтительноиспользованиебиодеградируемых полимеров.
В качестве биологически стабильных полимеров могут использоваться следующие полимеры: полиакриловая кислота и полиакрилаты такие как полиметилметакрилат, полибутилметакрилат, полиакриламид, полиакрилонитрилы, полиамиды, полиэфирамиды, полиэтиленамин, полиимиды, поликарбонаты, поликарбоуретаны, поливинилкетоны, поливинилгалогениды, поливинилиденгалогениды, поливиниловые эфиры, полиизобутилены, ароматические поливинилы, поливиниловые эфиры, поливинил пирролидоны, полиоксиметилены, политетраметилен оксид, полиэтилен, полипропилен, политетрафторэтилен, полиуретаны, полиэфирные уретаны, силиконовые полиэфирные уретаны, силиконовые полиуретаны, силиконовые поликарбонатные уретаны, полиолефиновые эластомеры, EPDM резины, фторсиликоны, карбоксиметилхитозаны, полиарилэфирные эфиркетоны, полиэфирные эфиркетоны, полиэтилен терефталат, поливалераты, карбоксиметилцеллюлоза, целлюлоза, вискоза, триацетат вискозы, нитраты целлюлозы, ацетаты целлюлозы, гидрок