Глазные композиции на основе полисахарида семян тамаринда и гиалуроновой кислоты
Иллюстрации
Показать всеГруппа изобретений относится к области офтальмологии. Глазные препараты используют при глазных болезнях в качестве заменителей слез, они содержат комбинацию гиалуроновой кислоты и полисахарида, известного как TSP (полисахарид семян Tamarindus indica). Глазные препараты, предложенные для применения в лечении синдрома сухого глаза, содержат, в комбинации, от 0,05 до 2 масс.% полисахарида семян тамаринда (TSP) и от 0,05 до 1 масс.% гиалуроновой кислоты в водном растворе. Изобретение обеспечивает при введении в комбинации гиалуроновой кислоты и TSP, синергическое действие в стимуляции возврата к нормальному состоянию конъюнктивальной слизистой оболочки, пораженной синдромом сухого глаза, индуцируя посредством этого заметное улучшение в количестве и морфологии конъюнктивальных микроворсинок. 3 н. и 13 з.п. ф-лы, 12 табл., 6 ил.
Реферат
Изобретение относится к глазным композициям (композициям, используемым при глазных болезнях) на основе полисахарида семян тамаринда (индийского финика) и гиалуроновой кислоты. Более конкретно, это изобретение относится к глазным растворам, показанным для применения в качестве заменителей слез, содержащим комбинацию гиалуроновой кислоты и полисахарида, известного как TSP (полисахарид семян Tamarindus indica), которые способны, при введении вместе в комбинации, действовать синергически в стимуляции возврата к норме в конъюнктивальной слизистой оболочке, пораженной синдромом сухого глаза, индуцируя заметное улучшение в количестве и морфологии микроворсинок конъюнктивы.
Как известно, поверхность глаза поддерживается постоянно влажной присутствием предроговичной слезной пленки, которая является организованным жидким структурным покрытием конъюнктивы и обнаженной поверхности глазного яблока. Крайне важно, что эта структура является количественно и качественно пригодной для получения должной очистки и защиты. Кроме того, эта слезная пленка содержит вещества с высокой бактерицидной способностью, такие как лизоцим и антитела, которые защищают глаза от атаки многочисленных антигенов.
В нормальных состояниях, слезы, которые являются результатом ряда растворов, экскретируемых различными железами в конъюнктивальном мешке, размещаются слоями на поверхности роговицы и конъюнктивы движениями век, образуя таким образом комплексную трехслойную структуру, содержащую:
- внутренний слой слизи, состоящий из смеси гликопротеинов (муцина, слизистого секрета), продуцируемых специализированными клетками (т.е. конъюнктивальными бокаловидными клетками), которые присутствуют в конъюнктивальном эпителии - указанный слой адсорбируется на роговице, превращая посредством этого роговичный эпителий в гидрофильную поверхность: если муцин отсутствует, эти эпителиальные клетки являются гидрофобными и не могут гидратироваться слезами;
- толстый промежуточный водный слой (секретируемый основными и вспомогательными слезными железами), состоящий в основном из воды, электролитов, белков, ферментов и муцина; этот слой простирается на указанной гидрофильной поверхности и имеет функцию обеспечения атмосферного кислорода роговичному эпителию, проявляя антибактериальную активность и вымывание любых инородных веществ и остатков;
- тонкий наружный липидный слой (секретируемый сальными тарзальными пальпебральными железами или Мейбомиевыми железами), имеющий следующие функции: задержку испарения нижележащего водного слоя, увеличение поверхностного натяжения для стабилизации этой пленки во избежание ее ускользания на кожу и смазывание век.
Движение век выдавливает слизь из конъюнктивальных клеток и вводит ее в конъюнктивальные своды, и оттуда она однородно распределяется на всей поверхности роговицы мигающими движениями глаз.
Описанная выше трехслойная структура образует комплексную физиологическую систему, имеющую основные функции защиты поверхности глаз, поддержания гидратации, смазывания и очистки роговичной поверхности и содействия в получении нормального зрения. Точное равновесие и непрерывное восстановление указанной физиологической системы является необходимым условием для выполнения ею указанных функций. Для реализации указанных равновесия и восстановления должно происходить постоянное, но не избыточное испарение воды из глазной жидкости для поддержания ее осмолярности при физиологическом уровне приблизительно 300 мОсм/л, и слезная пленка должна непрерывно распределяться на роговичной поверхности в результате моргания.
Не только эта слоистая структура различных компонентов является важной, но также присутствующие в ней растворенные вещества являются важными. Липиды наружного слоя расположены в виде двойной фазы: полярной фазы, смежной с промежуточным слоем, и более густой фазы при поверхности раздела с воздухом. Водная фаза обнаруживает вместо этого фиксированные ионные концентрации: в основном натрий, калий, кальций, магний, цинк, хлор и бикарбонат являются важными для поддержания осмолярности слез.
Целостность внутреннего слоя муцина представляет целостность основных элементов поддержания стабильности слезной пленки. Это связано с тем, что муцин усиливает смачиваемость роговичной поверхности, позволяет этой водной пленке прикрепляться к обнаженной поверхности непрерывным и гомогенным образом, защищая ее стабильность, и увеличивает вязкость слезной жидкости, препятствуя ее слишком быстрому вытеканию из конъюнктивального мешка. Как уже отмечалось, при отсутствии или недостаточности муцина роговица становится несмачиваемой и, вследствие нарушения равновесия между присутствующими электролитами и гликопротеинами, слезная пленка становится нестабильной и подвергается разрыванию с образованием сухих участков.
Различные заболевания или аномальные состояния глаза проявляются при нарушениях непрерывности слезной пленки как следствие, например, недостаточной частоты моргания, продолжительного применения контактных линз, введения некоторых системных лекарственных средств или, более часто, сенильной гипосекреции. Более часто, повреждение описанной выше эффективной смазывающей и защитной системы появляется в "синдроме сухого глаза", степень которого в сильной степени увеличивается, особенно вследствие атмосферного загрязнения и последующего возникновения аллергий нового типа. Фактически, синдром сухого глаза является наиболее частой патологией в офтальмологии, с коэффициентом между 10 и 15% всего населения. В этой связи, термин "сухой глаз", обычно используют для глазных состояний, происходящих из уменьшения или нестабильности глазной пленки, - характеризующихся с субъективной точки зрения, рядом раздражающих симптомов, включающих в себя ощущение жжения, ощущение чужеродного тела в глазах, светофобию и расплывчатое зрение, ощущение тяжести в глазах, легкое раздражение вследствие ветра, дыма и пыли и зрительные расстройства, - в то время как типичные изменения роговичной поверхности, встречающиеся в этой связи, называют обычно термином "keratoconjunctivitis sicca" (сухой кератоконъюнктивит).
В таких ситуациях имеет место дегенерация конъюнктивальных клеток, приводящая к увеличенной десквамации, потере микроскладок поверхности клеток, разрыванию мембран эпителиальных клеток и уменьшению количества муцинпродуцирующих бокаловидных клеток. По-видимому, конъюнктивальные эпителиальные клетки страдают и имеют уменьшенное количество микроворсинок до их полного исчезновения. Уменьшение количества микроворсинок является хорошей приближенной величиной, пропорциональной тяжести поражения и серьезности симптоматики. Эта анатомо-патологическая ситуация сопровождается, в различных степенях, инфильтрацией воспалительных клеток на уровне конъюнктивальных клеток (Cennamo G. L., Del Prete A., Forte R., Cafiero G-, Del Prete S., Marasco D., Impression cytology with scanning electron microscopy: a new method in the study of conjunctival microvilli, Eye (2007), 1-6).
Наряду с этим, синдром сухого глаза, лишенного защитного действия слезной пленки, предрасполагает к другим патологическим состояниям, таким как актинический, бактериальный, вирусный и аллергический кератоконъюнктивит.
Поскольку исследования патологий человека, показавшие все изменения, которые имеет место в сухом глазе, преклиническое исследование в модели животного с сухим кератоконъюнктивитом помогло понять естественную причину этих изменений (Gilbard J. P., Rossi S. R., Gray K. L.: A new rabbit model for keratoconjunctivitis sicca, Invest Ophthalmol. Vis. Sci. 28(2):225-228, (1987); Gilbard J. P., Rossi S.R., Gray K.L., Hanninen L.A.: Natural history of disease in a rabbit model for keratoconjunctivitis sicca, Acta Ophthalmol. (Suppl.) 792:95-101, (1989). Теперь известно, что сухой глаз развивается через четыре различные фазы:
1. Потеря воды из слезной пленки с увеличением осмолярности самой пленки.
2. Уменьшение плотности бокаловидных клеток и уменьшение роговичного гликогена (источника энергии для заживления возможных роговичных повреждений).
3. Увеличение роговичной десквамации (вследствие увеличения осмотического градиента между слезной пленкой и глазной поверхностью и уменьшения бокаловидных клеток, которые изымают воду из эпителиальных клеток конъюнктивы).
4. Дестабилизация поверхности раздела роговица-слезная пленка.
С диагностической точки зрения, синдром сухого глаза может быть детектирован и подвергнут мониторингу не только посредством оценивания его типичных симптомов, но также посредством хорошо установленных процедур, включающих в себя, наиболее часто, оценивание слезной секреции (тест Ширмера), оценивание времени, необходимого для разрывания слезной пленки после окончания мигания (времени разрыва, BUT), и оценивание цвета поверхности роговицы после окрашивания красителем розовым бенгальским или флуоресцеином.
Другим феноменом, который единодушно считают признаком неправильно структурированной глазной пленки, является уменьшение арборизации слизи (секрет кристаллизуется с образованием микроструктур, напоминающих папоротник). В нормальных условиях, слизь характеризуется кристаллизацией в виде папоротника при испарении при комнатной температуре из водного раствора. Феномен арборизации, который считают результатом взаимодействия электролитов с высокомолекулярными гликопротеинами слизи, проявляется после короткого периода времени из собранной слезной слизи из нижнего конъюнктивального свода конъюнктивы. Было определено, что различные формы указанного феномена, получаемые при помощи теста арборизации (т.е. Тип I, однородная арборизация; Тип II, хорошее количество арборизации с папоротникообразными структурами уменьшенного размера и пустыми пространствами; Тип III, арборизация присутствует только частично; Тип IV, арборизация отсутствует), связаны с нормальным или патологическим состоянием слезной жидкости. Плотная арборизация, например, считается выражением точного равновесия между муцином и электролитами, тогда как частичное присутствие или отсутствие слезной арборизации, которая детектируется в глазах, пораженных сухим кератоконъюнктивитом, обозначает количественное отсутствие глазной слизи или количественное изменение гликопротеинов или их окружения (т.е. рН, гидратации, электролитического равновесия).
Сухой кератоконъюнктивит обычно лечат жидкими препаратами для глазных болезней, обычно известными как "искусственные слезы", закапываемыми в виде капель восполнения или дополнения природного продуцирования слез. В самом простом случае, указанные препараты имеют только увлажняющее действие, так как они состоят из физиологических солевых растворов, нейтральных и изотонических со слезной пленкой, приготовленных на основе только хлорида натрия или на основе сбалансированных смесей различных электролитов.
Для преодоления недостатка уменьшенного удерживания внутри конъюнктивального мешка, который является типичным для таких солевых растворов, вводили искусственные препараты слез, которые сделаны вязкими добавлением высокомолекулярных агентов, обычно таких, как водорастворимые полимеры синтетического, полусинтетического или природного происхождения. Однако, было обнаружено, что, в случае указанных усилителей вязкости для придания благоприятных признаков композиции для применения в качестве искусственных слез, недостаточно того, что указанные усилители вязкости обычно увеличивают вязкость продукта, но также необходимо, чтобы образуемые таким образом дисперсии имели свойства близкие, насколько это возможно, к свойствам дисперсий муцина. А именно, указанные дисперсии должны вести себя по возможности как мукомиметики. Это требует, прежде всего, конкретного реологического поведения, т.е. неньютоновского (в частности, псевдопластического) поведения, сходного с реологическим поведением природных слез. В результате, только небольшое число макромолекулярных продуктов, которые могут быть использованы в качестве усилителей вязкости для искусственных слез, действительно способны обнаруживать сходное поведение.
Примерами композиций для применения в качестве искусственных слез, имеющих неньютоновское реологическое поведение, являются искусственные слезы, содержащие карбоксивиниловые полимеры, такие как Carbopol®, сложные эфиры целлюлозы, такие как метилцеллюлоза, и их спиртовые производные (например, гидроксипропилцеллюлоза и гидроксипропилметилцеллюлоза) и гиалуроновая кислота. Последняя является полисахаридом природного происхождения, присутствующая во многих тканях и жидкостях, как человека, так и животного, и используется в широком масштабе в препаратах для глазных болезней, благодаря явному псевдопластическому поведению ее водных растворов и вследствие ее хорошей способности связываться как с водой, так и со стенкой эпителиальных клеток.
Природным полисахаридным полимером, который может считаться включенным в цитируемую категорию, является полисахарид, полученный из семян дерева тамаринда Tamarindus indica, вечнозеленого растения, которое может достигать высоты 15 метров, которое производит в качестве плода боб и которое широко распространено в Индии, Африке и в целом на Дальнем Востоке, где оно культивируется прежде всего для получения пищевых продуктов. Этот плод содержит большие семена, имеющие высокий процент полисахаридов, которые имеют функцию накапливания и сохранения жизненно важных энергетических веществ.
Это семя, которое первоначально считалось побочным продуктом, нашло различные применения при его измельчении до порошкообразной формы (известной как "камедь тамаринда" или "порошок косточек тамаринда"). Наиболее важными из таких приложений являются применения в текстильной промышленности и в бумажной промышленности, где камедь тамаринда используют, соответственно, в качестве шлихтующего агента, и в пищевой промышленности, где ее используют в качестве загущающего, желирующего, стабилизирующего и связывающего агента в любом типе продуктов, как это делается с другими полисахаридными продуктами, такими как альгинаты, пектины, гуаровая камедь или камедь рожкового дерева. Необработанный порошок косточек плода тамаринда, который коммерчески доступен как таковой, содержит 63-73 масс.% полисахарида, 15-23 масс.% белкового материала, 3-8 масс.% жиров и масла и 2-4 масс.% золы, наряду с минорными количествами неочищенной клетчатки, таннинов и других примесей.
В фармацевтической области, фракция полисахаридов камеди тамаринда (полисахарида семян тамаринда, в дальнейшем называемого TSP) нашла обоснованное применение в качестве активного компонента заменителей слез и в качестве носителя для местных лекарственных средств пролонгированного высвобождения для глазных болезней, как описано, в частности, в Европейском патенте ЕР 0892636 (Farmigea) и в соответствующем Патенте США № 6056950, содержание которого включено здесь в качестве ссылки. Среди мукомиметических свойств, которые, по-видимому, имеет полисахаридная фракция камеди тамаринда, должна быть доказана описанная ранее способность "арборизации". Таким образом, подобно гиалуроновой кислоте, указанная фракция полисахаридов способна давать, при испарении, кристаллические продукты, имеющие морфологию, совершенно одинаковую с морфологией кристаллизованной слезной слизи.
В связи с предыдущим описанием, целью данного изобретения является определение фармакологического лечения для терапии синдрома сухого глаза, в котором заменитель слез должен не только оставаться в течение продолжительного времени на поверхности глаза и самоинтегрироваться с поверхностью этого эпителия, проявляя защитную роль в отношении их, но также быть способным содействовать восстановлению их целостности, в частности, содействовать быстрому возвращению к нормальному состоянию конъюнктивальной слизистой оболочки в целом в отношении количества и морфологии микроворсинок.
В рамках этих исследований, которые приводят к данному изобретению, обсуждается, что как известные растворы для лечения глазных болезней на основе TSP, так и более широко распространенные растворы на основе гиалуроновой кислоты, оказались способными производить улучшение в симптоматике сухого глаза, улучшение, которое находится в основе их успеха в продаже в лечении этого заболевания оказались способными производить улучшение в симптоматике сухого глаза, улучшение, которое находится в основе их успеха в продаже в лечении этого заболевания, но оба из этих растворов давали относительно скромные полезные результаты в отношении эффективности и быстрого восстановления в случае гистологических повреждений, которые являются типичными для рассматриваемой патологии, в частности, в отношении микроскопической структуры поверхности конъюнктивального эпителия.
На основании предыдущих обсуждений, было обнаружено в соответствии с данным изобретением, что конкретная комбинация активных ингредиентов TSP и гиалуроновой кислоты, примененных к глазной поверхности в едином продукте для лечения глазных болезней, приобретает новые терапевтические свойства, которые эти два продукта, взятые по отдельности, не имеют, в частности, в содействии более быстрому возвращению к нормальному состоянию конъюнктивальной слизистой оболочки, в частности, в отношении количества и морфологии микроворсинок. Восстановление нормальной целостности микроворсинок ассоциировано с более продолжительно длящимся действием улучшения признаков и симптомов, которые сопутствуют синдрому сухого глаза.
Согласно нескольким исследованиям, проводимым в отношении структуры полисахаридной фракции камеди тамаринда, установлено, что полисахарид семян тамаринда состоит из главной цепи глюкопиранозильных звеньев, связанных друг с другом через связи (1→4), с короткими боковыми цепями, состоящими из ксилопиранозильных звеньев, присоединенных к главной цепи через связи (1→6). Указанные ксилопиранозильные звенья являются одиночными или они могут быть связаны, в свою очередь, с единственными галактопиранозильными звеньями через связь (1→2). Сообщалось также дополнительное присутствие арабинофуранозильных звеньев. Таким образом, структура полисахарида семян тамаринда (TSP) может быт представлена следующим образом:
Процедура для экстракции, фильтрования и очистки этого полимера из исходного необработанного материала требует высокой технологической специализации для сохранения неизмененными функциональных характеристик, также в связи с высокой молекулярной массой, которая находится в диапазоне, в правильно очищенном продукте, от 600000 до 750000 Да.
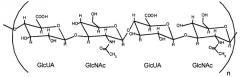
Гиалуроновая кислота определяется химически как гликозаминогликан, состоящий из чередующихся звеньев D-глюкуроновой кислоты (GlcUA) и N-ацетил-D-глюкозамина (GlcNAc), структура которого может быть представлена следующей формулой:
которая показывает два различных дисахаридных звена последовательно и в которой число n повторяющихся пар звеньев является таким, что молекулярная масса этого полисахарида составляет 50000 - несколько миллионов дальтон. Средняя молекулярная масса гиалуроновой кислоты, используемой в офтальмологии (в форме соответствующей натриевой соли) для растворов искусственных слез составляет обычно 700000-1 миллион Да.
In vivo, все карбоксильные группы гиалуроновой кислоты и N-ацетилглюкозамина полностью ионизированы, и придают высокую полярность молекуле гиалуроновой кислоты и, следовательно, высокую растворимость в воде. Благодаря ее высокой способности связывания как с водой, так и со стенкой клетки эпителия, гиалуроновую кислоту используют в качестве главного компонента во многих заменителях слез в лечении патологии сухого глаза.
В области исследований, связанных с данным исследованием, некоторые лабораторные тесты на основе применения способов магнитного резонанса (которые будут подробно описаны ниже) показали, что TSP способен взаимодействовать в растворе с гиалуроновой кислотой (НА), индуцируя конформационные изменения, которые в основном влияют на внутренние звенья глюкозы и галактозы TSP и ацетильные группы НА. Этот факт производит действие на способность этой смеси удерживать воду, которая, для некоторых соотношений концентраций, оказалась заметно более высокой, чем эта способность, показанная этими двумя полимерами в несмешанной форме.
Вследствие того, что способность удерживать воду является фундаментальной для адгезивных характеристик и характеристик биосовместимости полимера, подлежащего применению для лечения сухого глаза, исследование с использованием смеси TSP-HA было дополнительно продлено при помощи преклинических тестов на модели сухого глаза в крысе с атропином для оценки безвредности и переносимости этой смеси. На основании результатов, полученных на такой модели (также синтетически сообщенных в дальнейшем), можно утверждать, что смесь TSP и НА не обнаруживает отрицательных взаимодействий между этими двумя продуктами и что она стимулирует лучшее восстановление гисто-физиологических повреждений после острого уменьшения продуцирования слез.
Последующий клинический тест, проводимый в качестве предварительного (поискового) исследования на относительно ограниченном количестве пациентов (сообщенный далее) подтвердил эффективность предложенного лечения, показав явное синергическое действие комбинации TSP и НА.
Таким образом, данное изобретение конкретно обеспечивает препарат для глазных болезней для применения в качестве заменителя слез, содержащий, в комбинации, 0,05-2 масс.% полисахарида семян тамаринда и 0,05-1 масс.% гиалуроновой кислоты в водном растворе.
Термин "полисахарид семян тамаринда" (полисахарид семян Tamarindus indica TSP, иногда называемый также термином "ксилоглюкан") в данном контексте обозначает любую обогащенную полисахаридом фракцию, получаемую из камеди тамаринда (т.е. порошка косточек тамаринда), причем последняя является необработанным продуктом, в настоящее время доступным в продаже. Продается частично очищенная фракция полисахарида камеди тамаринда, например, Dainippon Pharmaceutical Co. LTD of Osaka, Japan, под товарным названием Glyloid®. Однако, для цели данного изобретения соответствующую полисахаридную фракцию предпочтительно дополнительно очищают с получением практически чистого полисахарида семян тамаринда.
Термин "гиалуроновая кислота", в контексте данного изобретения, обозначает ранее описанный полисахарид (обычно называемый также "гликозаминогликан"), в частности, в форме соли, обычно используемой для приготовления искусственных слез, т.е. в форме гиалуроната натрия.
Предпочтительно, препарат для глазных болезней согласно этому изобретению содержит, в комбинации с водным раствором, 0,1-1 масс.% полисахарида семян тамаринда и 0,1-0,5 масс.% гиалуроновой кислоты.
Предпочтительно, концентрации по массе в препарате для глазных болезней по данному изобретению содержат 0,1-1 масс.% полисахарида семян тамаринда и 0,1-0,5 масс.% гиалуроновой кислоты. Вариант, который конкретно использовали в представленной ниже экспериментальной работе и который обеспечивает превосходные клинические эффективности в отношении способности этих двух активных агентов кооперироваться в восстановлении нормального состояния конъюнктивального эпителия, содержит, в водном растворе, 0,2 масс.% полисахарида семян тамаринда и 0,4 масс.% гиалуроновой кислоты.
Предпочтительно, полисахарид семян тамаринда, используемый в препаратах этого изобретения, имеет молекулярную массу, находящуюся в диапазоне 450000 Да - 750000 Да (предпочтительно 600000-750000 Да), а гиалуроновая кислота имеет молекулярную массу, находящуюся в диапазоне 600000 Да - 1000000 Да (предпочтительно 700000 - 1000000 Да).
В препаратах искусственных слез по данному изобретению должны быть добавлены один или несколько корректирующих тоничность агентов для получения таким образом раствора с правильной величиной осмолярности. Для этой цели может быть использован любой из продуктов, используемый в настоящее время в данной области в качестве агентов тоничности, такой как, например, хлорид натрия, хлорид калия, маннит, декстроза, борная кислота, сорбит или пропиленгликоль.
Другими ингредиентами, которые могут быть включены в препарат, в соответствии с известной областью, являются кислоты или основания в качестве корректирующих рН агентов, а также буферы, такие как, например, фосфатный буфер (дигидрофосфат натрия и моногидрофосфат натрия) или ацетатный буфер (система ацетат-уксусная кислота). Другими буферами, которые могут быть использованы, являются боратный, цитратный, бикарбонатный буферы или тризма (тригидроксиметиламинометан)-буфер.
Эта композиция может также содержать консерванты и антимикробные агенты, такие как хлорид бензалкония, мертиолат натрия или тимерозал, метил-, этил- и пропилпарабен, хлорбутанол, фенилмеркурнитрат или фенилмеркурацетат, фенилэтиловый спирт, ацетат или глюконат хлоргексидина, а также хелатообразующие агенты, такие как эдетаты или ЭДТА. Вследствие проблем переносимости консервантов, предпочтительно не включать подобные ингредиенты в препараты для использования в качестве искусственных слез. Это является вполне возможным, когда продукт упакован в однодозовые контейнеры. Однако, в некоторых случаях и особенно, когда продукт находится в многодозовых контейнерах, добавление консервантов является необходимым.
Согласно следующему аспекту, данное изобретение относится к применению комбинации полисахарида семян тамаринда и гиалуроновой кислоты в водном растворе для получения препарата для лечения синдрома сухого глаза.
Как уже отмечалось, указанный заменитель или препарат слез предпочтительно содержит 0,05-2 масс.% полисахарида семян тамаринда и 0,05-1 масс.% гиалуроновой кислоты, и более предпочтительно он содержит 0,1-1 масс.% полисахарида семян тамаринда и 0,1-0,5 масс.% гиалуроновой кислоты.
Полисахарид семян тамаринда предложенного препарата для применения, описанного ниже, имеет молекулярную массу в диапазоне 600000 Да - 750000 Да, тогда как молекулярная масса гиалуроновой кислоты находится в диапазоне 700000 Да - 1000000 Да.
Данное изобретение описано также следующими не ограничивающими изобретение примерами, в соответствии с его некоторыми конкретными вариантами, которые иллюстрируют примеры готовых форм на основе ксилоглюкана и гиалуроновой кислоты, используемых в качестве заменителей слез, имеющих защитную и повторно эпителизирующую активность, в соответствии с тем, что экспериментально получено и сообщено в экспериментальном отчете, следующем ниже.
ПРИМЕРЫ ПРЕПАРАТОВ ИСКУССТВЕННЫХ СЛЕЗ
Пример 1
| Ингредиенты | масс.% |
| TSP | 0,1 |
| Гиалуроновая кислота | 0,1 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт получают с использованием следующих стадий:
- TSP и HA взвешивают в подходящий стеклянный сосуд;
- 90% доступной воды добавляют с легким перемешиванием до полного растворении этого продукта;
- добавляют требуемое количество маннита, продолжая перемешивание, и эту смесь оставляют при условиях перемешивания до полного растворения продукта;
- добавляют деионизованную воду до конечной массы (100%);
- добавляют одноосновный и двухосновный фосфат натрия до достижения желаемого рН;
- полученный таким образом раствор стерилизуют в автоклаве или, альтернативно, стерилизуют фильтрованием с использованием фильтра 0,22 микрон.
Пример 2
| Ингредиенты | масс.% |
| TSP | 0,1 |
| Гиалуроновая кислота | 0,4 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт получают так же, как в примере 1.
Пример 3
| Ингредиенты | масс.% |
| TSP | 0,2 |
| Гиалуроновая кислота | 0,1 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт готовят так же, как в примере 1.
Пример 4
| Ингредиенты | масс.% |
| TSP | 0,2 |
| Гиалуроновая кислота | 0,2 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт готовят так же, как в примере 1.
Пример 5
| Ингредиенты | масс.% |
| TSP | 0,2 |
| Гиалуроновая кислота | 0,4 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт готовят так же, как в примере 1.
Пример 6
| Ингредиенты | масс.% |
| TSP | 0,4 |
| Гиалуроновая кислота | 0,1 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт готовят так же, как в примере 1.
Пример 7
| Ингредиенты | масс.% |
| TSP | 0,4 |
| Гиалуроновая кислота | 0,2 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт готовят так же, как в примере 1.
Пример 8
| Ингредиенты | масс.% |
| TSP | 1,0 |
| Гиалуроновая кислота | 0,1 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт готовят так же, как в примере 1.
Пример 9
| Ингредиенты | масс.% |
| TSP | 1,0 |
| Гиалуроновая кислота | 0,4 |
| Маннит | 2,00 |
| Деионизованная вода | q.s. до 100 |
| Одноосновный фосфат и двухосновный фосфат натрия | q.s. до рН 7,0±0,5 |
Этот продукт готовят так же, как в примере 1.
Некоторые экспериментальные результаты, показывающие признаки полисахаридных комбинаций по этому изобретению и эффективность препаратов, содержащих их, приведены ниже, вместе с некоторыми графиками и фотографиями, показанными в сопутствующих рисунках, где:
Фигура 1 показывает, в форме гистограммы, результаты предварительного исследования эффективности композиции по данному изобретению в лечении синдрома сухого глаза, касающиеся оценивания конъюнктивальных микроворсинок, в абсолютных величинах.
Фигура 2 показывает результаты, в том же самом предварительном исследовании, оценивания конъюнктивальных микроворсинок, в виде варьирования фоновых величин.
Фигура 3 показывает изображение сканирующей (растровой) электронной микроскопии (SEM 7500x) конъюнктивального эпителия левого глаза пациента женского пола того же самого предварительного исследования, причем указанный пациент принадлежит к группе TSP+НА, перед обработкой.
Фигура 4 показывает изображение сканирующей (растровой) электронной микроскопии (SEM 7500x) конъюнктивального эпителия левого глаза того же самого пациента женского пола фигуры 3, после 60 дней обработки TSP+HA.
Фигура 5 показывает, в форме гистограммы, результаты того же самого предварительного исследования фиг. 1, касающиеся оценивания действий на субъективную симптоматику, в абсолютных величинах.
Фигура 6 показывает результаты, в предварительном исследовании, оценивания действий на субъективную симптоматику, в виде фоновых величин.
Фигура 7 показывает, в форме гистограммы, результаты того же самого предварительного исследования фиг. 1, касающиеся оценивания действий на объективную симптоматику, в виде абсолютных величин.
Фигура 8 показывает результаты, в том же самом предварительном исследовании, оцениваний действий на объективную симптоматику, в виде фоновых величин.
Фигура 9 показывает, в форме гистограммы, результаты того же самого предварительного исследования фиг. 1, касающиеся оценивания действия на цитологию, в виде абсолютных величин.
Фигура 10 показывает результаты, в том же самом предварительном исследовании, оценивания действий на цитологию, в виде вариации относительно фоновых величин.
Фигура 11 показывает, в форме гистограммы, результаты того же самого предварительного исследования фиг. 1, касающиеся общего балла (объединенного балла) предыдущего оценивания, в виде абсолютных величин.
Фигура 12 показывает результаты, в том же самом предварительном исследовании, объединенного балла предыдущих оцениваний, в виде вариации относительно базальных величин.
ЯМР-исследование смеси гиалуроновой кислоты (НА) и TSP в водном растворе
Полисахаридные гидрогели обеспечивают очень усложненную трехмерную структуру, в которую может быть включена вода. Содержание воды, тип взаимодействия, который имеет место между водой и полимерными материалами, а также распределение воды внутри самого полимера имеют решающее влияние на механические свойства, муко-адгезивность и являются основой высокой степени совместимости. Обычно различают три типа воды в полисахаридном геле: связанная вода, промежуточная вода и свободная вода.
Спектроскопия ядерно-магнитного резонанса (ЯМР) представляет собой один из наиболее применимых способов для исследования свойств структуры, мобильности и гидратации полимерных систем. В частности, очень полезным является измерение времени спин-спиновой релаксации (T2) или спин-решеточной релаксации (T1) ядер протонов воды. Время релаксации T2 представляет константное время, которое описывает затухание поперечного намагничивания во времени, в то время как время релаксации Т1 описывает возвращение процесса продольного намагничивания.
При растворении полисахарида в воде, молекулы воды образуют водородные связи в нем и, следовательно, их подвижность уменьшается, приводя к уменьшению как Т1, так и Т2. Однако, обычно детектируются не отдельные сигналы для связанной воды и свободной воды, а единый сигнал, который представляет взвешенное среднее вкладов, происходящих от этих двух типов воды. В результате, измеренный параметр ЯМР (T1 и/или T2) представляет взвешенное среднее этого параметра в свободном и связанном состоянии, в соответствии со следующим уравнением (уравнением 1):
где 1/Tobs описывает степень скорости релаксации (обратную величину времени T1 или T2), измеренную для воды в соответствующем растворе, 1/Tb является степенью скорости релаксации связанной воды и 1/Tf является степенью скорости релаксации свободной воды, равной степени скорости релаксации, измеренной в растворе, лишенном полимерного материала. Xb и Xf, соответственно обозначают молярную фракцию связанной и свободной воды.
Количество молекул связанной воды может быть выражено следующим образом, в зависимости от поверхности S этого полимера, на толщину К поверхностного слоя связанной воды и на общий объем воды V (уравнение 2):
При увеличении концентрации полимера, как Т1, так и Т2 уменьшаются как следствие увеличения поверхности полимера и, следовательно, количества молекул связанной воды, пока не произойдут конформационные вариации или саморегулируемые феномены в зависимости от самой концентрации; однако действие скорости поперечной релаксации (1/Т2) является более заметным, чем действие, отмечаемое на скорости продольной релаксации (1/Т1).
На основании этих причин, следующие эксперименты измерения скорости поперечной релаксации (1/Т2) в ядрах протонов воды проводили в следующих растворах:
a) растворах TSP, имеющих вариабельную концентрацию, от 0,1% (м/м) до 1%;
b) растворах HA, имеющих вариабельную концентрацию, от 0,1% (м/м) до 1%;
c) смесях, с