Способ пластики грыжи пищеводного отверстия диафрагмы
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к хирургии, и может быть использовано при операциях на органах брюшной полости, в частности при лечении грыж пищеводного отверстия диафрагмы, рефлюкс-эзофагита, резистентного к консервативной терапии. С целью снижения послеоперационных осложнений, за счет повышения механической прочности круглой связки печени, расширения области применения, дополнительно формируют биомеханический комплекс, для чего вокруг с внешней части круглой связки располагают каркас из сетчатого протеза трубчатой формы, выполненный из никелида титана с диаметром нити 60-90 мкм, далее, полученный биомеханический комплекс проводят позади пищевода и вокруг кардиоэзофагеального перехода с формированием «полупетли», а затем фиксируют к передней стенке желудка отдельными узловыми швами с интервалом 8-12 мм на расстоянии 10-20 мм от края малой кривизны желудка. 7 ил.
Реферат
Изобретение относится к медицине, а именно к хирургии, и может быть использовано при операциях на органах брюшной полости, в частности при лечении грыж пищеводного отверстия диафрагмы.
Частота выявляемости грыж пищеводного отверстия диафрагмы у пациентов с рефлюкс-эзофагитом достигает, по разным данным, 50%-80% [1, 2]. Данная проблема сохраняет актуальность еще и потому, что грыжи пищеводного отверстия диафрагмы, ассоциированные с рефлюкс-эзофагитом, приводят к развитию серьезных осложнений, таких как пептические язвы, стриктуры пищевода, развитие пищевода Баррета и рака пищевода [3]. Способы лечения грыж пищеводного отверстия диафрагмы преследуют несколько целей: повышение тонуса и укрепление нижнего пищеводного сфинктера, восстановление острого кардиоэзофагеального угла, удлинение абдоминального отдела пищевода, фиксация кардии и пищевода в брюшной полости. Однако ни один из существующих способов лечения грыж пищеводного отверстия диафрагмы не достигает всех целей в совокупности.
Известен способ лечения грыж пищеводного отверстия диафрагмы и гастроэзофагеального рефлюкса путем создания манжетки из дна желудка вокруг терминального отдела пищевода (фундопликация по Nissen) [4]. Таким образом достигается формирование надежного антирефлюксного клапана. Данная операция имеет ряд недостатков. Среди них наиболее существенными являются выраженная травматичность, в связи с необходимостью мобилизации желудка по большой кривизне, выраженная и частая дисфагия в послеоперационном периоде, рецидив рефлюкс-эзофагита, формирование параэзофагеальной грыжи, «gas-bloat» синдром.
Известен способ лечения грыж пищеводного отверстия диафрагмы путем создания фундопликационной манжетки на половину окружности пищевода (фундопликация по Toupet) [4]. Данный способ не требует широкой мобилизации желудка по большой кривизне, менее травматичен, реже вызывает дисфагию, однако сопряжен с большей частотой рецидивов рефлюкс-эзофагита, и при данном способе невозможно формирование полноценного жома, сравнимого с операцией Ниссена по функциональности.
Известны способы лечения грыж пищеводного отверстия диафрагмы путем фиксации малой кривизны желудка к преаортальной фасции (гастропексия по Hill) [5], или к передней брюшной стенке (передняя гастропексия по Boerema) [6].
Перечисленные способы обеспечивают надежную фиксацию абдоминального отдела пищевода и кардиального отдела желудка в брюшной полости. Недостатками является нефизиологичность жесткой фиксации малой кривизны, приводящая к нарушениям перистальтики желудка. Кроме того, операция Хилла технически сложна и чревата серьезными осложнениями в виде повреждения ветвей аорты и нерва Латарже.
Наиболее близким к предлагаемому является способ лечения грыж пищеводного отверстия диафрагмы, заключающийся в проведении кардиопексии с использованием круглой связки печени [7]. Круглая связка имеет кровоснабжение из малой артериальной ветви печеночной артерии, что предупреждает ее резорбцию при перемещении с целью пластики. Проведенная за пищеводом и фиксированная к передней стенке желудка круглая связка формирует постоянный острый угол Гиса и удерживает кардию и дистальную часть пищевода в интраабдоминальном положении. Круглая связка соединяет угол Гиса с левой долей печени, образуя единый комплекс, двигающийся содружественно при дыхательных экскурсиях, что наиболее физиологично. Способ технически прост и не требует широкой мобилизации желудка по большой и малой кривизне.
Однако недостатком известного способа является наличие в составе круглой связки печени жировой ткани, отсутствие прочного соединительнотканного матрикса, что отрицательно сказывается на ее биомеханических свойствах, обусловливает недостаточную прочность круглой связки, как пластического материала. Кроме того, выраженность тканевого массива круглой связки у разных категорий пациентов вариабельно, что может явиться препятствием при слабо выраженной круглой связке.
Новая техническая задача - повышение механической прочности круглой связки печени, снижение послеоперационных осложнений, расширение области применения.
Для решения поставленной задачи в способе пластики грыжи пищеводного отверстия диафрагмы, включающем выделение круглой связки печени, мобилизацию абдоминального отдела пищевода, кардиопексию круглой связкой печени, дополнительно формируют биомеханический комплекс, для чего вокруг поверхности круглой связки располагают каркас из сетчатого протеза трубчатой формы, выполненный из никелида титана с диаметром нити 60-90 мкм, далее, полученный биомеханический комплекс проводят позади пищевода и вокруг кардиоэзофагеального перехода с формированием «полупетли», а затем фиксируют к передней стенке желудка отдельными узловыми швами с интервалом 8-12 мм на расстоянии 10-20 мм от края малой кривизны желудка.
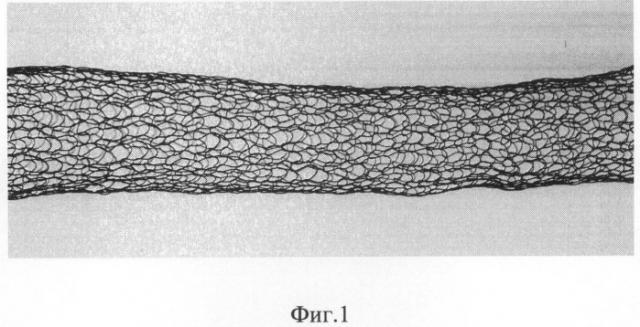
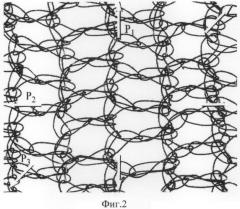
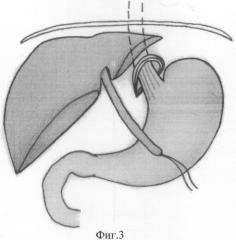
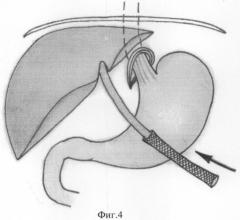
Способ осуществляют следующим образом. После обработки операционного поля по Гроссиху производят верхнесрединную лапаротомию. Мобилизуют левую долю печени, путем рассечения левой треугольной связки отводят ее кнаружи. Рассекают пищеводно-диафрагмальную связку с перевязкой ветвей диафрагмальных вен. Натяжением желудка книзу низводят кардиальный отдел желудка и пищевод под диафрагму, при наличии кардиодиафрагмальных сращений, рассекают их. Мобилизуют до 4-5 см дистального отдела пищевода и берут на держалку. Позади пищевода тупым путем формируют туннель в направлении к пищеводно-желудочному переходу. Отсекают круглую связку печени от пупочного кольца, выделяют ее на всем протяжении до свободного края печени, на свободный конец круглой связки накладываются два шва-держалки (Фиг.3). Для укрепления круглой связки используется сетчатый протез трубчатой формы (Фиг.1), изготовленный из сверхэластической никелидтитановой нити диаметром 60-90 мкм (Фиг.2). Длину протеза подбирают в соответствии с длиной круглой связки печени. С помощью держалок круглую связку протягивают через сетчатый никелидтитановый протез (Фиг.4), в результате формируют внешний каркас вокруг связки (Фиг.5). За счет эластических свойств протез адаптируют таким образом, чтобы он плотно фиксировал круглую связку печени. Сформированный комплекс из укрепленной протезом круглой связки печени проводят позади пищевода, заводят вокруг кардиоэзофагеального перехода в виде «полупетли», воссоздавая, таким образом, острый угол Гиса (Фиг 6). Свободный конец комплекса из никелидтитанового протеза и круглой связки печени фиксируют отдельными узловыми швами с интервалом 8-12 мм к передней стенке желудка на расстояние 10-20 мм от края желудка по малой кривизне (Фиг.7). Операционную рану ушивают послойно, наглухо.
Новым является то, что круглую связку печени дополнительно укрепляют сверхэластичным сетчатым протезом из никелидтитановой нити диаметром 60-90 мкм, что увеличивает ее прочность, при этом биохимическая инертность каркасного материала позволяет широко применять данный способ без опасения развития тканевых реакций на инородный материал, что было неоднократно доказано экспериментально. Со временем, вследствие биомеханической и биохимической совместимости имплантата с окружающими тканями, происходит прорастание соединительной и жировой ткани сквозь сетчатую структуру имплантата с образованием единого с каркасным материалом тканевого регенерата, что обеспечивает надежную фиксацию комплекса из круглой связки и никелидтитанового протеза к тканям, предотвращает смещение и отрыв круглой связки от места фиксации, что исключает рецидивы. Заданные параметры нити каркаса диаметром 60-90 мкм выдерживают механические деформации сетчатого каркаса, предотвращают растяжение круглой связки в послеоперационном периоде, что способствует профилактике формирования рецидивной грыжи. Эластичные свойства сетчатого никелида титана и соединительной ткани сходны, поэтому деформация образованного «биомеханического комплекса» - круглая связка-никелидтитановый каркас получается согласованной со смещением органов при дыхательных экскурсиях. Применение данного способа снижает риск послеоперационных осложнений, повышает прочность соединения и обеспечивает оптимальную физиологичность данной области.
Отсутствие в мировой литературе и в патентно-информационных источниках решений со сходной совокупностью существенных признаков свидетельствует о соответствии предложения авторами критериям «новизна» и «изобретательский уровень». Изобретение иллюстрируется схемами выполнения конкретных приемов и примерами отдельных этапов операций в эксперименте.
На иллюстрациях представлено:
Фиг.1. Сверхэластичный сетчатый имплантат трубчатой формы.
Фиг.2. Фрагмент сетчатого имплантата при увеличении.
Фиг.3. Схема этапа операции. На всем протяжении выделена круглая связка печени. На свободный конец наложены швы-держалки.
Фиг.4. Схема этапа операции. Начало формирования внешнего каркаса с помощью сверхэластичного сетчатого протеза из никелида титана.
Фиг.5. Схема этапа операции. Сформирован внешний каркас вокруг круглой связки печени.
Фиг.6. Схема этапа операции. Укрепленная сетчатым протезом круглая связка проведена за пищеводом и выведена на переднюю стенку желудка с формированием вокруг кардиоэзофагеального перехода «полупетли».
Фиг.7. Схема этапа операции. Конечный этап терес-кардиопексии круглой связкой и протезом из никелида титана. Укрепленная связка фиксирована к передней стенке желудка отдельными узловыми швами.
Проверочным тестом достижимости технического результата является экспериментальная апробация предлагаемого способа лечения грыж пищеводного отверстия диафрагмы, смоделированных на 11 беспородных собаках массой тела 10-16 кг. Эксперименты на животных выполнены в отделе экспериментальной хирургии Центральной научно-исследовательской лаборатории СибГМУ. Исследование проводили согласно этическим принципам, изложенным в "Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей", все манипуляции и выведение животных из опытов проводились под общей анестезией.
Пример 1 (беспородная собака массой тела 15 кг). После обработки операционного поля йодом и спиртом под общей анестезией с управляемым дыханием выполнили верхнесрединную лапаротомию. После ревизии брюшной полости мобилизовали левую долю печени рассечением левой треугольной связки. Левую долю печени отводили с помощью печеночных крючков, осуществляя доступ к диафрагме. Рассекали пищеводно-диафрагмальную связку, а затем мобилизовали 4 см абдоминального отдела пищевода, с взятием его на держалку. Круглую связку печени отсекали от пупочного кольца, выделяли ее на всем протяжении до свободного края печени. На свободный конец круглой связки печени накладывались два шва-держалки. С помощью держалок круглую связку протягивали через сетчатый протез из никелида титана, выполненный в форме трубки с диаметром сверхэластичной никелидтитановой нити 90 мкм, и выкроенный по длине круглой связки печени. За счет эластических свойств, протез фиксирует круглую связку печени на всем протяжении, образуя каркас вокруг связки. Натяжением желудка книзу смещали кардию и пищевод дистальнее. Позади пищевода тупым путем формировали туннель в направлении к пищеводно-желудочному переходу. Затем осуществили главное действие способа, заключающееся в терес-кардиопексии. Круглая связка, укрепленная каркасом из сверхэластичного никелида титана, с помощью держалок проводилась за пищеводом. Затем, укрепленную связку проводили вокруг кардиоэзофагеального перехода в виде «полупетли» и фиксировали оба края круглой связки 8 отдельными узловыми швами к передней стенке тела желудка на расстоянии 15 мм от малой кривизны, с интервалом между швами 8-10 мм. Операционную рану послойно ушили. В раннем и отдаленном послеоперационном периодах осуществляли клиническое наблюдение, рентгенологический и эндоскопический контроль, проводили гистологическое исследование препаратов.
Пример 2 (беспородная собака массой тела 12 кг). После обработки операционного поля по Гроссиху под общей анестезией с управляемым дыханием выполнили верхнесреднесрединную лапаротомию. Мобилизовали левую долю печени рассечением левой треугольной связки, левую долю отводили печеночными крючками. Рассекали пищеводно-диафрагмальную связку, выделяли 5 см абдоминального отдела пищевода, с взятием его на держалку. Позади пищевода тупым путем формировали туннель в направлении к пищеводно-желудочному переходу. Мобилизовали круглую связку печени путем отсечения от пупочного кольца, с последующим выделением ее на всем протяжении до свободного края печени. На свободный конец круглой связки печени накладывались два шва-держалки. С помощью держалок круглая связка протягивалась через сверхэластичный никелидтитановый сетчатый протез, выполненный в форме трубки с диаметром нити 60 мкм, выкроенный по длине круглой связки печени и адаптированный под диаметр круглой связки за счет эластических свойств. Натяжением желудка книзу смещали кардиальный отдел и пищевод дистальнее. Затем осуществили главное действие способа, заключающееся в терес-кардиопексии. Сформированный комплекс из круглой связки и сверхэластичного никелидтитанового протеза, с помощью держалок проводился за пищеводом. Затем укрепленную протезом связку проводили вокруг кардиоэзофагеального перехода в виде «полупетли» и фиксировали оба края круглой связки 6 отдельными узловыми швами к передней стенке тела желудка на расстоянии 15 мм от малой кривизны, с интервалом между швами 10-12 мм. Операционную рану послойно ушили. В раннем и отдаленном послеоперационном периодах осуществляли клиническое наблюдение, рентгенологический и эндоскопический контроль, проводили гистологическое исследование препаратов.
Результаты экспериментальной апробации подтверждают работоспособность предлагаемого способа и достижимость технического результата. Готовность операции к клиническому применению свидетельствует о соответствии предложения критерию «промышленно применимо».
Способ целесообразно применять при грыжах пищеводного отверстия диафрагмы, включая рецидивные варианты, гастроэзофагеальной рефлюксной болезни при неэффективности консервативной терапии.
Источники информации
1. Conrado L.M., Gurski R.R, da Rosa A.R., Simic A.P., Callegari-Jacques S.M. Is there an association between hiatal hernia and ineffective esophageal motility in patients with gastroesophageal reflux disease?// J Gastrointest Surg. - 2011. - Oct. - Vol.15. - №10. - 1756 p.
2. Dean C, Etienne D., Carpentier В., Gielecki J., Tubbs R.S., Loukas M. Hiatal hernias.// Surg Radiol Anat. - 2011. - Nov. 22.
3. Belhocine K., Galmiche J.P. Epidemiology of the complications of gastroesophageal reflux disease. // Dig Dis. - 2009. - Vol.27. - №1. - 7-13 p.
4. Bais J.E., Bartelsman J.F., Bonjer H.J., Cuesta M.A., Go P.M., Klinkenberg-Knol E.C., van Lanschot J.J., Nadorp J.H., Smout A.J., van der Graaf Y., Gooszen H.G. Laparoscopic or conventional Nissen fundoplication for gastro-oesophageal reflux disease: randomized clinical trial. The Netherlands Antireflux Surgery Study Group.// Lancet. - 2000 - Jan.15. - Vol.355. -№9199.- 170-174 p.
5. Toupet A. Technique d'oesophago-gastroplastie avec phrenogastropexie appliquee a la cure radicale des hernies hiatales et comme complement de l'operation de Heller dans les cardiospasmes.// Mem Acad Chir. - 1963. - 102. - 700 p.
6. Carol E.H. Scott-Conner. Chassin's operative strategy in esophageal surgery / Carol E.H. Scott-Conner. - New York: Springer, 2006. - 107 p.
7. Boerema W.J. Anterior gastropexy: a simple operation for hiatus hernia.// Aust N Z J Surg. -1969. - Nov. - Vol.39. - №2. -173-178 p.
Способ пластики грыжи пищеводного отверстия диафрагмы, включающий выделение круглой связки печени, мобилизацию абдоминального отдела пищевода, кардиопексию круглой связкой печени, отличающийся тем, что дополнительно формируют биомеханический комплекс, для чего вокруг с внешней части круглой связки располагают каркас из сетчатого протеза трубчатой формы, выполненный из никелида титана с диаметром нити 60-90 мкм, далее полученный биомеханический комплекс проводят позади пищевода и вокруг кардиоэзофагеального перехода с формированием «полупетли», а затем фиксируют к передней стенке желудка отдельными узловыми швами с интервалом 8-12 мм на расстоянии 10-20 мм от края малой кривизны желудка.