Способ получения сложных эфирных фторалкансульфиновых кислот
Иллюстрации
Показать всеИзобретение относится к способу получения сложных эфиров фторалкансульфиновых кислот. В частности, к получению сложных эфиров трифторметансульфиновой кислоты, называемой обычно "трифлиновой кислотой". Способ получения сложного эфира фторалкансульфиновой кислоты согласно изобретению отличается тем, что он включает в себя реакцию фторалкансульфиновой кислоты формулы:
с органическим карбонатом формулы
,
приводящую к образованию сложного эфира фторалкансульфиновой кислоты и диоксида углерода, который выделяется во время реакции. 11 з.п. ф-лы, 1 пр.
Реферат
Объектом настоящего изобретения является способ получения сложных эфиров фторалкансульфиновых кислот.
В частности, изобретение нацелено на получение сложных эфиров трифторметансульфиновой кислоты, называемой обычно “трифлиновой кислотой”.
Сложные алкиловые или ароматические эфиры трифлиновой кислоты, часто обозначаемые термином “трифлинат”, являются продуктами, описанными в литературе.
Были предложены различные способы синтеза указанных сложных эфиров.
Один из них заключается во взаимодействии спирта с активированной формой трифлиновой кислоты (хлорированная, фторированная).
Так Деннис Зауэр (Sauer Dennis T.) и Жан Шрив (Shreeeve Jeanne M.) [Inorganic chemistry (1971), 10(2), 358-362] описали присоединение метанола к трифторметансульфинилфториду.
Также, присоединение этанола к трифлинилхлориду в щелочной среде описано Джеймсом Хендриксоном (Hendrickson James B.) и Паулем Скиппером (Scipper Paul L.) [Tetrahedron (1976), 32(14), 1627-35].
В этих двух примерах трифторметансульфинильное звено выполняет функцию электрофильной частицы, и она может быть генерирована in situ.
Биллард, Грейнер и Ланглуа (Billard T., Greiner A. et Langlois B.) [Tetrahedron (1999), 55, 7243-50] описали активацию трифлината натрия оксихлоридом фосфора в этилацетате. Присоединение фенола приводит к фениловому эфиру трифлиновой кислоты F3C-SO-OPh с выходом 73%.
Другой путь синтеза основан на принципе нуклеофильной атаки трифлинатным ионом алкилирующего агента.
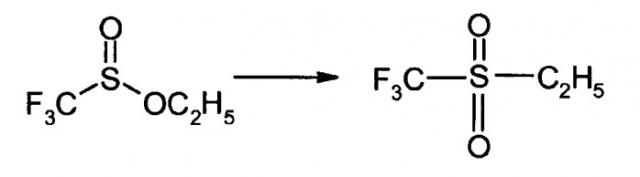
Взаимодействие трифлината калия и этилхлорида [Hendrickson James B., Giga Aziz, Wareing James, J. Amer. Chem. Soc. (1974), 96, 2275] приводит к получению не этилтрифлината F3C-SO-OC2H5, а главным образом продукта S-алкилирования, то есть к сульфону формулы F3C-SOO-C2H5.
Для получения алкилтрифлината была предложена [Hendrickson, James et al., loc. cit.] реакция трифлината калия с изопропил-п-нитробензолсульфонатом. Помимо применения труднодоступного реактива, выход изопропилтрифлината варьировался между 23 и 66%.
Сложность получения алкилтрифлината заключается также в том, что алкилтрифлинаты обладают способностью изомеризоваться в сульфон [Hendrickson, James et al., loc. cit.], как это иллюстрирует следующая реакция:
Фирма-заявитель задалась целью разработать способ, позволяющий получать сложные эфиры трифлиновой кислоты, избегая указанных неудобств.
Объектом настоящего изобретения является найденный заявителем способ получения сложного эфира фторалкансульфиновой кислоты, отличающийся тем, что он включает реакцию фторалкансульфиновой кислоты с органическим карбонатом, приводящую к образованию сложного эфира фторалкансульфиновой кислоты и диоксида углерода, который выделяется во время реакции.
Согласно предпочтительному варианту осуществления способа по изобретению получение сложного эфира трифлиновой кислоты осуществляют взаимодействием трифлиновой кислоты и диалкилкарбоната.
Ниже приведена реакционная схема процесса согласно изобретению с целью облегчения понимания изобретения, тем не менее не ограничивая ей объем патентной охраны изобретения (при этом R обозначает алкильную группу):
В соответствии со способом согласно изобретению осуществляют реакцию транс-этерификации, приводящую к получению алкилтрифлината, диоксида углерода и спирта, образующегося из органического карбоната.
В соответствии с предпочтительным вариантом осуществления способа согласно изобретению удаление диоксида углерода по мере его образования способствует получению сложного эфира фторалкансульфиновой кислоты.
Способ согласно изобретению применим, в частности, к фторалкансульфиновым кислотам, отвечающим следующей формуле:
в которой:
- Х обозначает атом водорода или атом фтора,
- n обозначает число в интервале от 1 до 8.
В частности, изобретение предоставляет перфторалкансульфиновые кислоты, отвечающие формуле (I), в которой Х представляет собой атом фтора.
В формуле (I) n изменяется в интервале от 1 до 8, но, предпочтительно, равно 1.
В качестве предпочтительных примеров фторалкансульфиновых кислот можно назвать следующие кислоты:
- дифторметансульфиновая кислота,
- трифторметансульфиновая кислота,
- перфторбутансульфиновая кислота,
- перфтороктансульфиновая кислота.
Изобретение более предпочтительно подходит для получения сложных эфиров трифторметансульфиновой кислоты или трифлиновой кислоты.
В соответствии со способом согласно изобретению фторалкансульфиновую кислоту вводят в реакцию с органическим карбонатом.
Органические карбонаты, применяемые в способе согласно изобретению, отвечают, в частности, следующей общей формуле:
R 1 -O-CO-O-R 2 (II)
в которой:
- R1 обозначает:
- алкильную группу, линейную или разветвленную, содержащую от 1 до 6 атомов углерода,
- циклоалкильную группу, содержащую от 5 до 6 атомов углерода,
- циклоалкильную группу, содержащую от 5 до 6 атомов углерода, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,
- фенильную группу,
- фенильную группу, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,
- R2 обозначает:
- алкильную группу, линейную или разветвленную, содержащую от 1 до 6 атомов углерода,
- циклоалкильную группу, содержащую от 5 до 6 атомов углерода,
- циклоалкильную группу, содержащую от 5 до 6 атомов углерода, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,
- фенильную группу,
- фенильную группу, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,
- R1 и R2 вместе могут образовать алкиленовую группу, содержащую от 2 до 6 атомов углерода.
Хотя R1 мог бы быть отличным от R2, желательно, заботясь об упрощении, чтобы R1 была идентична R2.
В качестве примеров групп R1 и R2 можно назвать алкильные группы, содержащие от 1 до 4 атомов углерода, предпочтительно, метил, этил, изопропил; циклогексильную группу; фенильную группу: фенильная группа замещена в положениях орто и орто' атомом галогена, предпочтительно, хлора или брома, или алкильной группой, линейной или разветвленной, содержащей от 1 до 4 атомов углерода.
В формуле (II) R1 и R2 могут образовать алкиленовую группу, предпочтительно, этиленовую или пропиленовую группу.
В качестве примеров органических карбонатов можно назвать: диметилкарбонат, диэтилкарбонат, диизопропилкарбонат, фенилкарбонат и трет-бутилкарбонат, этиленкарбонат, пропиленкарбонат.
Из указанного перечня предпочтительно выбирают диметилкарбонат или диэтилкарбонат.
Количество используемого органического карбоната, выраженное по отношению к трифторалкансульфиновой кислоте, обычно, по меньшей мере, равно стехиометрическому количеству.
Таким образом, соотношение между числом молей органического карбоната и числом молей фторалкансульфиновой кислоты изменяется, благоприятно, между 1 и 2 и находится, предпочтительно, в интервале от 1 до 1,2.
Присутствие воды в реакционной смеси влияет на выход реакции. Таким образом, предпочтительно, чтобы способ согласно изобретению осуществлялся в безводных условиях. Необходимо заботиться о том, чтобы реактивы были безводными. Количество воды в среде вплоть до 1% масс., приблизительно, может быть допустимым.
Температуру реакции выбирают таким образом, чтобы она была достаточна для осуществления реакции транс-этерификации и позволяла предотвратить конкурирующую реакцию изомеризации.
Температуру реакции выбирают, предпочтительно, в интервале от 0 до 100°С, и предпочтительно от 60 до 95°С.
Предпочтительно, реакцию проводят при атмосферном давлении.
Равным образом, могут быть использованы немного меньшие или большие значения давления.
Предпочтительно, реакцию проводят в атмосфере инертного газа, которым может быть азот или благородный газ, предпочтительно, аргон: причем азот является предпочтительным, в частности, принимая во внимание его низкую стоимость.
С практической точки зрения, способ согласно изобретению является простым для осуществления.
Различные реагенты могут быть введены в любом порядке.
Предпочтительно, кислоту предпочитают вводить на органический карбонат постепенно, по порциям или непрерывно.
Реакционную среду доводят до желаемой температуры, поддерживая реакционную среду при перемешивании.
Во время реакции происходит образование диоксида углерода, который удаляют в ходе реакции.
Согласно предпочтительному способу осуществления изобретения диоксид углерода удаляют по мере его образования.
Выделившийся диоксид углерода может быть, возможно, захвачен щелочным раствором, например, путем введения в очистную колонну с гидроксидом натрия или гидроксидом калия.
Продолжительность реакции изменяется от 2 до 20 часов, предпочтительно, от 5 до 10 часов.
По окончании реакции получают сложный эфир фторалкансульфиновой кислоты и спирт, который соответствует исходному органическому карбонату.
Сложный эфир фторалкансульфиновой кислоты выделяют из этой реакционной среды согласно обычным методикам разделения, в частности дистилляцией, предпочтительно, при пониженном давлении, изменяющемся, например, от 2 до 200 мбар, или кристаллизацией.
Способ согласно изобретению осуществляют, предпочтительно, в аппарате, способном противостоять коррозии, вызываемой реакционной средой.
С этой целью для части, контактирующей с реакционной средой, выбирают коррозионностойкие материалы, как сплавы на основе молибдена, хрома, кобальта, железа, меди, марганца, титана, циркония, алюминия, углерода и вольфрама, продаваемые под марками HASTELLOY®, или сплавы никеля, хрома, железа, марганца с добавками меди и/или молибдена, поставляемые в продажу под названием INCONEL®, и, в частности, сплавы HASTELLOY С 276 или INCONEL 600, 625 или 718.
Равным образом, можно выбрать нержавеющие стали, такие как аустенитные стали [Robert H. Perry et al., Perry's Chemical Engineers' Handbook, Sixth Edition (1984), page 23-44], и, в частности, нержавеющие стали 304, 304 L, 316 или 316 L. Используют сталь, имеющую содержание никеля самое большее 22% масс., предпочтительно, находящееся в интервале от 6 до 20%, более предпочтительно, находящееся в интервале от 8 до 14%.
Стали 304 и 304 L имеют содержание никеля, изменяющееся в интервале от 8 до 12%, и стали 316 и 316 L имеют содержание никеля, изменяющееся в интервале от 10 до 14%. В частности, прибегают к сталям 316 L.
Можно также прибегнуть к стеклующимся сталям с возможным добавлением ингибиторов коррозии, как, например, диоксида кремния или борной кислоты.
Совокупность различных стадий способа согласно изобретению может быть осуществлена непрерывно или периодически.
Способ согласно изобретению является особенно интересным, так как обладает многими преимуществами.
Указанный способ является простым и экономичным и не приводит к образованию сульфона.
Ниже приведены примеры реализации изобретения. Эти примеры даны для иллюстрации и не носят ограничительного характера.
В примерах определены степень конверсии и полученный выход.
Степень конверсии (СК) (ТТ) соответствует соотношению между числом молей образовавшегося продукта (сложный эфир трифторметансульфиновой кислоты) и числом молей введенного в реакцию субстрата (трифторметансульфиновая кислота).
Выход (ВР)(RR) соответствует соотношению между числом молей образовавшегося продукта (сложный эфир трифторметансульфиновой кислоты) и числом молей введенного в реакцию субстрата (трифторметансульфиновая кислота).
Пример
В стеклянный реактор объемом 20 мл загружали 13,4 г трифторметансульфиновой кислоты (0,1 моль).
Добавляли 5,9 г диэтилкарбоната (0,05 моль) и поддерживали смесь при 90°С в течение 10 часов.
По окончании реакции систему возвращали к комнатной температуре (20°С).
Анализ неочищенной реакционной среды методом ЯМР на ядрах 19F указывал на степень превращения трифлиновой кислоты 49% и выход этилтрифлината 49%.
Над реактором была смонтирована колонка Вигро (Vigreux), и всю систему поддерживали при температуре 58°С под давлением 175 мбар.
Собирали фракцию (9 г), отгонявшуюся при 38°С, которая представляла собой бесцветную жидкость, содержащую 89% масс. этилтрифторметансульфината.
1. Способ получения сложного эфира фторалкансульфиновой кислоты, отличающийся тем, что он включает реакцию фторалкансульфиновой кислоты с органическим карбонатом, приводящую к образованию сложного эфира фторалкансульфиновой кислоты и диоксида углерода, который выделяется в ходе реакции; причемфторалкансульфиновая кислота отвечает следующей формуле: в которой X обозначает атом водорода или атом фтора,n обозначает число в интервале от 1 до 8; и органический карбонат отвечает следующей общей формуле: в которой R1 обозначает:- алкильную группу, линейную или разветвленную, содержащую от 1 до 6 атомов углерода,- циклоалкильную группу, содержащую от 5 до 6 атомов углерода,- циклоалкильную группу, содержащую от 5 до 6 атомов углерода, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,- фенильную группу,- фенильную группу, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,- R2 обозначает:- алкильную группу, линейную или разветвленную, содержащую от 1 до 6 атомов углерода,- циклоалкильную группу, содержащую от 5 до 6 атомов углерода,- циклоалкильную группу, содержащую от 5 до 6 атомов углерода, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,- фенильную группу,- фенильную группу, замещенную одной, двумя или тремя алкильными группами, содержащими от 1 до 4 атомов углерода, и/или одним или двумя атомами галогена,- R1 и R2 вместе могут образовать алкиленовую группу, содержащую от 2 до 6 атомов углерода.
2. Способ по п.1, отличающийся тем, что фторалкансульфиновая кислота представляет собой дифторметансульфиновую кислоту, перфторалкансульфиновую кислоту, которая, предпочтительно, представляет собой трифторметансульфиновую кислоту, перфторбутансульфиновую кислоту, перфтороктансульфиновую кислоту.
3. Способ по п.1, отличающийся тем, что фторалкансульфиновая кислота представляет собой трифторметансульфиновую кислоту.
4. Способ по п.1, отличающийся тем, что органический карбонат отвечает формуле (II), в которой группы R1 и R2 обозначают алкильную группу, содержащую от 1 до 4 атомов углерода, предпочтительно метил, этил, изопропил; циклогексильную группу; фенильную группу: фенильная группа замещена в положениях орто и орто' атомом галогена, предпочтительно хлора или брома, или алкильной группой, линейной или разветвленной, содержащей от 1 до 4 атомов углерода, или группы R1 и R2 образуют алкиленовую группу, предпочтительно этиленовую или пропиленовую группу.
5. Способ по п.1, отличающийся тем, что органический карбонат представляет собой диметилкарбонат, диэтилкарбонат, диизопропилкарбонат, фенилкарбонат и трет-бутилкарбонат, этиленкарбонат, пропиленкарбонат.
6. Способ по п.5, отличающийся тем, что органический карбонат представляет собой диметилкарбонат или диэтилкарбонат.
7. Способ по п.1, отличающийся тем, что количество используемого органического карбоната, выраженное по отношению к трифторалкансульфиновой кислоте, является таким, что соотношение между числом молей органического карбоната и числом молей фторалкансульфиновой кислоты изменяется от 1 до 2 и находится, предпочтительно, в интервале от 1 до 1,2.
8. Способ по п.1, отличающийся тем, что реакцию проводят в безводных условиях.
9. Способ по п.1, отличающийся тем, что температуру реакции выбирают в интервале от 0°C до 100°C, предпочтительно от 60°C до 95°C.
10. Способ по п.1, отличающийся тем, что реакцию проводят при атмосферном давлении в атмосфере инертного газа.
11. Способ по п.1, отличающийся тем, что диоксид углерода удаляют по мере его образования.
12. Способ по п.1, отличающийся тем, что сложный эфир фторалкансульфиновой кислоты выделяют из полученной среды, содержащей сложный эфир фторалкансульфиновой кислоты и спирт, дистилляцией или кристаллизацией.