Пролекарства налмефена
Иллюстрации
Показать всеНастоящее изобретение относится к сложноэфирным пролекарственным формам налмефена формулы (I), где R1 обозначает C6-16алкил или C8-12алкиламино; или его фармацевтически приемлемой кислотно-аддитивной соли. Также в изобретении заявлены фармацевтические композиции, обладающие действием антагониста опиоидного рецептора, включающие фармацевтически приемлемый носитель и терапевтически активное количество соединения формулы (I). В изобретении описываются химические способы получения таких соединений и их использование при лечении расстройств злоупотребления веществами, таких как алкоголизм и алкогольная зависимость, и расстройств импульсивного контроля, таких как патологическое увлечение играми и шопомания. 5 н. и 9 з.п. ф-лы, 5 пр., 1 табл., 1 ил.
Реферат
Настоящее изобретение относится к сложноэфирным пролекарствам налмефена формулы (I), к фармацевтическим композициям, содержащим указанные соединения, к химическим способам получения таких соединений и к их применению для лечения расстройств, связанных с злоупотреблением веществами, таких как алкоголизм и алкогольная зависимость, и расстройств, таких как контроль над побуждениями, патологическое увлечение азартными играми и шопомания.
Налмефен представляет собой антагонист опиоидного рецептора, который был доступен в течение нескольких лет как инъекционный препарат ревекс (Revex®), применяемый для реверсирования эффектов опиоидов и в случаях передозировки опиоидов. Налмефен также описан в литературе как препарат для лечения расстройств, связанных с злоупотреблением веществами, таких как алкогольная зависимость, и расстройств контроля над побуждениями, таких как патологическое увлечение азартными играми и шопомания. Согласно системе IUPAC, он имеет следующее название: 17-циклопропилметил-4,5α-эпокси-6-метиленморфинан-3,14-диол и описывается указанной ниже структурой:
В Arch. Gen. Psychiatry, 56, 719-724 (1999) описывается двойное слепое плацебо-контролируемое исследование алкогольной зависимости, где волонтеры принимали пероральные дозы налмефена по 20 или 80 мг ежедневно в течение 12 недель, для оценки безопасности и эффективности этого препарата.
В публикации Alcoholism: в Clinical and Experimental Research, 31, 1179-1187 (2007), описывается многоцентровое, рандомизированное двойное слепое исследование, проведенное на запущенных алкоголиках, которым было рекомендовано принимать перорально от 10 до 40 мг налмефена, когда у них появлялась потребность в алкоголе. Исследование показало, что налмефен, по всей видимости, является эффективным и безопасным препаратом для снижения потребности в алкоголе у запущенных алкоголиков.
В EP-0250796 описываются пролекарства на основе алифатического, ароматического, карбонатного, карбаматного и сульфонатного сложного эфира большого числа 3-гидроксиморфинанов, которые не имеют горького вкуса и, в этой связи, подходят для использования в режиме перорального введения, такого как буккальное, назальное или сублингвальное введение.
В WO-03/070191 описывается защищенное от вскрытия устройство трансдермальной доставки, используемое при лечении или для предупреждения боли, включающее опиоид. Описываемое устройство для доставки содержит также ацилопиоидный антагонист, который высвобождается, когда токсикоман трясет устройство, с тем чтобы извлечь опиоид из устройства для доставки. Таким образом, опиоидный антагонист притупляет или подавляет эйфорические эффекты опиоида.
К сожалению, коммерчески используемые препараты налмефена создают терапевтически эффективные уровни в плазме крови лишь в течение ограниченного периода времени. Длительно действующие стандартные формы налмефена могли бы быть полезными для терапевтических целей и способствовать соблюдению пациентом предписанной схемы лечения, что очень важно при лечении расстройств злоупотребления веществами и расстройств импульсивного контроля.
Авторы обнаружили, что пролекарственные формы налмефена формулы (I) обеспечивают поддержание терапевтически релевантных уровней налмефена в плазме крови в течение длительного периода времени. В том случае, когда соединения формулы (I) вводятся внутримышечно, они могут обеспечивать поддержание терапевтически релевантных уровней налмефена в плазме крови в течение периода времени от нескольких недель до нескольких месяцев. А в том случае когда соединения формулы (I) вводятся перорально, они могут обеспечивать поддержание терапевтически релевантных уровней налмефена в плазме крови в течение нескольких дней.
Настоящее изобретение относится к соединению формулы (I)
включающему его любую стереохимически изомерную форму, где
R1 обозначает C6-16алкил или C8-12алкиламино;
или его фармацевтически приемлемая кислотно-аддитивная соль или сольват.
В контексте настоящего описания действительны следующие определения:
C8-12алкил обозначает прямые и разветвленные насыщенные углеводородные радикалы, содержащие от 8 до 12 атомов углерода, такие как, например, октил, нонил, децил, ундецил, додецил и т.п.; -C6-16алкил обозначает прямые и разветвленные насыщенные углеводородные радикалы, содержащие от 6 до 16 атомов углерода, такие как, например, гексил, гептил, октил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил и гексадецил и т.п.;
-C13-16алкил обозначает прямые и разветвленные насыщенные углеводородные радикалы, содержащие от 13 до 16 атомов углерода, такие как, например, тридецил, тетрадецил, пентадецил и гексадецил и т.п.
Термин "стереохимически изомерные формы" в контексте настоящего описания обозначает все возможные изомерные формы, которые могут существовать у соединений формулы (I). Если особо не оговорено или конкретно не указано иное, химическое название соединений относится к смеси всех возможных стереохимически изомерных форм, где указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. При этом стереогенные центры могут иметь R- или S-конфигурацию. Стереохимически изомерные формы соединений формулы (I) вполне определенно входят в область настоящего изобретения.
Абсолютная стереохимическая конфигурация соединений формулы (I) и используемых при их изготовлении промежуточных соединений может быть без труда определена специалистами в данной области с помощью известных методов, таких как, например, дифракция рентгеновских лучей.
Указанные выше фармацевтически приемлемые кислотно-аддитивные соли включают, в контексте настоящего описания, терапевтически активные нетоксичные формы кислотно-аддитивной соли, которые способны образовать соединения формулы (I). Указанные фармацевтически приемлемые кислотно-аддитивные соли могут быть получены при обработке основной формы соединения подходящей кислотой. Подходящие для этого кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например, хлористоводородная или бромистоводородная кислота, серную, азотную, фосфорную и аналогичные кислоты; или органические кислоты, такие как, например, уксусная, пропаноевая, гидроксиуксусная, молочная, пировиноградная, щавелевая (т.е. этандиоевая кислота), малоновая, янтарная (т.е. бутандиоевая кислота), малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, пара-толуолсульфоновая, цикламовая, салициловая, пара-аминосалициловая, памоевая и другие кислоты.
И, наоборот, указанные солевые формы при обработке соответствующим основанием могут быть превращены в свободную основную форму.
Соединения формулы (I) могут существовать как в виде несольватированных, так и сольватированных форм. Термин «сольват» используется в настоящем описании для обозначения молекулярной ассоциации, включающей соединение по настоящему изобретению и одну или несколько молекул фармацевтически приемлемого растворителя, например, воды или этанола. Термин «гидрат» используется в тексте настоящего описания, когда указанный растворитель представляет собой воду.
Пролекарство представляет собой фармакологическое вещество (лекарственное средство), которое вводится в неактивной (или в значительно менее активной) форме. Будучи введенным, пролекарство метаболизируется in vivo до своей активной исходной лекарственной формы. Применение пролекарств зачастую полезно, поскольку в некоторых ситуациях их легче ввести в организм, чем исходное лекарственное средство. Они могут, например, демонстрировать биодоступность при пероральном введении, тогда как исходное средство такой способностью не обладает. Пролекарство может также иметь повышенную растворимость в составе фармацевтических композиций в сравнении с исходным лекарственным средством или может обладать улучшенными вкусовыми качествами или его удобнее ввести в состав композиции.
Настоящее изобретение в одном варианте своего осуществления относится к соединениям формулы (I), где R1 обозначает C13-16алкил или C8-12алкиламино.
В другом варианте настоящее изобретение относится к тем соединениям формулы (I), где применимы одно или несколько из указанных ниже ограничений:
а) R1 обозначает С7алкил, C9алкил, C11алкил или C15aлкил; или
b) R1 обозначает н-гептил, н-нонил, н-ундецил или н-пентадецил; или
c) R1 обозначает C10алкиламино; или
d) R1 обозначает н-дециламино.
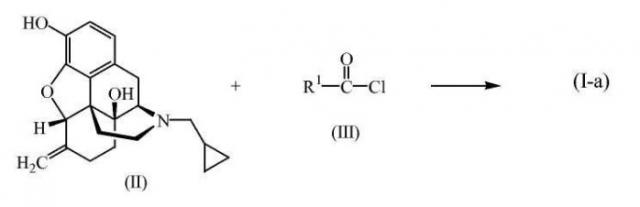
Соединения формулы (I-a), определяемые как соединения формулы (I), где R1 обозначает C6-16алкил, могут быть получены по известным методам этерификации при осуществлении реакции налмефена (II) с ацилгалогенидом формулы (III) в присутствии основания, с отбором кислоты, образующейся в ходе реакции. Заместитель R1 в ацилгалогениде формулы (III) определяется как C6-16алкил.
Соединения формулы (I-b), определяемые как соединения формулы (I), где R1 обозначает C8-12алкиламино, могут быть получены при осуществлении реакции налмефена (II) с изоцианатом формулы (IV).
Соединения по настоящему изобретению демонстрируют преимущества, определяемые тем, что они представляют собой длительно действующий антагонист опиоидного рецептора, которые применимы для лечения расстройств, связанных с злоупотреблением веществами, таких как алкоголизм и алкогольная зависимость, и расстройств контроля над побуждениями, таких как патологическое увлечение азартными играми и шопомания. Эта способность может быть подтверждена, например, при измерении содержания в плазме данных соединений после внутримышечного введения собакам, как описано в примере С.1.
Было также показано, что при пероральном введении пролекарственного соединения формулы (I) содержание в плазме налмефена определяется в течение более чем 8 дней после введения пролекарственного соединения формулы (I), в сравнении с ситуацией, где пероральное введение самого по себе налмефена приводило лишь к нескольким часам такого выявления.
В этой связи, соединения по настоящему изобретению дают возможность осуществлять введение с относительно длительными временными интервалами, такими как несколько дней, несколько недель, вплоть до нескольких месяцев, при этом фактическое время введения зависит от физической природы используемого соединения, способа введения, состава лекарственной формы фармацевтического препарата и состояния субъекта, подлежащего лечению. Соответственно, соединения по настоящему изобретению позволяют осуществлять более эффективную терапию: пролонгированное высвобождение налмефена облегчает поддержание стабильной концентрации в плазме при наличии нетоксичного терапевтически эффективного уровня, а способ введения способствует соблюдению субъектом предписанной схемы лечения. Соответственно, соединения по настоящему изобретению могут использоваться в качестве лекарственного средства, характеризующегося длительным высвобождением, или в качестве лекарственного средства с пролонгированным высвобождением.
Выражение, относящееся к «терапевтически релевантным» или «терапевтически эффективным» концентрациям в плазме налмефена, означает, что концентрация в плазме налмефена (свободного налмефена, который высвободился из пролекарственных соединений формулы (I) по настоящему изобретению) должна быть выше примерно 0,1 нг/мл.
В этой связи соединения формулы (I) по настоящему изобретению или их фармацевтически приемлемая кислотно-аддитивная соль или сольват могут использоваться в качестве лекарственного средства, в частности, могут использоваться в качестве лекарственного средства, применяемого для лечения расстройств, связанных с злоупотреблением веществами, таких как алкогольная зависимость и алкоголизм, и расстройств контроля над побуждениями, таких как патологическое увлечение азартными играми и шопомания. Кроме того, соединения формулы (I) по настоящему изобретению могут использоваться в качестве лекарственного средства, применяемого для ослабления потребности в алкоголе и его употребления у зависимых от алкоголя пациентов, а также для уменьшения приема алкоголя у зависимых пациентов.
Настоящее изобретение также относится к применению соединения формулы (I) или его фармацевтически приемлемой соли для получения лекарственного средства, предназначенного для лечения расстройств, связанных с злоупотреблением веществами, таких как алкогольная зависимость и алкоголизм, и расстройств контроля над побуждениями, таких как патологическое увлечение азартными играми и шопомания.
Кроме того, настоящее изобретение относится к способу лечения расстройств, связанных с злоупотреблением веществами или расстройств контроля над побуждениями у субъекта-млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли. Расстройства злоупотребления веществами включают алкогольную зависимость и алкоголизм. Расстройства контроля над побуждениями включают патологическое увлечение азартными играми и шопоманию.
Термины «лечение» и «терапия» в контексте настоящего описания обозначают лечебный, паллиативный и профилактический варианты лечения, которые включают реверсирование, облегчение, подавление прогрессирования или предупреждение развития заболевания, расстройства или состояния, к которым такой термин относится, или одного или нескольких симптомов такого заболевания, расстройства или состояния.
Дополнительно, настоящее изобретение относится к фармацевтическим композициям, включающим по меньшей мере один фармацевтически приемлемый носитель и терапевтически эффективное количество соединения формулы (I).
Для целей получения фармацевтических композиций по настоящему изобретению эффективное количество конкретного соединения в форме свободного основания или кислотно-аддитивной соли в качестве активного ингредиента объединяют при тщательном перемешивании по меньшей мере с одним фармацевтически приемлемым носителем, где указанный носитель может быть представлен в виде множества различных форм, в зависимости от формы препарата, желательного для введения препарата. Указанные фармацевтические композиции представляют собой стандартную лекарственную форму, подходящую предпочтительно для перорального введения, ректального введения, чрескожного введения или для парентерального введения инъекцией.
Так, например, при изготовлении композиций в виде пероральных лекарственных форм могут использоваться любые стандартные жидкие фармацевтические носители, такие как, например, вода, гликоли, масла, спирты и т.п., в случае изготовления жидких пероральных препаратов, таких как суспензии, сиропы, эликсиры и растворы; или твердые фармацевтические носители, такие как крахмалы, сахара, каолин, смазывающие вещества, связующие вещества, средства, способствующие разложению, и т.п., в случае порошков, пилюль, капсул и таблеток. В связи с легкостью введения таблетки и капсулы представляют собой наиболее удобную пероральную стандартную лекарственную форму, и в этом случае, что очевидно, используются твердые фармацевтические носители. В случае парентеральных инъецируемых композиций используемый фармацевтический носитель может в основном включать стерильную воду, хотя в композицию могут быть включены и другие ингредиенты для повышения растворимости активного ингредиента. Инъецируемые растворы могут быть получены, например, при использовании фармацевтического носителя, который включает солевой раствор, раствор глюкозы или их смесь. Инъецируемые суспензии могут быть также получены при использовании соответствующих жидких носителей, суспендирующих агентов и т.п. В композициях, подходящих для чрескожного введения, указанный фармацевтический носитель может необязательно включать средство, усиливающее проникновение, и/или подходящий смачивающий агент, необязательно в сочетании с небольшими пропорциями подходящих добавок, которые не оказывают выраженного неблагоприятного эффекта на кожу. Такие добавки могут быть выбраны для того, чтобы сделать более удобным нанесение активного ингредиента на кожу и/или облегчить получение желательных композиций. Указанные местные композиции могут вводиться различными способами, такими как трансдермальный пластырь, пластырь спот-он или мазь. Аддитивные соли соединений формулы (I), в связи с их повышенной водорастворимостью относительно соответствующей формы основания, в большей мере подходят для изготовления водных композиций.
Это особенно предпочтительно в процессе изготовления фармацевтических композиций по настоящему изобретению в виде стандартной лекарственной формы, в связи с легкостью введения и однородностью получаемой формы. Выражение «стандартная лекарственная форма» в контексте настоящего описания относится к физически дискретным единицам, подходящим в качестве стандартных дозировок, где каждая единица содержит заданное количество активного ингредиента, рассчитанного таким образом, чтобы это количество создавало желательный терапевтический эффект в сочетании с требуемым фармацевтическим носителем. Примеры таких стандартных лекарственных форм включают таблетки (в том числе таблетки с насечкой или с нанесенным на них покрытием), капсулы, пилюли, пакетики с порошком, облатки, инъецируемые растворы или суспензии, мерные дозы, соответствующие чайной ложке с верхом, столовой ложке с верхом и т.п., а также их определенные сочетанные варианты.
Для целей перорального введения фармацевтические композиции по настоящему изобретению могут быть представлены в виде твердых лекарственных форм, например, таблеток (как проглатываемых, так и жевательных таблеток), капсул или желатиновых капсул, получаемых традиционными способами, в сочетании с фармацевтически приемлемыми эксципиентами и носителями, такими как связующие вещества (например, прежелатинизированный кукурузный крахмал, поливинилпирролидон, гидроксипропилметилцеллюлоза и т.п.), наполнители (например, лактоза, микрокристаллическая целлюлоза, фосфат кальция и т.п.), смазывающие вещества (например, стеарат магния, тальк, диоксид кремния и т.п.), средства, способствующие разложению (например, картофельный крахмал, натрий-крахмалгликолят и т.п.), смачивающие вещества (например, лаурилсульфат натрия) и т.п. Такие таблетки могут также содержать покрытие, нанесенное по известным в данной области способам.
Жидкие препараты для перорального введения могут быть представлены в виде, например, растворов, сиропов или суспензий, или они могут быть изготовлены в виде сухого продукта, который впоследствии смешивается с водой и/или другим подходящим жидким носителем перед употреблением. Такие жидкие препараты могут быть получены стандартными способами, необязательно при использовании других фармацевтически приемлемых добавок, таких как суспендирующие агенты (например, сироп сорбита, метилцеллюлоза, гидроксипропилметилцеллюлоза или гидрогенизированные пищевые жиры), эмульгаторы (например, лецитин или аравийская камедь), неводные носители (например, миндальное масло, сложные масляные эфиры или этиловый спирт), подсластители, вкусовые вещества, средства, улучшающие вкус, и консерванты (например, метил- или пропил-пара-гидроксибензоат или сорбиновая кислота).
Фармацевтически приемлемые подсластители, используемые в фармацевтических композициях по настоящему изобретению, предпочтительно включают по меньшей мере один подсластитель с интенсивным вкусом, такой как аспартам, калий-ацесульфам, натрий-цикламат, алитам, гидроксихалконовый подсластитель, монелин, стевиозид-сукралоза (4,1'6'-трихлор-4,1',6'-тридезоксигалактосахароза) или предпочтительно, сахарин, натрий- или кальций-сахарин, и необязательно по меньшей мере один объемный подсластитель, такой как сорбит, маннит, фруктоза, сахароза, мальтоза, изомальтоза, глюкоза, гидрогенизированный глюкозный сироп, ксилит, карамель или мед. Подсластители с интенсивным вкусом традиционно используются в низких концентрациях. Так, например, в случае натрий-сахарина, указанная концентрация может варьировать от примерно 0,04% до 0,1% (вес/объем) от готовой композиции. Объемный подсластитель может эффективно использоваться в более высоких концентрациях и варьировать от примерно 10% до примерно 35%, предпочтительно от примерно 10% до примерно 15% (вес/объем).
Фармацевтически приемлемые вкусовые добавки, которые могут маскировать ингредиенты с горьким вкусом в композициях с низкой дозой, предпочтительно включают вкусовые вещества на основе фруктов, такие как вкусовые вещества на основе вишни, малины, черной смородины или клубники. Сочетание двух вкусовых веществ может приводить к очень хорошим результатам. В композициях с высокой дозой могут потребоваться более сильные фармацевтически приемлемые вкусовые вещества, такие как карамель, шоколад, освежающая мята, фантазийные композиции и т.п. Каждое вкусовое вещество может присутствовать в готовой композиции в концентрации, варьирующей от примерно 0,05% до 1% (вес/объем). При этом с успехом используются сочетания указанных более сильных вкусовых веществ. Предпочтительно, используются вкусовые вещества, которые не подвергаются какому-либо изменению или не теряют свой вкус и/или цвет в условиях данной композиции.
Соединения формулы (I) могут быть изготовлены с получением композиции для парентерального введения путем инъекции, обычно внутривенной, внутримышечной или подкожной инъекции, например, инъекции болюсом или непрерывной внутривенной инфузии. Композиции для инъекции могут быть представлены в стандартной лекарственной форме, например, могут иметь вид ампул или многодозовых контейнеров, включающих добавленный в них консервант. Они могут иметь вид суспензий, растворов или эмульсий в масляных или водных носителях и могут содержать включаемые при изготовлении композиций средства, такие как средства, способствующие поддержанию изотонических свойств, суспендирующие агенты, стабилизирующие средства и/или средства, способствующие диспергированию. В альтернативном варианте активный ингредиент может присутствовать в порошковой форме, которая впоследствии смешивается с подходящим носителем, например, стерильной, свободной от пирогенов водой, перед употреблением. Композиции для внутримышечного или подкожного введения представляют особый интерес. Такие фармацевтические композиции не должны вызывать выраженного раздражения тканей, или они вообще не должны вызывать раздражение тканей или воспаление в месте инъекции. Подходящие растворители включают, например, кунжутное масло или миглиол.
Соединения формулы (I) могут быть также изготовлены в виде ректальных композиций, таких как суппозитории или удерживающие клизмы, которые, например, содержат стандартные основы для суппозиториев, такие как какао-масло и/или другие глицериды.
Экспериментальная часть
Пример В.1
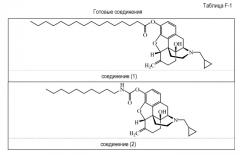
Добавляют по каплям пальмитоилхлорид (16,1 мл, 53,2 ммоль) в течение 30 минут при температуре окружающей среды к перемешанной смеси гидрохлорида налмефена (20,0 г, 1,0 эквивалент), толуола (400 мл, 20 мл/г) и триэтиламина (16,3 мл, 2,2 эквивалентов) в инертной атмосфере. Перемешивание при температуре окружающей среды продолжают в течение 16 часов. После этого, реакционную смесь промывают водой (400 мл, 20 мл/г). После разделения фаз органический слой сушат над сульфатом магния, фильтруют и фильтрат концентрируют при пониженном давлении. Выход: 30,8 г (95%).
ЯМР:
1H-ЯМР (400 МГц, ДМСО-d6) δ м.д. 0,08-0,16 (м, 2H), 0,43-0,53 (м, 2H), 0,81-0,89 (м, 4H), 1,14-1,42 (м, 26H), 1,53 (дт, J=12,78, 3,65, 3,46 Гц, 1H), 1,59-1,67 (м, J=7,55, 7,55, 7,55, 7,55 Гц, 2H), 1,96 (тд, J=12,02, 3,65 Гц, 1H), 2,07 (дт, J=13,66, 3,08, 2,90 Гц, 1H), 2,24 (тд, J=12,53, 4,91 Гц, 1H), 2,35 (т, J=6,04 Гц, 2H), 2,43-2,49 (м, 1H), 2,54 (т, J=7,43 Гц, 2H), 2,53-2,61 (м, 1H) 2,62-2,68 (м, 1H), 3,03 (дд, J=12,09, 6,55 Гц, 2H), 4,80 (д, J=1,76 Гц, 1H), 4,91 (ушир.с, 1H), 4,96 (с, 1H), 5,05 (д, J=1,26 Гц, 1H), 6,66 (д, J=8,06 Гц, 1H), 6,77 (д, J=8,31 Гц, 1Н).
LC-MS
HR-MS (ES+): Рассчитано для C37H56NO4 +: 578,4209. Найдено: 578,4199.
Элементный анализ
Аналитически рассчитано для C37H55NO4: С: 76,91; H: 9,59; N: 2,42. Найдено: С: 77,01; H: 9,96; N: 1,89.
Пример B.2
Суспензию гидрохлорида налмефена (20,0 г, 53,2 ммоль), толуола (400 мл, 20 мл/г), триэтиламина (8,9 мл, 1,2 эквивалента) и децилизоцианата (13,3 мл, 1,2 эквивалента) кипятят с обратным холодильником в течение 16 часов. Добавляют еще три порции децилизоцианата (соответственно, 2,2 мл, 0,2 эквивалента; 2,2 мл, 0,2 эквивалента и 4,4 мл, 0,4 эквивалента) в течение следующих 24 часов при температуре кипячения с обратным холодильником. После охлаждения реакционной смеси до температуры окружающей среды указанную смесь промывают водой (400 мл, 20 мл/г). Органический слой сушат над сульфатом магния, фильтруют и концентрируют при пониженном давлении. Остаток очищают при проведении хроматографии на колонке (диоксид кремния 60Ǻ 25-40 мкг, 100% этилацетат) с получением 17,4 г (63%) соединения (2).
ЯМР:
1H ЯМР (400 МГц, ДМСО-d6) δ м.д. 0,06-0,17 (м, 2H), 0,41-0,53 (м, 2H), 0,78-0,91 (м, 4H), 1,22-1,31 (м, 16H), 1,40-1,48 (м, 2H), 1,52 (дт, J=12,78, 3,56 Гц, 1H), 1,97 (тд, J=11,96, 3,53 Гц, 1H), 2,06 (дт, J=13,60, 3,53 Гц, 1H), 2,23 (тд, J=12,46, 5,04 Гц, 1H), 2,35 (дд, J=6,29, 3,78 Гц, 2H), 2,43-2,49 (м, 1H), 2,56 (дд, J=18,88, 5,79 Гц, 1H), 2,65 (дд, J=11,71, 4,15 Гц, 1H), 2,97-3,08 (м, 4H), 4,79 (д, J=1,51 Гц, 1H), 4,90 (с, 1H), 4,94 (с, 1H), 5,10 (д, J=1,01 Гц, 1H), 6,62 (д, J=8,06 Гц, 1H), 6,75 (д, J=8,31 Гц, 1H), 7,63 (т, J=5,67 Гц, 1H).
LC-MS:
HR-MS (ES+): Рассчитано для C32H47N2O4 +: 523,3536. Найдено: 523,3517.
Элементный анализ:
Аналитически рассчитано для C32H46N2O4: C: 73,53; H: 8,87; N: 5,36. Найдено: C: 74,73; H: 9,45; N: 5,58.
Пример B.3
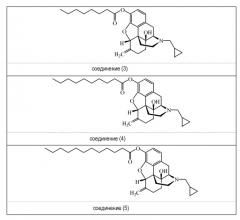
Добавляют по каплям октаноилхлорид (2,27 мл, 13,3 ммоль) в течение 30 минут при температуре окружающей среды к перемешанной смеси гидрохлорида налмефена (5 г, 1,0 эквивалент), толуола (100 мл, 20 мл/г) и триэтиламина (4,08 мл, 2,2 эквивалента) в инертной атмосфере. Перемешивание при температуре окружающей среды продолжают в течение 16 часов. Вносят дополнительно еще 0,15 мл (0,07 эквивалента) октаноилхлорида. Раствор перемешивают в течение 4 часов при температуре окружающей среды до завершения процесса превращения. Затем реакционную смесь промывают водой (400 мл, 20 мл/г). После разделения фаз органический слой сушат над сульфатом магния и фильтрат концентрируют при пониженном давлении с получением 5,98 г (96%) соединения (3).
ЯМР:
1H ЯМР (400 МГц, ДМСО-d6) δ м.д. 0,02-0,18 (м, 2Н), 0,38-0,55 (м, 2H), 0,76-0,94 (м, 4H), 1,18-1,41 (м, 10H), 1,53 (дт, J=12,78, 3,30 Гц, 1H), 1,58-1,70 (м, 2H), 1,96 (тд, J=12,09, 3,78 Гц, 1H), 2,07 (тд, J=13,72, 3,15, 3,02 Гц, 1H), 2,24 (тд, J=12,59, 5,04 Гц, 1H), 2,31-2,40 (м, 2H), 2,45-2,50 (м, 1H), 2,54 (т, 2H), 2,53-2,61 (м, 1H), 2,65 (дд, J=11,83, 4,28 Гц, 1H), 3,03 (дд, J=12,09, 6,55 Гц, 2H), 4,80 (д, J=1,76 Гц, 1H), 5,03 (ушир.с, 1H), 4,96 (с, 1H), 5,05 (д, J=1,26 Гц, 1H), 6,66 (д, J=8,31 Гц, 1H), 6,76 (д, J=8,06 Гц, 1H).
LC-MS: HRMS (ES+): Рассчитано для C29H39NO4 +: 466,2957. Найдено: 466,2967.
Пример B.4
Добавляют по каплям деканоилхлорид (2,77 мл, 13,3 ммоль) в течение 30 минут при температуре окружающей среды к перемешанной смеси гидрохлорида налмефена (5 г, 1,0 эквивалента), толуола (100 мл, 20 мл/г) и триэтиламина (4,08 мл, 2,2 эквивалента) в инертной атмосфере. Перемешивание при температуре окружающей среды продолжают в течение 16 часов. Далее реакционную смесь промывают водой (400 мл, 20 мл/г). После разделения фаз органический слой сушат над сульфатом магния, фильтруют и фильтрат концентрируют при пониженном давлении с получением 6,31 г (96%) соединения (4).
ЯМР:
1H ЯМР (400 МГц, ДМСО-d6) δ м.д. 0,09-0,15 (м, 2H), 0,43-0,52 (м, 2H), 0,82-0,89 (м, 4H), 1,15-1,42 (м, 14H), 1,53 (дт, J=12,84, 3,40 Гц, 1H), 1,63 (кв., J=7,30 Гц, 2H), 1,96 (тд, J=12,09, 3,78 Гц, 1H), 2,07 (дт, J=13,60, 3,27 Гц, 1H), 2,24 (тд, J=12,53, 5,16 Гц, 1H), 2,30-2,40 (м, 2H), 2,44-2,49 (м, 1H), 2,54 (т, J=7,55 Гц, 2H), 2,53-2,61 (м, 1H), 2,65 (дд, J=11,83, 4,28 Гц, 1H), 3,03 (дд, J=12,09, 6,55 Гц, 2H), 4,96 (ушир.с, 1H), 4,80 (д, J=1,76 Гц, 1H), 4,97 (с, 1H), 5,05 (д, J=1,51 Гц, 1H), 6,66 (д, J=8,06 Гц, 1H), 6,75-6,78 (м, 1H).
LC-MS: HRMS (ES+): Рассчитано для C31H43NO4 +: 494,3270. Найдено: 494,3265.
Пример B.5
Добавляют по каплям додеканоилхлорид (3,12 мл, 13,3 ммоль) в течение 30 минут при температуре окружающей среды к перемешанной смеси гидрохлорида налмефена (5 г, 1,0 эквивалента), толуола (100 мл, 20 мл/г) и триэтиламина (4,08 мл, 2,2 эквивалента) в инертной атмосфере. Перемешивание при температуре окружающей среды продолжают в течение 16 часов. Затем реакционную смесь промывают водой (400 мл, 20 мл/г). После разделения фаз органический слой сушат над сульфатом магния, фильтруют и фильтрат концентрируют при пониженном давлении с получением 6,36 г (92%) соединения (5).
ЯМР:
1H ЯМР (400 МГц, ДМСО-d6) δ м.д. 0,08-0,16 (м, 2H), 0,44-0,51 (м, 2H), 0,81-0,89 (м, 4H), 1,15-1,42 (м, 18H), 1,53 (дт, J=12,78, 3,30 Гц, 1H), 1,63 (кв., J=7,43 Гц, 2H), 1,96 (тд, J=12,09, 3,53 Гц, 1H), 2,06 (дт, J=13,60, 3,15 Гц, 1H), 2,24 (тд, J=12,46, 5,04 Гц, 1H), 2,29-2,40 (м, 2H), 2,45-2,49 (м, 1H), 2,53 (т, J=7,68 Гц, 2H), 2,53-2,60 (м, 1H), 2,65 (дд, J=11,96, 4,41 Гц, 1H), 3,03 (дд, J=11,96, 6,67 Гц, 2H), 4,99 (ушир.с, 1H), 4,80 (д, J=1,76 Гц, 1H), 4,96 (с, 1H), 5,05 (д, 1H), 6,66 (д, J=8,06 Гц, 1H), 6,76 (д, J=8,06 Гц, 1H).
LC-MS: HRMS (ES+): Рассчитано для C33H47NO4 +: 522,3583. Найдено: 522,3590.
С.1 Фармакокинетические (ФК) исследования in vivo на собаках (в/м инъекция): плазменные уровни налмефена
Проводят однократную внутримышечную инъекцию налмефена, соединения (1) или соединения (2), в концентрации 20 мг эквивалента налмефена/мл в кунжутном масле или в миглиоле трем собакам в дозе, равной 1 мг эквивалента налмефена/кг веса тела.
В качестве оцениваемого варианта сравнения используют композицию с быстрым высвобождением (IR) налмефена в концентрации 0,40 мг/мл в солевом растворе, путем внутримышечной инъекции (в/м) однократной дозы в количестве 0,02 мг эквивалента налмефена/кг веса тела.
Отбирают образцы крови в течение 27 дней в случае введения дозы композиции пролекарства и в течение 48 часов после введения дозы композиции с быстрым высвобождением налмефена. Образцы крови обрабатывают с получением плазмы. Далее указанные образцы плазмы анализируют по отдельности на наличие налмефена с использованием установленного LC-MS/MS-метода.
Анализ полученных фармакокинетических данных проводят на профилях индивидуальных концентраций плазмы по методу фармакокинетического анализа без компартментализации с использованием валидированного программного обеспечения WinNonlin (v. 4.0.1a).
Результаты:
Плазменные профили налмефена (нг/мл) после внутримышечного (в/м) введения дозы соединения (1) или IR композиции самого налмефена показаны на фиг.1.
Плазменные концентрации налмефена определялись до 20 дней после введения дозы соединения (2) и в течение 27 дней после введения дозы соединения (1).
C.2. Фармакокинетические (ФК) исследования in vivo на собаках (пероральное введение): плазменные уровни налмефена
Дозы по 10 мг/кг или 20 мг/кг веса тела соединения формулы (I) или самого налмефена в растворе 20% HP-β-CD (гидроксипропил-β-циклодекстрины) вводили собакам перорально.
Образцы крови отбирали в течение 192 часов после перорального введения. Образцы крови обрабатывали с получением плазмы. Плазменные образцы анализировали по отдельности на наличие налмефена с использованием установленного LC-MS/MS-метода.
Плазменная концентрация налмефена определялась в течение 192 часов после введения дозы соединения (2).
Описание чертежей
На фиг.1 показана плазменная концентрация налмефена (нг/мл), определяемая при измерении в течение 28-дневного периода после в/м введения композиции, содержащей налмефен и соединение (1).
1. Соединение формулы (I) где R1 обозначает C6-16алкил или C8-12алкиламино;или его фармацевтически приемлемая кислотно-аддитивная соль.
2. Соединение по п.1, где R1 обозначает C7алкил, C9алкил, С11алкил или C15алкил.
3. Соединение по п.1, где R1 обозначает C10алкиламино.
4. Соединение по п.1, представляющее собойили или или или
5. Соединение по п.1, представляющее собой
6. Фармацевтическая композиция, обладающая действием антагониста опиоидного рецептора, включающая фармацевтически приемлемый носитель и терапевтически активное количество соединения по любому из пп.1-5.
7. Способ получения фармацевтической композиции по п.6, отличающийся тем, что терапевтически активное количество соединения по любому из пп.1-5 тщательно перемешивают с фармацевтически приемлемым носителем.
8. Соединение по любому из пп.1-5, предназначенное для лечения расстройств, связанных с злоупотреблением веществами и расстройств контроля над побуждениями.
9. Соединение по п.8, где указанное соединение вводится внутримышечно или подкожно.
10. Соединение по любому из пп.1-5, предназначенное для получения лекарственного средства для лечения расстройств, связанных с злоупотреблением веществами, таких как алкоголизм и алкогольная зависимость, и расстройств контроля над побуждениями, таких как патологическое увлечение играми и шопомания.
11. Соединение по п.10, предназначенное для получения лекарственного средства, где указанное лекарственное средство вводится внутримышечно или подкожно.
12. Соединение по п.11, предназначенное для получения лекарственного средства, где указанное лекарственное средство представляет собой лекарственное средство с замедленным высвобождением.
13. Способ получения соединения формулы (I-a), представляющего собой соединение формулы (I) по п.1, в котором R1 обозначает C6-16алкил, включающий этерификацию, которая может быть проведена известными методами путем взаимодействия гидрохлорида налмефена (II) с ацилгалогенидом формулы (III) в присутствии основания, с отбором кислоты, высвобождаемой в ходе реакции
14. Способ получения соединения формулы (I-b), представляющего собой соединение формулы (I), где R1 обозначает C8-12алкиламино, включающий взаимодействие гидрохлорида налмефена (II) с изоцианатом формулы (IV)