Гели на основе гиалуроновой кислоты, включающие обезболивающие агенты
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности и представляет собой способ получения композиции наполнителя мягких тканей, включающий следующие стадии: получение компонента ГК (гиалуроновой кислоты), перекрестно-сшитого с помощью по меньшей мере одного перекрестно-сшивающего агента, выбранного из группы, состоящей из 1,4-бутандиолдиглицидильного эфира (БДДЭ), 1,4-бис(2,3-эпоксипропокси)бутана, 1,4-бисглицидилоксибутана, 1,2-бис(2,3-эпоксипропокси)этилена и 1-(2,3-эпоксипропил)-2,3 эпоксициклогексана; доведение рН указанного компонента ГК до pH больше приблизительно 7,2; и добавление раствора, содержащего лидокаин, к указанному компоненту ГК, имеющему указанный доведенный рН, с получением указанной композиции наполнителя мягких тканей. Изобретение обеспечивает улучшенную стабильность и когезионность. 2 н. и 10 з.п. ф-лы, 5 пр., 4 табл., 9 ил.
Реферат
Перекрестная ссылка на родственные заявки на изобретения
В этой заявке на изобретение заявлен приоритет предварительной заявки на патент США номер 61/085956, поданной 4 августа 2008 года, предварительной заявки на патент США номер 61/087934, поданной 11 августа 2008 года, предварительной заявки на патент США номер 61/096278, поданной 11 сентября 2008 года, не предварительной заявки на патент США номер 12/393768, поданной 26 февраля 2009 года, и не предварительной заявки на патент США номер 12/393884, поданной 26 февраля 2009 года, полное содержание которых включено здесь путем ссылки.
Область изобретения
Настоящее изобретение в общем относится к инъецируемым наполнителям мягких тканей и более конкретно относится к кожным и подкожным наполнителям на основе гиалуроновой кислоты, включающим обезболивающий агент.
Предшествующий уровень техники
Общеизвестно, что по мере старения людей на лице начинают отражаться эффекты силы тяжести, солнечного воздействия и многолетних движений лицевой мускулатуры, таких как улыбка, нахмуривание бровей, жевание и прищуривание глаз. Нижележащие ткани, которые придают коже молодой внешний вид, начинают разрушаться, часто приводя в результате к морщинкам от смеха, морщинкам от улыбки, эффекту "гусиных лапок" и лицевым морщинам, которые часто называются "эффектами старения".
В попытках лечить или корректировать эффекты старения разработаны наполнители мягких тканей, способствующие заполнению лицевых линий и складок и восстановлению утраты объема ткани вследствие утраты жира. Наполнители мягких тканей, таким образом, временно восстанавливают более мягкий более молодой внешний вид.
В идеале, наполнители мягких тканей являются стойкими, мягкими, сглаженными и имеют естественный внешний вид, будучи имплантированными в кожу или под кожу. Кроме того, наполнители мягких тканей легко имплантировать пациенту с использованием иглы тонкого калибра и они требуют низкой силы выталкивания для инъекции. Идеальные наполнители также могут не вызывать неблагоприятных побочных действий и могут быть инъецированы с минимальным дискомфортом для пациента или при отсутствии дискомфорта.
Основанные на коллагене наполнители мягких тканей разработаны около 20 лет назад, и в течение некоторого времени наполнители, основанные на бычьем коллагене, представляли собой единственные кожные наполнители, которые одобрены U.S. Food and Drug Administration (FDA) (Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов). Поскольку эти кожные наполнители основаны на бычьем материале, один из основных недостатков заключается в потенциальных аллергических реакциях у пациентов. Полагают, что приблизительно 3-5% людей проявляют серьезные аллергические реакции на бычий коллаген, таким образом требуя осторожного тестирования перед использованием этих наполнителей в отношении любого конкретного лица. Дополнительно к аллергическим реакциям основанные на коллагене наполнители быстро деградируют после инъекции и требуют частых введений для поддержания более гладкого, более молодого внешнего вида.
В феврале 2003 года композиции наполнителей на основе человеческого коллагена получили одобрение FDA. Эти коллагены обеспечивают преимущество, заключающееся в значительно уменьшенном риске аллергических реакций. Тем не менее, несмотря на уменьшенную частоту аллергических реакций, наполнители на основе человеческого коллагена все же страдают от быстрой деградации инъецированного продукта.
Поиск наполнителей, которые не вызывают аллергические реакции и поддерживают более гладкий более молодой внешний вид, привел к разработке продуктов, на основе гиалуроновой кислоты (ГК). В декабре 2003 года первый наполнитель на основе ГК был одобрен FDA. За ним быстро последовала разработка других наполнителей на основе ГК.
ГК, также известный как гиалуронан, представляет собой встречающийся в природе водорастворимый полисахарид, в частности глюкозаминогликан, который представляет собой основной компонент внеклеточного матрикса и широко распространен в животных тканях. ГК обладает превосходной биосовместимостью и не вызывает аллергические реакции после имплантации пациенту. Дополнительно, ГК обладает способностью связываться с большими количествами воды, превращая ее в превосходный агент, придающий объем мягким тканям.
Разработка наполнителей на основе ГК, которые демонстрируют идеальные свойства in vivo, а также идеальную хирургическую применимость, как оказалось, является трудной. Например, наполнители на основе ГК, которые демонстрируют желаемые свойства стабильности in vivo, могут быть настолько вязкими, что инъекция через иглы с тонким калибром, является трудной. Наоборот, наполнители на основе ГК, которые относительно легко инъецировать через иглы с тонким калибром, часто обладают относительно более плохими свойствами стабильности in vivo.
Один из способов преодоления этой проблемы заключается в применении перекрестно-сшитых наполнителей на основе ГК. Перекрестно-сшитая ГК образуется путем взаимодействия свободной ГК с перекрестно сшивающим агентом в подходящих условиях реакции. Хорошо известны способы получения наполнителей мягких тканей на основе ГК, включающих перекрестно-сшитую и свободную ГК.
Предложено включать некоторые терапевтические агенты, например обезболивающие агенты, такие как лидокаин, в инъецируемые композиции на основе ГК. К сожалению, инъецируемые композиции на основе ГК, которые включают лидокаин, во время способа приготовления, склонны частичной или почти полной деградации перед инъекцией, в особенности во время стадий высокотемпературной стерилизации и/или при помещении на хранение на любой значительный промежуток времени.
Задача композиций мягкого наполнителя на основе ГК и способов их получения и применения, как описано, заключаются в том, чтобы предложить наполнители мягких тканей, которые не вызывают аллергические реакции у пациентов, являются биосовместимыми и стабильными и применимы in vivo, и включают один или более чем один локальный обезболивающий агент.
Краткое описание изобретения
Описание настоящего изобретения относится к наполнителям мягких тканей, например кожным и подкожным наполнителям на основе гиалуроновой кислоты (ГК) и фармацевтически приемлемых солей ГК, например гиалуроната натрия (NaГК). Композиции на основе ГК, описанные в данном документе, включают терапевтически эффективное количество по меньшей мере одного обезболивающего агента. В одном из воплощений, например, обезболивающий агент представляет собой лидокаин. Композиции на основе ГК по настоящему изобретению, включающие по меньшей мере один обезболивающий агент, обладают улучшенной стабильностью, по сравнению с обычными композициями на основе ГК, включающими, например лидокаин, будучи подверженными способам стерилизации, таким как автоклавирование и/или при хранении в течение длительных периодов времени при температуре окружающей среды. Также предложены способы получения таких композиций на основе ГК, а также продукты, полученные при помощи таких способов.
В данном документе описаны композиции наполнителей для мягких тканей, где указанные композиции в общем содержат: компонент гиалуроновой кислоты (ГК), перекрестно-сшитый перекрестно сшивающим агентом, выбранным из группы, состоящей из 1,4-бутандиолдиглицидильного эфира (БДДЭ), 1,4-бис(2,3-эпоксипропокси)бутана, 1,4-бисглицидилоксибутана, 1,2-бис(2,3-эпоксипропокси)этилена и 1-(2,3-эпоксипропил)-2,3-эпоксициклогексана, и 1,4-бутандиолдиглицидильного эфира; и по меньшей мере один обезболивающий агент комбинированный с перекрестно-сшитым компонентом ГК.
В еще одном воплощении по меньшей мере один обезболивающий агент представляет собой лидокаин. В еще одном воплощении количество обезболивающего агента представлено в концентрации от приблизительно 0,1% до приблизительно 5,0 масс.% композиции. В еще одном воплощении обезболивающий агент представлен в концентрации от приблизительно 0,2% до приблизительно 1,0 масс.% композиции. В одном из воплощений, обезболивающий агент представляет собой лидокаин и представлен в концентрации приблизительно 0,3 масс.% композиции.
В еще одном воплощении композиция наполнителя мягких тканей обладает силой выталкивания от приблизительно 10 Н до приблизительно 13 Н, например, при скорости приблизительно 12,5 мм/минуту. В еще одном воплощении композиция обладает вязкостью от приблизительно 5 Па*с до приблизительно 450 Па*с, например измеренной при приблизительно 5 Гц.
В одном из воплощений компонент ГК представляет собой гель, например когезионный гидратированный гель. В одном из воплощений компонент ГК представляет собой перекрестно-сшитый гель ГК, имеющий не больше чем приблизительно от 1% до приблизительно 10% свободной ГК. Для задач данного описания свободная ГК включает действительно не сшитую перекрестной связью ГК, а также в незначительной степени сшитые перекрестной связью цепи и фрагменты ГК, все из которых представлены в растворимой в воде форме.
В других воплощениях компонент ГК содержит больше чем приблизительно 10%, например больше чем приблизительно 15%, например до или больше чем приблизительно 20% свободной ГК.
В еще одном воплощении компонент ГК представляет собой гель, содержащий частицы перекрестно-сшитой ГК в относительно текучей среде свободной ГК. В некоторых воплощениях компонент ГК имеет средний размер частиц больше чем приблизительно 200 мкм, например больше чем приблизительно 250 мкм.
В данном документе дополнительно описана композиция наполнителя мягких тканей, содержащая: компонент ГК, перекрестно сшитый с 1,4-бутандиолдиглицидильным эфиром (БДДЭ), где указанный ГК компонент обладает степенью перекрестного сшивания меньше чем приблизительно 5%, например приблизительно 2%, и обезболивающий агент, имеющий концентрацию от приблизительно 0,1% до приблизительно 5,0 масс.% композиции наполнителя мягких тканей, где обезболивающий агент представляет собой лидокаин.
В данном документе дополнительно описаны способы приготовления композиции наполнителя мягких тканей, где в способах осуществляют стадии: получения компонента ГК, перекрестно-сшитого с помощью по меньшей мере одного перекрестно-сшивающего агента, выбранного из группы, состоящей из 1,4-бутандиолдиглицидильного эфира (БДДЭ), 1,4-бис(2,3-эпоксипропокси)бутана, 1,4-бисглицидилоксибутана, 1,2-бис(2,3-эпоксипропокси)этилена и 1-(2,3-эпоксипропил)-2,3-эпоксициклогексана и 1,4-бутандиолдиглицидильного эфира или их комбинаций; доведения рН указанного ГК компонента к рН больше приблизительно 7,2; и добавления раствора, содержащего по меньшей мере один обезболивающий агент, к компоненту ГК, имеющему доведенный рН, с получением композиции наполнителя на основе ГК.
В еще одном воплощении композицию стерилизуют, например, путем автоклавирования, с образованием стерилизованной композиции, и где стерилизованная композиция стабильна при температуре окружающей среды в течение по меньшей мере приблизительно месяцев, например, по меньшей мере 9 месяцев, по меньшей мере приблизительно 12 месяцев, например по меньшей мере приблизительно 36 месяцев или больше.
В еще одном воплощении доведенный рН составляет больше приблизительно 7,5. В еще одном воплощении в способе дополнительно осуществляют стадию гомогенизации компонента ГК во время или после стадии добавления раствора содержащего по меньшей мере один обезболивающий агент. В еще одном воплощении на стадии гомогенизации композицию подвергают смешиванию с контролируемым усилием сдвига.
В еще одном воплощении на стадии получения компонента ГК осуществляют получение безводного свободного материала NaГК и гидратирования безводного свободного материала NaГК в щелочном растворе с получением щелочного свободного геля NaГК. В еще одном воплощении щелочной свободный гель NaГК имеет рН больше чем приблизительно 8,0. В еще одном воплощении рН составляет больше чем приблизительно 10.
В еще одном воплощении компонент ГК содержит больше чем приблизительно 20% свободной ГК и перекрестно-сшитый фрагмент компонента ГК имеет степень перекрестного сшивания меньше чем приблизительно 6% или меньше чем приблизительно 5%.
В еще одном воплощении композиция наполнителя мягких тканей имеет природу в виде частиц, которой содержит частицы перекрестно-сшитой ГК диспергированные в текучей растворимой среде ГК. В некоторых воплощениях средний размер таких частиц составляет по меньшей мере приблизительно 200 мкм, и в других воплощениях средний размер таких частиц составляет по меньшей мере приблизительно 250 мкм.
В данном документе дополнительно описана композиция наполнителя мягких тканей, содержащая: компонент гиалуроновой кислоты (ГК), перекрестно сшитый с помощью 1,4-бутандиолдиглицидильного эфира (БДДЭ), где указанный ГК компонент обладает степенью перекрестного сшивания меньше чем приблизительно 5%, и обезболивающий агент, имеющий концентрацию от приблизительно 0,1% до приблизительно 5,0 масс.% композиции наполнителя мягких тканей, где обезболивающий агент представляет собой лидокаин.
В конкретном воплощении изобретения дополнительно описан способ приготовления композиции наполнителя мягких тканей, при котором осуществляют стадии: получения безводного свободного материала NaГК и гидратирования безводного свободного материала NaГК в щелочном растворе с получением щелочного свободного геля NaГК; перекрестного сшивания свободного геля NaГК с помощью БДДЭ с образованием перекрестно-сшитой щелочной композиции ГК со степенью перекрестного сшивания меньше чем приблизительно 5% и рН больше приблизительно 7,2; добавления раствора, содержащего лидокаин HCl к компоненту ГК, имеющему доведенный рН, с получением указанной композиции наполнителя на основе ГК; гомогенизации композиции наполнителя на основе ГК, таким образом, с образованием гомогенизированной композиции наполнителя на основе ГК; и стерилизации гомогенизированной композиции наполнителя на основе ГК, таким образом с образованием стерилизованной композиции наполнителя на основе ГК, где композиция наполнителя мягких тканей имеет размер частиц больше чем приблизительно 200 мкм, например размер частиц больше чем приблизительно 250 мкм.
Краткое описание графических материалов
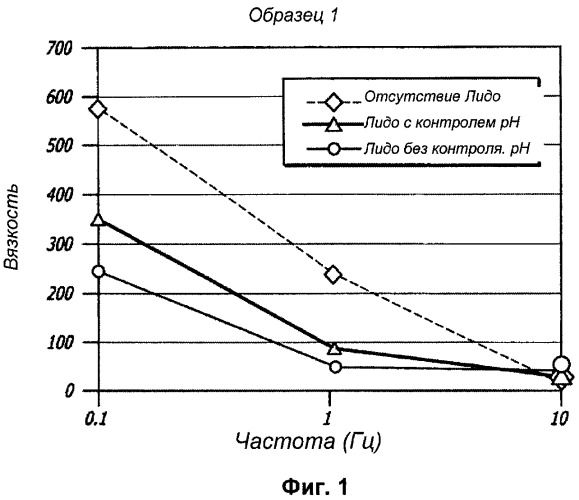
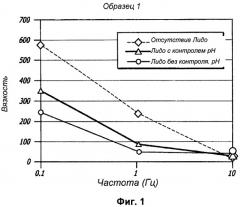
Фиг.1 графически иллюстрирует вязкость Образца 1, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
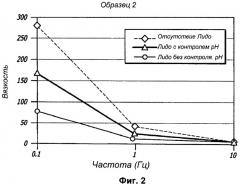
Фиг.2 графически иллюстрирует вязкость Образца 2, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
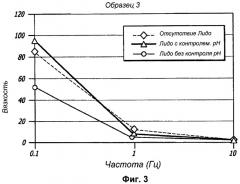
Фиг.3 графически иллюстрирует вязкость Образца 3, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
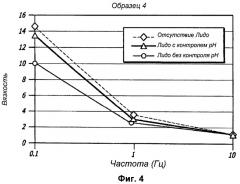
Фиг.4 графически иллюстрирует вязкость Образца 4, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
Фиг.5 графически иллюстрирует вязкость Образца 5, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
Фиг.6 графически иллюстрирует относительные характеристики вязкости/эластичности Образца 5, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
Фиг.7 графически иллюстрирует вязкость Образца 6, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
Фиг.8 графически иллюстрирует относительные характеристики вязкости/эластичности Образца 6, приготовленного без лидокаина, с лидокаином и доведением рН во время приготовления и с лидокаином, но без доведения рН во время приготовления, в зависимости от частоты сдвигового усилия.
Фиг.9 графически иллюстрирует концентрацию лидокаина в гелевой форме Образца 5 в примере 4, приготовленной при помощи способа в соответствии с тестом 2 в зависимости от времени.
Определения
Предполагается, что некоторые термины, используемые в описании, относятся к следующим определениям, как подробно изложено ниже. Когда определение терминов отклоняется от обычно используемого значения этого термина, тогда, если не указано иное, заявитель имеет намерение использовать приведенные ниже определения.
Используемый в данном документе термин "стабильный при автоклавировании" или "стабильный к автоклавированию" описывает продукт или композицию, устойчивую к деградации, таким образом, что продукт или композиция содержит по меньшей мере один, и предпочтительно все из следующих аспектов после эффективной автоклавируемой стерилизации: прозрачность, рН, силу выталкивания и/или реологические характеристики, концентрацию гиалуроновой кислоты (ГК), стерильность, осмолярность и концентрацию лидокаина.
Используемый в данном документе термин "центрифугирование" относится к процессу с использованием центробежных сил для равномерного распределения веществ с большей и меньшей плотностью. Центрифугирование обычно используют для отделения жидкой фазы от твердой или гелеобразной фазы. Существенные фазовые разделения, возникающие в результате центрифугирования, могут представлять собой по меньшей мере разделения, которые видны невооруженным глазом, например жидкая фаза и твердая фаза, четко разделенные, будучи видимыми невооруженным глазом.
Используемый в данном документе термин "высокомолекулярная ГК" описывает вещество ГК, имеющее молекулярную массу по меньшей мере от приблизительно 1,0 миллион Дальтон (м.м. ≥106 Да или 1 МДа) до приблизительно 4,0 МДа. Например, высокомолекулярная ГК в композиции по настоящему изобретению может иметь молекулярную массу приблизительно 2,0 МДа. В еще одном примере высокомолекулярная ГК может иметь молекулярную массу приблизительно 2,8 МДа.
Используемый в данном документе термин "низкомолекулярная ГК" описывает вещество ГК, имеющее молекулярную массу меньше чем приблизительно 1,0 МДа. Низкомолекулярная ГК может иметь молекулярную массу от приблизительно 200000 Да (0,2 МДа) до меньше чем приблизительно 1,0 МДа, например от приблизительно 300000 Да (0,3 МДа) до приблизительно 750000 Да (0,75 МДа).
Используемый в данном документе термин "степень перекрестного сшивания" относится к межмолекулярным соединениям, сшивающим индивидуальные молекулы полимера ГК или мономерные цепи в прочную структуру, или, как раскрыто в данном документе, композицию наполнителя мягких тканей. Кроме того, степень перекрестного сшивания для задач настоящего описания дополнительно определяется как процент массовой доли перекрестно-сшивающего агента к мономерным единицам ГК в перекрестно-сшитом фрагменте композиции на основе ГК. Она измеряется массовой долей мономеров ГК относительно перекрестно-сшивающего агента (мономеры ГК: перекрестно-сшивающий агент).
Используемый в данном документе термин "свободная ГК" относится к индивидуальным молекулам полимера ГК, которые не являются перекрестно-сшитыми или в незначительной степени перекрестно-сшиты (очень низкая степень перекрестного сшивания) с сильно перекрестно-сшитой (высокая степень перекрестного сшивания) макромолекулярной структурой, составляющей композицию наполнителя мягких тканей. Свободная ГК, как правило, остается растворимой в воде. Свободная ГК альтернативно может быть определена как "не являющийся перекрестно сшитым" или в незначительной степени перекрестно сшитый компонент макромолекулярной структуры, составляющей композицию раскрытого здесь наполнителя мягких тканей.
Используемый в данном документе термин "когезионный" представляет собой способность композиции на основе ГК сохранять свою форму и препятствовать деформации. На когезионность среди прочих факторов влияет доля молекулярной массы исходной свободной ГК, степень перекрестного сшивания, количество остаточной свободной ГК после перекрестного сшивания и рН композиции на основе ГК. Когезионная композиция на основе ГК противостоит фазовому разделению при тестировании в соответствии со способом, раскрытым здесь в примере 1.
Подробное описание изобретения
Описание настоящего изобретения в общем относится к наполнителям мягких тканей, например кожным и подкожным наполнителям на основе гиалуроновой кислоты (ГК) и фармацевтически приемлемых солей ГК, например гиалуронате натрия (NaГК). В одном из аспектов композиции на основе ГК, описанные в данном документе, включают терапевтически эффективное количество по меньшей мере одного обезболивающего агента, например лидокаина. Композиции на основе ГК по настоящему изобретению, включающие по меньшей мере один обезболивающий агент, обладают улучшенной стабильностью по сравнению с обычными композициями на основе ГК, включающими, например, лидокаин, будучи подверженными высоким температурам и давлениям, например таким, какие возникают во время способов стерилизации теплом и/или под давлением, например автоклавирование, и/или, например, во время хранения при температуре окружающей среды в течение длительного периода времени.
Стабильные композиции сохраняют по меньшей мере один из или все из следующих аспектов после эффективной стерилизации путем автоклавирования и/или при длительном хранении: прозрачность, рН для применения пациентом, сила выталкивания и/или реологические характеристики, концентрация ГК, стерильность, осмолярность и концентрация лидокаина. Также предложены методы или способы приготовления таких композиций на основе ГК, а также продукты, полученные при помощи таких методов или способов.
Используемый в данном документе термин "гиалуроновая кислота (ГК)" может относиться к любой из ее гиалуронатных солей и включает гиалуронат натрия (NaГК), гиалуронат калия, гиалуронат магния, гиалуронат кальция и их комбинации, но не ограничивается ими.
Как правило, концентрация ГК описанной здесь композиции предпочтительно составляет по меньшей мере 10 мг/мл и до приблизительно 40 мг/мл. Например, концентрация ГК в некоторых из композиций находится в диапазоне от приблизительно 20 мг/мл до приблизительно 30 мг/мл. Кроме того, например, в некоторых воплощениях композиции имеют концентрацию ГК приблизительно 22 мг/мл, приблизительно 24 мг/мл, приблизительно 26 мг/мл или приблизительно 28 мг/мл.
Дополнительно, концентрация одного или более чем одного обезболивающего агента представляет собой количество, эффективное для уменьшения боли, которую испытывают при инъекции композиции. По меньшей мере одно обезболивающее средство для местного введения может быть выбрано из группы амбукаина, амоланона, амилокаина, беноксината, бензокаина, бетоксикаина, бифенамина, бупивакаина, бутакаина, бутамбена, бутаниликаина, бутетамина, бутоксикаина, картикаина, хлорпрокаина, кокаэтилена, кокаина, циклометикаина, дибукаина, диметисоквина, диметокаина, диперодона, дициклонида, экгонидина, экгонина, этилхлорида, этидокаина, бета-эукаина, эупроцина, феналкомина, формокаина, гексилкаина, гидрокситетракаина, изобутил пара-аминобензоата, лейцинокаина мезилата, левоксадрола, лидокаина, мепивакаина, меприлкаина, метабутоксикаина, метилхлорида, миртекаина, наепаина, октакаина, ортокаина, оксетазаина, парэтоксикаина, фенакаина, фенола, пиперокаина, пиридокаина, полидоканола, прамоксина, прилокаина,прокаина, пропанокаина, пропаракаина, пропипокаина, пропоксикаина, псевдококаина, пиррокаина, ропивакаина, салицилового спирта, тетракаина, толикаина, тримекаина, золамина и их солей. В одном из воплощений по меньшей мере один обезболивающий агент представляет собой лидокаин, такой как в форме лидокаина HCl. Описанные в данном документе композиции могут иметь концентрацию лидокаина от приблизительно 0,1% до приблизительно 5 масс.% композиции, например от приблизительно 0,2% до приблизительно 1,0 масс.% композиции. В одном из воплощений композиция имеет концентрацию лидокаина приблизительно 0,3 масс.% (масс.%) композиции. Концентрация лидокаина в описанной в данном документе композиции может быть терапевтически эффективной, означая, что концентрация подходит для обеспечения терапевтической пользы, не причиняя пациенту вред.
В одном из аспектов изобретения предложен способ приготовления композиции на основе ГК, включающей эффективное количество лидокаина, где в способе готовят композицию предшественника, дополнительно содержащую перекрестно-сшитый гель на основе ГК, к ней добавляют раствор, содержащий лидокаин, например, в форме лидокаина HCl, и гомогенизируют смесь с получением когезионной по меньшей мере частично перекрестно-сшитой композиции на основе ГК, включающей лидокаин, которая стабильна при автоклавировании. Когезионный перекрестно-сшитый гель на основе ГК включает не больше чем от приблизительно 1% до приблизительно 10 об.% свободной ГК, например, не больше чем приблизительно 5% вещества свободной ГК.
В некоторых воплощениях настоящего изобретения компонент ГК композиций по настоящему изобретению, далее иногда, "композиции предшественника" представляет собой гидратированный когезионный гель. Когезионный гель по сравнению с не когезионным гелем лучше способен сохранять свою форму и противостоять деформации, например, после того, как его подвергнут усилию сдвига или другим деформациям. Автор настоящего изобретения обнаружил, что такие когезионные гели в меньшей степени существенно деградируют или станут не стабильными со временем, или будучи подверженными внешним стимулам, таким как стерилизация, по сравнению с некогезионными гелями.
Не желая быть связанными какой-либо теорией, полагают, что высокая когезионная способность композиции предшественника в некоторых воплощениях изобретения действует таким образом, чтобы частично или полностью предупреждать или препятствовать какому-либо разрушению или деградации перекрестно-сшитой ГК в композиции при добавлении лидокаина.
Полагают, что такая деградация может в основном возникать поскольку множество, возможно большинство перекрестно-сшитых гелей на основе ГК обычно готовят таким образом, что получают гели, которые не достаточно когезионны для предупреждения такой деградации при добавлении лидокаина. В настоящее время обнаружили, что добавление лидокаина к в достаточной мере когезионным композициям на основе ГК не вызывает существенной или значительной деградации композиции, и композиции сохраняют свою целостность с точки зрения реологии, вязкости, внешнего вида и других характеристик даже при хранении в течение длительного периода времени, например в течение периода времени по меньшей мере приблизительно 6 месяцев, приблизительно 9 месяцев, приблизительно 12 месяцев или приблизительно 36 месяцев или больше, например, при температурах окружающей среды, и даже после того, как их подвергают процедурам стерилизации, например автоклавированию.
Неожиданно обнаружили, что препараты перекрестно-сшитых композиций на основе ГК, включающих лидокаин, могут быть приготовлены таким образом, чтобы получить стабильные при стерилизации инъецируемые композиции ГК/лидокаин.
В данном документе дополнительно описан способ получения стабильных композиций на основе ГК, содержащих эффективное количество лидокаина, путем приготовления композиции предшественника, например, когезионного перекрестно-сшитого геля на основе ГК, добавления к гелю хлоргидрата лидокаина с образованием гелевой смеси ГК/лидокаин, и гомогенизации смеси с получением перекрестно-сшитой композиции на основе ГК, которая стабильна при автоклавировании.
В некоторых воплощениях композиция предшественник представляет собой когезивный гидратированный гель на основе ГК. Такой "когезивный" гель будет в общем включать не более от приблизительно 1% до приблизительно 10 об.% растворимой жидкой формы или свободной ГК. Полагают, что такие когезивные гели являются монофазными или по существу монофазными композициями, в том смысле, что менее чем от приблизительно 1 об.% до приблизительно 10 об.% композиции содержит свободную ГК.
В некоторых других воплощениях композиция предшественник представляет собой относительно не когезионный гидратированный гель на основе ГК. Такой "не когезионный" гель в общем включает больше чем 10%, например больше чем приблизительно 15%, например больше чем 20% или больше свободной ГК.
В некоторых воплощениях композиция предшественник может содержать первый компонент, включающий относительно высоко перекрестно-сшитые частицы ГК по существу в твердой фазе, и второй компонент, содержащий свободную или в относительно меньшей степени перекрестно-сшитую ГК по существу в жидкой фазе, в которой диспергированы в относительно высокой степени перекрестно-сшитые частицы.
В некоторых воплощениях композиции по настоящему изобретению имеют природу частиц и содержат частицы в относительно высокой степени перекрестно-сшитой ГК, диспергированной в среде со свободной ГК. В некоторых воплощениях средний размер таких частиц перекрестно-сшитой ГК составляет по меньшей мере приблизительно 200 мкм или по меньшей мере приблизительно 250 мкм. Такие композиции в виде частиц, как правило, менее когезионны по сравнению иным образом похожими композициями, в которых отсутствуют различимые частицы, или имеют частицы, имеющие средний размер меньше чем 200 мкм.
Например, в некоторых воплощениях композиция предшественник может быть получена путем прессования массы в относительно высокой степени перекрестно-сшитого геля на основе ГК через решето или сито с получением в относительно высокой степени перекрестно-сшитых частиц ГК, имеющих в общем однородный размер и форму. Эти частицы затем смешивают с веществом носителя, например количеством свободной ГК с получением геля.
В других воплощениях предложен способ получения основанной на ГК композиции, включающей эффективное количество лидокаина, где в способе готовят композицию предшественник, включающий по существу имеющий нейтральный рН по меньшей мере частично перекрестно-сшитый гель на основе ГК, и приводят рН геля до значения больше чем приблизительно 7,2, например от приблизительно 7,5 до приблизительно 8,0. В способе дополнительно осуществляют стадию комбинирования раствора, содержащего лидокаин, например, в форме лидокаина HCl, со слегка щелочным гелем после доведения рН и получения композиции на основе ГК, включающей лидокаин, которая стабильна к автоклавированию.
Еще в одном способе получения стабильной композиции на основе ГК, содержащей эффективное количество лидокаина, как описано, в общем осуществляют стадии: получения очищенного материала NaГК, например, в форме волокон; гидратирования материала; и перекрестного сшивания гидратированного материла с подходящим перекрестно-сшивающим агентом с образованием перекрестно-сшитого геля на основе ГК. В способе дополнительно осуществляют стадии нейтрализации и набухания геля, и добавления к гелю раствора, содержащего лидокаин, предпочтительно кислой соли хлоргидрата лидокаина, с образованием геля ГК/лидокаин. Дополнительно в способе осуществляют гомогенизацию геля ГК/лидокаин и упаковку гомогенизированного геля ГК/лидокаин, например, в шприцы для дозирования. Шприцы затем стерилизуют путем автоклавирования при эффективной температуре и давлении. В соответствии с описанием настоящего изобретения упакованные и стерилизованные когезионные гели NaГК/лидокаин проявляют улучшенную стабильность по сравнению с композициями на основе ГК, включающими лидокаин, которые изготовлены с использованием обычных способов.
Полагают, что продукты и композиции по настоящему изобретению являются стерильными при воздействии температур по меньшей мере от приблизительно 120°С до приблизительно 130°С и/или давлений по меньшей мере от приблизительно 12 фунтов на квадратный дюйм (PSI) (82,7 кПа) до приблизительно 20 фунт/кв.дюйм (137,9 кПа) во время автоклавирования в течение периода по меньшей мере приблизительно от 1 минуты до приблизительно 15 минут.
Продукты и композиции по настоящему изобретению также остаются стабильными при хранении в течение длительных периодов времени при комнатной температуре. Предпочтительно, композиции по настоящему изобретению остаются стабильными в течение периода по меньшей мере приблизительно двух месяцев, или по меньшей мере приблизительно шести месяцев, или по меньшей мере приблизительно 9 месяцев, или по меньшей мере приблизительно 12 месяцев, или по меньшей мере приблизительно 36 месяцев, при температурах по меньшей мере приблизительно 25°С. В конкретном воплощении композиции стабильны при температуре до приблизительно 45°С в течение периода по меньшей мере двух месяцев.
Способ получения включает, в одном из воплощений, исходную стадию получения неочищенного вещества ГК в форме безводных волокон или порошка ГК. Неочищенное вещество ГК может представлять собой ГК, ее соли и/или смеси. В предпочтительном воплощении вещество ГК содержит волокна или порошок NaГК, и еще более предпочтительно, NaГК из бактериального источника. В некоторых аспектах описания настоящего изобретения вещество ГК может быть получено из животного. Вещество ГК может представлять собой комбинацию неочищенных веществ, включающих ГК и по меньшей мере один другой полисахарид, например глюкозаминогликан (ГАГ).
В некоторых воплощениях вещество ГК в композиции почти полностью содержит или состоит из высокомолекулярной ГК. То есть почти 100% вещества ГК в композиции по настоящему изобретению может представлять собой высокомолекулярную ГК, как определено выше. В других воплощениях вещество ГК в композиции содержит комбинацию высокомолекулярной ГК и относительно низкомолекулярной ГК, как определено выше.
Вещество ГК в композиции может содержать от приблизительно 5% до приблизительно 95% высокомолекулярной ГК с балансом вещества ГК, включающим низкомолекулярную ГК. В типичном воплощении изобретения отношение высокомолекулярной к низкомолекулярной ГК составляет по меньшей мере приблизительно и предпочтительно больше чем 2 (масс. ≥2), где высокомолекулярная ГК имеет молекулярную массу больше 1,0 МДа.
Специалисту в данной области техники понятно, что выбор высоко- и низкомолекулярного вещества ГК и их относительные проценты или отношения зависят от желаемых характеристик, например силы выталкивания, модуля упругости, модуля вязкости и фазового угла, выраженного как отношение модуля вязкости к модулю упругости, когезионности и т.д. конечного основанного на ГК продукта. Дополнительную информацию, которая может быть полезна для понимания этого и других аспектов настоящего изобретения, смотри в Lebreton, публикация заявки на патент США №2006/0194758, полное описание которой включено в данный документ путем ссылки.
Гели на основе ГК могут быть приготовлены в соответствии с описанием настоящего изобретения сначала путем очистки сухого или неочищенного вещества ГК, обладающего желаемым отношением высокой/низкой молекулярной массы. Эти стадии в общем включают гидратирование безводных волокон ГК или порошка с желаемым отношением высокой/низкой молекулярной массы, например с использованием чистой воды, и фильтрования материала для удаления крупных чужеродных частиц и/или других примесей. Фильтрованное гидратированное вещество затем сушат и очищают. Высоко и низкомолекулярная ГК могут быть очищены раздельно или могут быть смешаны вместе, например в желаемом отношении непосредственно перед перекрестным сшиванием.
В одном из аспектов настоящего описания чистые безводные волокна ГК гидратируют в щелочном растворе с получением свободного щелочного NaГК геля. Любой подходящий щелочной раствор может быть использован для