Способ получения адамантилсодержащих бета-дикарбонильных соединений
Иллюстрации
Показать всеИзобретение относится к органической химии, а именно к способу получения адамантановых производных β-дикетонов, являющихся полупродуктами для органического синтеза и потенциальными лигандами для ионов металлов. Способ получения адамантилсодержащих β-дикарбонильных соединений из 1-адамантанола и β-дикарбонильных соединений осуществляют в среде органического растворителя при катализе кислотой Льюиса, где в качестве кислоты Льюиса применяют трифлат индия в количестве 5 мольных процентов, а в качестве органического растворителя 1,2-дихлорэтан, реакцию осуществляют при нагревании при температуре кипения до полного расходования исходных компонентов, взятых в эквимольных количествах. Техническим результатом является создание экологически безопасного и безвредного способа получения ряда адамантилсодержащих β-дикарбонильных соединений с использованием коммерчески доступных исходных соединений с хорошим выходом целевого продукта. 5 пр., 1 табл.
Реферат
Предлагаемое изобретение относится к органической химии, а точнее к способам получения адамантановых производных β-дикетонов, являющихся полупродуктами для органического синтеза и потенциальными лигандами для ионов металлов.
Известен способ получения 1-адамантилмалонового эфира с выходом 75% при нагревании 1,3-дегидроадамантана в избытке малонового эфира в течение 6 часов при 100ºС [Kogay B.E., Sokolenko W.A., Reactions of 1,3-dehydroadamantane (3.3.1-propellane system) with CH- and NH-acids. - Tetrahedron Lett. - 1983. - Vol.24, No.6. - P.613-616; Когай Б.Е., Соколенке В.А., Реакции 1,3-дегидроадамантана ([3.3.1]пропеллана) с CH- и NH-кислотами. - Изв. АН СССР сер. Хим. - 1982. - №1. - С.222]:
Известен способ получения α-(1-адамантил)-β-дикетонов, основанный на взаимодействии 1,3-дегидроадамантана и кетоэфиров в среде кипящего диэтилового эфира в атмосфере сухого, очищенного от кислорода и азота воздуха, в течение 4 ч. [Но, Б.И., Бутов Г.М., Мохов В.М., Паршин Г.Ю. Синтез адамантилзамещенных кетоэфиров. - Журн. Орган. Химии. - 2003. - Т.39, Вып.11. - С.1737-1738]:
R=Me (выход 83%), Ph (выход 90%)
Известен способ получения α-(1-адамантил)-β-дикетонов из 1,3-дегидроадамантана и полутора - двукратного избытка β-дикетона в среде кипящего диэтилового эфира, в атмосфере сухого, очищенного от кислорода азота, в течение 1-2 ч. [Но, Б.И., Бутов Г.М., Мохов В.М., Паршин Г.Ю. Синтез адамантилсодержащих циклических β-дикетонов. - Журн. Орган. Химии. - 2002. - Т.38, Вып.9. - С.1428]:
Известен способ получения α-(1-адамантил)-β-дикетонов, заключающийся во взаимодействии 1,3-дегидроадамантана с разнообразными фторсодержащими 1,3-дикетонами в среде кипящего абсолютного диэтилового эфира, в атмосфере сухого и очищенного от кислорода азота в течение 1,5-2 часов с выходами продуктов 83-98% [Бутов Г.М. и др. - Журн. Орган. Химии. - 2008. - Т.44, Вып.8. - С.1171 -1174]:
R=CF3, R'=CF3 (83%), Ph (93%), 4-Cl-С6Н4 (87%), 3,4-(МеО)2-С6Н3 (93%), 1,3-бензодиоксол-5-ил (88%), 2-фурил (97%), 2-тиенил (90%), 4-(1Н-пиррол1-ил)-С6Н4 (95%), t-Bu (86%).
R=CF2H, R'=Ph (98%)
Несмотря на высокие выходы продуктов адамантилирования β-дикарбонильных соединений 1,3-дегидроадамантаном реализация этого метода в промышленном масштабе ограничивается применением в качестве реакционной среды крайне огнеопасного диэтилового эфира, а также применением в реакции полутора - двукратного избытка β-дикарбонильных соединений, что требует возврата избыточного количества реагента, тем самым удорожая процесс.
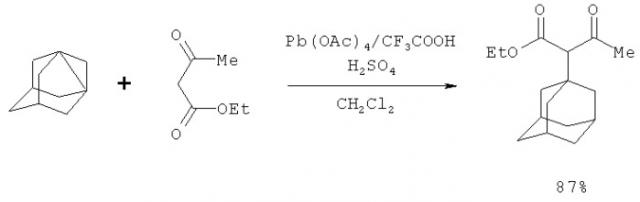
Известен способ получения адамантилацетоуксусного эфира (этил-2-(1-адамантил)-3-оксобутаноата) с выходом конечного продукта 87%, заключающийся в реакции адамантана с ацетоуксусным эфиром в присутствии тетраацетата свинца, трифторуксусной и концентрированной серной кислот в среде дихлорметана, общая продолжительность реакции составляет 40 ч. [Jones S.R., Mellor J.M. Introduction of bridgehead functionality via lead (IV) oxidation of hydrocarbons. - Synthesis. - 1976. - P.32-33]:
Применение в качестве реагента высокотоксичного тетраацетата свинца делает предлагаемый метод не экологичным.
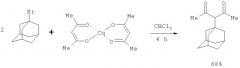
Известен способ получения адамантилацетилацетона (3-(1-адамантил)-2,4-пентандиона), заключающийся во взаимодействии 1-бромадамантана с ацетилацетонатом кобальта (II) при кипячении в течение 4 часов в среде хлороформа с выходом конечного продукта 68% [Marquet J., Moreno-Manas M., Pacheco P., Vallribera A. Dual mechanistic pathway in the alkylation of pentane-2,4-dione through its Co(II) complex. - Tetrahedron Lett. - 1988. - Vol.29. - №12. - P.1465-1468]:
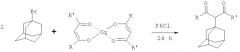
Впоследствии этот способ был распространен на получение ряда α-(1-адамантил)-β-дикетонов, при этом замена реакционной среды на хлорбензол позволила несколько повысить выход целевых продуктов за счет увеличения температуры реакции. Использование β-дикетоната цинка несколько менее эффективно, что показано на примере ацетилацетоната цинка, выход целевого продукта адамантилирования в этом случае составил 75%, по сравнению с 81% при использовании ацетилацетоната кобальта (II) [Gonzalez A., Guell F., Marquet J., Moreno-Manas M Alkylation of (3-diketones through teir Co(II), Co(III), and Zn(II) complexes. 1-bromadamantane as alkylating agent. - Tetrahedron Lett. - 1985. - Vol.26. - №31. - P.3735-3738; Gonzalez A., Marquet J., Moreno-Manas M. Metal complexes in organic synthesis. Preparation of α-(1-adamantyl)-β-dicarbonyl compounds and 4-(1-adamantyl)-3,5-disubstituted pyrazoles and isoazoles. - Tetrahedron. - 1986. - Vol.42, №15. - P.4253-4257]:
R=R'=Me (81%); R=Me, R'=Ph (89%); R=R'=Ph (80%), R=Me, R'=OEt (38%), R=R'=t-Bu (31%).
К недостаткам этого способа относится длительность проведения процесса (24 часа).
Известен способ получения адамантилацетилацетона (3-(1-адамантил)-2,4-пентандиона) с выходом конечного продукта 37%, основанный на взаимодействии 1-адамантанола или его нитрата с ацетилацетоном в среде нитрометана в течение 48 ч. при 25ºС при катализе концентрированными серной или хлорной кислотами. [Климочкин Ю.Н., Тилли Т.С., Моисеев И.К. Адамантилирование ацетилацетона. - Журн. Орган. Химии. - 1988. - Т.24, Вып.8. - С.1780-1781]:
X=H, NO2
Относительно низкий выход целевого продукта, использование токсичного нитрометана в качестве реакционной среды и длительность проведения реакции являются существенными недостатками этого способа.
Наиболее близким аналогом к заявляемому способу является получение адамантилмалоната из 1-адамантанола и диэтилмалоната в присутствии трифторида бора в среде н-гексана, выход в патенте не указан. [Patent №3859352 US, C07C 87/40, НКИ 260/563 Р]
Данный способ является экологически опасным из-за применения эквивалентных количеств кислоты Льюиса - трифторида бора, который является газообразным веществом, требующим особых мер безопасности.
Техническим результатом является создание экологически безопасного и безвредного способа получения ряда адамантилсодержащих Р-дикарбонильных соединений с использованием коммерчески доступных исходных соединений с хорошим выходом целевого продукта.
Технический результат достигается использованием в качестве катализатора трифлата индия. Адамантилсодержащие β-дикарбонильные соединения образуются при взаимодействии эквимольных количеств 1-адамантанола с β-дикарбонильными соединениями в среде 1,2-дихлорэтана при температуре кипения растворителя в присутствии 5 мольных % трифлата индия в соответствии со схемой:
R=R'=Me (Ia); R=R'=Ph (Ib); R=Me, R'=OEt (Ic); R=Ph, R'=OEt (Id); R=R'=OEt (Ie)
Реакцию контролируют хроматографически, время нагревания определяется полным расходованием исходных реагентов.
По окончанию реакции полученную массу обрабатывают раствором соляной кислоты, отделяют органическую фазу и удаляют растворитель. Очистку продукта осуществляют возгонкой в вакууме, перекристаллизацией или колоночной хроматографией.
| Таблица | |||
| Выходы адамантилсодержащих β-дикарбонильных соединений | |||
| № | β-ДИКАРБОНИЛЬНОЕ СОЕДИНЕНИЕ | ПРОДУКТ (время реакции, мин) | ВЫХОД ПРОДУКТА, % |
| 1 | 93 | ||
| 2 | 92 | ||
| 3 | 83 | ||
| 4 | 80 | ||
| 5 | 45 |
Пример получения 3-(1-адамантил)пентандиона-2,4 Ia.
В колбу, снабженную обратным холодильником, помещают 10 мл 1,2-дихлорэтана, 0,185 г (0,00033 моль) трифлата индия, приливают раствор 1 г (0,00657 моль) 1-адамантанола и 0,65 г (0,00657 моль) ацетилацетона в 25 мл 1,2-дихлорэтана. Реакционную массу нагревают, перемешивая при температуре кипения растворителя, в течение 1 ч. Реакционную массу выливают в делительную воронку, содержащую 20 мл 2 М соляной кислоты, органический слой отделяют, а водный экстрагируют тремя порциями хлороформа по 10 мл. Объединенные органические фазы упаривают на ротационном испарителе, остаток возгоняют в вакууме. Выход 1,43 г (93%). Т.пл.53ºС.
ИК-спектр (КВг), ν/см-1: 2974, 2910, 2893, 2846 (Csp3-Н), 1697, 1687 (С=O). Спектр ЯМР 1Н (399.78 МГц, CDCl3, δ, м.д.): 1.59-1.70 (м, 12Н, СН2), 1.96 (м, 3Н, СН), 2.18 (с, 6Н, СН3), 3.51 (с, 1Н, СН). Спектр ЯМР 13С (CDCl3, δ, м.д.): 28.64 (СН), 33.21 (СН3), 36.60 (СН2), 40.45 (СН2), 45.35 (С), 78.25 (СН), 204.61 (С=O). Масс-спектр (ЭУ, 70 эВ), m/z (1отн (%)): 234 [М+] (4), 192 (16), 135 (100).
Пример получения 2-(1-адамантил)-1,3-Дифенилпропандиона-1,3 Ib.
В колбу, снабженную обратным холодильником, помещают 10 мл 1,2-дихлорэтана, 0,185 г (0,00033 моль) трифлата индия, приливают раствор 1 г (0,00657 моль) 1-адамантанола и 1,47 г (0,00657 моль) дибензоилметана в 25 мл 1,2-дихлорэтана. Реакционную массу нагревают, перемешивая при температуре кипения растворителя, в течение 2 ч. Реакционную массу выливают в делительную воронку, содержащую 20 мл 2 М соляной кислоты, органический слой отделяют, а водный экстрагируют тремя порциями хлороформа по 10 мл. Объединенные органические фазы упаривают на ротационном испарителе, остаток перекристаллизовывают из метанола. Выход 2,17 г (92 %). Т.пл. 211°С.
ИК-спектр (ν, см-1, KBr): 3064(Csp2-H), 2906, 2891, 2843 (Csp3-H), 1697, 1653 (С=O), 1593, 1446 (Csp2-Csp2). Масс-спектр (ЭУ, 70 эВ, Iотн (%)): 340 (М+, 21), 253 (21), 135 (6), 105 (100).
Пример получения этил-2-(1-адамантил)-3-оксобутаноата Iс.
В колбу, снабженную обратным холодильником, помещают 10 мл 1,2-дихлорэтана, 0,185 г (0,00033 моль) трифлата индия, приливают раствор 1 г (0,00657 моль) 1-адамантанола и 0,86 г (0,00657 моль) ацетоуксусного эфира в 25 мл 1,2-дихлорэтана. Реакционную массу нагревают, перемешивая при температуре кипения растворителя, в течение 2 ч. Реакционную массу выливают в делительную воронку, содержащую 20 мл 2 М соляной кислоты, органический слой отделяют, а водный экстрагируют тремя порциями хлороформа по 10 мл. Объединенные органические фазы упаривают на ротационном испарителе, остаток хроматографируют на колонке с силикагелем, проводя элюирозание смесью гексана и этилацетата (10:3). Продукт представляет собой бесцветное масло. Выход 1,44 г (83 %).
ИК-спектр (ν, см-1, KBr): 2978, 2904, 2848 (Csp3-H), 1745, 1737, 1732, 1714, 1703 (С=O). Масс-спектр (ЭУ, 70 эВ, Iотн (%)): 264 (М+, 2), 222 (10), 135 (100), 119(8), 105 (5).
Пример получения этил-2-(1-адамантил)-3-оксо-3-фенилпропаноата Id.
В колбу, снабженную обратным холодильником, помещают 10 мл 1,2-дихлорэтана, 0,185 г (0,00033 моль) трифлата индия, приливают раствор 1 г (0,00657 моль) 1-адамантанола и 1,26 г (0,00657 моль) бензоилуксусного эфира в 25 мл 1,2-дихлорэтана. Реакционную массу нагревают, перемешивая при температуре кипения растворителя, в течение 2 ч. Реакционную массу выливают в делительную воронку, содержащую 20 мл 2 М соляной кислоты, органический слой отделяют, а водный экстрагируют тремя порциями хлороформа по 10 мл. Объединенные органические фазы упаривают на ротационном испарителе, остаток хроматографируют на колонке с силикагелем, проводя элюирование смесью гексана и этилацетата (10:3). Продукт представляет собой желтоватое масло. Выход 1,71 г (80 %).
ИК-спектр (ν, см-1, KBr): 3061(Csp2-H), 2978, 2904, 2848 (Csp3-H), 1745, 1732, 1693, 1681 (C=O), 1595, 1446 (Csp2-Csp2).Macc -спектр (ЭУ, 70 эВ, Iотн (%)): 326 (М+, 8), 308 (7), 252 (17), 235 (23), 135 (14), 105 (100).
Пример получения диэтил 1 -адамантилмалоната Iе.
В колбу, снабженную обратным холодильником, помещают 10 мл 1,2-дихлорэтана, 0,185 г (0,00033 моль) трифлата индия, приливают раствор 1 г (0,00657 моль) 1-адамантанола и 1,26 г (0,00657 моль) диэтилмалоната в 20 мл 1,2-дихлорэтана. Реакционную массу нагревают, перемешивая при температуре кипения растворителя, в течение 4 ч. Реакционную массу выливают в делительную воронку, содержащую 20 мл 2 М соляной кислоты, органический слой отделяют, а водный экстрагируют тремя порциями хлороформа по 10 мл. Объединенные органические фазы упаривают на ротационном испарителе, остаток хроматографируют на колонке с силикагелем, проводя элюирование смесью гексана и этилацетата (10:3). Продукт представляет собой бесцветное масло. Выход 0.86 г (45 %).
ИК-спектр (ν, см-1, KBr): 2980, 2906, 2848 (Csp3-Н), 1755, 1728 (C=O). Масс-спектр (ЭУ, 70 эВ, Iотн (%)): 294 (M+, 4), 220 (7), 135 (100), 105 (5).
Таким образом, взаимодействие 1-адамантанола с β-дикарбонильными соединениями в присутствии 5 мольных % трифлата индия в среде 1,2-дихлорэтана обеспечивает получение целевых адамантилсодержащих β-дикарбонильных соединений с хорошим выходом, при этом применяют экологичные, безвредные, коммерчески доступные реагенты, что делает способ промышленно применимым.
Способ получения адамантилсодержащих β-дикарбонильных соединений из 1-адамантанола и β-дикарбонильных соединений в среде органического растворителя при катализе кислотой Льюиса, отличающийся тем, что в качестве кислоты Льюиса применяют трифлат индия в количестве 5 мол.%, а в качестве органического растворителя 1,2-дихлорэтан, реакцию осуществляют при нагревании при температуре кипения до полного расходования исходных компонентов, взятых в эквимольных количествах.