Способ получения водорода
Иллюстрации
Показать всеИзобретение относится к области химии. Для получения водорода проводят реакцию паровой каталитической конверсии углеродсодержащей жидкости с получением продуктов реакции, содержащих водород. Продукты реакции направляют на вход катодного пространства для электролиза в высокотемпературном электролизере, на выходе из катодного пространства выделяют реакционный поток, содержащий синтез-газ, который направляют на каталитический синтез углеродсодержащей жидкости. В анодном пространстве, отделенном от катодного пространства электролитическим слоем, выделяют кислород. Углеродсодержащую жидкость возвращают в начало процесса на конверсию, а полученный в процессе синтеза углеродсодержащей жидкости водород очищают от оксидов углерода. 10 з.п. ф-лы, 1 ил.
Реферат
Изобретение относится к способу получения водорода из воды и может быть использовано в химической промышленности, для переработки углеводородов, а также в системах аккумулирования и транспорта энергии и как топливо в транспортных и стационарных энергоустановках.
Известен способ получения водорода из воды, описанный в патенте РФ №2135641, дата публ. 27.08.1999, МПК С25В 1/00. Известный способ получения водорода и синтез-газа (H2/CO) включает утилизацию диоксида углерода из природных газов, в которой подвергают электролизу переменным током воду, насыщенную под давлением 1,0 МПа двуокисью углерода. Степень очистки около 98%. Технический результат: способ исключает необходимость вводить в систему химические реагенты, соответственно повышает чистоту конечного продукта. Кроме того, в ходе электролиза диоксид углерода из природного газа заменяется образующимся на катоде газообразным водородом.
Способ позволяет производить синтез-газ, который можно использовать для дальнейших процессов синтеза спиртов, диметилового эфира, аммиака или других крупнотоннажных химических продуктов.
Однако описанный способ обладает рядом недостатков, к которым можно отнести функциональные и экономические ограничения применения способа, связанные с необходимостью выделения из природного газа больших расходов диоксида углерода (превышающих по массе расход водорода примерно в 20 раз), электролиз которого требует больших энергетических и капитальных затрат. Серьезной проблемой также является разделение конечных продуктов, резко снижающее эффективность способа.
Известен способ получения водорода и синтез-газа, содержащего в основном Н2 и СО, описанный в заявке на патент США №20090235587, дата публ. 24.09.2009, МПК C10J 3/16, в котором термохимическим образом преобразовывают углеродсодержащее топливо, чтобы произвести высокотемпературное тепло и смешанный газ, включающий воду, водород, угарный газ и углекислый газ; получение водяного пара за счет термохимического преобразования углеродсодержащего топлива, подачу пара по крайней мере к одной твердооксидной ячейке электролиза; разложение пара по крайней мере в одной твердооксидной ячейке электролиза, чтобы произвести водород и кислород; и объединение, по крайней мере, части угарного газа из смешанного газа с, по крайней мере, частью водорода, чтобы произвести синтез-газ. Недостатками данного решения являются относительно большие тепловые затраты на многостадийный нагрев потока, сложность аппаратурного оформления и возможность снижения эффективности твердооксидной ячейки электролиза в связи с относительно высокой вероятностью реакции с побочными продуктами термохимического преобразования углеродсодержащего топлива.
В то же время известен каталитический способ осуществления реакции паровой конверсии углеродсодержащей жидкости с получением продуктов реакции, содержащих водород и диоксид углерода, которые могут использоваться, например, в качестве топлива для топливных элементов (патент РФ на изобретение №2177366, дата публикации 2000.12.09). Сущность изобретения: способ осуществляется в реакторе с двумя фиксированными слоями катализатора. В качестве катализатора первого слоя используют катализатор, содержащий в качестве активного компонента металл IБ группы Периодической системы (медь, серебро, золото) и/или благородный металл, выбранный из группы, состоящей из платины, палладия, рутения, родия, иридия, нанесенный на графитоподобный углеродный носитель, катализатор первого слоя содержит активный компонент в количестве не менее 0.05 мас.%. В качестве катализатора второго слоя используют катализатор, содержащий металл VIII группы Периодической системы, выбранный из группы, состоящей из никеля, платины, палладия, рутения, родия, иридия. В реакционную смесь, поступающую на второй слой катализатора, предварительно вводят кислород или двуокись углерода с концентрацией не выше 50 об.%. Изобретение позволяет повысить эффективность процесса паровой конверсии углеродсодержащей жидкости с получением продуктов реакции, содержащих водород и диоксид углерода, путем расширения видов исходного сырья за счет использования водно-этанольных смесей, содержащих метанол, и предотвращения дезактивации катализаторов и образования побочных продуктов. Недостатком способа является необходимость дополнительного подвода воды к энергоустановке и затраты углеродсодержащей жидкости для получения водорода.
Цель настоящего изобретения состоит в том, чтобы создать новый способ, позволяющий снизить тепловые затраты на процесс получения водорода из воды, а также эффективно использовать тепловую энергию ядерного реактора.
Поставленная задача решается тем, что предложен:
Способ получения водорода, в котором проводят реакцию паровой каталитической конверсии углеродсодержащей жидкости с получением продуктов реакции, содержащих водород, при этом продукты реакции направляют на вход катодного пространства для электролиза в высокотемпературном электролизере, на выходе из катодного пространства выделяют реакционный поток, содержащий синтез-газ, который направляют на каталитический синтез углеродсодержащей жидкости, в анодном пространстве, отделенном от катодного пространства электролитическим слоем, выделяют кислород, углеродсодержащую жидкость возвращают в начало процесса на конверсию, а полученный в процессе синтеза углеродсодержащей жидкости водород очищают от оксидов углерода.
При этом:
- в качестве углеродсодержащей жидкости выбирают метанол или диметиловый эфир.
- синтез углеродсодержащей жидкости проводят при температуре выше 100°С и давлении выше 1 МПа в присутствии катализатора на основе металлов, выбранных из группы никель, медь, церий, цинк, алюминий, лантан, вольфрам, цирконий, железо, кобальт, рений, рутений, их смеси или соединения.
- конверсию углеродсодержащей жидкости ведут при температуре выше 100°С и давлении выше 0,1 МПа в присутствии катализатора на основе металлов, выбранных из группы медь, церий, цинк, алюминий, лантан, вольфрам, цирконий, никель, палладий, их смеси или соединения.
- нагрев углеродсодержащей жидкости перед конверсией ведут до температур 250-450°С через герметичные теплообменные поверхности.
- давление конверсии углеродсодержащей жидкости выбирают в диапазоне от 0,1 до 7,0 МПа.
- тепло, выделяемое при синтезе углеродсодержащей жидкости, отводят для нагрева реакционного потока.
- водород очищают от оксидов углерода за счет адсорбции, конденсации углеродсодержащей жидкости или мембранного разделения продуктов.
- путем регенеративного теплообмена углеродсодержащей жидкости с продуктами реакции, содержащими водород, изменяют температуры газовых потоков на входе и выходе паровой каталитической конверсии углеродсодержащей жидкости.
- на выходе паровой каталитической конверсии углеродсодержащей жидкости от продуктов реакции, содержащих водород, путем адсорбции или конденсации отделяют воду, которую возвращают на вход конверсии.
- в высокотемпературном электрохимическом процессе электролитический материал предпочтительно выбирают из группы, включающей легированный оксид циркония, легированный оксид церия, галлаты и протон-проводящие электролиты.
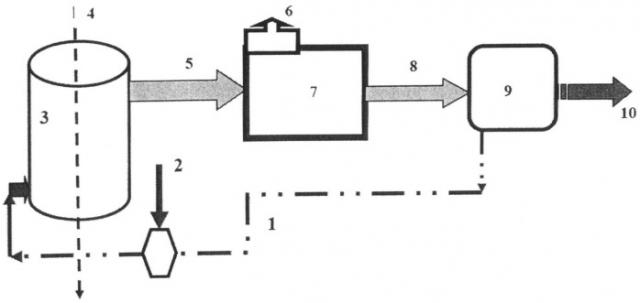
На фигуре дана схема реализации способа, где 1 - углеродсодержащая жидкость, 2 - водяной пар, 3 - каталитический реактор, 4 - теплоноситель, 5 - газообразные продукты реакции, 6 - кислород, 7 - высокотемпературный электролизер, 8 - синтез-газ, 9 - реактор синтеза, 10 - водород.
Примером реализации изобретения служит способ получения водорода из воды, описанный ниже.
В излагаемом примере осуществления изобретения в качестве углеродсодержащей жидкости 1 применяется метанол, что позволяет охарактеризовать особенности реализации изобретения применительно к процессам синтеза метанола из синтез-газа, хотя при реализации способа важным признаком является именно применение углеродсодержащей жидкости с составом, который установится после процесса синтеза, в который подают синтез-газ, полученный в высокотемпературном электрохимическом процессе.
Совокупность реакций, происходящих при реализации изобретения, изложена ниже:
Метанол 1 с давлением выше 3.5 МПа подогревают, например, регенеративным тепловым потоком, до температуры в диапазоне 100-160°С (на фигуре не показано) и нагретый поток 1 смешивают с перегретым потоком водяного пара высокого давления 2 до соотношения пар/метанол, например, равного 1,5-2,0. Образовавшийся поток направляют в каталитический реактор 3, в котором поток нагревают теплоносителем (например, дымовыми газами) 4 через герметичные теплообменные поверхности до температуры в диапазоне 250-350°С. Обычно для процесса используют цинк-хромовый катализатор синтеза метанола. Поскольку теплота для процесса получения водорода подводится извне, теплота сгорания водорода, полученного при паровой конверсии, на 15% превосходят теплоту сгорания прореагировавшего метанола. Степень конверсии метана по реакции (1) увеличивается с ростом отношения пар/газ и температуры нагрева, однако нагрев ограничен стойкостью соответствующих герметичных поверхностей. С другой стороны возможности нагрева теплоносителя также могут ограничивать его температуры, однако ниже температуры 250°С степень конверсии метана оказывается слишком низкой.
Газообразные продукты реакции 5 состоят из водорода, моноксида углерода и небольшого количества метана. Степень конверсии в оптимальных условиях составляет 90-99%, выход синтез-газа достигает 98% при 98%-ной селективности с образованием незначительного количества метана в качестве побочного продукта. Могут применяться катализаторы интерметаллического типа, применяемых для конверсии метанола до смеси газов, состоящей из водорода и оксида углерода, то есть синтез-газа. В катализатор для конверсии метанола в синтез-газ, содержащий никель, может быть дополнительно введен гидрид интерметаллического соединения формулы LaNi3Co2-xCrxHn, где 0,1<х<0,99, а n>0.
В последнее время для проведения процесса паровой конверсии метанола все чаще вместо традиционных медь-цинковых катализаторов используются катализаторы состава Cu-Се-Al, а также высокотемпературные катализаторы состава Zn/TiO2, которые имеют более высокую активность и стабильность работы, в том числе с применением микроканального реактора. Водород 10 на этой стадии настоящего изобретения не выводится, а выделяется на стадии синтеза метанола 1, например, при его конденсации.
Продукты реакции 5 направляют для электролиза в высокотемпературном электролизере 7, в котором при подводе электрической энергии осуществляют подачу продуктов реакции 5 на вход катодного пространства высокотемпературного электрохимического процесса (2), в то время как кислород 6 выделяют в анодном пространстве, отделенном от катодного электролитическим слоем. На выходе катодного пространства реакционный поток содержит преимущественно синтез-газ 8, который направляют на каталитический синтез метанола (2) с применением катализатора в реакторе синтеза 9.
Дальнейшая переработка синтез-газа 8 с составом, определяемым по выходу из высокотемпературного электрохимического процесса (2), может производиться путем одно- иди двухстадийного процесса: синтез метанола, а также, при необходимости, - его дегидратация с получением диметилового эфира (ДМЭ) и подачей непрореагировавшего метанола на дегидратацию. Метанол 1 и ДМЭ могут быть также переработаны в более тяжелые аналоги ДМЭ - полиоксиметилены с общей формулой СН3-(ОСН2)х-ОСН3 с помощью низкотемпературной (менее 100°С) каталитической дистилляции на кислотном катализаторе. В частности, смесь таких продуктов в интервалах х=3-8, называемая диметоксиметан (ДММ3-8). Степень превращения смеси СО+2Н2 в метанол 1 (степень конверсии) увеличивается с повышением давления и уменьшается с повышением температуры. Однако для увеличения скорости реакции необходимо повышение температуры. При этом, выбирая оптимальный температурный режим, необходимо учитывать образование побочных соединений: метана, высших спиртов, кислот, альдегидов, кетонов и эфиров. Оптимальный интервал температур, соответствующих наибольшему выходу продукта, определяется активностью катализатора, объемной скоростью газовой смеси и давлением. Процессы низкого давления (5-10 МПа) на медьсодержащих катализаторах осуществляют при температуре 220-280°С. Для цинк-хромового катализатора характерны более высокие давление (20-30 МПа) и температуры (350-400°С).
Расчеты показали, что выход синтез-газа 8 обеспечивает производство метанола 1 и/или ДМЭ/год при следующих технологических показателях двухстадийной схемы:
| Степень использования метанола, % | 98,00 |
| Кратность циркуляции | 6,000 |
| Катализатор синтеза метанола: | |
| Объемная скорость, нм3/м3·ч | 9743 |
| Объем, м3 | 98 |
| Число слоев | 4 |
| Катализатор синтеза ДМЭ: | |
| Объем, м3 | 19,6 |
| Производительность установки по ДМЭ, т/ч | 33,6 |
| Расход байпаса метанола, кг/ч | 13216,6 |
| Продувка, нм3/ч | 30355,8 |
| Состав конденсата, % масс | |
| ДМЭ | 40,915 |
| СН3ОН | 16,271 |
| Н2О | 42,814 |
| Температура на входе в реактор синт. мет., °С | 242,56 |
| Синтезированный метанол, нм3/ч | 33818,3 |
| Степень превращения CO+CO2 в СН3ОН, % | 87,9192 |
| Ст. превр. СО+CO2 в СН3ОН, в % от предельной | 97,6697 |
| Степень превращения CO2, % | 87,4741 |
| Степень превр. синтезированного СН3ОН в ДМЭ, % | 49,7120 |
| Байпас метанола в % от образованного, % | 27,0593 |
| Потери ДМЕ с продувкой, т/ч | 0,951 |
Суммарный выход продукционного газа (водорода) в отделении сепарации составляет 30 тыс. нм3/час.
Синтез метанола может использовать процесс, описанный в способе получения метанола и водорода (заявка РСТ №99/03807, заяв. 24.06.98 г., опубл. 28.01.1999 г., МКИ С07С 31/04), в котором синтез метанола могут проводить в одну или более стадий с выделением синтезированного метанола после каждой стадии, причем метанол отделяют от реакционного газа путем промывания холодной водой.
Синтез-газ, выходящий с электрохимической стадии имеет возможность проведения процесса получения метанола при объемном отношении (Н2-CO2/СО+СО3), равном 2,03-5,4, например, по технологии, описанной в патенте RU 2285660, заяв. 2004.04.29, в котором при определенной организации технологической схемы достигают максимальной сработки оксидов углерода в отделении синтеза метанола, а из продувочного газа после очистки получают водород. Продувочный газ после реактора синтеза может быть использован как продуктовый водород 10. При этом упрощается технологическая схема за счет исключения из нее стадий конверсии оксида углерода и очистки от диоксида углерода, а выброс оксидов углерода в атмосферу полностью отсутствует.
При совместном производстве водорода и метанола оксиды углерода служат сырьем для получения метанола в соответствии с приведенными ниже реакциями:
;
.
Таким образом, углерод природного газа не выбрасывается в атмосферу, а используется на получение продукта-метанола 1, а в процессе синтеза метанола происходит очистка продуктового водорода 10 от оксидов углерода.
По способу согласно настоящего изобретения синтезируемый метанол 1 не требуется разделять с ДМЭ и другими продуктами синтеза, поскольку в последующей стадии паровой конверсии все эти продукты большей частью будут переработаны до смеси газов 5, состоящей из водорода и оксида и диоксида углерода, то есть сырьевого синтез-газа с избытком по CO2.
Для процесса паровой конверсии ДМЭ, могут использоваться два типа катализаторов, а именно: 1) механически смещанные системы, состоящие из катализаторов гидратации ДМЭ в метанол и паровой конверсии образовавшегося метанола в водород со держащий газ; 2) бифункциональные катализаторы, содержащие активные центры, на которых обеспечивается конверсия метанола.
Таким образом, реакцию (2) частично проводят в высокотемпературном электрохимическом процессе при подводе электроэнергии и образовании на аноде продукционного кислорода, а окончательно в каталитическом синтезе метанола при отводе тепла, учитывающем экзотермический характер образования метанола из синтез-газа. Результирующий поток содержит не только метанол 1, который рассмотрен в данном примере, но и другие компоненты смеси, включая, например, диметиловый эфир, водяной пар, водород, моно- и диоксид углерода. Таким образом, реакцию паровой каталитической конверсии метанола (1) ведут с учетом данного состава по описанному выше процессу.
Суммарный процесс разложения воды в предложенном изобретении описывается реакцией (3), в которой удается получить из воды 2 водород 10 и кислород 6 высокой чистоты с необходимым для дальнейшего использования давлением.
Применение углеродсодержащей жидкости как регенерируемого сырья для получения водорода согласно настоящего изобретения уменьшает затраты на перекачку, упрощает процессы выделения водорода (конденсация), упрощает хранение промежуточного продукта, снижает температуры процессов конверсии и синтеза, повышает тепловую инерционность процессов, обеспечивает лучшее растворение CO2 в жидкости (снижение давления промежуточного продукта).
Таким образом, в предложенном изобретении удалось снизить тепловые затраты на процесс получения водорода из воды и эффективно использовать энергетический потенциал энерго- и теплоисточника, например, ядерного реактора, что позволяет рассчитывать на высокую экономическую эффективность.
Полученные продукты разложения воды - газообразные водород и кислород могут затем использовать в химической промышленности и металлургии, для переработки углеводородов, а также в системах аккумулирования и транспорта энергии и как топливо в транспортных и стационарных энергоустановках.
1. Способ получения водорода, в котором проводят реакцию паровой каталитической конверсии углеродсодержащей жидкости с получением продуктов реакции, содержащих водород, отличающийся тем, что продукты реакции направляют на вход катодного пространства для электролиза в высокотемпературном электролизере, на выходе из катодного пространства выделяют реакционный поток, содержащий синтез-газ, который направляют на каталитический синтез углеродсодержащей жидкости, в анодном пространстве, отделенном от катодного пространства электролитическим слоем, выделяют кислород, углеродсодержащую жидкость возвращают в начало процесса на конверсию, а полученный в процессе синтеза углеродсодержащей жидкости водород очищают от оксидов углерода.
2. Способ по п.1, отличающийся тем, что в качестве углеродсодержащей жидкости выбирают метанол или диметиловый эфир.
3. Способ по п.1, отличающийся тем, что синтез углеродсодержащей жидкости проводят при температуре выше 100°С и давлении выше 1 МПа в присутствии катализатора на основе металлов, выбранных из группы никель, медь, церий, цинк, алюминий, лантан, вольфрам, цирконий, железо, кобальт, рений, рутений, их смеси или соединения.
4. Способ по п.1, отличающийся тем, что конверсию углеродсодержащей жидкости ведут при температуре выше 100°С и давлении выше 0,1 МПа в присутствии катализатора на основе металлов, выбранных из группы медь, церий, цинк, алюминий, лантан, вольфрам, цирконий, никель, палладий, их смеси или соединения.
5. Способ по п.1, отличающийся тем, что нагрев углеродсодержащей жидкости перед конверсией ведут до температур 250-450°С через герметичные теплообменные поверхности.
6. Способ по п.1, отличающийся тем, что давление конверсии углеродсодержащей жидкости выбирают в диапазоне от 0,1 до 7,0 МПа.
7. Способ по п.1, отличающийся тем, что тепло, выделяемое при синтезе углеродсодержащей жидкости, отводят для нагрева реакционного потока.
8. Способ по п.1, отличающийся тем, что водород очищают от оксидов углерода за счет адсорбции, конденсации углеродсодержащей жидкости или мембранного разделения продуктов.
9. Способ по п.1, отличающийся тем, что путем регенеративного теплообмена углеродсодержащей жидкости с продуктами реакции, содержащими водород, изменяют температуры газовых потоков на входе и выходе паровой каталитической конверсии углеродсодержащей жидкости.
10. Способ по п.1, отличающийся тем, что на выходе паровой каталитической конверсии углеродсодержащей жидкости от продуктов реакции, содержащих водород, путем адсорбции или конденсации отделяют воду, которую возвращают на вход конверсии.
11. Способ по п.1, отличающийся тем, что в высокотемпературном электрохимическом процессе электролитический материал предпочтительно выбирают из группы, включающей легированный оксид циркония, легированный оксид церия, галлаты и протонпроводящие электролиты.