Конъюгат фолиевой кислоты и способ его получения
Иллюстрации
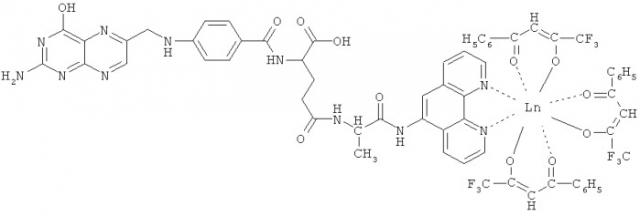
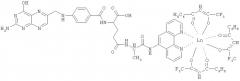
Показать всеИзобретение относится к конъюгагу фолиевой кислоты. Конъюгат включает фолиевую кислоту и хелат лантанида, связанные через спейсер L-аланин, соединенный с фенантролином, и имеет общую формулу:
где Ln представляет собой ион Eu3+, Tb3+, Sm3+, Dy3+, Yb3+, Nd3+, Er3+, Tm3+. Также предложен способ получения конъюгата. Изобретение позволяет получить конъюгат, который способен сохранять спектрально-люминесцентные свойства в биообъектах и выступать в качестве химически и спектрально стабильного молекулярного зонда. 2 н.п. ф-лы, 2 ил.
Реферат
Изобретение относится к синтезу конъюгата, содержащего фолиевую кислоту (ФК) и хелат лантанида, а также к способу получения конъюгата.
ФК является природным соединением, имеющим важное значение для переноса метильных групп в клетках, синтеза нуклеиновых кислот и белков в клетках и для роста самих клеток. ФК и ее производные, характеризуются наличием одной или двух карбоксильных групп глутаминовой кислоты (составная часть ФК). Карбоксильные группы ФК участвуют в образовании ковалентной связи со специальным спейсером - углеводородным мостиком, к которому «пришивается» с другой стороны хелат лантанида, выполняющий функцию метки. Хелат лантанида, как молекулярный зонд, обладает люминесцентными свойствами, позволяющими использовать его в составе конъюгата в качестве высокочувствительного зонда при биоисследованиях.
Активность фолатных рецепторов на большинстве опухолевых клеток заметно выше соответствующих значений для нормальных клеток (Cambell с сотр.: Cancer Res. 1991; 51:5329. Coney с сотр.: Cancer Res. 1991; 51:6125. Weirman с сотр.: Cancer Res. 1992; 52:3396). Это вызвало быстрый рост числа исследований по синтезу конъюгатов (комплексов) ФК с различными молекулярными компонентами, как объектами, нацеленными на опухолевые клетки-мишени.
Известен комплекс ФК с полисахаридами (патент РФ №2280650), который образован посредством ковалентной связи между карбоксильной группой фолиевой кислоты и гидроксильной группой полисахарида. Для определения эффекта селективного поглощения полисахаридного комплекса ФК в опухолевых клетках, регистрировалась интенсивность флуоресценции данного комплекса, меченного флуоресцеином, и ее распределение в клетках опухолевой ткани. Недостатком такого комплекса является спектральное наложение флуоресцентного свечения флуоресцеина и люминесценции клеточных биокомпонентов, а также широкополосная флуоресценция используемого красителя.
Известны конъюгаты производного ФК с нативными белками (патент РФ №2205662), полученные путем их непосредственного ковалентного связывания и, при необходимости, связывания через спейсер. Такие конъюгаты направлены исключительно на использование в терапии опухолей.
Известен конъюгат фолиевой кислоты с диэтилентриаминопентауксусной (diethylenetriaminepentaacetic) кислотой, маркированный 111In (111In-DTPA-Folate) [C.J. Mathias, S. Wang, DJ. Waters et al, J. Nucl. Med., 39(1998)1579; B.A. Siegel, F. Dehdashti, D.G. Mutch et al. J. Nucl. Med., 44(2003)700], представляющий радиоактивный медицинский препарат для сцинтиграфической диагностики злокачественных образований. Очевидно, что такой конъюгат при длительном использовании может быть опасным для живых организмов.
Известны конъюгаты фолиевой кислоты с тетрафенилпорфином [R. Schneider, F. Schmitt, C. Frochot et al, Bioorg. Medic. Chem., 13(2005)2799] или замещенным тетрафенилхлорином [J. Gravier, R. Schneider, C. Frochot et al, J. Med. Chem., 51 (2008) 3867], в структуре которых имеется спейсер. К недостаткам конъюгатов ФК с безметальными порфиринами или хлоринами можно отнести изменение их структуры при различных значениях pH среды. Кроме того, такие пигменты обладают короткоживущей, широкополосной флуоресценцией, чувствительной к незначительному химическому изменению локального окружения.
Задачей изобретения является синтез конъюгата фолиевой кислоты с хелатом лантанида, способного сохранять спектрально-люминесцентные свойства в биообъектах, т.е. выступать в качестве химически и спектрально стабильного молекулярного зонда.
Авторами синтезирован конъюгат «фолиевая кислота - спейсер - хелат лантанида» (ФК-L-аланин-(Фен)Ln(БТФА)3), структурная формула которого изображена ниже.
В качестве хелата лантанида используют комплексы с ионами Eu3+, Tb3+, Sm3+, Dy3+, Yb3+, Nd3+, Er3+, Tm3+. Применение указанного ряда трехвалентных ионов лантанидов в комплексных соединениях обусловлено тем, что для всех из них возможна сенсибилизация люминесценции в результате внутримолекулярного переноса энергии электронного возбуждения от органической части молекулы комплекса.
В предлагаемом конъюгате фолиевая кислота связана с хелатом лантанида через спейсер, т.е. между молекулярным зондом и фолиевой кислотой присутствует углеводородный мостик. Для реализации такого связывания спейсер должен иметь периферийные амино- (NH2) и карбокси- (COOH) группы. Аминогруппа спейсера присоединяется к гамма-карбоксильной группе концевого остатка глутамата фолиевой кислоты. Карбоксильная группа спейсера используется вначале для присоединения аминофенантролина, который впоследствии будет служить четвертым лигандом иона лантанида в результате образования координационных связей между атомами азота фенантролина и ионом лантанида. Благодаря этому, фенантролин, находясь в составе хелата лантанида, обеспечивает «пришивку» хелата лантанида через спейсер к фолиевой кислоте. В итоге образуется конъюгат «фолиевая кислота - спейсер - хелат лантанида».
В качестве спейсера использовано соединение с карбоксильной группой к аминофенантролину и аминогруппой к фолиевой кислоте, такое как L-аланин.
В качестве лигандов хелатных комплексов лантанида используют β-дикетоны с галогензамещенными алкильными группами и бензильными хромафорами.
Предлагаемый согласно изобретению конъюгат получен путем последовательного синтеза промежуточных компонентов.
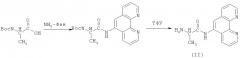
На первом этапе получения конъюгата был выполнен синтез 5-аминофенантролина (NH2-Фен) (I). Синтез NH2-Фен был реализован по известной методике [Preparation and Luminescence Properties of Hybrid Materials Containing Europium (III) Complexes Covalently Bonded to a Silica Matrix / H.R. Li [et al] // Chem. Mater. - 2002. - V.14, No.9. - P.3651-3655]. Исходным для его синтеза являлся нитрофенантролин, который был получен следующим образом. К раствору 1,10-фенантролина (1 г) в концентрированной серной кислоте (10 мл) добавляли смесь азотной (2 мл) и концентрированной серной кислоты (2 мл). После выдерживания смеси в течение 2 ч при 100°C, содержимое растворяли в воде и нейтрализовали щелочью. Светло-коричневые кристаллы выкристаллизовывали из этанола. Для получения NH2-Фен, к суспензии нитрофенантролина (1,14 г) в 40 мл ледяной уксусной кислоты добавляли раствор SnCl2·2H2O (7 г) в 40 мл концентрированной HCl. Раствор нагревали 2 ч при 100°C, после охлаждения нейтрализовали 20%-ным водным раствором NaOH. Выделившийся осадок отфильтровывали и высушивали. Схема синтеза I представлена ниже:
На втором этапе получали соединение L-аланин-Фен (II), путем присоединения NH2-Фен (I) к третбутоксикарбонил-L-аланину (BOC-L-аланин). Для этого к раствору BOC-L-аланина (0,192 г, 1 ммоль) в смеси безводного диметилсульфоксида (ДМСО) (5 мл) добавляли 1,1'-карбонилдиимидазол (КДИ) (0,194 г, 1,2 ммоль) и NH2-Фен (0,197 г, 1 ммоль). Полученную реакционную смесь перемешивали в атмосфере азота в течение 1 часа при комнатной температуре. Затем добавляли при перемешивании безводный диэтиловый эфир (100 мл), охлажденный до 0°C. Выпавшие белые кристаллы отфильтровывали и промывали диэтиловым эфиром, а затем высушивали под вакуумом. Для снятия BOC-защиты у L-аланина, к полученному соединению (0.2 г, 0.54 ммоль) добавляли трифторуксусную кислоту (ТФУ) (1,5 мл) и перемешивали при комнатной температуре в течение 2 часов. ТФУ из реакционной смеси удаляли под высоким вакуумом. Полученный осадок растворяли в безводном диметилформамиде (ДМФА). В полученный раствор добавляли холодный диэтиловый эфир до выпадения белого осадка L-аланин-Фен (II). Схема синтеза II представлена ниже:
В качестве спейсера использовано соединение с карбоксильной группой к аминофенантролину и аминогруппой к фолиевой кислоте, такое как L-аланин.
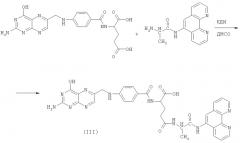
На третьем этапе - синтез промежуточного конъюгата «фолиевая кислота-L-аланин-фенантролин» (ФК-L-аланин-Фен, (III)). Синтез конъюгата ФК-L-аланин-Фен проводили по методике, использованной при синтезе конъюгата ФК с диметиловым эфиром хлорина e6 [Конъюгат диметилового эфира хлорина e6 с фолиевой кислотой: синтез, фотофизические и фотохимические свойства / А.В. Воробей [и др.] II Сборник статей Международной научной конференции «Молекулярные, мембранные и клеточные основы функционирования биосистем" - Минск: Изд. центр БГУ, Часть 1. - 2008. - С.39-41]. Для синтеза конъюгата III использовали ФК фирмы «Sigma». Остальные коммерческие реагенты, используемые для синтеза, подвергались предварительной очистке. К раствору фолиевой кислоты (0,1 г, 0,2 ммоль) в смеси безводного ДМСО (10 мл) и пиридина (3 мл) добавляли 1,1'-карбонилдиимидазол (0,037 г, 0,22 ммоль) и L-аланин-Фен (II) (0,083 г, 0,2 ммоль) растворенный в 3 мл ДМСО. Полученную реакционную смесь перемешивали в атмосфере азота в течение 10 часов при комнатной температуре. Затем продукты реакции отфильтровывали и в фильтрат добавляли безводный диэтиловый эфир (100 мл), охлажденный до 0°C. Выпавшие желтые кристаллы отфильтровывали и промывали диэтиловым эфиром, а затем высушивали под вакуумом. Схема синтеза III представлена ниже:
В качестве хелата лантанида были избраны β-дикетонатные комплексы лантанидов (Ln(БТФА)3 (IV), где БТФА - бензоилтрифторацетон, Ln-Eu3+, Tb3+, Sm3+, Dy3+, Yb3+, Nd3+, Er3+, Tm3+.
Синтез β-дикетонатных комплексов лантанидов проводили по следующей методике: навеску β-дикетона растворяли в этаноле, и при интенсивном перемешивании добавляли водный раствор NaOH концентрацией 1 моль/л до pH=7. В полученную смесь добавляли водный раствор нитрата лантанида - Ln(NO3)3 до выпадения осадка. Осадок отфильтровывали, промывали смесью воды и этаноле в соотношении 1:1 и сушили до постоянного веса. Структура IV изображена ниже:
В качестве лигандов хелатных комплексов лантанида используют)3-дикетоны с галогензамещенными алкильными группами и бензильными хромафорами.
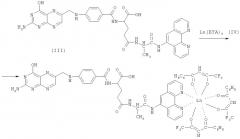
На последнем (четвертом) этапе синтеза предлагаемый согласно изобретению конъюгат «фолиевая кислота - спейсер-хелат лантанида» (ФК-L-аланин-(Фен)Ln(БТФА)3) получали следующим образом: к 10 мг конъюгата ФК-L-аланин-Фен (III) в 3 мл ДМСО добавляли комплекс Ln(БТФА)3 (IV) в стехиометрическом соотношении 1:1, растворенного в 3 мл ДМСО и перемешивали в течение трех часов, а затем в реакционную смесь добавляли охлажденную дистиллированную воду до выпадения кристаллов конъюгата.
Заявляемый конъюгат может быть использован в качестве высокочувствительного люминесцентного зонда при биоисследованиях. В частности, он может быть применен для выявления экспрессирующих фолатный рецептор клеток. Согласно литературным данным [Катеп В.A., Smith А.K. Review of folate receptor alpha cycling and 5-methyltetrahydrofolate accumulation with an emphasis on cell models in vitro // Drug Delivery Rev. - 2004. - V.56. - P.1085-1097], при ряде онкологических заболеваний наблюдается повышенная экспрессия фолатных рецепторов быстро делящимися опухолевыми клетками. Поскольку как свободная, так и конъюгированная фолиевая кислота селективно и с высоким сродством связываются с фолатным рецептором [Zhao X., Li Н., Lee R.J. Targeted drug delivery via folate receptors. // Expert Opin Drug Deliv. - 2008. - V.5, No.3. - P.309-319], то полученный нами коньюгат обеспечит селективную доставку зондов (хелаты лантанидов) в опухолевые клетки.
Возможность определения экспрессирующих фолатный рецептор клеток с использованием синтезированного конъюгата показана нами на примере злокачественно трансформированных клетках эпителия шейки матки (клетки HeLa). Клетки культивировали в питательной среде 199, содержащей низкую концентрацию (2·10-8 моль/л) фолиевой кислоты. Для проверки способности полученного конъюгата связываться с клетками в монослое в культуральную среду вводили конъюгат ФК-L-аланин-(Фен)Eu(БТФА)3. Использовали монослой при конфлюентности 70-90% и концентрацию конъюгата 5·10-7 моль/л. Клетки инкубировали с конъюгатом в течение 3-х часов после чего трижды промывали охлажденным физиологическим раствором для удаления не связавшегося конъюгата. Связывание клетками конъюгата определяли по интенсивности люминесценции европия с использованием флуоресцентной микроскопии. Выявлено резкое усиление люминесценции инкубированных с конъюгатом клеток при условиях возбуждения и регистрации люминесценции европия, что свидетельствует о связывании конъюгата с клетками. В контрольном эксперименте в культуральную среду перед введением конъюгата добавляли свободную фолиевую кислоту в высокой концентрации (1·10-4 моль/л) и наблюдали выраженное снижение связывания с клетками конъюгата. Поскольку свободная фолиевая кислота выступает в роли конкурента конъюгату в связывании с фолатными рецепторами, полученные данные свидетельствуют об определяющей роли фолатного рецептора в связывании конъюгата с клетками HeLa, т.е. конъюгат может служить эффективным зондом для определения экспрессирующих фолатный рецептор клеток.
Примером доказательства решения поставленной задачи являются спектральные исследования конъюгата ФК-L-аланин-(Фен)Eu(БТФА)3 и промежуточных продуктов его синтеза.
На фигуре 1 представлены спектры поглощения I (NH2-Фен), кривая 1; ФК, кривая 2 и промежуточного конъюгата III («фолиевая кислота-L-аланин-фенантролин» (ФК-L-аланин-Фен)), кривая 3 в этиловом спирте. Спектр поглощения I имеет интенсивную полосу поглощения при 263 нм с длинноволновым нисходящим до -330 нм крылом. Спектр поглощения ФК в УФ-области имеет максимумы при 286 и 361 нм. Спектр поглощения III кривая 3 существенно отличается от спектров поглощения исходных веществ, что является доказательством образования конъюгата ФК-L-аланин-Фен. Для конъюгированной молекулы длинноволновая полоса поглощения претерпевает гипсохромный сдвиг до 335 нм (по сравнению с полосой ФК - 361 нм). Аналогичным образом смещается и вторая полоса поглощения ФК (286 нм), которая в конъюгате локализована при 278 нм.
Спектр поглощения конъюгата ФК-L-аланин-(Фен)Eu(БТФА)3 в ДМФА изображен на фигуре 2, кривая 1. Его отличие от спектра поглощения III на фигуре 2, кривая 1 состоит в увеличении относительной интенсивности полосы при 326 нм, которой соответствует поглощение органических аддендов иона европия (БТФА). Возбуждение при λ=283 нм приводит к появлению сложного спектра люминесценции (фигура 2, кривая 2) - одновременно наблюдается очень слабое свечение свободной ФК с максимумом при - 475 нм, слабое свечение с максимумом при 333 нм (свечение III) и интенсивная люминесценция иона европия в области 580-710 нм с узкой и интенсивной полосой при 613 нм. Кривая 3 на фигуре 2 - спектр возбуждения люминесценции при λрег=613 нм полностью соответствует поглощению органических лигандов иона европия (поглощению БТФА). Последнее может свидетельствовать о возбуждении иона европия через поглощение промежуточного конъюгата III, подтверждая химическое связывание хелата европия IV с промежуточным конъюгатом III, т.е. образование полученного конъюгата ФК-L-аланин-(Фен)Eu(БТФА)3.
1. Конъюгат фолиевой кислоты, включающий фолиевую кислоту и хелат лантанида, связанных через спейсер L-аланин, соединенный с фенантролином, имеющий общую формулу: при этом лантанид представляет собой ион Eu3+, Tb3+, Sm3+, Dy3+, Yb3+, Nd3+, Er3+, Tm3+.
2. Способ получения конъюгата фолиевой кислоты, заключающийся в том, что берут нитрофенантролин, полученный из раствора 1,10-фенантролина и концетпрированной серной кислоты, добавляют в него смесь азотной и концентрированной серной кислоты, смесь выдерживают в течение 2 ч при 100°C, растворяют в воде и нейтрализуют щелочью, выкристаллизовывают из этанола кристаллы нитрофенантролина; к суспензии нитрофенантролина и ледяной уксусной кислоты добавляют раствор SnCl2·2H2O в концентрированной HCl, выделившийся осадок отфильтровывают и высушивают, и затем к раствору BOC-L-аланина, в смеси безводного диметилсульфоксида (ДМСО) добавляют 1,1'-карбонилдиимидазол и NH2-Фен, полученную реакционную смесь перемешивают в атмосфере азота в течение 1 ч при комнатной температуре и добавляют безводный диэтиловый эфир, охлажденный до 0°C, выпавшие кристаллы отфильтровывают и промывают диэтиловым эфиром, высушивают под вакуумом, осадок растворяют в безводном диметилформамиде, в раствор добавляют диэтиловый эфир до выпадения осадка L-аланин-Фен, который после фильтрации промывают эфиром и сушат под вакуумом; к раствору фолиевой кислоты (ФК) в смеси безводного ДМСО и пиридина добавляют 1,1'-карбонилдиимидазол и L-аланин-Фен растворенный в ДМСО, полученную реакционную смесь перемешивают в атмосфере азота в течение 10 ч при комнатной температуре, продукты реакции отфильтровывают и в фильтрат добавляют при перемешивании безводный диэтиловый эфир охлажденный до 0°C, выпавшие кристаллы ФК-L-аланин-Фен отфильтровывают и промывают диэтиловым эфиром, а затем высушивают под вакуумом; к раствору ФК-L-аланин-Фен в ДМСО добавляют комплекс Ln(БТФА)3, растворенный в ДМСО, перемешивают в течение трех часов и добавляют в реакционную смесь охлажденную дистиллированную воду до выпадения кристаллов конъюгата ФК-L-аланин-(Фен)Ln(БТФА)3.