Способ определения родия в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления меди из rhxcuy
Иллюстрации
Показать всеИзобретение относится к аналитической химии, а именно к способам определения содержания ионов металлов для определения в питьевых и природных водах методом инверсионной вольтамперометрии (ИВ). Способ определения родия в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления меди из RhxCuy согласно изобретению заключается в том, что родий (III) в растворе переводят в хлоридный комплекс и проводят вольтамперометрическое определение, при этом накопление ионов родия на сажевом электроде в перемешиваемом растворе в присутствии ионов меди (II) проводят в течение 60-120 секунд с последующей регистрацией анодных пиков селективного электроокисления меди из интерметаллического соединения RhxCuy при скорости развертки потенциала 60-100 мВ/с при потенциалах электролиза минус 0,8 В на фоновом электролите 1 М HCl, а концентрацию ионов родия определяют по высоте анодного пика меди на вольтамперной кривой в диапазоне потенциалов от 0,1 до 0,2 В относительно насыщенного хлоридсеребряного электрода методом добавок аттестованных смесей. Изобретение обеспечивает возможность снизить предел и нижнюю границу определяемых содержаний родия (III) по пику электроокисления меди из интерметаллического соединения RhxCuy. 2 ил., 2 пр.
Реферат
Способ определения родия в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления меди из RhxCuy.
Изобретение относится к аналитической химии, а именно к способам определения содержания ионов металлов для определения в питьевых и природных водах методом инверсионной вольтамперометрии (ИВ).
Известен метод полярографического определения родия на платиновом электроде. При определении используется платиновая проволока на фоне 0,1 N NaNO3. Волна наблюдается при потенциале электролиза 0,2 В относительно насыщенного каломельного электрода. Определяемая концентрация родия составила 4,5×10-3 г/л [Бардин М.Б., Ляликов Ю.С., Темянко В.С. «Полярографическое определение некоторых благородных металлов с применением платиновых электродов» // Сб. «Анализ благородных металлов». - 1959. - М.: АН СССР, - С.80-87]. Недостатком метода является низкая чувствительность и использование дорогостоящей платиновой проволоки.
Известен метод определения родия инверсионной вольтамперометрии с использованием стеклоуглеродного электрода в растворе 1 М HCl с добавлением соли Hg(I). Электродом сравнения служит насыщенный каломельный электрод. В исследованиях концентрация родия составляла 2×10-5 г/л. Потенциал электролиза - 0,5 В, время электролиза составляет 6 мин [Попов Г.Н., Пнев В.В., Захаров М.С. «Определение родия методом инверсионной вольтамперометрии» // Журнал аналитической химии. - 1972. - Т.27. - Вып.12. - С.2456-2458]. Недостатком метода является низкая чувствительность и использование токсичных соединений ртути.
Известен метод определения родия в водном растворе методом пленочной полярографии на твердых электродах в 0,1 М HCl с добавлением Hg(NO3)2. Определяемая концентрация родия составила 1,03×10-4 г/л [Чемерис М.С., Колпакова Н.А., Стромберг А.Г., Васильев Ю.Б. «Механизм разряда и ионизации ионов родия и иридия на графитовом электроде в присутствии ионов ртути (II)» // Электрохимия - 1976. - Т.12. - №.5. - С.717-722]. Недостатком метода является низкая чувствительность и использование солей токсичной ртути.
Известен метод определения родия вольтамперометрическим методом [Шифрис Б.С., Колпакова Н.А. «Совместное определение родия и иридия методом инверсионной вольтамперометрии в медно-никелевых концентратах» // Журнал аналитической химии. - 1982. - Т.37. - Вып.12. - С.2217-2220] (прототип). Определение родия проводят по следующей методике. В качестве фонового электролита используют раствор 0,5 М HCl. Электроосаждение проводилось при потенциале электролиза Еэ=-0,6 В относительно насыщенного каломельного электрода, время накопления tнак составляет от 1 до 25 мин. В качестве модификатора поверхности электрода используется соль ртути (II). Недостатком метода является использование токсичных солей ртути и низкая чувствительность 1 мг/л.
В работе была поставлена задача снизить предел и нижнюю границу определяемых содержаний родия (III) по пику электроокисления меди из интерметаллического соединения RhxCuy, полученном после осаждения Rh-Cu на сажевом электроде методом ИВ.
Поставленная задача достигается тем, что родий (III) переводят в растворе в хлоридный комплекс и проводят вольтамперометрическое определение. Накопление ионов родия на сажевом электроде (СЭ) в перемешиваемом растворе в присутствии ионов меди (II) проводят в течение 60-120 секунд с последующей регистрацией анодных пиков селективного электроокисления меди из интерметаллического соединения RhxCuy при скорости развертки потенциала 60-100 мВ/с при потенциалах электролиза минус 0,8 В на фоновом электролите 1 М HCl, концентрацию ионов родия определяют по высоте анодного пика меди на вольтамперной кривой в диапазоне потенциалов от 0,1 до 0,2 В относительно насыщенного хлоридсеребряного электрода методом добавок аттестованных смесей. Новым в способе является то, что для получения полезного сигнала, зависящего от концентрации родия (III), используется процесс электроокисления меди из ИМС RhxCuy.
В предлагаемом способе впервые установлена способность осадка родия с медью окисляться с поверхности СЭ. В качестве индикаторного применяли СЭ модифицированный медью (в прототипе применяли графитовый электрод). Использование таких электродов обусловлено высокой химической и электрохимической устойчивостью графита, широкой областью рабочих потенциалов, а также простотой механического обновления поверхности и требованиям техники безопасности. Нижняя граница определяемых содержаний по данному методу составила 0,1 мг/дм3 (в прототипе 1 мг/дм3).
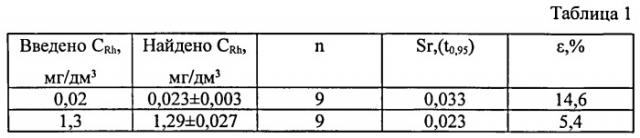
Результаты определения родия из ИМС на СЭ модифицированным медью приведены в: таблице 1 результат определения родия (III) в фоновом электролите (1 М HCl) и таблице 2 результат определения родия (III) в водопроводной воде. Как видно из таблиц, максимальная погрешность измерений составляет порядка 15%. Расчет определяемых концентраций родия проводится по методу «Введено-найдено».
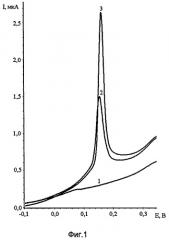
Проводят накопление ионов родия (III) на поверхность сажевого электрода в перемешиваемом растворе в присутствии ионов меди (II) в течение 60-120 с при потенциале электролиза минус 0,8 В. При потенциале минус 0,8 В анодный пик достигает своего предельного значения. Дальнейшее увеличение потенциала электролиза вызывает пассивацию поверхности электрода водородом и количество меди электровосстановленной на поверхности СЭ снижается, что приводит к искажению формы или уменьшению пика ИМС меди с родием, поэтому выбирался потенциал электролиза минус 0,8 В. Измерения проводились на фоне 1 М HCl, с последующей регистрацией анодных пиков в накопительном режиме и съемки вольтамперограмм при скорости развертки 60-100 мВ/с. Концентрацию ионов родия (III) определяют по высоте анодного пика меди в диапазоне потенциалов от 0,1 до 0,2 В относительно насыщенного хлоридсеребряного электрода (нас. х.с.э). На фиг.1 представлены вольтамперные кривые электроокисления осадка RhxCuy с поверхности СЭ модифицированного медью. Кривая 1 - фон 1М HCl, где CCu(II) равна 0,01 мг/дм3, кривая 2 - CRh(III) равна 0,02 мг/дм3, кривая 3 - CRh(III) равна 0,04 мг/дм3.
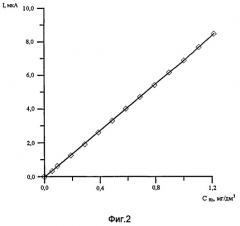
Таким образом, установленные условия впервые позволили количественно определять содержание ионов родия (III) на основе реакции селективного электроокисления меди из ИМС RhxCuy, полученного на стадии предварительного электроконцентрирования в интервале 0,1-10 мг/дм3 (фиг.2).
Предлагаемый вольтамперометрический способ позволил существенно улучшить метрологические характеристики анализа родия (III); повысить чувствительность определения (0,1·мг/дм3), что на порядок ниже по сравнению с прототипом.
Примеры конкретного выполнения
Пример 1. (фиг.1). Измерения были проведены на искусственных смесях. 10 мл фонового электролита (1М HCl) помещают в кварцевый стаканчик. Не прекращая перемешивания, проводят электролиз раствора, при Еэ=-0,8 В и при τэ=100 сек, снимают вольтамперную кривую электроокисления при скорости развертки 80 мВ/с. Затем добавляют аттестованный раствор Cu (II) 0,01 мл из 10 мг/дм3 и проводят электрохимическое концентрирование осадка при аналогичных условиях. Отсутствие пиков на вольтамперной кривой в интервале от 0,1 до плюс 0,2 В свидетельствует о чистоте фона. Вносят добавку стандартного образца родия 0,02 мл из 0,1 мг/дм3, регистрируют аналитический сигнал родия при потенциале накопления -0,8 В. Затем вносят еще одну добавку стандартного образца родия 0,02 мл из 0,1 мг/дм3 и регистрируют аналитический сигнал родия при аналогичных условиях. По разнице токов пиков меди вычисляют концентрацию родия в растворе. Пик тока меди регистрируют в диапазоне потенциалов от 0,1 до 0,2 В (нас. х.с.э.).
Пример 2. Измерения родия были проведены в водопроводной воде (таблица 2). 100 мл раствора, помещают в коническую колбу и выпаривают до минимального объема. Количественно переносят раствор в кварцевый стакан объемом 20 мл и добавляют 37% HCl, чтобы в 10 мл водного раствора концентрация по соляной кислоте составила 1М, для перевода солей родия в хлориды.
Снимают фоновую кривую: 10 мл фонового электролита (1М HCl) помещают в кварцевый стаканчик, добавляют аттестованный раствор Cu (II) 0,01 мл из 10 мг/дм3, не прекращая перемешивания, проводят электролиз раствора, при Еэ=-0,8 В и при τэ=100 сек, снимают вольтамперную кривую электроокисления при скорости развертки 80 мВ/с. Отсутствие пиков на вольтамперной кривой в интервале от 0,1 до плюс 0,2 В свидетельствует о чистоте фона.
Добавляют аликвотную часть 1-2 мл полученного раствора и снимают вольтамперную кривую электроокисления при потенциале накопления -0,8 В. Затем вносят добавку стандартного образца родия 0,02 мл из 0,1 мг/дм3 и регистрируют аналитический сигнал при потенциале накопления -0,8 В. По разнице токов пиков меди вычисляют концентрацию родия в растворе. Пик тока меди регистрируют в диапазоне потенциалов от 0,1 до 0,2 В (нас. х.с.э.).
Таким образом, впервые установлена способность количественного анализа родия по пикам селективного электроокисления меди из интерметаллического соединения RhxCuy.
Способ может быть применен в любой химической лаборатории, имеющей компьютеризированные анализаторы типа СТА и ТА.
Предложенный способ может быть использован для определения родия в водных растворах.
Способ определения родия в водных растворах методом инверсионной вольтамперометрии по пику селективного электроокисления меди из RhxCuy, заключающийся в том, что родий (III) в растворе переводят в хлоридный комплекс и проводят вольтамперометрическое определение, отличающийся тем, что накопление ионов родия на сажевом электроде в перемешиваемом растворе в присутствии ионов меди (II) проводят в течение 60-120 с с последующей регистрацией анодных пиков селективного электроокисления меди из интерметаллического соединения RhxCuy при скорости развертки потенциала 60-100 мВ/с при потенциалах электролиза минус 0,8 В на фоновом электролите 1 М HCl, концентрацию ионов родия определяют по высоте анодного пика меди на вольтамперной кривой в диапазоне потенциалов от 0,1 до 0,2 В относительно насыщенного хлоридсеребряного электрода методом добавок аттестованных смесей.