Способ неинвазивного определения кислородного статуса тканей
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к лучевой терапии, и может быть использовано для неинвазивного определения кислородного статуса тканей опухоли и окружающих нормальных тканей. Для этого указанные ткани подвергают воздействию радиомодифицирующего агента. Затем методом оптической диффузионной спектроскопии осуществляют сканирование исследуемых тканей до, а также несколько раз после воздействия радиомодифицирующего агента. Далее вычисляют концентрации окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей. Затем выводят графики динамики концентраций окисленного, восстановленного и общего гемоглобина, кислородного статуса исследуемых тканей. По графику динамики кислородного статуса тканей опухоли и окружающих нормальных тканей, в случае повышения кислородного статуса тканей опухоли, вычисляют временной интервал с максимальной разницей значений кислородного статуса тканей опухоли и окружающих нормальных тканей. Данный интервал расценивают как оптимальный для максимального повреждающего действия ионизирующего излучения на ткани опухоли и безопасный для окружающих нормальных тканей. По графикам динамики концентраций окисленного, восстановленного и общего гемоглобина определяют механизм воздействия радиомодифицирующего агента на исследуемые ткани. Способ позволяет устанавливать параметры радиомодифицирующего воздействия, такие как вид агента, временной интервал воздействия, доза радиомодифицирующего агента, оптимальные для максимального повреждающего действия ионизирующего излучения на ткани опухоли и безопасные для окружающих нормальных тканей. 3 з.п. ф-лы, 3 ил.
Реферат
Изобретение относится к медицине, а именно к лучевой терапии, и может быть использовано для определения параметров радиомодифицирующего воздействия (вид агента, временной интервал воздействия, доза радиомодифицирующего агента), оптимальных для максимального повреждающего действия ионизирующего излучения на ткани опухоли и безопасных для окружающих нормальных тканей.
Кислородный статус определяется как уровень насыщения крови кислородом, выражается в процентах и рассчитывается как отношение концентраций окисленного гемоглобина и общего гемоглобина (суммы окисленного и восстановленного). Кислородный статус опухолевой ткани рассматривается в настоящее время как ключевой фактор, определяющий прогноз заболевания и эффективность лечебных воздействий. При наличии обширных зон гипоксии эффективность лучевой терапии снижается за счет феномена репарации сублетальных повреждений, которая становится возможной вследствие отсутствия фиксации кислородом однонитевых разрывов ДНК. Объем гипоксических зон и степень выраженности гипоксии не могут быть прогнозированы в зависимости от размера, стадии, гистологического строения, степени дифференцировки и локализации опухоли. Для повышения радиочувствительности ткани опухоли в организм вводят радиомодифицирующие агенты, повышающие уровень ее оксигенации. Изучение динамики кислородного статуса опухоли и нормальных тканей под влиянием радиомодифицирующих агентов необходимо с целью оптимизации дозо-временных параметров данного воздействия.
Известен способ контроля уровня оксигенации опухоли при радиомодифицирующем воздействии по статье «Pentoxifylline enhances tumor oxygenation and radiosensitivity in rat rhabdomyosarcomas during continuous hyperfractionated irradiation», Strahlenther Onkol 2004; 180:306-14. авторов Friedrich Zywietz, Lothar Bohm, Christoph Sagowski, Wolfgang Kehrl. В качестве способа контроля используется прямое полярографическое исследование с использованием электродов, вводимых в исследуемые ткани до и после радиомодифицирующего воздействия. Данный способ является инвазивным и не дает картины пространственного распределения уровня оксигенации в нормальных и опухолевых тканях.
Оптические методы (ИК-спектроския, оптическая диффузионная томография) дают возможность неинвазивного определения кислородного статуса тканей на основе информации о локальных изменениях оптических параметров (поглощение и рассеяние) и визуализации локальных метаболических процессов в исследуемой области. Данные методы позволяют определять концентрации окисленного и восстановленного гемоглобина и, соответственно, выделять участки с различным насыщением крови кислородом.
По патенту RU 2341306, МПК A61N 5/067 (2006.01) от 19.07.2007 г. известен способ лечения онкологических больных. Больному проводят лазерную диагностику и определяют индекс микроциркуляции в тканях пальцев рук до начала окклюзионной пробы и после окклюзионной пробы, а также показатель сатурации кислородом до и непосредственно перед завершением окклюзионной пробы, затем больному вводят радиомодифицирующие вещества и через 1-1,5 ч повторно определяют показатели микроциркуляции и сатурации, и при значении этих показателей в определенных пределах проводят сеанс лучевой терапии.
Недостатком данного способа является то, что о кислородном статусе ткани опухоли судят на основе косвенной информации о насыщении крови кислородом нормальных тканей (пальцев рук). При этом не учитывается, что радиомодифицирующие агенты могут оказывать различное влияние на кислородный статус нормальных и опухолевых тканей. Кроме того, показатели кислородного статуса тканей снимаются двукратно, до и после радиомодифицирующего воздействия. Для определения временного интервала, оптимального для максимального повреждающего действия на ткани опухоли и безопасного для близлежащих нормальных тканей, необходимо многократное определение кислородного статуса ткани опухоли и окружающих нормальных тканей.
Ближайшим аналогом разработанного способа является способ неинвазивного определения кислородного статуса исследуемых тканей, известный по патенту RU 2437617, МПК А61В 5/145 (2006.01) от 27.05.2010 г.
Методом оптической диффузионной спектроскопии проводят исследование тканей опухоли и окружающих нормальных тканей, вычисляют концентрации окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей, выводят распределения окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей в виде двумерного изображения.
Недостатком данного способа является невозможность изучить динамику концентраций окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей и определить оптимальные дозо-временные параметры и механизмы радиомодифицирующего воздействия. Кроме того, однократное определение кислородного статуса не позволяет судить о патофизиологических механизмах ответа тканей опухоли на воздействие различных радиомодифицирующих агентов.
Задачей, на решение которой направлено данное изобретение, является разработка способа неинвазивного определения кислородного статуса исследуемых тканей, при котором вычисляют временной интервал, оптимальный для максимального повреждающего действия ионизирующего излучения на ткани опухоли и безопасный для окружающих нормальных тканей, а также определяют механизм воздействия радиомодифицирующего агента на исследуемые ткани.
Указанный технический результат достигается благодаря тому, что разработанный способ неинвазивного определения кислородного статуса исследуемых тканей, так же как и способ, который является ближайшим аналогом, включает исследование тканей опухоли и окружающих нормальных тканей методом оптической диффузионной спектроскопии, вычисление концентраций окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей, выведение распределений окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей в виде двумерного изображения.
Новым в разработанном способе неинвазивного определения кислородного статуса исследуемых тканей является то, что исследуемые ткани подвергают воздействию радиомодифицирующего агента, концентрации окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей вычисляют до, а также несколько раз с определенным интервалом после воздействия радиомодифицирующего агента, выводят графики динамики концентраций окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей, по графику динамики кислородного статуса тканей опухоли и окружающих нормальных тканей при повышении кислородного статуса тканей опухоли вычисляют временной интервал с максимальной разницей значений кислородного статуса тканей опухоли и окружающих нормальных тканей, его расценивают как оптимальный для максимального повреждающего действия ионизирующего излучения на ткани опухоли и безопасный для окружающих нормальных тканей, по графикам динамики концентраций окисленного, восстановленного и общего гемоглобина определяют механизм воздействия радиомодифицирующего агента на исследуемые ткани.
В первом частном случае реализации разработанного способа неинвазивного определения кислородного статуса исследуемых тканей в качестве радиомодифицирующего агента используют различные радиомодифицирующие агенты, обладающие различными механизмами действия, с последующим анализом их эффективности.
Во втором частном случае реализации разработанного способа неинвазивного определения кислородного статуса исследуемых тканей в качестве радиомодифицирующего агента используют пентоксифиллин.
В третьем частном случае реализации разработанного способа неинвазивного определения кислородного статуса исследуемых тканей в качестве радиомодифицирующего агента используют радиомодифицирующий агент в различной дозировке с последующим анализом его эффективности в различных дозировках.
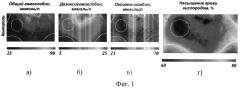
На фиг.1 представлены изображения двумерного распределения: концентраций общего (а), восстановленного (б) и оксисленного (в) гемоглобина, а также кислородного статуса (г) экспериментальной опухоли лимфосаркомы Плисса и окружающих нормальных тканей перед введением радиомодифицирующего агента.
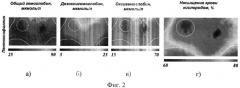
На фиг.2 представлены изображения двумерного распределения: концентраций общего (а), восстановленного (б) и окисленного (в) гемоглобина, а также кислородного статуса (г) экспериментальной опухоли лимфосаркомы Плисса и окружающих нормальных тканей через 30 мин после введения радиомодифицирующего агента (пентоксифиллина).
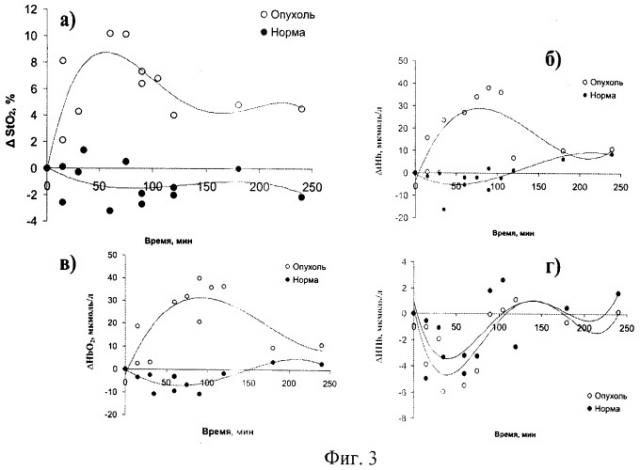
На фиг.3 представлены графики динамики кислородного статуса (а) и концентраций общего tHb (б), окисленного HbO2 (в), восстановленного HHb (г) гемоглобина в экспериментальной опухоли лимфосаркомы Плисса и в окружающих нормальных тканях после введения радиомодифицирующего агента (пентоксифиллина в дозе 10 мг/кг).
На фиг.1 и 2 в качестве примеров представлены двумерные изображения распределения: концентраций общего (а), восстановленного (б) и оксисленного (в) гемоглобина, а также кислородного статуса (г) экспериментальной опухоли лимфосаркомы Плисса и окружающих нормальных тканей до и через 30 мин после введения пентоксифиллина в дозе 10 мг/кг. Сплошной линией обозначен контур экспериментального животного. Пунктиром обозначена зона опухоли. Изображения представлены в псевдоцветной радужной палитре, где оттенки синего соответствуют минимальным значениям, красного - максимальным значениям определяемого параметра.
В разработанном способе осуществляется многократное исследование методом оптической диффузионной спектроскопии и получение изображений опухолей и нормальных тканей. На изображениях оконтуриваются зоны, соответствующие зоне опухоли и зоне окружающих нормальных тканей.
Затем на основе информации о концентрациях окисленного, восстановленного, общего гемоглобина и кислородною статуса исследуемых тканей до и в каждой временной точке после воздействия радиомодифицирующего агента строятся графики временной динамики обозначенных параметров.
На фиг.3 представлены графики динамики кислородного статуса (а) и концентраций общего tHb (б), окисленного HbO2 (в), восстановленного ННЬ (г) гемоглобина в экспериментальной опухоли лимфосаркомы Плисса и в окружающих нормальных тканях после введения пентоксифиллина.
Динамика получена при повторных исследованиях, проводимых каждые 15-30 мин в течение 4 часов. На графике динамики кислородного статуса (а) исследуемых тканей видно, что пентоксифиллин вызывал повышение кислородного статуса в тканях опухоли (белые точки) уже в первые 15 минут, которое сохранялось в течение 100 минут, после чего кислородный статус снижался до исходных значений.
Для подбора оптимальных параметров облучения необходимы данные о радиочувствительности как новообразования, так и окружающих нормальных тканей. Поэтому важно отметить, что в окружающих нормальных тканях (черные точки) препарат не оказал выраженного влияния на их кислородный статус.
Последнее имеет существенное значение в тех случаях, когда необходимо направленно повысить радиочувствительность опухоли к проводимой лучевой терапии, не оказывая влияния на окружающие нормальные ткани.
Таким образом, по графику динамики кислородного статуса тканей опухоли и окружающих нормальных тканей выбираем временной интервал, в течение которого кислородный статус опухоли остается повышенным по сравнению с исходным значением. При этом разница значений кислородного статуса ткани опухоли и окружающих нормальных тканей должна быть максимальной. Этот временной интервал расценивают как оптимальный для максимального повреждающего действия ионизирующего излучения на ткани опухоли и безопасный для окружающих нормальных тканей.
При использовании разработанного способа возможна оценка эффективности различных радиомодифицирующих агентов. С этой целью выбирается ряд радиомодифицирующих агентов, обладающих различными механизмами действия. Проводится мониторинг кислородного статуса исследуемой опухоли под воздействием этих различных радиомодифицирующих агентов. Выбирается радиомодифицирующий агент, с помощью которого возможно оказать максимальное повреждающее действие на исследуемый вид опухоли.
С использованием разработанного способа возможен выбор оптимальной дозировки радиомодифицирующего агента. С этой целью выбирается ряд различных доз агента в рамках его терапевтического интервала. Проводится мониторинг кислородного статуса опухоли под воздействием различных доз агента, выбирается минимальная доза из тех, при которых наблюдается максимальный подъем кислородного статуса.
Разработанный способ позволяет не только определить оптимальные дозо-временные параметры, но и выявить механизмы воздействия радиомодифицирующего агента на исследуемые ткани. Причинами изменения кислородного статуса исследуемых тканей могут быть изменение скорости потребления кислорода, изменение скорости доставки кислорода или оттока крови. Известно, что повышение уровня дезоксигемоглобина в тканях наблюдается в случае увеличения потребления кислорода или увеличения оттока крови, повышение уровня оксигемоглобина - в случае повышения его поступления, а общего гемоглобина - при повышении кровенаполнения.
В случае пентоксифиллина в первые часы после введения препарат не вызывает снижения потребления кислорода, однако он способен временно повысить приток насыщенной кислородом крови к опухоли и тем самым индуцировать повышение ее кислородного статуса.
1. Способ неинвазивного определения кислородного статуса исследуемых тканей, включающий исследование тканей опухоли и окружающих нормальных тканей методом оптической диффузионной спектроскопии, вычисление концентраций окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей, выведение распределений окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей в виде двумерного изображения, отличающийся тем, что исследуемые ткани подвергают воздействию радиомодифицирующего агента, концентрации окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей вычисляют до, а также несколько раз с определенным интервалом после воздействия радиомодифицирующего агента, выводят графики динамики концентраций окисленного, восстановленного и общего гемоглобина и кислородного статуса исследуемых тканей, по графику динамики кислородных статусов тканей опухоли и окружающих нормальных тканей при повышении кислородного статуса тканей опухоли вычисляют временной интервал с максимальной разницей значений кислородного статуса тканей опухоли и окружающих нормальных тканей, его расценивают как оптимальный для максимального повреждающего действия ионизирующего излучения на ткани опухоли и безопасный для окружающих нормальных тканей, по графикам динамики концентраций окисленного, восстановленного и общего гемоглобина определяют механизм воздействия радиомодифицирующего агента на исследуемые ткани.
2. Способ неинвазивного определения кислородного статуса тканей по п.1, отличающийся тем, что в качестве радиомодифицирующего агента используют различные радиомодифицирующие агенты, обладающие различными механизмами действия, с последующим анализом их эффективности.
3. Способ неинвазивного определения кислородного статуса тканей по п.1, отличающийся тем, что в качестве радиомодифицирующего агента используют пентоксифиллин.
4. Способ неинвазивного определения кислородного статуса тканей по п.1, отличающийся тем, что в качестве радиомодифицирующего агента используют радиомодифицирующий агент в различной дозировке с последующим анализом его эффективности в различных дозировках.