Способ стимуляции эндогенной продукции цитокинов и гемопоэтических факторов
Иллюстрации
Показать всеИзобретение относится к медицине и может быть использовано для профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов. Предложен способ стимуляции эндогенной продукции цитокинов и гемопоэтических факторов, основанный на введении в организм пациента препарата, представляющего собой двуцепочечную геномную фрагментированную ДНК человека с размером фрагментов 200-6000 пар оснований. Препарат применяют в таблетированной форме в количестве 3 таблеток, содержащих 5 мг активной субстанции препарата, ежедневно на протяжении 1-14 дней. Изобретение обеспечивает повышение эффективности стимуляции. 1 н.п. ф-лы, 21 ил.
Реферат
Изобретение относится к медицине и может быть использовано для профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов.
В настоящее время в терапии заболеваний, обусловленных дисфункцией иммунной системы, используются иммуномодулирующие и иммуностимулирующие препараты различного происхождения, которые, в основном, делятся на три группы: эндогенные, экзогенные и синтетические.
К иммуномодуляторам эндогенного происхождения относятся иммунорегуляторные пептиды, а также их рекомбинатные или синтетические аналоги: тактивин, тималин, тимоген, производные тимопоэтина - имунофан, миелопид. Также к группе эндогенных иммуномодуляторов относятся цитокины и иммуноглобулины.
Цитокины - низкомолекулярные гормоноподобные биомолекулы, продуцируемые активированными иммунокомпетентными клетками и являющиеся регуляторами межклеточных взаимодействий. Их несколько групп - интерлейкины (около 12), факторы роста (эпидермальный, фактор роста нервов), колониестимулирующие факторы, хемотаксические факторы, фактор некроза опухолей. Интерлейкины являются главными участниками развития иммунного ответа на внедрение микроорганизмов, формирования воспалительной реакции, осуществления противоопухолевого иммунитета и др. Наиболее известны лекарственные формы цитокинов, такие как беталейкин, ронколейкин, лейкинферон, суппозитоферон, реаферон, виферон, гриппферон, кипферон.
Иммуноглобулины представлены такими фармакопейными препаратами как антигеп, пентаглобин, цитотект, гепатект, октагам, сандоглобулин, веноглубулин, афинолейкин.
Подавляющее большинство экзогенных иммуномодуляторов - это вещества микробного происхождения, в основном бактериального и грибкового.
К медицинскому применению разрешены такие средства микробного происхождения, как БЦЖ, пирогенал, продигиозан, нуклеинат натрия, рибомунил, бронхомунал, ликопид и др. Все они обладают способностью усиливать функциональную активность нейтрофилов и макрофагов. Так ликопид оказывает иммуномодулирующее действие, прежде всего, за счет активации клеток фагоцитарной системы иммунитета (нейтрофилов и макрофагов). Последние путем фагоцитоза уничтожают патогенные микроорганизмы и в то же время секретируют медиаторы естественного иммунитета - цитокины (интерлейкин-1, фактор некроза опухоли, колониестимулирующий фактор, гамма интерферон), которые, воздействуя на широкий спектр клеток-мишеней, вызывают дальнейшее развитие защитной реакции организма.
К третьей группе иммуномодуляторов относятся синтетические вещества, полученные в результате направленного химического синтеза. К синтетическим иммуномодуляторам относится также большинство индукторов интерферонов. Индукторы интерферонов представляют собой разнородное по составу семейство высоко- и низкомолекулярных синтетических и природных соединений, объединенных способностью вызывать в организме образование собственного (эндогенного) интерферона. В фармакопеи представлены следующие препараты левамизол, диуцифон, полиоксидоний, глутоксим, галавит, полудан, амиксин неовир, йодантипирин, ридостин, циклоферон.
В отельную группу можно выделить иммуномодуляторы на основе нуклеиновых кислот ксеногенного или синтетического происхождения. Препараты на основе нуклеиновых кислот (натрия дезоксирибонуклеат, натрия нуклеинат, оксиметилурацил) восстанавливают баланс про- и противовоспалительных цитокинов.
Иногда лекарственные препараты, активирующие (восстанавливающие) функцию системы клеточного и/или гуморального иммунитета, называют иммуностимуляторами. Общепринятой классификации иммуномодуляторов, оказывающих преимущественно стимулирующее влияние на иммунитет, нет. Можно определить общее свойство и иммуномодуляторов и иммуностимуляторов как иммунокоррекция, связанная с продукцией цитокинов, ростовых факторов, хемокинов и других молекул иммунитета.
Таким образом, сегодня известен широкий спектр иммуномодуляторов, рассчитанных на множество конкретных случаев. Иммунная система состоит из ряда тесно связанных в функциональном плане компонентов, задача которых заключается в элиминации из организма чужеродных веществ антигенной природы. У каждого из компонентов этой системы могут быть свои относительно специфические агенты. В этой связи поиск новых средств, используемых в иммунокорригирующей терапии, является важным направлением в клинической практике.
К основным аналогам заявленного изобретения можно отнести способ активации продукции цитокинов клетками периферической крови препаратом ликопид, в основе механизма иммуномодулирующего действия которого лежит активация фагоцитирующих клеток (макрофаги, нейтрофилы) / Хаитов P.M., Пинегин Б.В. Иммуномодуляторы и некоторые аспекты их клинического применения // Клиническая медицина. 1996. Т. 74, №8. С.7-12/ [1], / Хаитов P.M., Пинегин Б.В. Иммуномодуляторы: механизм действия и клиническое применение // Иммунология. 2003. №3. С.199/ [2]. Ликопид представляет собой синтезированный универсальный фрагмент клеточной оболочки практически всех бактерий глюкозаминилмурамилдипептид - ГМДП (N-ацетилглюкозаминил-N-ацетилмурамилаланил-D-изоглутамин). Он активирует клетки моноцитарно-макрофагального звена, стимулируя продукцию ими воспалительных цитокинов / Андронова Т.М., Пинегин Б.В. Иммуномодулятор ликопид: современный подход к лечению заболеваний инфекционной природы // Медицинская картотека. 1999. №1. С.23-25 / [3], / Иванов В.Т., Хаитов P.M., Андронова Т., Пинегин Б.В. Ликопид - новый отечественный иммуномодулятор // Иммунология. 1996. №2. С.4-6/ [4].
Недостатком способа является относительно низкое иммуномодулирующего действие.
Также известен способ активации иммуномодулирующих свойств организма препаратом D-глюкуроновой кислоты, которая является одним из основных компонентов гликозаминогликанов экстрацеллюлярного матрикса /Laurent TC, Fraser JR. Hyaluronan. FASEB J. 1992 Apr; 6(7): 2397-404/ [5]. Эти структуры с высоким содержанием глюкуроновой кислоты участвуют в регуляции ряда процессов: клеточной адгезии, продукции различных цитокинов, хемокинов и экспресии их рецепторов /Camenisch TD, McDonald JA. Hyaluronan: is bigger better? Am J Respir Cell Mol Biol. 2000 Oct; 23(4): 431-3/ [6], функций дендритных клеток /Termeer CC, Hennies J, Voith U, Ahrens T, Weiss JM, Prehm P, Simon JC. Oligosaccharides of hyaluronan are potent activators of dendritic cells. J Immunol. 2000 Aug 15; 165(4): 1863-70/ [7]. Известно применение D-глюкуроновой кислоты в качестве средства, избирательно стимулирующего грануломоноцитопоэз /Патент RU №2020936/ [8] и функциональную активность нейтрофильных лейкоцитов /Патент RU №205813 7/ [9]. Кроме того, показано наличие у D-глюкуроновой кислоты противоаллергического действия /Патент RU №2240801/ [10]. D-глюкуроновая кислота может применяться в качестве средства, обладающего способностью стимулировать Th-зависимый тип иммунного ответа /Патент RU 2347562/ [11].
Недостатком способа также является относительно низкое иммуномодулирующего действие.
Кроме того, известен способ активации иммунокомпетентных клеток к продукции цитокинов полумягкими иммуностимулирующими олигонуклеотидами С класса /Патент US 2005/037731 20051020/ [12], /Патент WO 2006/135434 20061221/ [13]. Олигонуклеотиды С класса индуцируют секрецию интерферона-α, интерлейкина-10 иммунокомпетентными клетками, а также стимулирует активность натуральных киллеров.
Однако и этот способ имеет недостаток, связанный с относительно низким иммуномодулирующим действием.
Дополнительно к представленным можно указать, что в последнее время было описано несколько разных классов CpG олигонуклеотидов. Один класс CpG эффективен для активации В-клеток, но обладает относительно слабой активностью в отношении индукции интерверона и активации натуральных киллерных клеток; этот класс был назван В-классом. CpG олигонуклеотиды В-класса, как правило, полностью стабилизированы и включают неметилированный CpG динуклеотид с определенным предпочтительным сочетанием оснований /Патент WO 2006/135434 20061221/ [14], /Патент США 6194388/ [15], /Патент США 6207646/ [16], /Патент США 6214806/ [17], /Патент США 6218371/ [18], /Патент США 6239116/ [19]. Представители другого класса CpG олигонуклеотидов активируют В-клетки и натуральные киллерные клетки и индуцируют интерфероны; этот класс был обозначен как С-класс. CpG олигонуклеотиды С-класса, который был охарактеризован первым, как правило, полностью стабилизированы, включают последовательность В-класса и GC-обогащенный палиндром или близкую к палиндрому структуру /US 10/224523 20020819/ [20], /PCT/US02/26468 - WO 03/015711/ [21].
Однако и эти вещества, и способы их применения характеризуются относительно низкой эффективностью активирования продукции цитокинов, обусловленной тем, что известные воздействуют только на различные группы иммунокомпетентных клеток как периферической крови, так и локализующихся в других отделах организма и не затрагивают клетки других тканей организма.
Известны способы и средства для профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов.
Известен способ регулирования эндогенной продукции цитокинов и гемопоэтических факторов, в соответствии с которым в качестве препарата используют окисленный глутатион, или/и его фармацевтически приемлемые соли, или/и его фармацевтически приемлемые производные, которые вводятся парентерально или локально совместно с пролонгатором полужизни указанного окисленного глутатиона, или/и его фармацевтически приемлемых солей, или/и его фармацевтически приемлемых производных /RU 2153351/ [22].
Недостатком способа является относительно низкая эффективность профилактики и лечения заболеваний.
Известен способ, основанный на использовании в качестве стимулятора эндогенной продукции цитокинов и гемопоэтических факторов глутатиона окисленного, представляющего собой димер глутатиона восстановленного, со структурой гамма-глутамилцистеинилглицина, в котором две молекулы трипептида с вышеозначенной структурой соединены друг с другом ковалентной дисульфидной связью между цистеиновыми остатками, причем, в качестве действующего вещества используется эффективное количество глутатиона окисленного, лекарственная форма которого представляет собой инъекционный раствор глутатиона окисленного в фармацевтически приемлемом растворителе в концентрации 0,01-2,0%, при этом, для усиления и продления лечебного эффекта инъекционный раствор дополнительно содержит фармацевтически приемлемый компонент, способный продлить пребывание глутатиона в окисленной форме, например перекись водорода в концентрации 0,003%, а парентеральное введение фармакологического средства в виде инъекционной лекарственной формы предусматривает его использование в дозах 0,01-0,5 мг на кг массы тела от одной и более инъекций в день курсами длительностью один и более дней или непрерывно до момента достижения лечебного эффекта/RU 2089179/[23].
Препарат Глутоксим® является фармакологическим аналогом окисленного глутатиона (GSSG). Механизмом действия препарата является регулируемая эскалация редокс-состояния клеток. Новый уровень редокс-систем и динамики фосфорилирования ключевых белков сигнал-передающих систем и транскриптационных факторов (NFkB и АР-1), в первую очередь, иммунокомпетентных клеток, определяет иммуномодулирующий и системный цитопротекторный эффект препарата. Глутоксим оказывает дифференцированное воздействие на нормальные (стимуляция пролиферации и дифференцировки) и трансформированные (индукция апоптоза - генетически программированной клеточной гибели) клетки. Среди иммунобиохимических эффектов препарата следует выделить: стимулирующее действие препарата на каскадные механизмы фосфатной модификации основных белков сигнал-передающих систем; инициацию системы цитокинов, в том числе эндогенной продукции ИЛ-1, ИЛ-6, фактора некроза опухоли, интерферона, эритропоэтина, воспроизведение эффектов ИЛ-2 посредством индукции экспрессии его рецепторов /http://www.glutoxim.ru - Инструкция по медицинскому применению препарата Глутоксим/ [24].
Однако указанный способ стимуляция эндогенной продукции цитокинов и гемопоэтических факторов обладает относительно низкой эффективностью профилактики и лечения, обусловленной тем, что стимуляция эндогенной продукции цитокинов и гемопоэтических факторов, в первую очередь, происходит в иммунокомпетентных клетках и не дополняется продукцией цитокинов другими соматическими не иммунокомпетентными клетками организма.
Наиболее близким к предлагаемому является способ лечения онкологических заболеваний, основанный на введении в организм пациента препарата цитостатической группы и препарата фрагментированной аллогенной двуцепочечной геномной ДНК по патенту РФ №2429019, в котором защищена последовательность и количество введения пациенту указанных препаратов. Результаты свидетельствуют о том, что экзогенная ДНК, введенная в организм экспериментальных мышей в сочетании с кросслинкирующим цитостатиком ЦФ, приводит к торможению роста экспериментальных опухолей мыши
Заявляемый настоящим изобретением результат заключается в повышении эффективность профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов.
Требуемый результат достигается введением в организм пациента препарата, стимулирующего эндогенную продукцию цитокинов и гемопоэтических факторов, в качестве которого используют препарат Панаген (№ ЛСР-004429/08), представляющий двуцепочечную геномную фрагментированную ДНК человека с размером фрагментов 200-6000 пар оснований.
Кроме того, требуемый результат достигается тем, что, препарат Панаген используют в таблетированной форме в количестве 3 таблетки, содержащих 5 мг активной субстанции препарата Панаген, ежедневно на протяжении 1-14 дней от начала приема препарата или до момента достижения лечебного эффекта.
Повышение эффективности профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов, как будет показано ниже, в предложенном способе достигается тем, что, стимуляция эндогенной продукции цитокинов и гемопоэтических факторов осуществляется не только иммунокомпетентными клетками организма, но и клетками других тканей и органов.
В более широком плане задачей настоящего изобретения является расширение арсенала средств, обладающих иммуномодулирующей активностью и которые могут быть использовано для профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов.
Наиболее важным отличием пути активации двуцепочечной ДНК (дцДНК), в отличие от прототипов сравнения, является ее непосредственное воздействие на сверхэкспрессию интеферонов (ИФН) I типа как в антигенпрезентирующих клетках, так и в любых других соматических клетках организма. Показано, что ИФН I типа, в особенности ИФН-Р, наиболее важны для иммуномодулирующего каскада, стимулированного дцДНК /Martin DA, Elkon KB. Intracellular mammalian DNA stimulates myeloid dendritic cells to produce type I interferons predominantly through a toll-like receptor 9-independent pathway. Arthritis Rheum. 2006 Mar; 54(3): 951-62./ [25]. Фактически все эффекты опосредованной дцДНК клеточной активации, в том числе увеличение количества цитокинов, молекулярных маркеров процессинга и созревания, устойчивость к вирусным инфекциям, блокируются анти ИФН-β антителами. Каскад, индуцируемый дцДНК, не зависит от TLR, MyD88 и TRIF (не зависит от активации CpG) [12-21].
В современной литературе отсутствуют указания на предлагаемый способ повышения эффективности профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов и которая осуществляется не только иммунокомпетентными клетками организма, но и клетками других тканей и органов.
Следовательно, предложение отвечает критериям новизны и изобретательского уровня.
Ниже приводятся теоретические и экспериментальные данные, подтверждающие, что изобретение отвечает и критерию практической (промышленной) применяемости.
Сравнение иммуномодулирующих свойств препарата было выполнено со стандартными иммуномодуляторами, доступными в качестве коммерческих препаратов. Также в экспериментах сравнения был использован препарат поли I/поли C который являлся модельной молекулой двуцепочечной нуклеиновой кислоты в экспериментах по анализу иммуномодулирующих свойств дцДНК и обнаружению и характеристике сенсорных молекул дцДНК /Matsumoto M, Seya Т. TLR3: interferon induction by double-stranded RNA including poly (I:C). Adv Drug Deliv Rev. 2008 Apr 29; 60(7): 805-12/ [26], /Hausmann S, Marq JB, Tapparel C, Kolakofsky D, Garcin D. RIG-I and dsRNA-induced IFNbeta activation. PLoS One. 2008; 3(12): е3965./ [27].
На чертежах представлены:
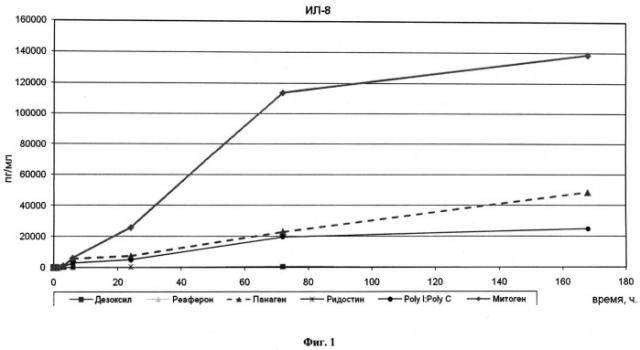
на фиг.1 - динамика продукции ИЛ-8 мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.2 - динамика продукции ИЛ-18 мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.3 - динамика продукции VEGF мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.4 - динамика продукции ИНФ-г мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.5 - динамика продукции МСР мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.6 - динамика продукции ИЛ-6 мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.7 - динамика продукции ИЛ-10 мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.8 - динамика продукции ИЛ-1 бета мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.9 - динамика продукции ИЛ-1РА мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.10 - динамика продукции ФНО-α мононуклеарными клетками крови при стимуляции различными препаратами (Продукция цитокина пг/мл по оси Y соответствует разнице стимулированной препаратом и спонтанной продукции).
на фиг.11 - уровень продукции ИЛ-6 (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.12 - уровень продукции ФНО-α (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.13 - уровень продукции ИЛ-8 (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.14 - уровень продукции ИЛ-1β (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.15 - уровень продукции ИЛ-10 (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.16 - уровень продукции ИЛ-1РА (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.17 - уровень продукции VEGF (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.18 - уровень продукции ИЛ-2 (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.19 - уровень продукции ИЛ-18 (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.20 - уровень продукции ИНФ-г (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
на фиг.21 - уровень продукции МСР (пг/мл) мононуклеарными клетками, соответствующий разнице стимулированной препаратами и спонтанной продукции.
Предложенный способ, который заключается в повышении эффективности профилактики и лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов и которая осуществляется не только иммунокомпетентными клетками организма, но и клетками других тканей и органов реализуется следующим образом.
Пример реализации способа.
Согласно изобретению стимулятором эндогенной продукции цитокинов и гемопоэтических факторов является препарат Панаген (№ ЛСР-004429/08), представляющий двуцепочечную геномную фрагментированную ДНК человека с размером фрагментов 200-6000 пар оснований.
Способ лечения заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов, включает использование таблетированной формы препарата в количестве 3 таблетки, содержащих 5 мг активной субстанции препарата Панаген, ежедневно на протяжении 1-14 дней от начала приема препарата или до момента достижения лечебного эффекта.
В последнее несколько лет было описано и экспериментально обосновано новое свойство двуцепочечной фрагментированной ДНК активировать продукцию иммунных молекул не только иммунокомпетентными клетками организма и клетками периферической крови, но и клетками других типов, включая мышечные клетки /Takeshita F, Ishii KJ. Intracellular DNA sensors in immunity. Curr Opin Immunol. 2008 Aug; 20(4): 383-8./ [28], /Coban C, Koyama S, Takeshita F, Akira S, Ishii KJ. Molecular and cellular mechanisms of DNA vaccines. Hum Vaccin. 2008 Nov-Dec; 4(6): 453-6/ [29]. Основными иммунными молекулами при такой индукции являются интерфероны первого типа и набор провоспалительных цитокинов. Индукция сверхэксперссии интерферонов как в иммунных, так и других соматических клетках организма, и активация за счет этого иммунной системы связана с проведением внутриклеточного сигнала и фосфорилированием ТВК1 киназой IRF-3 (IRF-7) транскрипционных факторов /Martin DA, Elkon KB. Intracellular mammalian DNA stimulates myeloid dendritic cells to produce type I interferons predominantly through a toll-like receptor 9-independent pathway. Arthritis Rheum. 2006 Mar; 54(3): 951-62/ [25], /Ishii KJ, Akira S. Potential link between the immune system and metabolism of nucleic acids. Curr Opin Immunol. 2008 Oct; 20(5): 524-9./ [30]. Также важным в продукции провоспалительных цитокинов и запуска иммунного ответа клетки является формирование инфламосом под воздействием двуцепочечной фрагментированной ДНК. Индукция продукции иммунных молекул осуществляется за счет взаимодействия двуцепочечной ДНК со специфическими цитозольными сенсорами, такими как DAI, NOD, STING, RIG, NALP молекулами /Barber GN. Cytoplasmic DNA innate immune pathways. Immunol Rev. 2011 Sep; 243(1): 99-108./ [31], /Yanai H, Ban T, Wang Z, Choi MK, Kawamura T, Negishi H, Nakasato M, Lu Y, Hangai S, Koshiba R, Savitsky D, Ronfani L, Akira S, Bianchi ME, Honda K, Tamura T, Kodama T, Taniguchi T. HMGB proteins function as universal sentinels for nucleic-acid-mediated innate immune responses. Nature. 2009 Nov 5; 462(7269): 99-103./ [32]. И таким образом способ активации продукции цитокинов препаратом Панаген состоит в активации к продукции цитокинов 1) иммунокомпетентных клеток и 2) в активации всех соматических клеток организма, включая мышечные, через специфические сенсорные молекулы DAI, NOD, STING, RIG, NALP к продукции интерферонов первого типа и провоспалительных цитокинов [31, 32].
Для подтверждения того, что предложенный способ позволяет достигнуть требуемого результата, приведем его теоретическое и экспериментальное обоснование.
Рассмотрим теоретическую основу используемого способа.
Цитокипы - это низкомолекулярные белковые регуляторные вещества, которые образуют универсальную сеть медиаторов, характерную как для иммунной системы, так и для клеток других органов и тканей. Под контролем цитокинов протекают все клеточные события: пролиферация, дифференцировка, апоптоз, специализированная функциональная активность клеток. Они регулируют гемопоэз, межклеточные и межсистемные взаимодействия, обеспечивают согласованность эндокринной и нервной систем в норме и в ответ на патологические воздействия. Эффекты каждого цитокина на клетки характеризуются плейотропностыо, спектр эффектов разных медиаторов перекрывается и, в основном, конечное функциональное состояние клетки зависит от влияния нескольких цитокинов, действующих синергично. Таким образом, система цитокинов представляет собой универсальную, полиморфную регуляторную сеть медиаторов, предназначенных для контроля процессов, протекающих в клетке, а так же функциональной активности клеточных элементов в кроветворной, иммунной и других гомеостатических системах организма /Сенников С.В., Силков А.Н. Методы определения цитокинов // Цитокины и воспаление. 2005. Т.4, №1. С.22-27./ [33].
Контроль и регуляция гемопоэза осуществляется множеством цитокинов, которые способны активировать гемопоэтические клетки (индуцировать их переход из GO- в G1-фазу клеточного цикла), регулировать направленность их дифференцировки в различные ростки кроветворения, стимулировать их пролиферацию и созревание, а также подавлять чрезмерное производство отдельных клеточных типов. Цитокины оказывают регуляторное влияние, как на стволовые гемопоэтические клетки, так и па их зрелых потомков, определяя их функциональную активность.
Для лечения злокачественных опухолей широко применяется химиотерапия. Возможность достижения эффекта химиотерапии в значительной степени зависит от ее интенсивности. Повышение интенсивности ограничено токсичностью, то есть повреждающим действием цитостатиков на здоровые клетки и ткани. Токсичность многообразна, но одним из наиболее распространенных и опасных ее видов является миелотоксичность или повреждение клеток костного мозга. Перспективным подходом для борьбы с миелотоксичностью при химиотерапии является применение препаратов, ускоряющих пролиферацию и дифферепцировку предшественников гемопоэза, что позволяет сократить период цитопении и снизить риск развития инфекционных осложнений различной локализации и степени тяжести. В настоящее время известно около 30 цитокинов, влияющих на клетки-предшественники гемопоэза различной степени зрелости, принадлежащие к различным росткам кроветворения. Наиболее широкое применение для преодоления миелосупрессии получили такие гемоцитокины как: гранулоцитарный и гранулоцитарно-макрофагальный колониестимулирующий фактор (Г-КСФ и ГМ-КСФ). Применение этих факторов позволяет быстро преодолеть повреждение косного мозга, вызванное применением цитостатиков. Однако эти препараты очень дороги и обладают рядом недостатков в связи с из плохой переносимостью примерно у трети пациентов. Поэтому разработка препаратов, обладающих непосредственной высокой гемостимулирующей активностью, либо активирующих клетки к продукции гемоцитокинов, является одной из актуальных задач современной медицины.
Целью данного исследования было оценить влияние препарата Панаген на продукцию цитокинов мононуклеарными клетками цельной крови ex vivo в сравнении с аналогичными уже существующими иммуностимулирующими препаратами (Ридостин, Дезоксил и др.).
Ниже приводится экспериментальное доказательство участия экзогенных фрагментов дцДНК в активации противоракового иммунного ответа.
Используемые методики.
На первом этапе работы была оценена динамика продукции 14 цитокинов моно-нуклеарными клетками крови в зависимости от времени инкубации и активации клеток различными препаратами. Проводилось определение спонтанной продукции цитокинов ех vivo, что позволяет оценить активацию клеток крови в организме обследуемого донора, и индуцированной митогеном, или одним из препаратов, продукции - что демонстрирует потенциальную возможность к секреции цитокинов.
В данных экспериментах использовали образец крови одного условно здорового добровольца в возрасте XX лет. Свежеотобранную периферическую венозную кровь в количестве 20 мл в стерильных условиях смешивали с 80 мл культуральной среды DMEM, содержащей гепарин (2,5 ед/мл), гентамицин (100 мкг/мл) и L-глютамин (0,6 мг/мл). Для проведения экспериментов по спонтанной продукции цитокинов 2 мл полученной разбавленной крови в стерильных условиях переносили во флаконы, которые инкубировали при 37°С в течение разных промежутков времени (1, 3, 6, 24, 72, 168 часов соответственно). После этого клетки крови осаждали на микроцентрифуге при 10000 g в течение 3 мин, супернатант переносили в новую пробирку, замораживали и хранили при -70°С до проведения количественного анализа цитокинов.
Одновременно с экспериментами по спонтанной продукции проводили опыты по стимуляции продукции цитокинов различными препаратами. Для этого 2 мл разбавленной крови в стерильных условиях переносили во флакон и добавляли по 10 мкл раствора 2 мл/мл одного из препаратов: Дезоксил - 1% раствор для инъекций (натриевая соль дезоксирибонуклеиновой кислоты), Ридостин - смесь натриевых солей двуспиральной рибонуклеиновой кислоты и одноцепочечной РНК, 8 мг/амп, производство ЗАО "Вектор-Медика", Реаферон-ЕС - 3 млн МЕ/амп, интерферон-альфа 2 рекомбинантный, лиофилизат для приготовления раствора для инъекций, производство ЗАО "Вектор-Медика", Кольцове, Новосибирск, Панаген субстанция 5 мг/мл, производство ООО «Панаген» и polyinosinic-polycytidylic acid Potassium salt - синтетический аналог двуспиральной РНК, Sigma. Инкубацию и подготовку проб проводили так же, как и при анализе спонтанной продукции. Опыты по стимуляции продукции цитокипов комплексом митогепов (смесь ФГА, Con A, LPS по 4, 4 и 2 мкг/мл соответственно) проводили согласно инструкции из набора «ЦИТОКИН-СТИМУЛ-БЕСТ».
Концентрацию ИНФ-γ, ИНФ-α, ФНО-α, ИЛ-1β, ИЛ-6, ИЛ-8, ИЛ-10, ИЛ-2, ИЛ-4, ИЛ-17, ИЛ-18, VEGF, МСР и рецепторного антагониста ИЛ-1 (ИЛ-1РА) в исследуемых образцах измеряли с помощью "sandwich″-варианта твердофазного иммуноферментного анализа с соответствующими наборами реагентов производства ЗАО «Вектор-Бест» (Новосибирск).
Рассмотрим влияние препарата ДНК на продукцию цитокинов клетками цельной крови в сравнении с коммерческими иммуномодулирующими препаратами.
Исследование стимуляции различными препаратами целого ряда цитокинов клетками цельной крови одного добровольца показало, что субстанция препарата Панаген стимулирует продукцию ИЛ-8, ИЛ-18, МСР, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1-РА, ФНО-α, VEGF и ИНФ-γ (Фиг.1-10). Причем стимуляция этих цитокинов, за исключением VEGF, детектировалась уже через 6 часов инкубации. При сравнении уровней стимуляции продукции цитокинов субстанцией препарата Панаген и набором митогенов было установлено, что Панаген более эффективно стимулирует продукцию ИЛ-18 (от 1,6 до 6,3 раз в зависимости от времени инкубации) и ИЛ-1 бета (от 1,8 до 4,2 раз). Стимуляция продукции МСР и ИЛ1-РА была примерно одинаковой как в случае митогена, так и в случае Панагена, а синтез ИЛ-8, ИНФ-г, ИЛ-6, ИЛ-10 и ФНО-α более эффективно стимулирует комплекс митогенов.
Набор цитокинов, продукцию которых стимулирует препарат Poly I:Poly С, полностью совпадает таковым для Панагена (Фиг.1-10). Различия заключаются только в уровне стимуляции некоторых цитокинов. Так Панаген (в точке 24 ч) более эффективно стимулирует продукцию ИЛ-18, ИЛ-1β и ФНО-α, а препарат Poly I:Poly С - ИНФ-γ и МСР. Препарат Poly I:Poly С представляет собой калиевую соль синтетического аналога двуспиральной РНК, а субстанция препарата Панаген - это смесь двуцепочечных фрагментов геномной ДНК человека размером 200-6000 п.о. с небольшим содержанием белков ядерного матрикса, которая выделена из плацент здоровых рожениц. То есть в состав обоих препаратов входят довольно длинные полимерные отрицательно заряженные молекулы. Поэтому можно предположить, что механизм их действия на активацию синтеза определенного набора цитокинов может быть сходным и ключевыми в этом случае являются структура и заряд молекулы.
Аналогом препарата Панаген является препарат Дезоксил, который представляет собой натриевую соль дезоксирибонуклеиновой кислоты, получаемую в результате ферментативного гидролиза ДНК молок лососевых рыб. Однако при добавлении данного препарата к клеткам цельной крови не было обнаружено какого-либо стимулирующего эффекта этого препарата на продукцию цитокинов. Несмотря на предполагаемую схожесть Панагена, Poly I:Poly С и Дезоксила отсутствие эффекта последнего может быть связано со способом его производства и обработки ДНК, сильной деградацией ДНК, а так же ее гетерологичностью.
Препарат Ридостип (Натрия рибонуклеат) относится к иммуномодулирующим средствам и его активным веществом является смесь натриевых солей двуспиральной рибонуклеиновой кислоты и одноцепочечной РНК. Данный препарат относится к индукторам интерферона и является стимулятором фагоцитоза. При анализе стимуляции продукции цитокинов при помощи Ридостина было установлено, что этот препарат приводит к незначительной стимуляции продукции МСР, ИЛ-6, ИЛ-1Ра и ИЛ-8. Стимуляция наблюдалась в 10 и более раз менее эффективная по сравнению с препаратом Панаген, Poly I:Poly С и комплексом митогенов. Использование Реаферона - рекомбинантного интерферона альфа2а приводило лишь к очень слабой стимуляции продукции ИЛ-6 и ИЛ-1РА.
При оценке динамики продукции цитокинов в зависимости от времени инкубации было установлено, что значительный уровень стимуляции продукции цитокинов достигается уже через 6 часов инкубации. Однако пик продукции цитокинов и выход на плато происходит в промежутке 6-24 часа. Инкубация более 24 часов приводила к неоднозначным результатам. Так продукция ИЛ-8, VEGF и МСР увеличивалась, уровень ИЛ-18, ИГФ-γ и ФНО-α снижался, а уровень ИЛ-6, ИЛ-10, ИЛ-1β и ИЛ-1РА сохранялся приблизительно на одном и том же уровне. Изменения в продукции некоторых цитокинов при длительной инкубации могут быть связаны с паракринным эффектом. Поэтому наиболее адекватной точкой для оценки спонтанной и активированной продукции цитокинов является 24 ч.
Таким образом, в результате проведенного сравнительного анализа можно сделать вывод, что субстанция препарата Панаген способна оказывать значительный стимулирующий эффект на продукцию целого ряда цитокинов (ИЛ-8, ИЛ-18, МСР, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1-РА, ФНО-α, и ИНФ-γ) мононуклеарами цельной крови. Графики, отражающие стимуляцию продукции цитокинов, клетками цельной крови в сравнении с коммерческими иммуномодулирующими препаратами представлены на фиг.1-10.
Рассмотрим влияние препарата ДНК на продукцию цитокинов клетками цельной крови здоровых добровольцев в сравнении с коммерческими иммуномодулирующими препаратами.
На этом этапе работы проводилась оценка достоверности данных по стимуляции субстанцией препарата Панаген продукции цитокинов мононуклеарными клетками в сравнении с Дезоксилом, Ридостином и комплексом митогенов.
Для этого использовали образцы крови семи условно здоровых добровольцев. Свежеотобранную периферическую венозную кровь в количестве 2 мл в стерильных условиях вносили во флакон, содержащий 8 мл культуральной среды DMEM, гепарин (2,5 ед/мл), гентамицин (100 мкг/мл) и L-глютамин (0,6 мг/мл). Для проведения экспериментов по спонтанной продукции цитокинов 2 мл полученной разбавленной крови в стерильных условиях переносили во флакон, который инкубировали при 37°С в течение 24 часов. После этого клетки крови осаждали на микроцентрифуге при 10000 g в течение 3 мин, супернатант переносили в новую пробирку, замораживали и хранили при -70°С до проведения количественного анализа цитокинов.
Параллельно проводили эксперименты по стимуляции продукции цитокинов разными препаратами. Для этого во флаконы, содержащие по 1 мл разбавленной крови, добавляли раствор одного из препаратов: субстанция препарата Панаген, раствор Дезоксила, и раствор Ридостинадо конечной концентрации 10 мкг/мл, а также комплекс митогенов из набора «цитокин-стимул-бест». Все флаконы, содержащие разбавленную кровь с препаратами, инкубировали, центрифугировали, а затем получали и хранили образцы для последующего количественного анализа, как описано выше.
Концентрацию ИНФ-γ, ФНО-α, ИЛ-1β, ИЛ-6, ИЛ-8, ИЛ-10, ИЛ-2, ИЛ-18, VEGF, МСР и рецепторного антагониста ИЛ-1 (