Способ лечения патологии глаза с помощью фокусированного ультразвука высокой интенсивности и устройство для его осуществления
Иллюстрации
Показать всеИзобретение относится к медицинской технике, а именно к средствам лечения патологии глаза фокусированным ультразвуком высокой интенсивности. Устройство содержит по меньшей мере одно глазное кольцо, проксимальный конец которого выполнен с возможностью наложения на глазное яблоко, и средства для генерации фокусированного ультразвукового пучка высокой интенсивности, установленные на дистальном конце глазного кольца. Использование изобретения позволяет повысить точность и безопасность лечения глаукомы за счет лечения всей окружности глаза за один этап. 14 з.п. ф-лы, 10 ил.
Реферат
Настоящее изобретение в целом относится к хирургическому лечению патологии глаз, и более конкретно относится к устройству и способу генерации фокусированного ультразвука высокой интенсивности для воздействия по меньшей мере на один кольцевой сегмент ресничного тела глаза, поврежденного глаукомой.
Хорошо известно, что в области офтальмологической патологии глаукома является существенной проблемой для здравоохранения, поскольку от 1 до 2% населения страдают от данной патологии, и глаукома является основной причиной слепоты.
Всемирная организация здравоохранения считает глаукому третьей причиной слепоты в мире, ответственной за 15% выявленных случаев слепоты, 2,4 миллиона человек в год.
Развитие глаукомы является медленным. Глаукома является коварным заболеванием, поскольку на первой стадии протекает бессимптомно; пациент не чувствует какой-либо боли или какой-либо визуальной проблемы. Когда проявляются первые нарушения зрения, повреждения обычно уже являются значительными, и поэтому необратимыми.
Слепота в результате глаукомы поражает как центральное, так и периферическое зрение, и поэтому оказывает существенное влияние на способность индивидуума вести независимую жизнь.
Глаукома является оптической нейропатией, т.е. заболеванием оптического нерва, обычно развивающимся при повышенном внутриглазном давлении. Давление внутри глаза возрастает, и это связано с внешним видом и функцией оптического нерва. Если давление остается высоким в течение длительного периода времени, происходит полная потеря зрения. Высокое давление развивается в глазу из-за нарушения баланса внутренней жидкости.
Глаз является полой структурой, содержащей прозрачную жидкость, называемую «водянистой влагой». Водянистая влага образуется в задней камере глаза ресничным телом. Жидкость, вырабатывающаяся с достаточно постоянной скоростью, проходит вокруг хрусталика, через зрачковую апертуру в переднюю камеру глаза. Находясь в передней камере, жидкость выходит из глаза двумя различными путями. В «увеосклеральном пути» жидкость просачивается между мышечными волокнами из ресничного тела. Этот путь составляет примерно десять процентов отводимой жидкости у человека. Первичным путем выведения водянистой влаги у человека является выведение через «канальцевый» путь, включающий трабекулярную сеть и Шлеммов канал.
При повышенном давлении в глазу водянистая влага накапливается, поскольку не может отходить достаточно быстро. При накоплении жидкости внутриглазное давление (ВГД) внутри глаза возрастает. Повышенное ВГД сжимает аксоны оптического нерва, а также может нарушать сосудистое снабжение оптического нерва. Оптический нерв передает зрительную информацию из глаза в головной мозг. Некоторые оптические нервы оказываются более восприимчивыми к аномально повышенному давлению, чем в других глазах.
Единственным терапевтическим подходом, доступным в настоящее время для лечения глаукомы, является снижение внутриглазного давления.
Клиническое лечение глаукомы обеспечивается в ступенчатом режиме. Медикаменты часто являются первым вариантом лечения, за исключением врожденной глаукомы, где операция является первичным способом лечения.
При местном или пероральном применении эти медикаменты действуют, либо снижая выработку водянистой влаги, либо повышая ее отток. Применяемые в настоящее время медикаменты могут оказывать серьезные побочные эффекты, включая застойную сердечную недостаточность, респираторный дистресс, гипертензию, депрессию, камни в почках, апластическую анемию, половую дисфункцию и смерть.
Обычно применяемыми медикаментами являются простагландин или его аналоги, такие как латанопрост (Ксалатан), биматопрост (Люмиган) и травопрост (Траватан), которые повышают увеосклеральный отток водянистой влаги; местные антагонисты бета-адренергических рецепторов, такие как тимолол, левобунолол (Бетаган), бетаксолол, которые снижают выработку водянистой влаги ресничным телом; альфа-2-адренергические агонисты, такие как бримонидин (Альфаган), действующие по двойному механизму, снижая выработку водянистой влаги и повышая увеосклеральный отток; менее селективные симпатомиметики, такие как эпинефрин и дипивефрин (Пропин), повышающие отток водянистой влаги через трабекулярную сеть и возможно, отток через увеосклеральный путь; мистические агенты (парасимпатомиметики), такие как пилокарпин, действующие путем сокращения ресничной мышцы, сжимая трабекулярную сеть и обеспечивая повышение оттока водянистой влаги; ингибиторы карбоангидразы, такие как дорзоламид (Трусопт), бринзоламид (Азопт), ацетазоламид (Диамокс), обеспечивающие снижение выработки водянистой влаги путем ингибирования карбоангидразы в ресничном теле. Двумя основными предписанными медикаментами в настоящее время являются местно применяемые аналоги простагландина и бета-блокаторы.
Согласие принимать медикаменты является главной проблемой более чем у половины больных глаукомой, не следующих правильному режиму приема дозы. Фиксированные комбинации также широко предписываются, поскольку они улучшают согласие благодаря упрощению медикаментозного лечения.
Когда медикамент не способен в достаточной мере снизить давление, часто применяют хирургическую операцию в качестве следующего этапа лечения глаукомы. Для лечения глаукомы проводят как лазерные, так и обычные операции. В целом эти операции являются временным решением, поскольку они пока не являются полностью удовлетворительным лечением глаукомы.
Имеется два различных подхода к лечению глаукомы: хирург старается либо улучшить дренаж водянистой влаги, либо снизить ее выработку.
Наиболее практикуемыми операциями, направленными на улучшение дренажа водянистой влаги, являются: каналопластика, лазерная трабекулопластика, лазерная периферическая иридотомия (в случае закрытоугольной глаукомы), трабекулотомия, глубокая не-перфорирующая склерэктомия и дренажные имплантаты для лечения глаукомы.
Наиболее практикуемой операцией, направленной на снижение выработки водянистой влаги, является методика циклодеструкции. Когда циклодеструкцию выполняют посредством лазера, она называется циклофотокоагуляцией. Для достижения циклодеструкции может применяться фокусированный ультразвук высокой интенсивности.
Каналопластика является современной, не-пенетрирующей процедурой, разработанной для усиления и восстановления естественной дренажной системы глаза для обеспечения уменьшения ВГД. Каналопластика использует проникающую микрокатетерную технологию в простой и минимально инвазивной процедуре. При выполнении каналопластики врач создает крошечный разрез для обеспечения доступа в канал глаза. Микрокатетер проводится в канале вокруг радужки, расширяя главный дренажный канал и его более мелкие коллекторные каналы посредством инъекции стерильного геле-подобного материала. Затем катетер удаляют, внутри канала помещают нить и затягивают ее. При открытии канала давление внутри глаза ослабевает.
Для лечения открытоугольной глаукомы может применяться лазерная трабекулопластика. Лазерное пятно нацеливают на трабекулярную сеть для стимуляции открытия сети, для обеспечения большего оттока водянистой влаги. Обычно за один раз лечат половину угла.
Существует два типа лазерной трабекулопластики:
- при аргонной лазерной трабекулопластики (АЛТ) применяется лазер для открытия дренажного угла глаза,
- при селективной лазерной трабекулопластики (СЛТ) применяется низкоуровневый лазер для получения того же самого результата.
Лазерная периферическая иридотомия может применяться у пациентов, подверженных или страдающих закрытоугольной глаукомой. Во время лазерной иридотомии лазерную энергию используют для создания маленького отверстия по всей толщине радужки. Это отверстие уравновешивает давление между передней и задней частью радужки, вызывая продвижение радужки в заднем направлении.
Наиболее частой обычной операцией, проводимой для глаукомы, является трабекулотомия. В склеральной стенке глаза формируют клапан частичной толщины, и под клапаном создают окно для удаления части трабекулярной сети. Затем склеральный клапан свободно пришивают на место. Это позволяет жидкости оттекать из глаза через это отверстие, приводя к снижению внутриглазного давления и образованию подушки или водяного пузырька на поверхности глаза.
Трабекулотомия связана со многими проблемами. Фибробласты, присутствующие в эписклере, пролиферируют и мигрируют, и могут вызывать рубцевание склерального клапана. Возможен неблагоприятный исход из-за рубцевания, в частности у детей и лиц молодого возраста. Исходно успешная трабекулотомия становится неудачной в восьми процентах случаев спустя три-пять лет после операции. Для минимизации фиброза хирурги в настоящее время наносят антифибротические агенты, такие как митомицин С (ММС) и 5-фторурацил (5-ФУ), на склеральный клапан во время операции. Применение этих агентов повышает процент успешных случаев трабекулотомии, но также повышает распространенность гипотонии. Гипотония является проблемой, развивающейся в том случае, когда водянистая влага оттекает из глаза слишком быстро. Давление в глазу падает слишком низко (обычно ниже 6,0 мм рт.ст.); структура глаза сжимается и зрение снижается. Антиметаболиты, прямо нанесенные на операционный участок, могут применяться для улучшения хирургического прогноза, особенно при высоком риске неблагоприятного исхода (у чернокожих пациентов, при ювенильной глаукоме…).
Трабекулотомия создает путь для оттока водянистой влаги с поверхности глаза. В то же самое время, она создает путь для проникновения в глаз бактерий, обычно живущих на поверхности глаза и век. Если это происходит, может развиться внутренняя инфекция глаза, называемая эндофтальмитом. Эндофтальмит часто ведет к постоянной и глубокой потере зрения. Эндофтальмит может развиться в любое время после трабекулотомии. Другим фактором, вносящим вклад в развитие инфекции, является расположение подушки. Глаза, в которых трабекулотомия выполнена ниже, примерно в пять раз больше подвержены риску инфекции глаза, чем глаза, имеющие верхнюю подушку. Таким образом, исходную трабекулотомию проводят вверху под веком, в назальном либо височном квадранте.
В дополнение к рубцеванию, гипотонии и инфекции, имеются другие осложнения трабекулотомии. Подушка может течь и приводит к глубокой гипотонии. Подушка может раздражаться и нарушать нормальную слезную пленку, приводя к расплывчатому зрению. Пациенты с подушками обычно не могут носить контактные линзы. Все осложнения трабекулотомии являются следствием того факта, что жидкость отводится от внутренней части глаза к внешней поверхности глаза.
Недавно было описана новая хирургическая методика, названная не-перфорирующей глубокой склерэктомией ab extemo. Эта методика позволяет избежать открывания передней камеры глаза, и соответственно снижает риск послеоперационных осложнений. Главным ограничением этой методики является то, что она является очень трудной хирургической методикой, и только некоторые хирурги способны выполнить ее успешно.
Когда трабекулотомия или склерэктомия не приводит к успешному снижению глазного давления, следующим хирургическим этапом часто является шунтирующее устройство для водянистой влаги. Имеется несколько различных дренажных имплантатов для лечения глаукомы. Они включают оригинальный имплантат Мольтено, трубчатый шунт Байервельда, или клапанные имплантаты, такие как клапанный имплантат Ахмеда для лечения глаукомы или Экспресс Мини Шунт и имплантаты Мольтено с барическим гребнем последнего поколения. Они показаны для пациентов с глаукомой, не отвечающих на максимальное лечение медикаментами, с безуспешной предшествующей операцией осторожного фильтрования (трабекулотомии). Полую трубку вставляют в переднюю камеру глаза и имплантируют пластину под конъюнктивой для обеспечения потока водянистой влаги из глаза в камеру, называемую подушкой.
Предшествующий уровень техники включает ряд таких устройств для шунтирования водянистой влаги, такой как US 4936825, US 5127901, US 5180362, US 5433701, US 4634418, US 4787855, US 4946436, US 20040015140 A1 и US 5360399.
С шунтирующими устройствами для водянистой влаги связаны многие осложнения. Утолщенная стенка рубцовой ткани, развивающаяся вокруг пластиковой пластины, придает некоторое сопротивление оттоку, и во многих глазах ограничивает снижение глазного давления. В некоторых глазах развивается гипотония из-за того, что поток через трубку не ограничен. Операция включает манипуляции в задней части орбиты, и у многих пациентов развивается дисбаланс глазных мышц, и послеоперационное двоение в глазах. Далее, из-за открывания поверхности глаза создается путь для проникновения бактерий в глаз, и возможно развитие эндофтальмита.
Все стратегии, упомянутые выше, направлены на улучшение дренажа водянистой влаги. Другая стратегия состоит в разрушении существенной части округлого внутриглазного органа, расположенного позади радужки: ресничного тела. Этот орган, и в частности двойной слой эпителиальных клеток, ответствен за выработку водянистой влаги. Разрушение значительной части ресничного тела - методика, называемая циклодеструкцией, снижает выработку водянистой влаги и соответственно, снижает внутриглазное давление.
Наиболее распространенная в настоящее время методика, применяемая при циклофотокоагуляции, достигается с лазерным диодом (810 нм). Во время операции циклофотокоагуляции хирург направляет лазер на белую часть глаза (склеру). Лазер проходит через склеру к ресничному телу. Лазер повреждает части ресничного тела так, что оно производит меньше водянистой влаги, что приводит к снижению глазного давления. Процедуру проводят под местной анестезией. Проблема циклофотокоагуляции состоит в необходимости многих импульсов вокруг глазного яблока, чтобы разрушить значительную часть ресничного тела. В каждой точке хирург помещает вручную лазерный аппликатор в контакте со склерой примерно на 2 мм от лимба и с наклоном, в идеале перпендикулярным поверхности глаза. Затем он осуществляет лазерный импульс.Затем он передвигает аппликатор к следующему участку для следующего лазерного импульса. Эта осуществляемая вручную методика является полностью эмпирической, невоспроизводимой, длительной и не простой. Далее, хирург начинает лазерный импульс без какого-либо контроля точного положения и направления лазерного пучка и без какой- либо информации о результате воздействия пучка на ресничное тело.
DE 4430720 описывает аппарат для диодной лазерной циклофотокоагуляции для усовершенствования методики и снижения риска эмпирической манипуляции. Как показано на фигурах 2а и 3 из D 4430720, аппарат включает лазерные средства (3, 33) для нанесения лазерного излучения при циклофотокоагуляции, и ультразвуковую головку (4, 40) ультразвукового биомикроскопа для контроля указанной циклофотокоагуляции, и средства фиксации для удерживания лазерных средств и ультразвуковой головки.
Ультразвуковая головка генерирует ультразвук низкой интенсивности для получения эхографических изображений высокого разрешения для участка, подлежащего лечению.
Средства фиксации служат как для стабилизации глаза пациента в ходе лечения, так и для удержания на месте жидкости в глазу пациента. Средства фиксации включают два цилиндра: внешний цилиндр 20а, и внутренний цилиндр 20b. Внешний цилиндр приспособлен к расположению на глазу пациента. Внутренний цилиндр предназначен для поддержки лазерных средств и ультразвуковых средств. Внутренний цилиндр примыкает к внешнему цилиндру и приспособлен к вращению относительно внешнего цилиндра.
Как описано в DE 4430720, во время лечения лазерные средства генерируют лазерное излучение точно для циклофотокоагуляции точных зон участка, подлежащего лечению. Затем ультразвуковую головку и лазерные средства размещают путем вращения внутреннего цилиндра для лечения другой точной зоны интересующего участка. Эти этапы повторяют до обработки всей окружности глаза.
Этот способ является неудобным в том, что необходимо повторять операцию (т.е. вращать внутренний цилиндр, получать изображение, проверять расположение аппарата на месте, производить лазерный импульс) много раз для лечения всего необходимого участка. Другими словами, операцию нужно повторять много раз, чтобы обработать всю окружность глаза.
Кроме того, данный способ может вызывать повреждение зрительной функции (из-за ошибок в размере пятна, нарушения расположения ультразвуковой головки, лазерных средств и средств фиксации, и т.д.).
Кроме того, учитывая размер обрабатываемого участка (глаза) и размер такого устройства, легко представить сложность манипуляции таким аппаратом, в частности, вращения внутреннего цилиндра, включающего лазерные средства и ультразвуковые средства, не вызывающего перемещения внешнего цилиндра.
Наконец, необходимость многократного повторения манипуляций увеличивает время операции и таким образом, фактор риска ошибок.
Для преодоления этих недостатков уже представляли применение контролируемой ультразвуковой энергии при лечении глаукомы. "Therapeutic ultrasound in the treatment of glaucoma. I. Experimental model - Coleman DJ, Lizzi FL, Driller J, Rosado AL, Chang S, Iwamoto T, Rosenthal D - PMID: 3991121 (PubMed) 1985 Mar; 92(3): 339-46" раскрывает лечение глаукомы путем применения фокусированного ультразвука высокой интенсивности (ФУВИ) на ресничном теле для обеспечения фильтрации и фокального разрушения ресничного эпителия для лечения повышенного внутриглазного давления неинвазивным способом. Аппарат, связанный с данным лечением с помощью контролируемой ультразвуковой энергией при лечении глаукомы, также описан в US 4484569. Однако таким аппаратом, произведенным и распространяемым под торговым названием SONOCARE, было очень трудно манипулировать. Далее, такой аппарат позволяет лечить только одну точечную зону за один раз. Таким образом, как раскрыто выше по отношению к лазерным методикам, каждый импульс необходимо повторять много раз для лечения всей окружности глаза, и весь аппарат нужно держать, размешать и калибровать много раз, что таким образом, занимает очень много времени (т.е. размещение ультразвуковых средств, проверка положения ультразвуковых средств по отношению к точечному участку, который нужно лечить, с оптическими и эхографическими устройствами наблюдения, заполнение устройства соединительной жидкостью, и производство ультразвукового импульса).
Таким же образом, предшествующий уровень техники включает международную заявку на патент WO 02/38078, обучающую способу лечения глаза, включая глаукому, включающему этапы идентификации области глаза, например, такой как Шлеммов канал, фокусирование устройства, способного направлять ФУВИ на область, такого как преобразователь диапазона 4-33 мм, генерирующего ФУВИ энергию от устройства на область, в котором перенос энергии от устройства к области приводит к увеличению температуры области.
Даже если данный способ обеспечивает лечение глаукомы неинвазивным способом, он представляет то неудобство, что необходимо повторять операцию много раз для лечения глаза по окружности.
Кроме того, могут разрушаться ткани, соседние с областью лечения, что приводит к расплывчатому зрению, дисбалансу мышц глаза или двоению в глазах. Таким образом, необходимо применять такую систему получения изображения, как сканирующая ультрасонография или система отображения магнитного резонанса, называемая ОМР, для идентификации области, подлежащей лечению, с большей точностью, и для оценки изменений в глазу субъекта после каждой операции.
Соответственно, применение данного способа для лечения глаукомы является трудным и дорогостоящим.
Имеется потребность в точном, безопасном, эффективном и недорогом способе лечения патологии глаза путем простого и безопасного применения фокусированного ультразвука высокой интенсивности для подлежащего лечению глаза, и устройстве для него.
Вышеупомянутая потребность удовлетворяется с помощью воплощений, описанных в настоящем описании изобретения, которое, в отличие от других видов лазерного или ФУВИ лечения, позволяет лечить всю окружность глаза за один этап, без необходимости манипуляции устройством во время процедуры.
В одном воплощении раскрывается способ лечения патологии глаза путем воздействия фокусированным ультразвуком высокой интенсивности по меньшей мере на одну область глаза.
Указанный способ включает по меньшей мере следующие этапы, на которых: помещают на глаз устройство, выполненное с возможностью направления фокусированного ультразвука высокой интенсивности по меньшей мере на два кольцевых сегмента, и воздействуют энергией фокусированного ультразвука высокой интенсивности на указанные сегменты для разрушения по меньшей мере двух кольцевых сегментов ресничного тела в глазу.
Энергией фокусированного ультразвука высокой интенсивности воздействуют по меньшей мере на два кольцевых сегментах, соответствующих по меньшей мере двум сегментам ресничного тела глаза, для их разрушения.
Частота фокусированного ультразвука высокой интенсивности находится в диапазоне от примерно 1 до 20 МГц, и более предпочтительно, в диапазоне от примерно 5 до 10 МГц.
Энергия, генерируемая каждым кольцевым преобразователем, является энергией ультразвукового излучения длительностью менее 60 секунд, и более предпочтительно, менее 20 секунд.
Глаз предпочтительно охлаждают во время лечения.
Каждый кольцевой сегмент представляет собой угол от 5 до 160°, и предпочтительно угол 44°.
В другом воплощении раскрывается устройство для лечения патологии глаза.
Устройство содержит по меньшей мере одно глазное кольцо, причем проксимальный конец указанного кольца выполнен с возможностью наложения на глазное яблоко, и средства для генерации ультразвукового пучка, установленные на дистальном конце глазного кольца.
Указанные средства, установленные на дистальном конце глазного кольца, выполнены с возможностью генерирования фокусированного ультразвукового пучка высокой интенсивности.
В соответствии с другим воплощением изобретения, указанные средства, установленные на дистальном конце глазного кольца, выполнены с возможностью генерирования рассеянного ультразвукового пучка.
Глазное кольцо состоит из усеченного конического элемента, открытого на обоих концах, малое основание которого является проксимальным концом, а большое основание является дистальным концом.
Проксимальный конец усеченного конического элемента содержит внешний кольцевой фланец, пригодный для наложения на глазное яблоко.
Проксимальный конец усеченного конического элемента содержит кольцевую бороздку, соединенную по меньшей мере с одним рукавом, образованным в усеченном коническом элементе и соединенным с всасывающим устройством.
Внутренний диаметр проксимального конца усеченного конического элемента является по существу равным диаметру роговицы плюс 2-6 мм, и более предпочтительно, равным сумме диаметра роговицы и величины в 4 мм.
Внутренний диаметр проксимального конца усеченного конического элемента, в зависимости от диаметра роговицы пациента, может составлять от 12 до 18 мм, а внутренний диаметр дистального конца усеченного конического элемента может составлять от 26 до 34 мм.
Высота усеченного конического элемента составляет от 8 до 12 мм.
Усеченный конический элемент выполнен из силикона медицинского качества или полимера медицинского качества.
Указанные средства генерации фокусированной ультразвуковой энергии высокой интенсивности состоят по меньшей мере из двух преобразователей, более предпочтительно 6 преобразователей, установленных на дистальном конце усеченного конического элемента таким образом, что указанные преобразователи выступают по направлению к оси вращения указанного усеченного конического элемента.
Указанные преобразователи могут быть изготовлены из пьезокомпозиционного материала или из пьезокерамического материала, или из других материалов, подходящих для получения ультразвука высокой интенсивности. Указанные преобразователи сами могут быть фокусирующими и иметь торическую форму, или цилиндрическую форму, или сферическую форму, или эллиптическую форму, либо могут быть плоскими, и применяться в комбинации с фокусирующей системой, такой как акустические линзы или акустические рефлекторы, с большим разнообразием форм и материалов, расположенной под указанными плоскими кольцевыми преобразователями или перед ними. Акустические рефлекторы хорошо известны в области лечебного ультразвука, и в настоящее время обычным путем применяются при наружной ударно-волновой литотрипсии (Focusing water shock waves for lithotripsy by various ellipsoid reflectors - Muller M. - Biomed Tech (Beri). 1989 Apr; 34(4):62-72).
В соответствии с другим воплощением изобретения, указанные средства генерации динамически фокусированной ультразвуковой энергии высокой интенсивности содержат по меньшей мере два плоских преобразователя, имеющих форму цилиндрического сегмента, установленных на дистальном конце усеченного конического элемента таким образом, что указанные преобразователи выступают по направлению к оси вращения указанного усеченного конического элемента.
Альтернативно, указанные средства генерации рассеянного ультразвукового пучка являются средствами генерации нефокусированного ультразвука высокой интенсивности и содержат по меньшей мере два преобразователя, имеющих форму кольцевого плоского сегмента, установленного на дистальном конце усеченного конического элемента таким образом, что указанные преобразователи выступают по направлению к оси вращения указанного усеченного конического элемента.
Указанные преобразователи соединены с блоком управления.
Указанное устройство содержит две группы из трех преобразователей, разделенные двумя неактивными секторами.
Преобразователи последовательно включаются блоком управления, или одновременно включаются указанным блоком управления.
Одно преимущество устройства в соответствии с настоящим изобретением состоит в том, что средства генерации ультразвукового пучка, установленные на дистальном конце глазного кольца, включают множество преобразователей, расположенных в соответствии с характером лечения.
Это позволяет лечить глаз по всей окружности одновременно. Действительно, в отличие от способов и аппаратов, раскрытых, например, в US 4484569 и в DE 4430720, аппарат в соответствии с изобретением позволяет лечить глаз без необходимости многократного повторения операции.
Что касается US 4484569 и в DE 4430720, изобретение обеспечивает следующее:
- упрощение операционной процедуры путем обеспечения устройства, обеспечивающего лечение глаза за один раз; более того, поскольку аппарат помещают и устанавливают на глазу, аппарат остается в одном положении, поэтому лечение может быть осуществлено всей окружности глаза без необходимости для оператора перемещать или удерживать аппарат,
- обеспечение воспроизводимой процедуры; более того, в отличие от аппарата предшествующего уровня техники, устройство по настоящему изобретению не требует многократного перемещения для лечения различных зон области, подлежащей лечению.
- создание протяженных повреждений, охватывающих большие области ресничного тела, в отличие от аппарата предшествующего уровня техники, который создает только точечные повреждения и требуется много первичных повреждений для эффективного лечения,
- уменьшение времени операции, что снижает фактор риска ошибок, и таким образом улучшается качество лечения,
- обеспечение лечения, которое меньше зависит от оператора, поскольку очень легко выполняется, ему очень легко обучить в крайне короткий срок обучения, и оно является относительно автоматизированным во время лечения.
В случае предложенного лечения необходимо понять, что схема лечения соответствует форме участков, подлежащих лечению. В случае лечения ресничного тела схема лечения может быть кольцевой или полукольцевой. В других случаях схема лечения может быть эллиптической, или шестиугольной или восьмиугольной.
Предпочтительно средства генерации ультразвукового пучка содержат корпус, преобразователи, расположенные по периферии корпуса в соответствии со схемой лечения. Более предпочтительно, преобразователи могут быть размещены по периферии всего или части корпуса. Например, в одном воплощении преобразователи размещены по окружности вдоль всей или части окружности корпуса 8.
Далее описаны различные воплощения изобретения. В дополнение к аспектам, описанными в этом кратком изложении, дополнительные аспекты станут ясными при ссылке на чертежи и со ссылкой на последующее подробное описание.
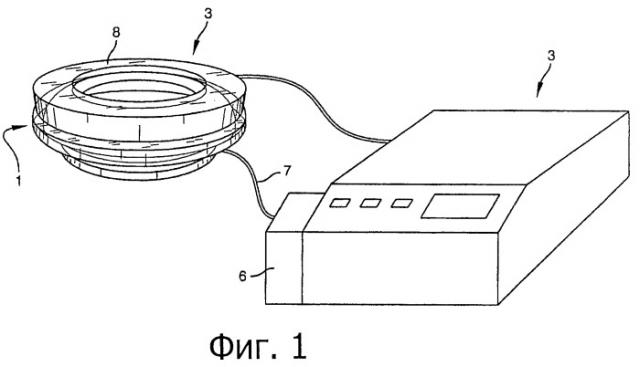
Фигура 1 - схематический вид в перспективе устройства для лечения патологии глаза путем воздействия фокусированного ультразвука высокой интенсивности в соответствии с изобретением,
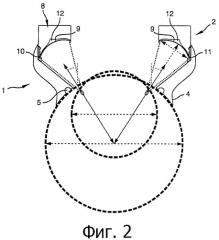
фигура 2 - увеличенное изображение устройства в соответствии с изобретением, расположенное на глазу, подлежащем лечению,
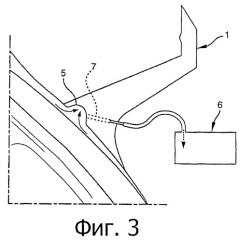
фигура 3 - частичный вид вертикального разреза глазного кольца устройства в соответствии с изобретением,
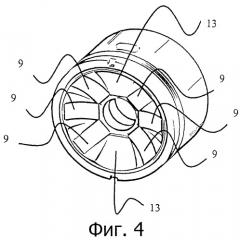
фигура 4 - схематический вид в перспективе преобразователей, удерживаемых глазным кольцом устройства в соответствии с изобретением,
фигура 5 - вид сверху устройства, правильно расположенного на глазу, подлежащем лечению,
фигура 6 - вид сбоку устройства, правильно расположенного на глазу, подлежащем лечению, как показано на фигуре 5,
фигура 7 - вид сбоку устройства во время генерации ФУВИ энергии,
фигура 8 - трехмерное представление областей, поврежденных ФУВИ энергией в соответствии с изобретением,
фигура 9 - изображение другого воплощения устройства в соответствии с изобретением, расположенного на глазу, подлежащем лечению, вид в вертикальном разрезе,
фигура 10 - изображение последнего воплощения устройства в соответствии с изобретением, особо приспособленного для повышения скорости транспорта лекарства через ткань глаза, вид в вертикальном разрезе.
Далее раскрыты способ и устройство, подходящие для лечения глаукомы; тем не менее очевидно, что специалист в данной области техники может приспособить способ и устройство для лечения любой офтальмологической патологии, требующей хирургического вмешательства, не выходя из объема изобретения.
Что касается фигуры 1, устройство в соответствии с изобретением включает глазное кольцо 1, в котором проксимальный конец указанного глазного кольца пригоден для наложения на глазное яблоко, подлежащее лечению, и (см. фигуру 2) средства 2 для генерации фокусированной ультразвуковой энергии высокой интенсивности, где указанные средства фиксируются на дистальном конце глазного кольца. Указанные средства соединяются с блоком управления 3, включая генератор излучения и средства установки параметров излучения, таких как частота, мощность и продолжительность каждого излучения, число всплесков излучения (т.е. число включенных преобразователей), и т.д. Генератор излучения является по меньшей мере генератором синусоидальных колебаний с заданной частотой от 5 до 15 МГц, и предпочтительно от 7 до 10 МГц, усилитель и измеритель мощности.
Что касается фигур 1 и 2, глазное кольцо 1 состоит из усеченного конического элемента, открытого на обоих концах, в котором малое основание является проксимальным концом, а большое основание является дистальным концом.
Что касается фигуры 2, проксимальный конец усеченного конического элемента 1 содержит внешний кольцевой фланец 4, подходящий для наложения на внешнюю поверхность глазного яблока, примерно на 2 мм от лимба, где лимб является соединением между роговицей и склерой глазного яблока. Проксимальная сторона кольцевого фланца 4 имеет вогнутый профиль, при этом радиус кривизны вогнутого профиля по существу равен радиусу кривизны глазного яблока.
Проксимальный край усеченного конического элемента 1 содержит кольцевую бороздку 5, соединенную с всасывающим устройством 6 (фигура 1) по меньшей мере одним рукавом 7, проходящим через усеченный конический элемент 1 и выходящим в кольцевую бороздку, указанное всасывающее устройство 6 управляется блоком управления 3.
Очевидно, что всасывающее устройство 6 может быть независимым, не выходя за пределы объема изобретения.
Когда усеченный конический элемент 1 накладывают на глаз, и работает всасывающее устройство 6, придавливание кольцевой бороздки 5 обеспечивает деформацию конъюнктивы глаза, указанная деформация образует о-кольцо в кольцевой бороздке 5. Усеченный конический элемент 1 затем тесно сцепляется таким образом, что указанный усеченный конический элемент отслеживает микродвижения глаза во время всего лечения, занимающего меньше 2 минут, поддерживает центральное положение устройства на зрительной оси.
Усеченный конический элемент 1 выполняют из силикона медицинского качества, который является мягким материалом, совместимым при контакте с конъюнктивой.
Очевидно, что усеченный конический элемент 1 может быть выполнен из любого материала, подходящего для медицинских целей, хорошо известного специалистам в данной области техники, и биосовместимость которого может быть подтверждена, такого как биосовместимый ПВХ, не выходя за рамки объема изобретения.
Что касается фигур 1 и 2, средства 2 для генерации фокусированного ультразвука высокой интенсивности состоят из стационарной коронки 8, удерживающей множество преобразователей 9, внешний радиус указанной стационарной коронки по существу равен внутреннему диаметру дистального конца усеченного конического элемента 1. Внешний край стационарной коронки 8 из преобразователей 9 включает кольцевую бороздку 10, взаимодействующую с кольцевым выступом 11, проходящим в усеченном коническом элементе 1 поблизости от его дистального конца таким образом, что стационарная коронка 8 удерживается на дистальном конце усеченного конического элемента 1. Таким образом, стационарная коронка 8 выступает в направлении к оси вращения указанного усеченного конического элемента 1. Указанные преобразователи 9 удерживаются на проксимальном крае стационарной коронки 8. Каждый преобразователь 9 является сегментом, имеющим вогнутый профиль, вогнутость соответствует глазному яблоку, и более конкретно приведена в соответствие с ресничным телом, как показано на фигуре 2. Проксимальный край стационарной коронки 8 содержит кольцевую бороздку 12, в которой проходят соединительные кабели преобразователей 9, не показанные на фигуре 2.
Что касается фигуры 4, стационарная коронка 8 из преобразователей 9 содержит две группы, каждая из трех преобразователей 9, разделенные двумя неактивными секторами 13. Каждый преобразователь 9 является цилиндрическим сегментом, способным воздействовать на часть окружности ресничного тела в 44°, с внутренним диаметром 12,8 мм и внешним диаметром 28 мм.
Следует отметить, что стационарная коронка 8 может содержать два или боле преобразователей 9, распределенных по окружности любым образом, не выходя из объема изобретения.
Преобразователи 9 последовательно включаются блоком управления 3 для разрушения ресничного тела по всей или части окружности, при этом каждый преобразователь 9 обеспечивает внутреннее повреждение в форме, согласующейся с формой ресничных тел из дуги или окружности (т.е. повреждения в форме прямых линий в пределах восьмиугольника).
В этом воплощении, приспособленном для лечения глаукомы, внутренний диаметр проксимального конца усеченного конического элемента 1 является по существу равным диаметру роговицы плюс 2-6 мм.
Внутренний диаметр проксимального конца усеченного конического элемента 1, в зависимости от диаметра роговицы пациента, составляет от 12 до 18 мм, а внутренний диаметр дистального конца усеченного конического элемента составляет от 26 до 34 мм.
Высота усеченного конического элемента 1 составляет от 8 до 12 мм. Таким образом, при правильном расположении усеченного конического элемента 1 на глазу, подлежащем лечению, как описано далее, все ресничн