Антиинфекционные функционализированные поверхности и способы их получения
Иллюстрации
Показать всеИзобретение относится к области медицины. Медицинское устройство, имеющее антиинфекционную поверхность, включающую функционализирующий слой, нанесенный на нее, и антиинфекционное средство, нанесенное на функционализирующий слой, включающий по меньшей мере одну частицу или функциональную группу, способствующую присоединению к нему антиинфекционного средства, и по меньшей мере одну частицу или функциональную группу, способствующую прикреплению функционализирующего слоя к поверхности, где антиинфекционное средство представляет собой дендример четвертичного аммония. Изобретение обеспечивает получение антиинфекционного средства на поверхности. 12 з.п. ф-лы, 3 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к субстратам с антиинфекционными поверхностями. В частности, предложены способы для функционализирования поверхностей различных материалов с целью включения активных участков поверхности для связывания антиинфекционных средств.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОМУ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Активированный или функционализированный слой, который связан или, другими словами, размещен на поверхности субстрата, представляет собой прослойку между субстратом и другими материалами, такими как органические или металлические материалы.
Необходимость контролирования инфекции является жизненно важной для большинства, начиная от представителей общественного здравоохранения, руководителей больниц и школ и т.п., заканчивая отдельными гражданами. Обычно контроль инфекции может быть достигнут с помощью топического применения дезинфектантов, антисептиков, антибактериальных средств и т.п. на поверхностях, которые часто контактируют с инфекционными агентами. Распространенные дезинфектанты включают соединения активный хлор, такой как гипохлориты, хлорамины, дихлоризоцианурат и трихлоризоцианурат, мокрый хлор, диоксид хлора и т.п., активный кислород, включающий пероксиды, такие как надуксусная кислота, персульфат калия, перборнокислый натрий, перкарбонат натрия и пергидрат мочевины, йодосоединения, такие как йодповидон, настой йода, йодинированные неионные сурфактанты, концентрированные спирты, такие как этанол, н-пропанол или изопропанол и смеси вышеперечисленных веществ; 2-феноксиэтанол и 1- и 2-феноксипропанолы, производные фенола, крезолы, галогенированные фенолы, такие как гексахлорофен, триклозан, трихлорфенол, трибромфенол, пентахлорфенол, Dibromol и соли вышеперечисленных веществ, катионные сурфактанты, включающие катионы четвертичного аммония, такие как бензалкония хлорид, цетил триметиламмония бромид или хлорид, дидецилдиметиламмония хлорид, цетилпиридиния хлорид, бензетония хлорид и другие, и нечетвертичные соединения, такие как хлоргексидин, глюкопротамин, октендина дигидрохлорид и т.д.; сильные окислители, такие как озон и раствор перманганата; тяжелые металлы и их соли, такие как коллоидное серебро, нитрат серебра, хлорид ртути, фенилртутные соли, медь, сульфат меди, оксид-хлорид меди и т.п., сильные кислоты (фосфорная, азотная, серная, сульфаминовая, толуолсульфоновая кислоты) и щелочные металлы (натрия, калия, кальция гидроксиды). Тем не менее, многие из этих соединений вредны для тканей млекопитающих. Более того, эти соединения обладают кратковременным эффектом и постоянно требуют повторного нанесения.
Антибиотики могут вводиться с целью остановки инфекции у индивидуумов. Тем не менее, подобное введение не всегда эффективно. Для многочисленных медицинских применений, включающих ортопедию, травму, применение в спинальной и общей хирургии, где потенциал для развития инфекции представляет собой серьезные опасения, единичное применение антисептика или лечение антибиотиками не является подходящим. Например, инфекция может представлять собой изнуряющее осложнение тотальной артропластики сустава (TJA). В то время как некоторые инфекции можно лечить только путем супрессии антибиотиком, здесь всегда требуется более агрессивная терапия, такая как двухэтапная реимплантация. Лечение послеартропластических инфекций в 1999 году стоило более 200 млн долларов только в США. Spangehl M.J., et al., J. Bone Joint Surg. Am., 1999, 81(5), 672-682. TJA инфекции развиваются, когда бактерии колонизируют поверхность импланта. Эти виды тогда формируют резистентную биологическую пленку на поверхности импланта, которая сводит к нулю нормальный ответ организма антибиотикам.
Устройства внешней фиксации предоставляют временное, но необходимое жесткое ограничение для облегчения сращения перелома. Тем не менее, для пациентов существует риск развития инфекции по спицевому каналу на стороне, выступающей над кожей - спица контактирует с тканями вплоть до костной. Подобные осложнения могут привести к сепсису и остеомиелиту, которые могут потребовать секвестрэктомии для коррекции. Даже самые строгие манипуляции со спицами и соблюдение постпроцедурных протоколов имеют только ограниченый эффект. Исследования показали, что подобные протоколы не снижают риск развития инфекции. Davies, R., et al. J. Bone Joint Surg. Br., 2005, 87-B, 716-719.
При минимально инвазивных спондилодезах, транспедикулярные винты сначала имплантируются в кость позвонка, и затем стержни фиксируются к головкам винтов для иммобилизации и стабилизации поврежденных сегментов. Винты и стержни проходят через кожу пациента в позвоночное пространство через канюлированный канал. В качестве внешней фиксации винты и стержни также являются подверженными инфекциям по спицевому каналу; благодаря прохождению имплантов через кожу, возможность контактирования и/или прохождения через вредоносные бактерии сильно возрастает.
Катетеры и шунты помещаются в любую полость тела и сосуды для облегчения инъекции, дренирования или обмена жидкостями. Инфекции представляют собой распространенное явление в месте постановки катетера и сильно зависят от того, сколько времени будет катетеризирован пациент. Например, Kass сообщает об уровне инфекции фактически в 100% для пациентов с постоянным отведением мочи через мочевые катетеры в открытую систему в течение более чем 4 дней. Kass, E. H., Trans. Assoc. Am. Physicians, 1956, 69, 56-63.
Таким образом, существует необходимость в антиинфекционных поверхностях, которые могли бы применяться в областях, особенно склонных к заселению инфекционными агентами, таких как общественные места, общие зоны в зданиях, крепления и т.п. Более того, имеется необходимость в субстратах и материалах с антиинфекционными поверхностями, таких как медицинские устройства, включающие импланты, винты, стержни, спицы, катетеры, стенты, хирургические инструменты и т.п., что может предотвратить инфекции с помощью проактивного элиминирования бактерий, которые пытаются колонизировать поверхность устройства как до, так и после операции.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В соответствии с одним или более воплощений, способы предоставлены для функционализирования поверхностей различных материалов с целью включения активного участка поверхности, с которым связаны антиинфекционные средства.
В зависимости от применения, заинтересованная поверхность функционализируется в соответствии с подходящим функционализационным способом, и антиинфекционный агент размещается на функционализированной поверхности.
Фактически любая поверхность, которая может быть функционализирована, является подходящей для включения антиинфекционного средства в соответствии с описанными воплощениями. Примеры таких поверхностей включают металлы, сплавы, полимеры, пластики, керамику и стекло. Таким образом, антиинфекционные поверхности, как описано выше, могут наноситься универсально в любых окружающих условиях, например, в окружающих условиях хирургической процедуры или по всей территории операционной или больницы, таким образом элиминируя множество, если не все, источники инфекции единовременно и непрерывно.
Функционализирование субстратов в соответствии с данным изобретением может достигаться различными путями. Например, возможно функционализировать поверхность полимерного субстрата, такого как, но не ограниченного полиамидами, полиуретанами, полиэфирами, поликетонами, полиэстерами, полиимидами, арамидами, полифторолефинами, эпоксидными смолами, силиконами или смесями, содержащими данные полимеры при помощи оксида, алкоксида или смешанноого оксидного-алкоксидного слоя с применением алкоксидных предшественников. Такие функционализированные поверхности полимеров могут быть использованы для ковалентного связывания следующих материалов или слоев на поверхности, которая в данном изобретении включает антиинфекционные частицы. Например, субстраты, содержащие кислотообразующие протоны, такие как -OH или -NH группы, функционализируются при помощи их реакции с алкоксидами Группы IV. Данная процедура приносит продукт молекулярной адгезии, который связан с поверхностью блок-полимера, но ограничивается материалами, которые имеют кислотообразующие группы на их поверхности.
Также возможно сформировать адгезивный покрывающий слой, который может быть в дальнейшем функционализирован адгезивными продуктами с помощью нагревания самоагрегированного слоя функционализированной фосфоновой кислоты на нативной окисленной поверхности субстрата или осажденного оксида, полученного из алкоксидного предшественника.
Множество одной или более частиц антиинфекционного покрытия может быть связано с функциональной группой по меньшей мере одной функционализированной органофосфоновой частицей. Подобные нативные оксиды обнаруживаются на металлах, включающих, но не ограничивающихся титаном и его сплавами; нержавеющей сталью; сплавами кобальта и хрома; и никелем, молибденом, танталом, цирконием, магнием, а также сплавами, их содержащими.
В другом воплощении функционализирование поверхности кремния может быть достигнуто с помощью процесса, в котором самоагрегированная пленка органофосфоновой кислоты связана с нативной или синтезированной поверхностью кремния, выстланной оксидным слоем как пленкой соответствующего фосфоната. Пленка фосфонатов функционализируется для обеспечения ковалентного связывания биологических молекул, варьирующихся по размерам от малых пептидов до огромных протеинов с множественными субъединицами, с поверхностью кремния.
В дополнительном воплощении антиинфекционные пептид-модифицированные связанные с поверхностью пленки фосфонатов могут быть связаны с металлическими поверхностями и полимерными поверхностями, функционализированными при помощи оксидов, полученных из алкоксидов.
Предполагается, что способы модификации антиинфекционной поверхности, описанные выше, могут элиминировать необходимость в пассивировании, зачастую необходимом этапе изготовления металлических имплантов. Процессы, такие как описанные выше, предоставляют слои, связанные с поверхностями металлов, и трансформируют оксиды поверхности в химически и физически устойчивые образцы, при этом элиминируя источник коррозии в устройствах, таких как металлические импланты.
Антиинфекционные средства, как обсуждалось выше, могут включать бактерицидные и бактериостатические средства, такие как дезинфектанты, антисептики и антибиотики. Не все бактерицидные и бактериостатические средства могут применяться в качестве антисептиков для тканей млекопитающих, поскольку могут оказывать на них неблагоприятный эффект. Некоторые воплощения данного изобретения могут применяться в случаях, которые не включают контакт антиинфекционной поверхности с тканями млекопитающих, таких как внутренние поверхности санитарно-технического оборудования, строительных материалов, вентилляционного трубопровода, чистых помещений и т.д. В подобных случаях могут применяться известные антиинфекционные средства, такие как дезинфектанты, которые не будут подходить для применения в случаях, в которых контакт с тканями млекопитающих будет предполагаемым или возможным.
В некоторых воплощениях соединения, которые могут применяться в качестве антисептиков у людей, включают правильно разведенные растворы хлора, такие как раствор Daquin, 0,5% раствор гипохлорита натрия или калия с pH, измененным до pH 7-8 или 0,5-1% раствор бензолсульфохлорамида, некоторые йодные растворы, такие как йодоповидон, пероксиды, такие как растворы пергидрата мочевины и pH-буферированный 0,1-0,25% раствор надуксусной кислоты с или без примеси антисептиков, применяемые в основном в качестве кожных антисетиков, слабые органические кислоты, такие как сорбиновая кислота, бензойная кислота, молочная кислота и салициловая кислота, некоторые соединения фенола, такие как гексахлорофен, триклозан и Dibromol, и катионоактивные соединения, такие как 0,05-0,5% раствор бензалкония, 0,5%-4% раствор хлоргексидина, 0,1-2% раствор октендина.
В других воплощениях антиинфекционные средства, применяемые в случаях, включающих возможный контакт с тканями млекопитающих, могут включать соединения четвертичного аммония, такие как холин и производные холина, дендримеры четвертичного аммония, серебро, медь, катионные активные центры; серебро и медь.
Как будет очевидно специалистам в данной области техники, способ функционализирования, применяемый для связывания или, другими словами, прикрепления конкретного антиинфекционного агента, в соответствии с данным изобретением, зависит от химической природы антиинфекционного агента.
Устройства, изготовленные в соответствии с данным описанием изобретения, предоставляют множество клинических преимуществ. Например, у частично внешних устройств вышеупомянутые антиинфекционные поверхности могут уничтожить виды бактерий на поверхности контакта устройство-кожа, таким образом препятствуя развитию инфекции по ходу спиц. Устройства, включающие антиинфекционные поверхности, могут препятствовать колонизации поверхностей имплантов инфекционными организмами, потенциально снижая частоту развития глубокой инфекции, особенно в популяции с высоким риском. В катетерах и шунтах с антиинфекционными поверхностями потенциальный риск инфекции минимизируется путем уничтожения бактерий, перемещающихся вверх по пути интубации в организм пациента. Другим примером является тотальное эндопротезирование тазобедренного сустава; антиинфекционные бедренные стержни могут уничтожать виды бактерий и ингибировать формирование биологической пленки на поверхности контакта устройство-ткань, препятствуя бактериальной колонизации замещения тазобедренного сустава, что может привести к расшатыванию из-за инфекции и может потребовать затрат и болезненной операции по ревизии бедра. Антиинфекционное средство высоко стабильно в физиологических условиях. Антиинфекционное средство не вымывается из исходного материала, поэтому не существует нежелательного вторичного результата. Благодаря нанометровым размерам антиинфекционное средство не служит препятствием для желаемых свойств металлической поверхности, что может быть критично для функции устройства, такого как имплант. Антиинфекционное средство является невидимым для невооруженного глаза и не скрывает опознавательные признаки, включающие цветное анодирование или маркировку продукта.
Устройства в соответствии с данным описанием не ограничиваются медицинскими устройствами. Например, устройства, воплощающие данные описания, могут включать крепления, структуры, оборудование, ограждения и т.п., имеющие антиинфекционные поверхности.
КРАТКОЕ ОПИСАНИЕ ФИГУР
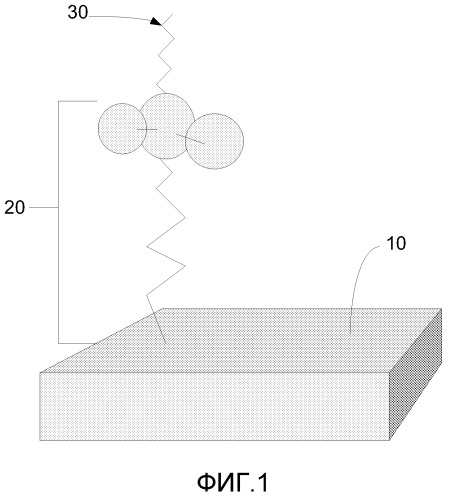
ФИГ.1 отображает схематическое изображение антиинфекционного средства, связанного с поверхностью в соответствии с по меньшей мере одним воплощением данного описания.
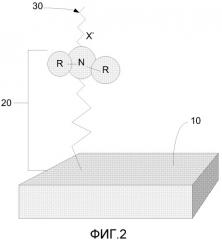
ФИГ.2 отображает антиинфекционное средство, связанное с поверхностью в соответствии с по меньшей мере одним воплощением данного описания.
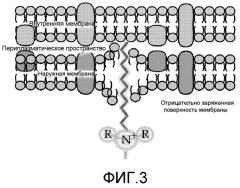
ФИГ.3 отображает способ действия антиинфекционного средства в соответствии с по меньшей мере одним воплощением данного описания.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
В последующем описании с целью объяснения специфические номера, материалы и конфигурации выложены с целью предоставления полного понимания изобретения. Специалистам в данной области техники будет очевидно, тем не менее, что изобретение может применяться без этих специфических деталей. В некоторых примерах хорошо известные свойства могут опускаться или упрощаться, чтобы не затруднять понимание данного изобретения. Более того, упоминание в данном детализировании таких фраз, как “одно воплощение” или “воплощение” означает, что конкретное свойство, структура или характеристика, описанные в связи с воплощением, включены по меньшей мере в одно воплощение изобретения. Появление фраз, таких как “в одном воплощении” в различных местах в детализации не обязательно относится к одному и тому же воплощению.
В целом, в соответствии с одним и более воплощений, способы предоставлены для функционализирования поверхностей различных материалов для включения активных участков поверхности, с которыми связываются антиинфекционные средства. В зависимости от применения, заинтересованная поверхность функционализируется и антиинфекционное средство размещается на функционализированной поверхности для предоставления устройств с антиинфекционными поверхностями.
Теперь в отношении ФИГ.1, в целом, поверхность 10, в соответсвии с данным описанием, включает функционализирующий слой 20 и антиинфекционное средство 30.
Поверхность 10 может быть фактически любым материалом, который подходит для получения функционализирующего слоя 20. Примеры таких материалов включают металлы, сплавы, полимеры, пластики, керамику, кремний, стекло и поверхности с кислотообразующими протонами, такими как -OH или -NH группы.
Функционализирующий слой 20 может быть любым слоем, подходящим для конкретного применения. Природа и композиция функционализирующего слоя 20 зависит от поверхности 10, которая предполагает включение антиинфекционного средства 30, и антиинфекционного средства 30, которое должно связываться с функционализирующим слоем 20. Например, как описано в более подробных деталях ниже, далее, возможно функционализировать поверхность субстрата полимера 10 с помощью слоя оксида, алкоксида или смеси оксида-алкоксида с применением предшественника алкоксида. Подобные функционализированные поверхности полимера могут использоваться для ковалентного связывания следующих материалов или слоев антиинфекционного средства 30 с поверхностью.
Другие функционализирующие слои 20 могут включать функционализированные фосфоновые кислоты, размещенные на нативных оксидах поверхности субстрата; функционализированные фосфоновые кислоты, размещенные на слое оксида, как прямо осажденные на подлежащий субстрат, так и полученные из предшественников алкоксидов; для поверхностей, которые содержат кислотообразующие протоны, такие как -OH или -NH группы, реагирующие также с алкоксидами Группы IV; для поверхностей с кремниевой поверхностью, самоагрегированную пленку фосфоновой кислоты, связанную с нативной или синтезированной поверхностью кремния, покрытой оксидом, в качестве пленки соответствующего фосфоната; и т.п.
Поверхности металлов, которые могут быть применены, включают титан и его сплавы; нержавеющую сталь; сплавы кобальта и хрома; никель, молибден, тантал, цирконий, магний, марганец, ниобий, а также сплавы, их содержащие и т.п.
Антиинфекционные средства 30, которые могут быть примени tys в связи с вышеописанными воплощениями, могут включать бактерицидные и бактериостатические средства, включающие дезинфектанты, антисептики и антибиотики. Дезинфектанты включают активный хлор, такой как гипохлориты, хлорамины, дихлоризоцианурат и трихлоризоцианурат, мокрый хлор, диоксид хлора и т.п., активный кислород, включающий пероксиды, такие как надуксусная кислота, персульфат калия, перборнокислый натрий, перкарбонат натрия и пергидрат мочевины, йодосоединения, такие как йодповидон, настой йода, йодинированные неионные сурфактанты, концентрированные спирты, такие как этанол, н-пропанол или ихопропанол и смеси вышеперечисленных веществ; 2-феноксиэтанол и 1- и 2-феноксипропанолы, производные фенола, крезолы, галогенированные фенолы, такие как гексахлорофен, триклозан, трихлорфенол, трибромфенол, пентахлорфенол, Dibromol и соли вышеперечисленных веществ, катионные сурфактанты, включающие катионы четвертичного аммония, такие как бензалкония хлорид, цетил триметиламмония бромид или хлорид, дидецилдиметиламмония хлорид, цетилпиридиния хлорид, бензетония хлорид и другие, и нечетвертичные соединения, такие как хлоргексидин, глюкопротамин, октендина дигидрохлорид и т.д.; сильные окислители, такие как озон и раствор перманганата; тяжелые металлы и их соли, такие как коллоидное серебро, нитрат серебра, хлорид ртути, фенилртутные соли, медь, сульфат меди, оксид-хлорид меди и т.п., сильные кислоты (фосфорная, азотная, серная, сульфаминовая, толуолсульфоновая кислоты) и щелочные металлы (натрия, калия, кальция гидроксиды).
Не все бактерицидные и бактериостатические средства могут применяться в качестве антисептиков для тканей млекопитающих, поскольку могут оказывать на них неблагоприятный эффект. Специалистам в данной области техники будет очевидно, что некоторые воплощения данного изобретения могут применяться в случаях, которые не включают контакт антиинфекционной поверхности с тканями млекопитающих, таких как внутренние поверхности санитарно-технического оборудования, строительных материалов, вентилляционного трубопровода, чистых помещений и т.д. В таких случаях могут применяться известные антиинфекционные средства, такие как дезинфектанты, которые не будут подходить для применения в случаях, в которых контакт с тканями млекопитающих будет предполагаемым или возможным.
Далее указаны некоторые соединения, которые могут применяться в качестве антисептиков для людей: правильно разведенные растворы хлора, такие как раствор Daquin, 0,5% раствор гипохлорита натрия или калия с pH, измененным до pH 7-8 или 0,5-1% раствор бензолсульфохлорамида, некоторые йодные растворы, такие как йодоповидон, пероксиды, такие как растворы пергидрата мочевины и pH-буферированный 0,1 - 0,25% раствор надуксусной кислоты с или без примеси антисептиков, применяемые в основном в качестве кожных антисетиков, слабые органические кислоты, такие как сорбиновая кислота, бензойная кислота, молочная кислота и салициловая кислота, некоторые соединения фенола, такие как гексахлорофин, триклозан и Dibromol, и катионоактивные соединения, такие как 0,05-0,5% раствор бензалкония, 0,5%-4% раствор хлоргексидина, 0,1-2% раствор октендина.
В предпочтительных воплощениях антиинфекционные средства, применяемые в случаях, которые подразумевают возможный контакт с тканями млекопитающих, включают, но не ограничиваются соединениями четвертичного аммония, такими как холин и производные холина, дендримеры четвертичного аммония, серебро, медь, катионные активные центры. Соединения четвертичного аммония (“quats”) с длинными алкильными цепями обладают доказанными биоцидными свойствами благодаря разрыванию клеточной оболочки. Nakagawa, Y., et al., Appl. Environ. Microbiol., 1984, 47:3, 513-518 включен в настоящую заявку во всей полноте посредством ссылки. Катионная функциональная группа четвертичного аммония приближается и разрывает клеточную мембрану бактерии. Дендримеры четвертичного аммония изначально показывают сходную биоцидную активность, и при комбинации с функциональными группами или молекулами с биоцидными свойствами могут еще больше усиливать антимикробную активность за счет повышения концентрации. Серебро и медь обладают отмеченными олигодинамическими эффектами по отношению к микроорганизмам. Исследование предполагает, что ионы серебра и меди денатурируют протеины организмов-мишеней путем связывания с реакционноспособными группами. Данное связывание приводит к преципитации и дезактивации. Известно также, что серебро затрагивает энзимы и метаболические процессы. Катионные активные центры электростатически притягиваются к клеточным стенкам бактерий, которые заряжены отрицательно. Катионные антимикробные пептиды обладают ингибирующими эффектами по отношению к регуляторным механизмам организма-мишени.
В известных областях применения может быть полезным функционализировать антиинфекционное средство, в случае чего антиинфекционное средство может включать кислотную функционализированную группу, где кислота представлена, например, органофосфорной, карбоновой, сульфоновой, сульфиновой, фосфиновой, фосфоновой, фосфорной или гидроксамовой кислотами.
Теперь в отношении ФИГ.2, воплощение применения антиинфекционной поверхности представляет собой модифицированную поверхность Самоагрегированного Монослоя Фосфоната (AI-SAMP) 20, ковалентно связанную с поверхностью 10 имплантируемого материала. Здесь антиинфекционное средство 30 представляет собой катионную функциональную группу четвертичного аммония, которая связана с поверхностью с помощью SAMP. Ковалентная связь создает исключительно сильное соединение между обрабатываемой поверхностью и материалом, к которому она применяется. Schwartz, J., et al., Mat. Sci. Engr. C, 2003, 23, 395-400, переданный в данной заявке во всей полноте посредством ссылки. Поскольку SAMP является одной крупной молекулой, он полностью покрывает материал, к которому применяется, и обеспечивает тотальное покрытие импланта независимо от типа или текстуры материала импланта. Ковалентное связывание солей четвертичного аммония переводит quats в нерастворимое состояние, обеспечивая длительную антиинфекционную активность. Смотрите, например, Nakagawa, Y., et al., Appl. Environ. Microbiol., 1984, 47:3, 513-518.
Как показано на ФИГ.3, катионная функциональная группа четвертичного аммония приближается и разрывает клеточную мембрану бактерии.
Методы функционализирования.
Несколько способов являются подходящими для функционализирования поверхности. Для специалистов в данной области техники будет очевидно, что способы функционализирования, применяемые для связывания или, другими словами, для прикрепления конкретного антиинфекционного средства в соответствии с данным изобретением, зависят от химической природы антиинфекционного средства и заинтересованной поверхности.
Возможно функционализировать поверхность полимерного субстрата, такого как, но не ограниченного, полиамидами, полиуретанами, полиэфирами, поликетонами, полиэстерами, полиимидами, арамидами, полифторолефинами, эпоксидными смолами, силиконами или смесями, содержащими данные полимеры при помощи оксида, алкоксида или смешанных оксидного-алкоксидных слоев с применением алкоксидных предшественников. Такие функционализированные поверхности полимеров могут быть использованы для ковалентного связывания следующих материалов или слоев антиинфекционного средства на поверхности. Поверхность полимера может быть покрыта слоем оксида металла (оксидный адгезивный слой).
В одном воплощении поверхность полимера может быть покрыта непрерывным адгезивным слоем оксида, т.е., слоем, который сформирован матриксом отдельных молекул, которые химически связаны и соединены друг с другом, в отличие от отдельных молекул, покрывающих поверхность. В данном воплощении молекулы алкоксида металла связаны вместе по меньшей мере одним участком поверхности полимера для формирования непрерывного слоя и далее превращения в оксидный функционализирующий слой.
Дополнительно возможно сформировать адгезивный покрывающий слой, который в дальнейшем может быть функционализирован с помощью адгезивных активных центров путем нагревания самоагрегированного слоя функционализированной фосфоновой кислоты на нативной окисленной поверхности субстрата. Данный процесс, детально описанный в US Patent Application Publication 2004/0023048, переданной в данной заявке во всей полноте посредством ссылки, предоставляет на нативной окисленной поверхности материала мульти-сегментный, содержащий в основе фосфор, покрывающий слой, имеющий дифункциональный участок с органофосфоновой кислотой в основе, связанный с нативной окисленной поверхностью материала, и связующий участок, связанный с участком, содержащим в основе органофосфоновую кислоту. В соответствии с данным процессом, покрывающий слой, содержащий в основе фосфор, может иметь множество функционализированных частиц органофосфоната, связанных с нативной окисленной поверхностью субстрата с помощью фосфорной связи, и множество одного или более антиинфекционных покрывающих частиц, каждая из которых связана с функциональной группой по меньшей мере одной функционализированной органофосфорной частицы. При связывании посредством комплекса металла, последний дополнительно характеризуется как полученный из металлического реактива, предпочтительно реактива алкоксида металла.
Другой функционализирующий процесс может быть применен в зависимости от субстрата для функционализирования и желаемой антиинфекционной частицы. Например, возможно функционализировать субстраты, содержащие кислотообразующие протоны, такие как -OH или -NH группы, путем их реакции с алкоксидами Группы IV. Данная процедура приносит продукт молекулярной адгезии, который связан с поверхностью блок-полимера, но является ограниченной материалами, которые имеют кислотообразующие группы на их поверхности. Этот способ детально описан в Dennes, T. J. et al., High-Yield Activation of Scaffold Polymer Surfaces to Attach Cell Adhesion Molecules. J. Am. Chem. Soc. 2007, 129, 93-97; и Dennes, T. J.; Schwartz, J. Controlling Cell Adhesion on Polyurethanes. Soft Matter 2008, 4, 86-89, оба из которых переданы в данной заявке во всей полноте посредством ссылки.
Органические SAM'ы могут быть ковалентно связаны с поверхностью субстрата оксида металла или оксида кремния. Формирование самоагрегированного органического монослоя на поверхности субстрата оксида металла или оксида кремния может привести к появлению у субстрата оксида металла или оксида кремния верхнего слоя, имеющего поверхностный слой, состоящий из алкоксидов переходных металлов, выбранных из Группы IVB, Группы VB, Группы VB или Группы VIB Периодической Таблицы, ковалентно связанных с ним, где алкоксиды связаны атомами переходных металлов с атомами кислорода поверхности субстрата верхнего слоя; и к реакции алкоксидов переходных металлов поверхностного слоя с органическим соединением, способным реагировать с алкоксидом переходного металла с формированием органического лиганда, ковалентно связанного с переходным металлом, таким образом формируя органический самоагрегированный монослой на поверхности субстрата, ковалентно связанный в области атома переходного металла с атомами кислорода поверхности субстрата. Этот способ детально описан в US Patent №6,146,767 (смотрите, например, кол. 3, строки 1-22 и Примеры), переданном в данной заявке во всей полноте посредством ссылки. Подходящие кислотные функциональные группы, которые могут взаимодействовать с алкоксидами металлов, включают, например, карбоновую, сульфоновую, сульфиновую, фосфиновую, фосфоновую, фосфорную или гидроксамовую кислоты.
Например, способы, детально описанные в US Patent №6,645,644 (смотрите, например, кол. 4, строки 15-33 и Примеры), переданном в данной заявке во всей полноте посредством ссылки, включают формирование слоя лиганда фосфата или фосфоната, ковалентно связанного с поверхностью субстрата, несущего гидроксид, который включает покрытие несущего гидроксид субстрата фосфорной кислотой или органической фосфоновой кислотой и нагревание покрытого субстрата до тех пор, пока фосфорная кислота или органическая фосфоновая кислота ковалентно связаны с субстратом. Когда субстрат представляет собой металл или сплав металла, фосфорная кислота формирует покрытие из неорганического фосфата, который богат на свободные гидроксильные группы.
Как покрытия из монофосфатов и полифосфатов переходных металлов, гидроксильные группы доступны для добавления антиинфекционного средства.
В другом воплощении функционализирование поверхности кремния может достигаться с помощью процесса, где самоагрегированная пленка из органофосфоновой кислоты связана с нативной или синтезированной покрытой слоем оксида поверхностью кремния, как пленка соответствующего фосфоната. Пленка фосфоната функционализируется для обеспечения ковалентного связывания биологических молекул, варьирующих по размеру от малых пептидов до огромных протеинов с множественными субъединицами, с поверхностью кремния. Связывание антител с подобными поверхностями обеспечивает селективное распознавание широкого ряда молекул, включая антигены на поверхностях бактериальных патогенов и паразитов. Данный способ детально описан в Midwood et al., Easy and Efficient Bonding of Biomolecules to an Oxide Surface of Silicon. Langmuir 2004, 20, 5501-5505, переданном в данной заявке во всей полноте посредством ссылки. Экспериментальные детали представлены на странице 5501, колонка 2 - страница 5502, колонка 2, смотрите также обсуждение на страницах 5502-5504 и сопутствующие фигуры.
В дополнительных воплощениях связанные с поверхностью фосфонатные пленки могут применяться для функционализирования титана и его сплавов (таких как Ti-6Al-4V) для прикрепления антиинфекционных пептидов. Как известно в данной области техники, титан и его сплавы обладают высокой механической прочностью и являются устойчивыми к химической коррозии и, таким образом, являются предпочтительными материалами для хирургических имплантов, которые могут контактировать с костью. Данный способ детально описан в Gawalt et al., Bonding Organics to Ti Alloys: Facilitating Human Osteoblast Attachment and Spreading on Surgical Implant Materials” Langmuir 2003, 19, 200-204, переданном в данной заявке во всей полноте посредством ссылки. Экспериментальные детали представлены на странице 200, колонка 2 - страница 201, колонка 2, смотрите также обсуждение на страницах 201-204 и сопутствующие фигуры.
Адгезия Оксида Металла
Техники адгезии оксида металла включают оксидный адгезивный слой, связанный с поверхностью такового с помощью координационных групп, где оксидный адгезивный слой представляет собой алкоксид металла, соответствующий общей формуле M-O-R, где M является атомом металла. Оксидный адгезивный слой представляет собой слой, который подвергался таким процессам, но не ограничивался пиролизом, воздействием микроволн, полным гидролизом и/или частичным гидролизом. Техника хорошо подходит, например, для полимеров или металлов. Функционализированные поверхности, такие как функционализированные металлы или полимеры, могут применяться для ковалентного связывания последующих материалов или слоев антиинфекционного средства на поверхности.
Подходящие полимерные субстраты включают любой полимер, который может быть функционализирован, и могут включать любое из множества веществ, включающих синтетические и/или натуральные молекулы полимеров. Примеры подходящих субстратов полимеров включают, но не ограничиваются полиамидами, полиуретанами, полимочевиной, полиэфирами, поликетонами, полиимидами, полифульфидами, полисульфоксидами, полисульфонами, политиофенами, полипиридинами, полипирролами, полиэстерами, силиконами, полисилоксанами, полисахаридами, фторполимерами, амидами, имидами, полипептидами, полиэтиленом, полистиролом, полипропиленом, эпоксидным стеклопластом, жидкокристаллическими полимерами, термопластиком, бисмалеимидтриазиновыми (BT) смолами, полимерами бензоциклобутена, Ajinomoto Buildup Films (ABF), пленками с низким коэфициентом термального расширения (CTE) из стекла и эпоксидов и смесями, включающими данные полимеры. Оксидный адгезивный слой прикрепляется к поверхности полимера при помощи ковалентного связывания между координационной группой на поверхности полимера и металлом алкоксида металла.
Алкоксиды переходных металлов являются частично полезными для данного изобретения. Металлы Группы 3-6 и 13-14 Периодической Таблицы являются предпочтительными металлами для композиций данного изобретения. Предпочтительными металлами являются цирконий (Zr), алюминий (Al), титан (Ti), гафний (Hf), тантал (Ta), ниобий (Nb), ванадий (V) и олово (Sn), среди которых наиболее предпочитаемыми являются цирконий (Zr), титан (Ti) и тантал (Ta). В зависимости от позиции переходного металла в Периодической Таблице, алкоксид переходного металла будет иметь от трех до шести алкоксидных групп или смесь из оксо и алкоксидных групп. Предпочтительные алкоксидные группы имеют от 2 до 4 атомов углерода, такие как этоксид, пропоксид, изо-пропоксид, бутоксид, изо-бутоксид, трет-бутоксид и фторированный алкоксид. Наиболее предпочтительными алкоксидами металлов являются циркония тетра(трет-бутоксид), титана тетра(трет-бутоксид) и тантала пентаэтоксид.
Методы получения композиций и устройств в соответствии с данным воплощением включают активацию поверхности полимера, включающую стадии: а) контактирования алкоксида металла с поверхностью; б) подвержение алкоксида металла состояниям, соответствующим формированию адгезивного слоя на поверхности, включающей ок