Способ получения биотоплива, где теплоту от реакций образования углерод-углеродных связей используют для проведения реакций газификации биомассы
Иллюстрации
Показать всеИзобретение относится к способу получения C2-C36 линейных или разветвленных углеводородов и кислородсодержащих углеводородов. Способ включает: а) проведение эндотермической реакции газификации с реагентом из биомассы при температуре менее или равной примерно 750 K, с получением синтез-газа, при этом температура является оптимальной для реакции утилизации синтез-газа или для реакции образования углерод-углеродных связей; б) проведение экзотермической реакции утилизации синтез-газа или реакции образования углерод-углеродных связей с синтез-газом стадии (а), без какой-либо промежуточной обработки синтез-газа стадии (а), при температуре выше или равной температуре реакции газификации, выполняемой на стадии (а), где реакция производит C2-C36 линейные или разветвленные углеводороды или кислородсодержащие углеводороды и теплоту, и в) использование теплоты, выделяемой при реакции утилизации синтез-газа или реакции образования углерод-углеродных связей стадии (б), в эндотермической реакции газификации стадии (а). Предложенное изобретение обеспечивает энергетически эффективный путь для получения топлива и химикатов из возобновляемых ресурсов биомассы. 16 з.п. ф-лы, 19 табл., 8 пр., 7 ил.
Реферат
Данное изобретение было осуществлено при поддержке правительства Соединенных Штатов по решению следующих организаций: DOE DE-FG02-84ER13183. Соединенные Штаты обладают определенными правами на это изобретение.
Здесь заявлен приоритет согласно предварительной заявке на патент, серийный номер 60/785471, зарегистрированной 24 марта 2006, которая включена в этот документ.
В настоящую эпоху уменьшения запасов нефти и политической нестабильности в странах, богатых нефтью, промышленное сообщество должно развивать пути использования мировых ресурсов обильной и возобновляемой биомассы для получения новых источников энергии и химических промежуточных продуктов [1]. Например, транспортный сектор требует топливо, которое может быть эффективно преобразовано в энергию и которое обладает высокой удельной энергией. Химическая промышленность требует функциональных молекул, таких как олефины (например, этилен, пропилен) и альдегиды (например, формальдегид), которые можно использовать для получения полимерных материалов. Особенность, которая делает полученные из биомассы углеводы особенно перспективным классом соединений для дополнения (или, в некоторых случаях, замены) нефти в упомянутых областях, состоит в том, что стехиометрические элементарные звенья этих соединений обладают атомным составом H:C:O, равным 2:1:1. Таким образом, углеводы являются идеальными кандидатами для преобразования в газовые смеси H2/CO. Эти виды газов обычно называют «синтез-газ». Синтез-газ можно преобразовать путем синтеза Фишера-Тропша (Fischer-Tropsch) на катализаторах на основе железа и кобальта [2] с получением линейных длинноцепочечных алканов для использования в качестве дизельного топлива. Синтез-газ можно также преобразовать на катализаторах на основе меди [3] с получением метанола для применения в качестве сырья для получения олефинов, формальдегида и бензина.
Хотя получение синтез-газа из биомассы в течение многих лет признавали в качестве многообещающей основы, откуда можно получить множество ценных продуктов, стандартные пути для получения синтез-газа из биомассы не являются чрезвычайно эффективными из-за того, что требуют высоких температур. Например, непосредственная каталитическая газификация биомассы требует температуру 800 K и выше [4]. Двухстадийная газификация биомассы также требует высоких температур: быстрый пиролиз биомассы (при примерно 773 K), за которым следует паровой риформинг получаемого биомасла (при примерно 1000 K) [5, 6]. Более того, газификация биомассы обычно приводит к сложному набору биопродуктов, включающему смолу (летучие органические соединения), обуглившееся вещество (твердые углеродсодержащие материалы) и легкие углеводороды, также как и соединения NOx и SOx, полученные в процессах высокотемпературного горения [1, 4-6].
Относительно недавним и быстро растущим применением биомассы является ее использование при производстве биодизельного топлива посредством переэтерификации растительных масел и животных жиров [1, 7, 8]. Реакция переэтерификации дает малоценный поток отходов глицерина, который часто содержит концентрации глицерина в воде от 50 до 80% [8]. Получающийся излишек привел к падению цен на глицерин в США от примерно 2100 долларов США за метрическую тонну в 1995 до менее 1000 долларов США за метрическую тонну в 2003 (для 97% глицерина фармакологического качества (Фармокапеи США), цены предоставлены Procter&Gamble). Настоящее производство (2006) биодизельного топлива в США и Европе составляет 108 и 2×108 литров в год, соответственно. Из-за налоговых льгот и других экономических стимулов, предоставляемых некоторыми национальными правительствами, ожидается удвоение этих величин в очень близком будущем [8, 9]. В отношении налоговых льгот для биодизельного топлива в США см. IRS Publication No. 378 и разделах 6426(c), 6427(e) и 40А Закона о внутреннем налогообложении.
Глицерин можно также получать путем ферментации Сахаров, таких как глюкоза [10]. В отличие от ферментации глюкозы с получением этанола, при которой получают этанол при концентрации только примерно 5% масс. в воде, при ферментации глюкозы с получением глицерина можно получить глицерин при концентрации примерно 25% масс. [10]. Эта более высокая концентрация глицерина в сравнении с этанолом снижает энергетические затраты, требуемые для удаления воды из кислородсодержащего углеводородного топлива. Действительно, одной из наиболее энергоемких стадий при получении этанола топливного качества из глюкозы, является стадия дистилляции [11, 12]. Другой путь получения глицерина из глюкозы и других Сахаров состоит в гидрировании глюкозы до сорбитола [13, 14], за которым следует гидрогенолиз сорбитола до полиолов, имеющих низкие молекулярные массы [15, 16].
В предыдущей работе, написанной в соавторстве с некоторыми авторами настоящего изобретения [17-19] было показано, что растворы полиолов в воде (например, этиленгликоль, глицерин, сорбитол) можно было бы преобразовать посредством риформинга в водной фазе в смесь газов H2/CO2, содержащую низкие уровни CO (например, 500 частей на миллион) на платиновых катализаторах на носителе при температуре приблизительно 500 K. Эти способы риформинга в водной фазе приводят к низким соотношениям CO:CO2 в потоке выходящего газа, так как реакция сдвига в водяном газе (СВГ) чрезвычайно благоприятна при высоких парциальных давлениях воды, образованной при этих условиях реакции (например, 2,5 МПа (25 бар)). Таким образом, условия реакции риформинга в водной фазе не являются благоприятными для получения синтез-газа, в котором требуется высокое соотношение CO:CO2. Другие исследователи изучали риформинг глицерина в паровой фазе. Czermik et al. [20] сообщали о высокой селективности выработки H2 путем парового риформинга глицерина при высоких температурах (1023 K) на промышленном катализаторе риформинга лигроина, на основе никеля. Suzuki et al. [21] также наблюдали высокую селективность выработки H2 путем парового риформинга глицерина при высоких температурах (873 K) на 3% Ru/Y2O3 катализаторе, однако они применяли высокую объемную скорость продувочного газа в экспериментах. Следовательно, остается необходимость в разработке лучшей каталитической системы для конверсии глицерина в паровой фазе при низких температурах.
Хорошо известен синтез Фишера-Тропша (Ф-Т) для получения синтетических углеводородов из синтез-газа. Его осуществляли в больших масштабах немцы во время второй мировой войны для производства жидкого топлива из угля. Основная реакция Ф-Т является следующей:
где -(CH2)- представляет основное элементарное звено углеводородных продуктов. Синтез Ф-Т является чрезвычайно экзотермическим, что приводит к тому, что теплоперенос представляет собой значительный фактор при конструировании реактора Ф-Т.
Значительное количество исследований было выполнено для максимизации способностей синтеза в реакции Ф-Т. См., например, патент US 6696501, в котором описан способ конверсии природного газа или другого ископаемого топлива в высшие углеводороды. Здесь в способе используют сочетание парового риформинга ископаемых топлив с получением синтез-газа, за которым следует синтез Ф-Т и второй паровой риформинг отходящего газа. Преобразованный отходящий газ затем подают назад в реактор Ф-Т.
См. также патент US 6976362, в котором описан способ интеграции образования синтез-газа, реакции Ф-Т и реакции сдвига в водяном газе для получения CO2, алифатических углеводородов и водорода, и затем сжигания водорода в камере сгорания газа турбины для получения электричества.
Как вкратце было отмечено выше, важным параметром для определения теоретического максимального выхода синтетических углеводородов в реакции Ф-Т является стехиометрическое число СЧ, определяемое как:
Теоретически, выход синтетических углеводородов является наибольшим, когда СЧ=2,0 и CO не реагирует дополнительно с образованием CO2 посредством реакции сдвига в водяном газе. В этом случае соотношение H2/CO будет равно СЧ, то есть 2,0, что теоретически дает наибольший выход синтетических углеводородов.
Биомасса включает в первую очередь углеводы (например, крахмал и целлюлозу). Одним из способов конверсии этих соединений в жидкое топливо является ферментация с получением жидких спиртов, таких как этанол и бутанол. Технология конверсии полученного из зерна крахмала в этанол посредством гидролиза, ферментации и дистилляции хорошо разработана, и существуют экономические преимущества в конверсии лигноцеллюлоз в этанол (например, путем разработки новых энзимов для гидролиза целлюлозы). Преимущества этанола в качестве транспортного топлива состоят в том, что он является жидкостью и имеет высокое октановое число (октановое число, согласно исследованиям, составляет 130). Однако, этанол в качестве топлива обладает несколькими значительными присущими ему недостатками по сравнению с длинноцепочечными алканами: (1) этанол обладает меньшей удельной энергией по сравнению с нефтью (например, приблизительно 2·104 БТЕ(британская тепловая единица)/литр для этанола по сравнению с 3·104 БТЕ/литр для нефти); (2) этанол полностью смешивается с водой, что приводит к значительной абсорбции воды в топливе, и (3) он обладает относительно низкой температурой кипения (73°C), что приводит к избыточному испарению при повышенных температурах. Однако наиболее важно, что способ ферментации, используемый для получения биоэтанола из углеводов, приводит к водному раствору, содержащему только примерно от 5 до 10% масс. этанола. Значительное количество энергии требуется для дистилляции этанола из воды для получения этанола топливного качества. Действительно, общий энергетический баланс производства биоэтанола не является очень благоприятным, и установлено, что количество энергии, требуемой для получения биоэтанола, приблизительно равно (или больше) энергоемкости получаемого этанола [11, 12, 36].
Длинноцепочечные алканы включают огромное большинство компонентов нефтяного транспортного топлива (разветвленные алканы в бензине, линейные алканы в дизельном топливе). Преобразование возобновляемых ресурсов биомассы в жидкие алканы является поэтому привлекательным вариантом переработки. Наиболее примечательно то, что жидкие алканы, получаемые из биомассы, (1) можно распределять, используя уже эксплуатируемую инфраструктуру для полученных из нефти продуктов; (2) можно добавлять в существующее нефтяное хранилище для дальнейшей переработки (например, смешанные топлива) и (3) можно сжигать в существующих двигателях внутреннего сгорания без изменения двигателя или топлива.
Данное изобретение представляет собой способ производства углеводородов или кислородсодержащих углеводородов, предпочтительно от C2 до C36 углеводородов и/или кислородсодержащих углеводородов. В предпочтительном воплощении изобретения жидкие алканы (то есть C5 и длиннее, линейные, разветвленные или циклические) можно получать непосредственно из соединений, полученных из биомассы, включающих полисахариды, моносахариды и полиолы (например, глицерин) посредством интегрированного способа, включающего каталитическую конверсию в газовые смеси H2/CO (синтез-газ) и синтез Фишера-Тропша (или другие реакции образования углерод-углеродных связей). Стадию синтеза Фишера-Тропша можно выполнять последовательно за стадией конверсии глицерина или, что важно, обе реакции можно соединить путем интеграции активных центров для каждой реакции внутри одного каталитического слоя. Таким образом, в одном воплощении данного изобретения, каталитическое преобразование глицерина и синтезы Фишера-Тропша соединены в реакторной системе с двумя слоями. В предпочтительном порядке действий преобразование сырьевого реагента в синтез-газ выполняют, используя катализатор, включающий Pt-Re на углеродном носителе. Затем завершают реакцию образования углерод-углеродных связей, используя катализатор, включающий Ru/TiO2.
В другом воплощении изобретения каталитическую конверсию глицерина и синтез Фишера-Тропша совмещают в одном реакторе, предпочтительно используя один слой катализатора, включающий физическую смесь Pt-Re/C и Ru/TiO2. Альтернативно, как описано в разделе подробное описание изобретения, способ можно выполнять в одном реакторе, но используя один, два или более отдельных каталитических слоев, причем каждый слой содержит один или более отдельных катализаторов. Например, способ можно выполнять, используя один каталитический слой, содержащий гомогенный катализатор двойного назначения, или способ можно выполнять, используя один каталитический слой, содержащий два или более катализаторов, физически смешанных друг с другом, или способ можно выполнять, используя два или более каталитических слоев в многослойной или ступенчатой конфигурации. Во всех этих воплощениях данного изобретения получают жидкие алканы с Sc5+ от примерно 46% до примерно 64% при содержании углерода от примерно 15% до примерно 50% в продуктах, содержащихся в органической жидкой фазе (см. Примеры). Водный жидкий продукт из интегрированного способа содержит от примерно 5% до примерно 15% масс. метанола, этанола и ацетона, которые можно отделить от воды посредством дистилляции и использовать в химической промышленности или повторно использовать для конверсии в газовые продукты. Этот интегрированный способ значительно улучшает экономику «зеленого» синтеза Фишера-Тропша путем уменьшения капитальных затрат и увеличения теплового кпд реакций. Таким образом, значительным преимуществом настоящего изобретения является то, что оно позволяет включать реакторы Фишера-Тропша меньшего масштаба в качестве компонентов биоперерабатывающего завода. Настоящее изобретение можно также использовать для переработки отходов глицерина из биодизельных установок в жидкое топливо. Более того, объединение (а) конверсии биомассы в синтез-газ и (б) синтеза Фишера-Тропша приводит к синергетическому действию этих способов. Объединяя эти две реакции в одном реакторе, избегают сильно эндотермических или экзотермических стадий, которые возникают в результате протекания реакций по отдельности.
Значительным преимуществом настоящего изобретения является то, что путем объединения реакции газификации и реакции образования углерод-углеродных связей в «одном сосуде» устраняют ингибирующий эффект парциального давления CO на скорость реакции газификации, путем потребления CO в том же реакторе (в реакции образования углерод-углеродных связей).
Таким образом, данное изобретение представляет собой способ производства углеводородов (предпочтительно), кислородсодержащих углеводородов и других органических соединений. Способ включает выполнение двух реакций, одна из которых экзотермическая, а другая эндотермическая, и использование теплоты от экзотермической реакции для поставки (по меньшей мере, частично) энергии, требующейся для проведения эндотермической реакции. Таким образом, способ включает выполнение эндотермической реакции газификации с реагирующим веществом в виде биомассы при температуре, меньшей или равной примерно 750 K, для получения синтез-газа. Способ дополнительно включает выполнение экзотермической реакции образования углерод-углеродных связей (или, вообще, любой экзотермической реакции утилизации синтез-газа, такой, как синтез метанола или синтез простого диметилового эфира) с синтез-газом, полученным в эндотермической реакции. Экзотермическую реакцию выполняют при температуре, большей или равной температуре реакции газификации, выполняемой на стадии (а). В предпочтительном воплощении в экзотермической реакции получают углеводороды (так же как и теплоту). Теплоту, выделяемую при экзотермической реакции утилизации синтез-газа, или из реакции образования углерод-углеродных связей, направляют обратно в способ (то есть, используют) для того, чтобы предоставить (по меньшей мере, частично) энергию, требуемую для проведения эндотермической реакции газификации.
Более конкретно, данное изобретение относится к способу производства углеводородов и кислородсодержащих углеводородов. Первое воплощение изобретения включает выполнение эндотермической реакции газификации с реагирующим веществом в виде биомассы (предпочтительно, полисахаридом, моносахаридом и/или полиолом) при температуре, менее или равной примерно 750 K, с получением синтез-газа. Экзотермическую реакцию утилизации синтез-газа или реакцию образования углерод-углеродных связей затем выполняют, используя синтез-газ, образованный на первой стадии, при температуре, выше или равной температуре начальной реакции газификации. В экзотермической реакции получают углеводороды или кислородсодержащие углеводороды, и теплоту. Теплоту, выделяемую при реакции утилизации синтез-газа или реакции образования углерод-углеродных связей, затем используют при проведении эндотермической газификации. Таким образом, теплоту, выделенную при экзотермической реакции, используют для проведения (по меньшей мере частично) эндотермической реакции газификации.
Предпочтительно выполнять эндотермическую реакцию газификации при температуре, менее или равной примерно 750 K (и более предпочтительно ≤ примерно 625 K, еще более предпочтительно ≤ примерно 575 K, и еще более предпочтительно ≤ 550 K). Как было замечено ранее, реакции можно выполнять в двух отдельных реакторах или в одном реакторе с одним, двумя или более отдельными каталитическими слоями и используя один, два или более катализаторов.
Другое воплощение изобретения представляет собой способ производства линейных или разветвленных углеводородов или кислородсодержащих углеводородов от C2 до C36. Способ включает выполнение эндотермической реакции газификации с потоком реагента, включающим биомассу, при температуре менее или равной примерно 750 K (и более предпочтительно примерно ≤625 K, еще более предпочтительно примерно ≤575 K, и еще более предпочтительно примерно ≤550 K) для получения синтез-газа. Экзотермическую реакцию Фишера-Тропша осуществляют так, что синтез-газ образуется при температуре выше или равной температуре реакции газификации, в которой получают углеводороды и/или кислородсодержащие углеводороды от C2 до C36 и теплоту. Теплоту, выделяемую в реакции Фишера-Тропша используют в эндотермической реакции газификации, таким образом делая способ в целом весьма энергетически эффективным.
Намного более предпочтительно, чтобы эндотермическая реакция газификации протекала при температуре, которая является оптимальной для утилизации синтез-газа или для реакции образования углерод-углеродных связей. Это условие приводит к суммарной, объединенной реакции, которая является наиболее эффективной по соответствию теплоты, выделяемой при экзотермической реакции, теплоте, требуемой для эндотермической реакции. Таким образом, когда экзотермическая реакция является реакцией Фишера-Тропша, предпочтительно, чтобы как реакция Фишера-Тропша, так и реакция газификации протекали при температуре, оптимальной для реакции Фишера-Тропша.
В предпочтительном воплощении изобретения как эндотермическая реакция газификации, так и экзотермическая реакция утилизации синтез-газа или реакция образования углерод-углеродных связей, выполняются одновременно в одном реакторе. Альтернативно, две реакции могут протекать в отдельных реакторах с тем, чтобы теплоту, выделяемую при экзотермической реакции, направлять обратно, чтобы поставить тепло в эндотермическую реакцию газификации. Реактор может быть любой известной на настоящее время или разработанной в будущем конструкции, до тех пор, пока конструкция реактора обеспечивает использование теплоты от экзотермической реакции в эндотермической реакции. В настоящем уровне техники хорошо известно конструирование реакторных систем для максимизации объединения теплоты между двумя или более реакциями, и мы не будем здесь обсуждать его подробно. См., например, ссылки (33) и (34).
Предпочтительное сырье для эндотермической реакции газификации включает биомассу или соединения, полученные из биомассы, включающие, но не ограничивающиеся этим, целлюлозные материалы, лигноцеллюлозные материалы, полисахариды, моносахариды, полиолы и им подобные. Предпочтительно сырье, включающее моносахариды и/или глицерин. Термин «биомасса», как он здесь используется, относится к органическим материалам, вырабатываемым растениями, таким как листья, корни, зерна и стебли, так же как и к отходам жизнедеятельности животных и микроорганизмов (например, навоз), без ограничений. Обычные источники биомассы включают (без ограничений): (1) сельскохозяйственные отходы, такие как стебли злаков, солома, кожура стручков, остатки сахарного тростника, жмых, скорлупа орехов и навоз крупного рогатого скота, домашней птицы и свиней; (2) древесные материалы, такие как древесина или кора, опилки, древесная стружка и отходы размольной машины; (3) городские отходы, такие как использованная бумага и изрезанные газеты, и (4) сельскохозяйственные культуры, используемые в качестве источника энергии, такие как тополя, ивы, просо, люцерна, бородатая трава, зерно, соевые бобы и подобное. Термин «реагент, полученный из биомассы» относится к любым реагентам, которые можно получить из биомассы путем любых известных в настоящее время средств или средств, которые могут быть разработаны в будущем, включающим (без ограничений) полисахариды, моносахариды, полиолы, кислородсодержащие углеводороды, сахара, крахмалы и подобное, например, этандиол, этандион, глицерин, глицеральдегид, альдотетрозы, альдопентозы, альдогексозы, кетотетрозы, кетопентозы, кетогексозы и альдитолы.
Предпочтительной экзотермической реакцией образования углерод-углеродных связей является реакция Фишера-Тропша. Реакцию газификации можно выполнить, используя один или более катализаторов, включающих металлы Группы VIIIB (Fe, Co, Ni, Ru, Rh, Pd, Os, Ir и Pt) или любой катализатор, перечисленный в разделе подробного описания изобретения. Катализатор можно нанести или не наносить на любой подходящий носитель (см. список примеров носителей в разделе подробного описания изобретения).
В предпочтительном воплощении изобретения эндотермическую реакцию газификации выполняют, используя реагирующее сырье, включающее глицерин, и экзотермическая реакция утилизации синтез-газа или реакция образования углерод-углеродных связей является реакцией Фишера-Тропша. Также можно использовать другие экзотермические реакции (такие как синтез метанола или синтез простого диметилового эфира).
Для того, чтобы более близко подобрать температуры двух реакций, предпочтительно, чтобы реакцию газификации выполняли, используя по меньшей мере один катализатор, включающий металл Группы VIIIB или сочетание металлов Группы VIIIB, и более предпочтительно, по меньшей мере еще один катализатор, включающий платину, рутений, рений (металл Группы VIIB) или их сочетание. Катализатор можно при желании нанести на носитель, что, вообще, является предпочтительным, так как такие нанесенные катализаторы становятся более стабильными во времени (см. раздел подробного описания изобретения). Можно использовать любой подходящий носитель. Предпочтительные носители включают, без ограничения, углерод, так же как и оксиды алюминия, церия, циркония и марганца и сочетания любых из них. В наиболее предпочтительном варианте изобретения используют один или более катализаторов, включающих платину, рутений, сочетание платины и рутения, или сочетание платины и рения, и катализатор наносят на носитель, выбираемый из группы, состоящей из углерода, Al2O3, CeO2, ZrO2, MgO, ZrO и их сочетания.
Таким образом, в настоящем изобретении реагирующие вещества, получаемые из биомассы, преобразуют в смесь газов H2 и CO (то есть синтез-газ); синтез-газ используют для получения топлива и химикалий посредством реакции Фишера-Тропша, синтеза метанола или других реакций образования углерод-углеродных связей. В предпочтительном варианте синтез-газ получают из глицерина над катализатором(рами), включающим платину. Как показано в приведенных здесь Примерах, настоящий способ обеспечивает выход синтез-газа с высокими процентами и высокой селективностью при температурах, которые значительно ниже по сравнению с обычной температурой газификации биомассы. В настоящем изобретении по меньшей мере часть эндотермической теплоты для стадии образования синтез-газа поставляют из экзотермической теплоты реакции образования углерод-углеродных связей. В настоящем изобретении температурные диапазоны этих каталитических процессов устанавливают так, чтобы они перекрывались или почти перекрывались, что является новой особенностью в области производства органических соединений при использовании синтез-газа в качестве сырья. Таким образом, настоящее изобретение предоставляет энергетически эффективный путь получения топлива и химических веществ из возобновляемых источников биомассы вообще и из глицерина в частности.
Получение синтез-газа из биомассы в течение многих лет рассматривалось в качестве многообещающей базы, из которой можно получить множество ценных продуктов. Однако обычное получение синтез-газа из биомассы требует очень высоких температур, которые ограничивают эффективность всего способа. Как здесь показано, каталитическое получение синтез-газа из биомассы (в частности, глицерина) можно производить так, чтобы оно происходило при температурах (примерно от 550 K до менее примерно 750 K и предпочтительно, менее примерно 620 K), которые значительно ниже, чем те, которые используют, применяя обычную непосредственную каталитическую газификацию биомассы (при 800 K) [4] или применяя обычную двухстадийную газификацию биомассы, которая включает быстрый пиролиз биомассы (при 773 K) [5, 6], за которой следует паровой риформинг получаемого био-масла (при 1000 K).
Важно, что в настоящем изобретении низкие температуры стадии газификации совпадают или почти совпадают с температурами, используемыми для синтезов Фишера-Тропша и метанола (вообще, для реакций утилизации синтез-газа). В результате по меньшей мере часть (и возможно всю) теплоту, требуемую для эндотермической стадии газификации, можно поставлять в виде теплоты, выделяемой при высоко экзотермической реакции утилизации синтез-газа или реакции образования углерод-углеродных связей. В частности, газификация глицерина (предпочтительный реагент) для получения CO и H2 протекает посредством следующей стехиометрической реакции:
Эндотермическая теплота этой реакции соответствует примерно 24% теплоты сгорания глицерина. Экзотермическая теплота, получаемая путем преобразования CO и H2 из глицерина для получения жидких алканов (например, октана) путем синтеза Фишера-Тропша соответствует примерно 28% теплоты сгорания глицерина. (Данное число включает небольшое количество теплоты, высвобождаемой при реакции сдвига в водяном газе (CO+H2O→CO2+H2), для подгонки соотношения газов H2:CO в соответствии со стехиометрией всей реакции.) Объединение стадии реакции газификации и синтеза Фишера-Тропша таким образом приводит к следующему слегка экзотермическому процессу, с теплотой, которая составляет только примерно 4% от теплоты сгорания глицерина.
Таким образом, очень значительное преимущество настоящего изобретения состоит в том, что реакция газификации работает при использовании сырья, имеющего высокую концентрацию глицерина (25% масс. и выше). Таким образом, настоящее изобретение коммерчески притягательно для создания органических соединений с дополнительными ценными характеристиками из большого (и возрастающего) количества глицерина, который получают в качестве побочного продукта при производстве биодизельного топлива. В частности, синтез-газ, получаемый из глицерина, можно использовать для получения метанола, важного реагента в процессе переэтерификации, благодаря чему уменьшают стоимость получения биодизельного топлива путем утилизации глицеринового побочного продукта.
Как показано подробно ниже, вообще предпочтительно использовать условия фазовой реакции, достигаемые путем испарения концентрированного водного раствора глицерина (например, 25-50% масс), приводящего к низкому парциальному давлению воды.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
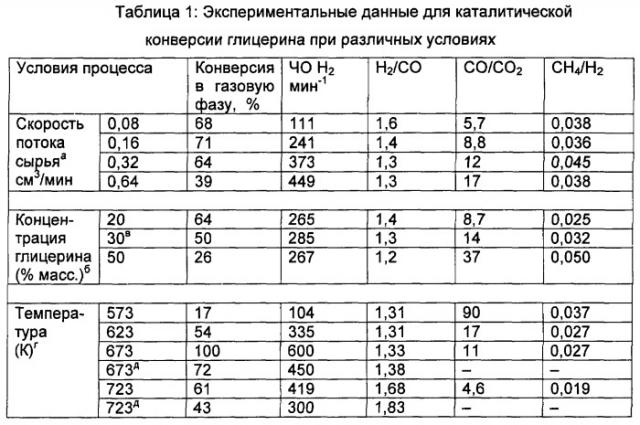
Фиг.1A, 1B, 1C и 1D представляют собой графические изображения изменений степени конверсии в газофазные продукты (Фиг.1A), частоту оборота H2 (Фиг.1B), молярное соотношение CO/CO2 (Фиг.1C), и соотношение C2 к H2, умноженное на 100 (Фиг.1D) для платиновых катализаторов, нанесенных на Al2O3 (■), CeO2/ZrO2 (▲), C (▼), ZrO2 (♦) и MgO/ZrO (o). Степень конверсии в газовую фазу вычисляют следующим образом: (число атомов углерода в потоке газофазного продукта / полное число атомов углерода, подаваемых в реактор) × 100. Реакции выполняли при 0,1 МПа (1 бар) и 623 K с подачей 0,32 см3 / мин 30% масс. водно-глицеринового раствора через 1,0 г платиновых катализаторов, нанесенных на оксид, или через 0,060 г Pt/C катализатор. ▼* показывает точку после 72 часов рабочего цикла.
Фиг.2A, 2B, 2C и 2D представляют собой графические изображения изменений степени конверсии глицерина в газофазные продукты (Фиг.2A) и молярных соотношений для риформинга в газовой фазе 30% масс. глицерина (Фиг.2B) при давлении 0,1 МПа (1 бар) (■), 50% глицерина при 0,1 МПа (1 бар) (▲) и 30% глицерина при 2 МПа (20 бар) (●) с 0,090 г Pt/C при 623 K. Изменение степени конверсии глицерина в газофазные продукты (Фиг.2C) и молярные соотношения (CO/CO2 - закрашенные значки, H2/CO - незакрашенные значки) для риформинга в газовой фазе 30% масс. глицерина (Фиг.2D) при 0,1 МПа (1 бар) с Pt:Ru/C при 548 K (треугольники: 0,435 г катализатора) и 573 K (квадраты: 0,513 г катализатора) и с Pt:Re/C при 498 K (перевернутые треугольники: 0,535 г катализатора) и 523 K (кружки: 0,535 г катализатора). Скорость подачи жидкости составляет 0,16 см3/мин для Фиг.2A и 2B и 0,08 см3/мин для Фиг.2C и 2D.
Фиг.3 представляет собой схему примерной реакционной кинетической установки, которая может быть использована для оценки настоящего изобретения. (Поток H2 используют только в течение каталитического восстановления).
Фиг.3A, 3B и 3C являются схематическими представлениями реактора и расположения каталитических слоев, которые можно использовать в настоящем изобретении. На Фиг.3A изображено расположение одного реактора с одним слоем. На Фиг.3B изображено расположение одного реактора со многими слоями, на Фиг.3C изображено расположение двух реакторов.
Фиг.4A и 4B представляют собой графические изображения изменения степени конверсии глицерина в газофазные продукты (Фиг.4A) и молярное соотношение для риформинга в газовой фазе потока 0,16 см3/мин 30% масс. глицерина (Фиг.4B) при 0,1 МПа (1 бар) и 623 K для системы с одним слоем (0,090 г Pt/C: открытые символы) и для системы с двумя слоями (0,090 г Pt/C, 1,0 г Pt/CeO2/ZrO2: закрытые символы).
Фиг.5 представляет собой графическое изображение молекулярно-массовых распределений для сухого синтез-газа (■) и совместно подаваемых воды (♦), ацетона (●), этанола (▲) и ацетола (▼). Экспериментальные условия были такими, как показаны в Табл.2. Линия АШФ нанесена с α=0,83.
Фиг.6 представляет собой графическое изображение степени конверсии в газофазные продукты (♦), молярное соотношение CO/CO2 (■) для обработки в газовой фазе 30% масс. водно-глицеринового сырья при 548 K и 0,83 МПа (8,3 бар). Степень конверсии в газовую фазу рассчитывали следующим образом (количество атомов C в потоке газофазного продукта / полное количество атомов C, подаваемых в реактор) × 100. Реакции выполняли, используя сырьевой раствор при 0,08 см3/мин через 520 мг катализатора.
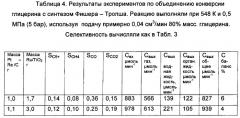
Фиг.7 представляет собой графическое изображение молекулярно-массовых распределений для объединенных экспериментов по конверсии глицерина с синтезом Фишера-Тропша при использовании 1,0 г Pt-Re/C с 1,7 г Ru/TiO2 (■) и 3,0 г Ru/TiO2 (●). Линия АШФ нанесена с α=0,8.
ПОДРОБНОЕ ОПИСАНИЕ
В основе настоящего изобретения лежит регламентированная процедура реакции, в которой температура эндотермической реакции газификации приведена в соответствие с оптимальной температурой для экзотермической реакции образования углерод-углеродных связей (например, синтез Фишера-Тропша) или, в более общем смысле, реакции утилизации синтез-газа (например, синтез метанола или синтез простого диметилового эфира). Путем разумного выбора условий реакций и катализаторов для каждой реакции можно выполнять две реакции на оптимальных уровнях и при примерно одинаковой температуре (или при относительно близких температурах). Теплоту из экзотермической реакции образования углерод-углеродных связей затем используют для проведения эндотермической реакции газификации.
Таким образом, на Фиг.1 показаны результаты для рабочих характеристик различных нанесенных платиновых катализаторов для риформинга в газовой фазе при 623 K и атмосферном давлении при использовании сырьевого раствора, включающего 30% масс. глицерина в воде. Катализатор, включающий Pt, нанесенную на Al2O3, ZrO2, CeO2/ZrO2 или MgO/ZrO2, демонстрирует относительную быструю дезактивацию в течение рабочего цикла. Таким образом, хотя эти катализаторы можно использовать в настоящем изобретении, они не являются предпочтительными. Pt/C катализатор показывает стабильную конверсию глицерина в синтез-газ в течение по меньшей мере 72 часов. См. Фиг.1А. Описанный здесь катализатор с наиболее кислотным носителем, Pt/Al2O3, показывает период стабильной каталитической активности в течение первых 30 часов, за которым следует период быстрой дезактивации катализатора. Это поведение является характеристикой фронта дезактивации, который движется от входного отверстия реактора к выходному отверстию, и наступление быстрой дезактивации возникает, когда фронт достигает выхода реактора. Описанный здесь катализатор с наиболее основным носителем, MgO/ZrO2, показывает быструю дезактивацию для всего рабочего цикла. Наиболее стабильным из испытанных катализаторов на оксидном носителе, как видно, является Pt на СеО2/ZrO2. Однако, рабочая характеристика этого катализатора еще менее предпочтительна, чем у платины, нанесенной на углерод.
На Фиг.1В показана производительность по H2 на различных катализаторах в оценках частоты оборота (ЧО), где производительность нормировали к числу поверхностных атомов платины, которое определяли путем предельной адсорбции CO при 298 K. Частота оборота для получения водорода, определенная таким образом, выше (например, по меньшей мере в 10 раз), чем величины для получения водорода путем риформинга в водной фазе при 500 K с платиновым катализатором, нанесенным на оксид алюминия (см., например, 19). Производство H2 из глицерина с Pt/C катализатором соответствует приблизительно производству энергии 160 Ватт на грамм катализатора (используя более низкую теплоту сгорания H2). Так как этот катализатор производит газ с соотношением H2:CO приблизительно 1,3, содержание энергии в выходящем газе соответствует приблизительно 300 Ватт на грамм катализатора.
Различные профили дезактивации, показанные на Фиг.1А и 1В для различных испытываемых катализаторов предполагают, что носитель играет важную роль в процессе дезактивации. Соотношение H2:CO для потока продукта из Pt/C катализатора равно приблизительно 1,3 (см. Табл.1), что соответствует стехиометрии реакции 3. Напротив, соотношение H2:CO, полученное с другими катализаторами, было выше 1,5, что показывает вклад других реакций, таких как реакция сдвига в водяном газе (СВГ). Это поведение более ясно демонстрируется посредством соотношения CO:CO2, как показано на Фиг.1С. Начальное соотношение CO:CO2 для Pt/C составляет 12, в то время как оно меньше 3 для других катализаторов. Таким образом, видно, что реакции СВГ способствует присутствие оксидного носителя, как описано в других исследованиях реакции СВГ с нанесенн