Гомологи фосфатазы фосфатидной кислоты и их применение
Иллюстрации
Показать всеНастоящее изобретение относится к области биотехнологии и может быть использовано в пищевой промышленности. Из Mortierella alpina получен новый ген, который кодирует фосфатазу фосфатидной кислоты (ЕС 3.1.3.4), определена открытая рамка считывания и выведена аминокислотная последовательность фермента, названного MaPAP1. Описано получение рекомбинантного белка путем трансформации клеток-хозяев, где при использовании в этом качестве дрожжевых клеток или клеток липидпродуцирующих грибков обеспечивается не только увеличение общего содержания жирных кислот (ЖК), но и изменение жирнокислотного состава клетки, выражающееся, в частности, в повышении отношения количества арахидоновой кислоты к общему количеству ЖК. 8 н.п. ф-лы, 7 табл., 2 ил., 8 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Это описание изобретения притязает на приоритет заявки на патент Японии № 2007-181899 (поданной 11 июля 2007).
Настоящее изобретение относится к новым генам фосфатазы фосфатидной кислоты.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Жирные кислоты являются важными компонентами липидов, таких как фосфолипиды и триацилглицерины. Жирные кислоты, содержащие две или более ненасыщенных связей, в совокупности именуются полиненасыщенными жирными кислотами (PUFA) и, как известно, включают арахидоновую кислоту, дигомо-γ-линоленовую кислоту, эйкозапентаеновую кислоту и докозагексаеновую кислоту. Некоторые из этих полиненасыщенных жирных кислот не могут синтезироваться в организме животного, и такие полиненасыщенные жирные кислоты должны заимствоваться в качестве незаменимых жирных кислот из пищевых источников. Полиненасыщенные жирные кислоты широко распространены. В качестве примера, арахидоновую кислоту получают при разложении липидов, экстрагированных из надпочечников и/или печеней животных. Однако количество полиненасыщенных жирных кислот, содержащихся в органах животных, является небольшим, и их невозможно получить в достаточном количестве для больших запасов при простом экстрагировании или выделении из органов животных. По этой причине методы с использованием микроорганизмов были разработаны для получения полиненасыщенных жирных кислот путем культивирования различных микроорганизмов. Известно, что, в первую очередь, микроорганизмы рода Mortierella продуцируют липиды, содержащие арахидоновую кислоту и другие полиненасыщенные жирные кислоты.
Также предпринимались другие попытки для продуцирования полиненасыщенных жирных кислот в растениях. Полиненасыщенные жирные кислоты образуют запасные липиды, такие как триацилглицерины, и, как известно, аккумулируются в клетках микроорганизмов или семенах растений.
Триацилглицерины, являющиеся запасными липидами, продуцируются in vivo следующим образом. Перенос ацильной группы происходит на глицерол-3-фосфат с помощью глицерол-3-фосфат-ацилтрансферазы с образованием лизофосфатидной кислоты (LPA), на которую перенос ацильной группы далее происходит с помощью LPA-ацилтрансферазы с образованием фосфатидной кислоты. Эта фосфатидная кислота, в свою очередь, подвергается дефосфорилированию с помощью фосфатазы фосфатидной кислоты с образованием диацилглицерина, на который затем переносится ацильная группа с помощью диацилглицерол-ацилтрансферазы с образованием триацилглицерина.
В вышеприведенном каскаде реакций фосфатидная кислота (в дальнейшем также именуемая «РА» или «1,2-диацил-sn-глицерол-3-фосфат») служит не только в качестве предшественника триацилглицерина, но также в качестве предшественника для биосинтеза глицерофосфолипидов диацильного типа. В дрожжах или других микроорганизмах РА-цитидилтрансфераза действует на РА и цитидин-5'-трифосфат (СТР) с вызовом синтеза CDP-диацилглицерина (CDP-DG), который в свою очередь используется для биосинтеза различных фосфолипидов.
Как описано выше, известно, что дефосфорилирование РА при биосинтезе диацилглицерина (в дальнейшем также именуемого «DG») катализируется фосфатазой фосфатидной кислоты (Е.С. 3.1.3.4; в дальнейшем также именуемой «РАР»). Известно, что этот фермент РАР присутствует у всех организмов, простирающихся от бактерий до позвоночных животных. Кроме того, у грибов РАР является ключевым ферментом биосинтеза триацилглицеринов (которые являются запасными липидами), начинающегося с РА.
Известно, что дрожжи Saccharomyces cerevisiae, которые являются грибком, имеют два типа РАР (непатентный документ 1). Один фермент является Mg2+-зависимой РАР (РАР1), а другой фермент является Mg2+-независимой РАР (РАР2). В качестве гена, кодирующего первый фермент, был известен ген РАН1. Однако поскольку мутанты pah1Δ обладают РАР1-активностью, существуют другие возможные гены, ответственные за РАР1-активность. С другой стороны, в качестве генов, кодирующих РАР2, были известны гены DPP1 и LPP1, и они в значительной степени ответственны за РАР2-активность у дрожжей. Кодируемые этими генами ферменты имеют широкую субстратную специфичность и, как известно, действуют также на диацилглицеролпирофосфат (DGPP), лизофосфатидную кислоту, сфингооснование-фосфат и изопреноид-фосфат и т.д. с вызовом их дефосфорилирования.
В других грибах было подтверждено присутствие этих гомологов, но нет сообщения об их функции, и т.п.
Было известно, что в липидпродуцирующих грибах, Mortierella alpina, РАР-активностью обладает микросомальная фракция (непатентный документ 2).
Непатентный документ 1: Trends Biochem. Sci., 31(12), 694-699, 2006.
Непатентный документ 2: Biochemical Society Transactions, 28, 707-709, 2000.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ПРОБЛЕМЫ, КОТОРЫЕ ДОЛЖНЫ БЫТЬ РАЗРЕШЕНЫ НАСТОЯЩИМ ИЗОБРЕТЕНИЕМ
Однако ранее описанные гены РАР не были исследованы на их способность к изменению жирнокислотной характеристики композиций жирных кислот, продуцируемых клетками-хозяевами, в которые введены и в которых экспрессируются эти гены РАР. Существует потребность в идентификации нового гена, который позволяет продуцировать жиры и масла с требуемой жирнокислотной характеристикой и/или обогащением требуемыми жирными кислотами при введении в клетки-хозяева или экспрессии в них.
СПОСОБЫ РАЗРЕШЕНИЯ ПРОБЛЕМ
Целью настоящего изобретения является обеспечение белка или нуклеиновой кислоты, которые позволяют продуцировать жиры и масла с требуемой жирнокислотной характеристикой и/или обогащением требуемыми жирными кислотами при экспрессии в клетках-хозяевах или введении в них.
Для достижения вышеприведенной цели авторы настоящего изобретения выполнили большие объемы напряженных работ. Во-первых, был проведен анализ маркерных экспрессируемых последовательностей (EST) на липидпродуцирующем грибе, Mortierella alpina, для получения последовательностей, разделяющих высокую идентичность с известными генами РАР. Для получения полноразмерной открытой рамки считывания (ORF), кодирующей РАР, гены далее клонировали путем отбора из кДНК-библиотеки или ПЦР. В результате предпринятия попытки ввести эти гены в клетки-хозяева с высокой пролиферативной активностью (например, дрожжевые клетки) для продуцирования, тем самым, требуемой композиции жирной кислоты, авторы настоящего изобретения добились успеха в клонировании гена, относящегося к новой РАР, которая делает возможной продукцию композиции жирной кислоты, отличной от смеси, продуцируемой хозяином, не несущим этот ген. Это привело к завершению настоящего изобретения. То есть, настоящее изобретение представляет собой следующие изобретения:
(1) Нуклеиновую кислоту, включающую нуклеотидную последовательность, указанную в любом из подпунктов (а)-(е) ниже:
(а) нуклеотидную последовательность, которая кодирует белок, состоящий из аминокислотной последовательности с делецией, заменой или добавлением одной или нескольких аминокислот в аминокислотной последовательности, указанной в SEQ ID NO: 2, и обладающий активностью фосфатазы фосфатидной кислоты;
(b) нуклеотидную последовательность, которая поддается гибридизации в жестких условиях с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, состоящей из SEQ ID NO: 4, и которая кодирует белок, обладающий активностью фосфатазы фосфатидной кислоты;
(c) нуклеотидную последовательность, которая состоит из нуклеотидной последовательности, идентичной на 70% или больше нуклеотидной последовательности, состоящей из SEQ ID NO: 4, и которая кодирует белок, обладающий активностью фосфатазы фосфатидной кислоты;
(d) нуклеотидную последовательность, которая кодирует аминокислотную последовательность, идентичную на 70% или больше аминокислотной последовательности, состоящей из SEQ ID NO: 2, и которая кодирует белок, обладающий активностью фосфатазы фосфатидной кислоты; или
(e) нуклеотидную последовательность, которая поддается гибридизации в жестких условиях с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, кодирующей белок, состоящий из аминокислотной последовательности, указанной в SEQ ID NO: 2, и которая кодирует белок, обладающий активностью фосфатазы фосфатидной кислоты.
(2) Нуклеиновую кислоту в соответствии с (1) выше, которая включает нуклеотидную последовательность, указанную в любом из подпунктов (а)-(с) ниже:
(а) нуклеотидную последовательность, которая кодирует белок, состоящий из аминокислотной последовательности с делецией, заменой или добавлением 1-10 аминокислот в аминокислотной последовательности, указанной в SEQ ID NO: 2, и обладающий активностью фосфатазы фосфатидной кислоты;
(b) нуклеотидную последовательность, которая поддается гибридизации в условиях использования 2 х SSC при 50οС с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, состоящей из SEQ ID NO: 4, и которая кодирует белок, обладающий активностью фосфатазы фосфатидной кислоты; или
(c) нуклеотидную последовательность, которая кодирует аминокислотную последовательность, идентичную на 90% или больше аминокислотной последовательности, состоящей из SEQ ID NO: 2, и которая кодирует белок, обладающий активностью фосфатазы фосфатидной кислоты.
(3) Нуклеиновую кислоту, включающую нуклеотидную последовательность, указанную в любом из подпунктов (а)-(с) ниже, или ее фрагмент:
(а) нуклеотидную последовательность, указанную в SEQ ID NO: 4;
(b) нуклеотидную последовательность, кодирующую белок, состоящий из аминокислотной последовательности, указанной в SEQ ID NO: 2; или
(с) нуклеотидную последовательность, указанную в SEQ ID NO: 1.
(4) Нуклеиновую кислоту, включающую нуклеотидную последовательность, указанную в любом из подпунктов (а)-(е) ниже:
(а) нуклеотидную последовательность, которая кодирует следующий белок:
белок, который состоит из аминокислотной последовательности с делецией, заменой или добавлением одной или нескольких аминокислот в аминокислотной последовательности, указанной в SEQ ID NO: 2, и который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты;
(b) нуклеотидную последовательность, которая поддается гибридизации в жестких условиях с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, состоящей из SEQ ID NO: 4, и которая кодирует следующий белок:
белок, который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты;
(c) нуклеотидную последовательность, которая состоит из нуклеотидной последовательности, идентичной на 70% или больше нуклеотидной последовательности, состоящей из SEQ ID NO: 4, и которая кодирует следующий белок:
белок, который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты;
(d) нуклеотидную последовательность, которая кодирует следующий белок:
белок, который состоит из аминокислотной последовательности, идентичной на 70% или больше аминокислотной последовательности, состоящей из SEQ ID NO: 2, и который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты; или
(e) нуклеотидную последовательность, которая поддается гибридизации в жестких условиях с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, кодирующей белок, состоящий из аминокислотной последовательности, указанной в SEQ ID NO: 2, и которая кодирует следующий белок:
белок, который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты;
(5) Нуклеиновую кислоту в соответствии с (4) выше, которая включает нуклеотидную последовательность, указанную в любом из подпунктов (а)-(с) ниже:
(а) нуклеотидную последовательность, которая кодирует следующий белок:
белок, который состоит из аминокислотной последовательности с делецией, заменой или добавлением 1-10 аминокислот в аминокислотной последовательности, указанной в SEQ ID NO: 2, и который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты;
(b) нуклеотидную последовательность, которая поддается гибридизации в условиях использования 2 х SSC при 50οС с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, состоящей из SEQ ID NO: 4, и которая кодирует следующий белок:
белок, который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты; или
(c) нуклеотидную последовательность, которая кодирует следующий белок:
белок, который состоит из аминокислотной последовательности, идентичной на 90% или больше аминокислотной последовательности, состоящей из SEQ ID NO: 2, и который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты.
(6) Белок, указанный в подпункте (а) или (b) ниже:
(а) белок, который состоит из аминокислотной последовательности с делецией, заменой или добавлением одной или нескольких аминокислот в SEQ ID NO: 2, и который обладает активностью фосфатазы фосфатидной кислоты; или
(b) белок, который состоит из аминокислотной последовательности, идентичной на 70% или больше аминокислотной последовательности, состоящей из SEQ ID NO: 2, и который обладает активностью фосфатазы фосфатидной кислоты.
(7) Белок, указанный в подпункте (а) или (b) ниже:
(а) белок, который состоит из аминокислотной последовательности с делецией, заменой или добавлением одной или нескольких аминокислот в SEQ ID NO: 2, и который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, состоящий из указанной выше аминокислотной последовательности, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты; или
(b) белок, который состоит из аминокислотной последовательности, идентичной на 70% или больше аминокислотной последовательности, состоящей из SEQ ID NO: 2, и который обладает способностью к обеспечению жирнокислотной характеристики, в которой гарантируется большая степень по крайней мере одного или нескольких показателей i)-vi), указанных ниже, в жирнокислотной характеристике хозяина, экспрессирующего белок, состоящий из указанной выше аминокислотной последовательности, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты.
(8) Белок, состоящий из аминокислотной последовательности, указанной в SEQ ID NO: 2.
(9) Рекомбинантный вектор, включающий нуклеиновую кислоту в соответствии с любым из (1)-(5) выше.
(10) Трансформант, трансформированный рекомбинантным вектором в соответствии с (9) выше.
(11) Композиция жирной кислоты, полученная путем культивирования трансформанта в соответствии с (10) выше, в жирнокислотной характеристике которой по крайней мере один или несколько показателей i)-vi), указанных ниже, больше чем в жирнокислотной характеристике продукта культивирования, полученного путем культивирования хозяина, который не трансформирован рекомбинантным вектором в соответствии с (9) выше:
i) содержание олеиновой кислоты;
ii) отношение содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношение содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношение общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношение содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительный показатель содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты.
(12) Способ приготовления композиции жирной кислоты, который включает получение композиции жирной кислоты в соответствии с (11) выше из продукта культивирования, полученного путем культивирования трансформанта в соответствии с (10) выше.
(13) Пищевой продукт, включающий композицию жирной кислоты в соответствии с (11) выше.
ПРЕИМУЩЕСТВА НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
РАР настоящего изобретения предоставляет хозяину возможность продуцировать композицию жирной кислоты жирных кислот, жирнокислотная характеристика которой отличается от жирнокислотной характеристики композиции жирной кислоты, продуцируемой хозяином, не несущим РАР. В результате РАР настоящего изобретения делает возможным обеспечение липидов, имеющих требуемые свойства и действия, и является полезной при применении в пищевых продуктах, косметических средствах, мылах и т.п.
Кроме того, РАР настоящего изобретения позволяет увеличить способность к продукции жирных кислот и запасных липидов и, следовательно, является предпочтительной в качестве средства увеличения выработки полиненасыщенных жирных кислот в микроорганизмах и растениях.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 демонстрируется последовательность кДНК MaPAP1 в соответствии с настоящим изобретением вместе с ее расшифрованной аминокислотной последовательностью.
На фиг. 2 демонстрируется совмещение расшифрованной аминокислотной последовательности MaPAP1p (SEQ ID NO: 2) с аминокислотными последовательностями белков семейства РАР2. На этой фигуре три сегмента с двойным подчеркиванием представляют консенсусные области, консервативные среди ферментов семейства РАР2, а «*» представляет аминокислотный остаток, необходимый для РАР-активности.
ЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым генам для фосфатазы фосфатидной кислоты, происходящим из рода Mortierella, характеризующейся дефосфорилированием фосфатидной кислоты с образованием диацилглицерина.
Фосфатаза фосфатидной кислоты (РАР) в настоящем изобретении является ферментом, катализирующим реакцию, в которой фосфатидная кислота подвергается дефосфорилированию с образованием диацилглицерина. Субстратом для РАР в настоящем изобретении является, как правило, но без ограничения, фосфатидная кислота.
Нуклеиновые кислоты настоящего изобретения, кодирующие фосфатазу фосфатидной кислоты
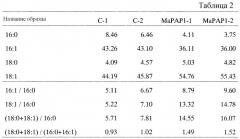
Фосфатаза фосфатидной кислоты (РАР) в настоящем изобретении включает MaPAP1. В таблице 1 ниже резюмировано соответствие между кДНК, CDS (кодирующей белок последовательностью), ORF и аминокислотными последовательностями нуклеиновой кислоты, кодирующей MaPAP1.
То есть, последовательности, относящиеся к РАР настоящего изобретения, включают SEQ ID NO: 2 (аминокислотную последовательность MaPAP1), SEQ ID NO: 4 (последовательность, являющуюся областью ORF MaPAP1), SEQ ID NO: 3 (последовательность, являющуюся областью CDS MaPAP1) и SEQ ID NO: 1 (нуклеотидную последовательность кДНК MaPAP1). Среди них SEQ ID NO: 3 соответствует нуклеотидам 105-1223 SEQ ID NO: 1, в то время как SEQ ID NO: 4 соответствует нуклеотидам 105-1220 SEQ ID NO: 1 или нуклеотидам 1-1116 SEQ ID NO: 3.
Нуклеиновые кислоты настоящего изобретения включают одноцепочечные и двухцепочечные ДНК, а также комплементарные им РНК, которые могут или иметь природное происхождение, или быть искусственно приготовлены. ДНК включают, но без ограничения, геномные ДНК, кДНК, соответствующие геномным ДНК, химически синтезированные ДНК, амплифицированные с помощью ПЦР ДНК, а также их комбинации и гибриды ДНК/РНК.
Предпочтительные варианты осуществления нуклеиновых кислот настоящего изобретения включают (а) нуклеотидную последовательность, указанную в SEQ ID NO: 4; (b) нуклеотидную последовательность, кодирующую белок, состоящий из аминокислотной последовательности, указанной в SEQ ID NO: 2; и (с) нуклеотидную последовательность, указанную в SEQ ID NO: 1.
Указанные выше нуклеотидная последовательность, указанная в SEQ ID NO: 4, нуклеотидная последовательность, кодирующая белок, состоящий из аминокислотной последовательности, указанной в SEQ ID NO: 2, и нуклеотидная последовательность, указанная в SEQ ID NO: 1, являются последовательностями, продемонстрированными в таблице 1.
Для получения этих нуклеотидных последовательностей данные, касающиеся нуклеотидных последовательностей: EST или геномных ДНК из организмов, обладающих РАР-активностью, можно использовать для поиска нуклеотидной последовательности, кодирующей белок, обдающий высокой степенью идентичности с известными белками, обладающими РАР-активностью. Предпочтительными организмами, обладающими РАР-активностью, являются липидпродуцирующие грибы, включающие, но без ограничения, M. alpina.
Для анализа EST сначала готовят библиотеку кДНК. В отношении методов приготовления библиотеки кДНК можно привести ссылку на “Molecular Cloning, A Laboratory Manual 3rd ed.” (Cold Spring Harbor Press (2001)). В альтернативном случае можно использовать имеющийся в продаже набор для приготовления библиотеки кДНК. Методы приготовления библиотеки кДНК, подходящей для настоящего изобретения, являются, в качестве примера, следующими. А именно, соответствующий штамм M. alpina, липидпродуцирующего гриба, засевают в соответствующую среду и подвергают предварительному культивированию в течение соответствующего периода времени. Условия культивирования, подходящие для этого предварительного культивирования, включают, например, состав среды из 1,8% глюкозы, 1% дрожжевого экстракта и рН 6,0, период культивирования, составляющий 3 дня, и температуру культивированию, составляющую 28οС. Продукт предварительного культивирования затем подвергают основному культивированию при соответствующих условиях. Составом среды, подходящим для основного культивирования, может быть, например, 1,8% глюкозы, 1% соевого порошка, 0,1% оливкового масла, 0,01% Adekanol, 0,3% KH2PO4, 0,1% Na2SO4, 0,05% CaCl2 .2H2O, 0,05% MgCl2 .6H20 и рН 6,0. Условиями культивирования, подходящими для основного культивирования, могут быть, например, аэробное культивирование с постоянным перемешиванием при 300 оборотах в минуту, 1 vvm (отношение количества подводимого воздуха к емкости сосуда для культивирования), 26οC в течение 8 дней. Во время культивирования можно добавлять подходящее количество глюкозы. В соответствующие моменты времени во время основного культивирования отбирают образцы продукта культивирования, из которых затем собирают клетки для приготовления обшей РНК. Для приготовления общей РНК можно использовать любой известный метод, такой как метод с использованием гуанидина гидрохлорида/CsCl. Результирующую общую РНК можно обработать, используя имеющийся в продаже набор для очистки поли(А)+РНК. Кроме того, библиотеку кДНК можно приготовить с использованием имеющегося в продаже набора. Затем нуклеотидную последовательность любого клона из приготовленной таким образом библиотеки кДНК определяют, используя праймеры, которые сконструированы на основе вектора, для того чтобы сделать возможным определение нуклеотидной последовательности вставки. В результате можно получить EST. Например, при использовании для приготовления библиотеки кДНК набора для клонирования ZAP-cDNA GigapackIII Gold (Stratagene) можно выполнить прямое клонирование.
После анализа с помощью BLASTX оказалось, что ген MaPAP1 настоящего изобретения идентичен на 57,4% нуклеотидной последовательности, кодирующей происходящий из Neurospora crassa гомолог диацилглицеролпирофосфат-фосфатазы (DPP1) (входящий № CAD70721), имеющей наименьший Е-показатель (т.е. демонстрирующей наибольшую идентичность), и идентичен на 59,3% аминокислотной последовательности этого гомолога.
Настоящим изобретением также охватываются нуклеиновые кислоты, функционально эквивалентные нуклеиновой кислоте, включающей вышеприведенную нуклеотидную последовательность, указанную в SEQ ID NO:4 (в дальнейшем также именуемой «нуклеотидная последовательность настоящего изобретения»), или нуклеотидную последовательность, кодирующую белок, состоящий из аминокислотной последовательности, указанной в SEQ ID NO:4 (в дальнейшем также именуемой «аминокислотная последовательность настоящего изобретения»). Предполагается, что выражение «функционально эквивалентный» означает, что белок, кодируемый нуклеотидной последовательностью настоящего изобретения, или белок, состоящий из аминокислотной последовательности настоящего изобретения, обладает РАР-активностью. Помимо этой РАР-активности белок, кодируемый нуклеотидной последовательностью настоящего изобретения, или белок, состоящий из аминокислотной последовательности настоящего изобретения, может обладать способностью к обеспечению жирнокислотной характеристики, в котором гарантируется большая степень по крайней мере одного или нескольких показателей:
i) содержания олеиновой кислоты;
ii) отношения содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты;
iii) отношения содержания олеиновой кислоты к содержанию пальмитиновой кислоты;
iv) отношения общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты;
v) отношения содержания жирных кислот С18 к содержанию жирных кислот С16; и
vi) относительного показателя содержания арахидоновой кислоты, дигомо-γ-линоленовой кислоты и/или γ-линоленовой кислоты;
в жирнокислотной характеристике хозяина, экспрессирующего белок, чем в жирнокислотной характеристике хозяина, не экспрессирующего этот белок (такой белок в дальнейшем также именуется «белком, обладающим способностью к обеспечению жирнокислотной характеристики, обеспечиваемой РАР в настоящем изобретении»).
Конкретным примером является нуклеиновая кислота, включающая нуклеотидную последовательность, кодирующую белок, обладающий способностью к обеспечению жирнокислотной характеристики, которая удовлетворяет по крайней мере одному или нескольким следующим условиям:
i) содержание олеиновой кислоты составляет 46% или больше, предпочтительно 48% или больше, 50% или больше, 52% или больше, 54% или больше;
ii) отношение содержания пальмитолеиновой кислоты к содержанию пальмитиновой кислоты составляет 7,0, предпочтительно 8,0 или больше, 8,5% или больше;
iii) отношение содержания олеиновой кислоты к содержанию пальмитиновой кислоты составляет 7,5 или больше, предпочтительно 8,0 или больше, 10,0 или больше, 12,0 или больше, 13,0 или больше;
iv) отношение общего содержания стеариновой и олеиновой кислот к содержанию пальмитиновой кислоты составляет 8,0 или больше, предпочтительно 10,0 или больше, 12,0 или больше, 14,0 или больше, 14,5 или больше;
v) отношение содержания жирных кислот С18 к содержанию жирных кислот С16 составляет 1,1 или больше, предпочтительно 1,2 или больше, 1,3 или больше, 1,4 или больше; и
vi) содержание арахидоновой кислоты составляет 0,45 или больше, предпочтительно 0,50 или больше, 0,53 или больше, 0,55 или больше, содержание дигомо-γ-линоленовой кислоты составляет 0,34 или больше, предпочтительно 0,40 или больше, 0,42 или больше, 0,45 или больше, и/или содержание γ-линоленовой кислоты составляет 0,55 или больше, предпочтительно 0,65 или больше, 0,67 или больше, 0,70 или больше, 0,75 или больше (все вышеприведенные числа указывают на отношение к общему содержанию жирных кислот, когда ген РАР настоящего изобретения экспрессируется в продуцирующих арахидоновую кислоту дрожжевых клетках),
когда указанная выше нуклеотидная последовательность настоящего изобретения встроена в экспрессионный вектор pYE22m (Biosci. Biotech. Biochem., 59. 1221-1228, 1995) и трансформирована в являющегося дрожжами хозяина, штамм EH13-15 Saccharomyces cerevisiae (Appl. Microbiol. Biotechnol., 30, 515-520, 1989), и результирующий трансформант культивируют для сбора клеток, которые затем анализируют на жирные кислоты с помощью способов, описанных в примере 6 ниже. Более предпочтительной является нуклеиновая кислота, включающая нуклеотидную последовательность, кодирующую белок, обладающий как РАР-активностью, так и указанной выше способностью к обеспечению жирнокислотной характеристики, обеспечиваемой РАР в настоящем изобретении.
Одним из характерных признаков композиции жирной кислоты настоящего изобретения является высокое содержание арахидоновой кислоты. Арахидоновая кислота, субстрат, представляемый химической формулой С20Н32О2 и имеющий молекулярную массу 304,47, является карбоновой кислотой, содержащей 20 атомов углерода и имеющей 4 двойные связи ([20:4(n-6]), и относящейся к члену (n-6)-рядов. Арахидоновая кислота присутствует в качестве важного фосфолипида (в частности, фосфатидилэтаноламина, фосфатидилхолина, фосфатидилинозита) в мембранах клеток животных и содержится в большом количестве в головном мозге. Кроме того, арахидоновая кислота служит в качестве исходного материала для ряда эйкозаноидов (например, простагландина, тромбоксана, лейкотриена), образуемых с помощью каскада реакций с вовлечением арахидоновой кислоты, и также важна в качестве вторичного мессенджера при межклеточной передаче сигналов. С другой стороны, арахидоновая кислота синтезируется из линолевой кислоты в организме животного. Однако, у некоторых животных, в зависимости от их в