Способ изготовления кардиоимплантата из сплава на основе никелида титана с модифицированным ионно-плазменной обработкой поверхностным слоем
Иллюстрации
Показать всеИзобретение относится к изготовлению кардиоимплантатов из сплава на основе никелида титана с эффектом памяти формы (ЭПФ) и сверхэластичности с модифицированным ионно-плазменной обработкой поверхностным слоем, предназначенных для длительной эксплуатации в сердечно-сосудистой системе организма и обладающих коррозионной стойкостью, биосовместимостью и нетоксичностью в биологических средах. Описан способ изготовления кардиоимплантата, включающий: изготовление кардиоимплантата, химическую и электрохимическую очистку его поверхности, обработку поверхности кардиоимплантата потоками ионов кремния, полученных путем распыления кремниевого катода в вакууме, в режиме высокодозовой ионной имплантации с флюенсом (0,5÷6,0)×1017 см-2 с получением поверхностного модифицированного слоя толщиной 80-95 нм, состоящего, по меньшей мере, из двух подслоев: наружный подслой толщиной 20-25 нм содержит кислород, углерод, кремний и титан при следующем соотношении элементов, ат.%: кислород 25-65, углерод 1-5, кремний 1-10, титан - остальное; промежуточный подслой толщиной 60-70 нм содержит кислород, углерод, кремний, титан и никель при следующем соотношении элементов, ат.%: кислород 5-30, углерод 1-5, кремний 10-30, никель 1-50, титан остальное, причем максимальную концентрацию кремний достигает на глубине 30-35 нм от поверхности. Модифицированный поверхностный слой с измененным составом не обладает выраженной поверхностью раздела между подслоями, характерной для осажденного слоя. 8. з.п. ф-лы, 1 ил.
Реферат
Изобретение относится к изготовлению кардиоимплантатов из сплава на основе никелида титана с эффектом памяти формы (ЭПФ) и сверхэластичности с модифицированным ионно-плазменной обработкой поверхностным слоем, предназначенных для длительной эксплуатации в сердечно-сосудистой системе организма и обладающих коррозионной стойкостью, биосовместимостью и нетоксичностью в биологических средах.
Известны биосовместимые многокомпонентные наноструктурные покрытия (МНП) для имплантатов (RU 2281122, A61L 27/02, A61K 6/02, опубл. 10.08. 2006)[1], работающие под нагрузкой, выполнены на основе карбонитрида титана с введением дополнительных элементов, улучшающих механические и трибологические свойства покрытия, а также обеспечивающие его биоактивность, биосовместимость и нетоксичность. Суммарные концентрации основных и дополнительных элементов в покрытии имеют следующее соотношение:
1.2 < ∑ X i ∑ X j < 20
где Xi - суммарная концентрация основных элементов Ti, C, N в покрытии, Yj - суммарная концентрация дополнительных элементов Ca, Zr, Si, K, Mn, O, P в покрытии, при этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат.%: Ti 30-50, C 15-40, N 0.5-30, O 5-25, Ca 0-7, Zr 0-20, Si 0-30, P 0-1.5, Mn 0-1.0, К 0-1.0. Для измерения физико-механических и трибологических свойств МНП осаждались на подложки из титанового сплава марки ВТ 1-0, никелевого сплава Целит-Н, кобальтового сплава Целит-К, а также никелида титана.
Недостатком известного способа является то, что материалы, на которые осаждали МНП, кроме никелида титана, не могут быть использованы для изготовления кардиоимплантатов, в частности для закупорки ушка левого предсердия зонтичного устройства, так как они не обладают термической памятью формы или сверхэластичностью в диапазоне температур человеческого тела.
Недостатком данного способа также является сложность достижения указанного компонентного состава элементов в МНП покрытии.
Описан способ формирования наноструктурированного биосовместимого покрытия на имплантатах (RU 2448741, A61L 27/30, A61L 27/56, A61F 2/28, опубл. 27.04.2012)[2], который заключается в осаждении на поверхность имплантата пленки поликремния в реакторе. Полученную пленку поликремния подвергают химическому травлению для образования наноструктурированного приповерхностного слоя пористого поликремния. Травление пленки поликремния осуществляют при погружении имплантата в смесь, содержащую 50-55% водный раствор тетрафтороборной кислоты (HBF4), 70-90% водный раствор азотной кислоты (HNO3) и анионное поверхностно-активное вещество на основе аммонийной соли перфторсульфокислоты RfPSC3NH4 в количестве 5·10-3-10-2 (мас.%), где Rf-C8F17, или C2 F5OC3F6OC2F4, или C6F13CH2CH2. Используют водные растворы кислот при соотношении их объемных частей: HBF4:HNO3, как (100-800):(1:1,1), с последующей промывкой имплантата деионизованной водой и сушкой. Расширяются технологические возможности способа вне зависимости от используемых материалов и конструктивных особенностей имплантатов.
Недостатком данного способа является то, что пленка поликремния на поверхности материалов, выбранных из ряда: металлы (титан, сплавы титана, сталь), металлокерамика и стеклокерамика, в результате химического травления приобретает пористую структуру. Такой приповерхностный слой на основе поликремния с пористой структурой не может играть роль барьерного слоя при контакте с биосредой (кровь, мягкие и твердые ткани организма человека), препятствующего выходу в нее ионов никеля. Другим недостатком известного приповерхностного слоя является его хрупкость и относительно невысокая адгезионная прочность сцепления с поверхностью имплантата, в результате чего это покрытие может разрушаться при деформации имплантата, что будет нарушать сплошность барьерного слоя.
Известен способ поверхностной обработки материалов с памятью формы, таких как сплавы на основе никелида титана (US 2006157159, A61L 27/06, A61L 27/50, C23C 14/48, С23С 8/36, опубл. 2006.07.20)[3], с использованием методов ионно-пучковой или плазменно-иммерсионной имплантации или осаждения ионов с целью изменения поверхностных свойств данных материалов для использования, в первую очередь, в качестве медицинских материалов. Поверхность, обработанная азотом, кислородом и углеродом, становиться биоинертной, что может быть достигнуто также после ионной имплантации других химических элементов, например, таких как кремний.
Недостатком известного способа является то, что в нем описаны методы плазменно-иммерсионной ионной имплантации и осаждения покрытий на медицинские конструкции из сплавов на основе никелида титана, основанные на ионно-пучковых и плазменных методах обработки поверхности, позволяющие получать тонкие покрытия, сравнительно небольшой толщины - не более 100 нм, которые обладают теми же недостатками известного источника [2].
Также в известном способе отмечено, как рекомендация, что кремний может быть использован для создания биоинертной поверхности имплантата. Однако не приведены какие-либо данные о химическом составе в поверхностном слое, в том числе о содержании атомов никеля и его изменении после ионно-пучковой или ионно-плазменной обработки сплава на основе никелида титана с использованием потоков ионов кремния.
Наиболее близким по технической сущности является способ получения материала на основе никелида титана с ЭПФ (RU 2191842, C22C 19/03, C23C 14/06, опубл. 27.10.2002)[4] с поверхностным слоем, модифицированным путем ионной имплантации легирующими элементами, в качестве которых выбраны кислород, углерод, титан и/или цирконий, имеет глубину модифицированного слоя 50-300 нм, а состав модифицированного слоя имеет следующее соотношение элементов, ат.%: кислород 25-75, углерод 5-10, титан и/или цирконий 20-50, никель 0-20. Кроме того, в качестве основы выбран никелид титана следующего состава, ат.%: никель 49-51, титан - остальное. Материал с такими элементами и при данной их концентрации в модифицированном слое имеет высокую коррозионную стойкость как в исходном состоянии, так и после многократных циклов деформирования в режиме нагрузка-разгрузка, а также низкую растворимость ионов никеля в агрессивных средах.
Недостатком известного способа является то, что материал на основе никелида титана с ЭПФ с поверхностным слоем, модифицированным путем ионной имплантации упомянутыми в изобретении легирующими элементами, хоть и обладает низкой растворимостью никеля в биохимических растворах, но этого фактора не достаточно для использования данного материала на основе никелида титана с ЭПФ для изготовления кардиоимплантатов, так как это не обеспечивает быструю интеграцию имплантата с организмом животного или человека путем создания на его поверхности органической пленки, изолирующей неорганический (металлический) материал от прямого контакта с кровью.
Задачей предлагаемого изобретения является разработка способа изготовления кардиоимплантата из сплава на основе никелида титана с модифицированным ионноплазменной обработкой поверхностным слоем. Полученный предлагаемым способом кардиоимплантат с модифицированным поверхностным слоем обладает биосовместимостью, коррозионной стойкостью и отсутствием токсичности.
Указанный технический результат достигается тем, что способ изготовления кардиоимплантата из сплава на основе никелида титана с модифицированным ионно-плазменнной обработкой поверхностным слоем включает ионную имплантацию легирующих элементов в поверхностный слой кардиоимплантата с флюенсом (0,5÷6,0)×1017 см-2, при этом сначала изготавливают кардиоимплантат, затем осуществляют химическую и электрохимическую очистку его поверхности, далее проводят обработку поверхности кардиоимплантата потоками ионов кремния, полученных путем распыления кремниевого катода в вакууме, в режиме высокодозовой ионной имплантации с получением поверхностного модифицированного слоя толщиной 80-95 нм, состоящего, по меньшей мере, из двух подслоев:
наружный подслой толщиной 20-25 нм содержит кислород, углерод, кремний и титан при следующем соотношении элементов, ат.%:
| кислород | 25-65 |
| углерод | 1-5 |
| кремний | 1-10 |
| титан | остальное; |
промежуточный подслой толщиной 60-70 нм содержит кислород, углерод, кремний, титан и никель при следующем соотношении элементов, ат.%:
| кислород | 5-30 |
| углерод | 1-5 |
| кремний | 10-30 |
| никель | 1-50 |
| титан | остальное, |
причем максимальную концентрацию кремний достигает на глубине 30-35 нм от поверхности.
Исходный сплав на основе никелида титана имеет следующий состав химических элементов, ат.%:
| Титан | 49.00-49.50 |
| Никель | 50.50-51.00. |
Исходный сплав на основе никелида титана имеет дополнительно примеси внедрения O, N, C и замещения Fe, Co до 0.2 ат.%.
Сплав на основе никелида титана имеет температуру завершения обратного мартенситного превращения (Ак) при его нагреве не более 23°C.
Сплав на основе никелида титана имеет величину обратимой неупругой деформации не менее 6%.
Кардиоимплантат для закупорки ушка левого предсердия выполнен в виде зонтичного устройства (далее по тексту зонтичное устройство).
Химическую очистку кардиоимплантата проводят в смеси азотной и плавиковой кислот при температуре 50°С.
Электрохимическую очистку кардиоимплантата проводят в смеси кислот CH3COOH (97%):HCIO4(70%), взятых в соотношении 3:1 об.ч.
Обработку поверхности кардиоимплантата потоками ионов кремния проводят при ускоряющем напряжении 40-80 кВ, при частоте следования импульсов 50-100 Гц в течение 5-60 минут.
Использование сплава на основе никелида титана, в частности, в диапазоне следующих составов, ат.%:
| титан | 49.00-49.50 |
| никель | 50.50-51.00 |
в сердечно-сосудистой хирургии в качестве материала для кардиоимплантатов связано с наличием у данного сплава ценных механических свойств, таких как термическая память формы, сверхэластичность. В частности, упомянутый двойной сплав на основе никелида титана может иметь дополнительно примеси внедрения O, N, C и замещения Fe, Co до 0.2 ат.%. Содержание такого небольшого количества указанных примесей не оказывает существенного влияния на его функциональные свойства. Используемый сплав на основе никелида титана имеет температуру завершения обратного мартенситного превращения (Ак) при его нагреве не более 23°C и величину обратимой неупругой деформации не менее 6%.
Указанные свойства сплава на основе никелида титана необходимы при изготовлении кардиоимплантатов определенных конструкций, требующих восстановления их формы при температуре человеческого тела, а также для их длительной работы в органах сердечно-сосудистой системы под нагрузкой (мышечное давление на конструкцию со стороны стенок сосудов).
Присутствие значительной доли атомов никеля в сплаве (50.50-51.00 ат.%) обуславливает необходимость создания барьерного слоя, препятствующего проникновению ионов никеля в биосреду (ткани и жидкости - кровь, лимфа крови) в результате коррозионных процессов, протекающих на поверхности кардиоимплантата из сплава на основе никелида титана при контакте с биологическими тканями и жидкостями и сопровождающихся выделением ионов никеля. Увеличение концентрации атомов никеля в тканях выше допустимого уровня способствует ухудшению биологической совместимости имплантата, оказывает на организм токсическое и аллергическое воздействие, может приводить к возникновению воспалительных процессов.
Известно, что модификация поверхности кардиоимплантатов из сплавов на основе никелида титана может приводить к изменению механических характеристик поверхностных слоев сплавов.
Несмотря на значительное количество [1-4] опубликованных экспериментальных данных, проблема поиска оптимальных методов обработки поверхности кардиоимплантатов из сплава на основе никелида титана с ЭПФ до сих пор не решена.
Настоящим изобретением предложен способ изготовления кардиоимплантата из сплава на основе никелида титана с модифицированным ионно-плазменнной обработкой поверхностным слоем.
Кардиоимплантат в частном исполнении представляет собой зонтичное устройство и может быть изготовлен из трубки сплава на основе никелида титана с помощью лазерной резки и формующих шаблонов; таким образом, получают каркасную заготовку зонтичного устройства.
Затем проводят химическую и электрохимическую очистку каркасной заготовки зонтичного устройства, которая заключается в удалении дефектов лазерной резки типа наплывов, брызг и уменьшении толщины оксидной пленки.
Выбор кремния как химического элемента для легирования поверхностных слоев сплава на основе никелида титана позволит решить некоторые из перечисленных проблем благодаря его химическим (электронный аналог углерода), физическим (частично растворяется в решетке титана с образованием ограниченного твердого раствора замещения и образует биоинертные, нерастворимые фазы на основе титана, никеля и кремния, которые могут являться основой для синтеза композиционной металлокерамики на основе титана и кремния) и биологическим (высокая совместимость с живыми клетками) свойствам.
Ионно-плазменная обработка поверхности кардиоимплантата потоками ионов кремния сопровождается распылением поверхностного слоя, его текстурированием и понижением класса шероховатости, что повышает возможность клеток прикрепиться к поверхности кардиоимплантата, а развитый поверхностный ландшафт становится естественным резервуаром внеклеточного матрикса, то есть питательной среды, которая всегда окружает живую клетку.
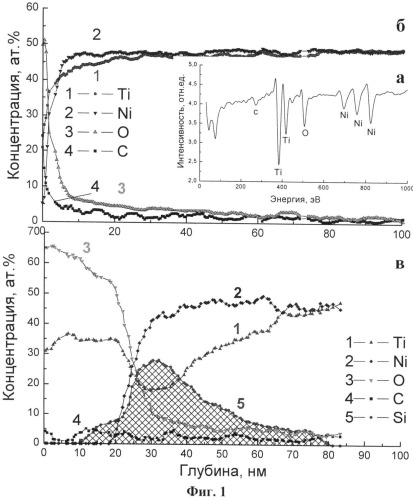
Проведенные эксперименты по модификации поверхностного слоя кардиоимплантата из сплава на основе никелида титана путем обработки поверхности кардиоимплантата потоками ионов кремния, полученных путем распыления кремниевого катода в вакууме, в режиме высокодозовой ионной имплантации с флюенсом (D), равным (0,5 -6,0)х1017 см-2 показывают, что в поверхностном слое толщиной 80-95 нм формируется кремнийсодержащий слой, максимальная концентрация атомов кремния в котором достигает 30 ат.% на глубине 30-35 нм (см. фиг 1).
Заявленный интервал флюенса обеспечивает требуемую, заранее заданную концентрацию атомов добавляемых (легирующих) химических элементов - кремния, кислорода и углерода, их распределение по глубине модифицированного поверхностного слоя в процессе ионной обработки, а также толщину модифицированного слоя (см. фиг 1).
Необходимые для достижения технического результата величины флюенса в заявленных пределах получают варьированием параметрами ионно-плазменной обработки, а именно ускоряющим напряжением 40 - 80 кВ, частотой следования импульсов 50-100 Гц и временем обработки 5-60 минут. В настоящем изобретении в разделе осуществления изобретения приведен один пример достижения необходимой заявленной величины флюенса. На основе профессиональных знаний в области ионно-плазменной обработки специалист в состоянии получить и другие величины флюенса в заявленных пределах, варьируя вышеизложенными технологическими параметрами обработки.
На фиг.1 представлены Ожэ-спектр, соответствующий составу исходного образца в слое на глубине ~10 нм (а), профили распределения концентрации основных элементов в поверхностных слоях сплава TiNi перед (б) и после ионной модификации кремнием (в).
В условиях ионной имплантации происходит перераспределение концентрации элементов в поверхностном слое кардиоимплантата из сплава на основе никелида титана, приводящее к существенному уменьшению содержания никеля в наружном подслое толщиной от 20 до 35 нм вплоть до их полного отсутствия на глубину до 20 нм от поверхности кардиоимплантата.
В результате ионно-плазменного воздействия поверхностный слой кардиоимплантата из сплава на основе никелида титана фрагментируется на глубину более 15 мкм с образованием зеренно-субзеренной структуры с размерами субзерен в диапазоне значений от 100 нм до 1000 нм. Измельчение зеренной структуры в поверхностной области кардиоимплантата из сплава на основе никелида титана приводит к повышению коррозионной стойкости поверхностного слоя в биосреде за счет существенного увеличения концентрации межзеренных границ и активизации в их окрестности окислительных реакций по отношению к титану, быстрому образованию оксидной пленки на основе титана и, как следствие, значительному повышению потенциала перепассивации Епп.
Таким образом, в процессе воздействия ионами кремния на поверхность кардиоимплантата из сплава на основе никелида титана, которая осуществлялась в ионно-плазменной установке, происходит модификация поверхностной области кардиоимплантата в виде формирования поверхностного слоя, состоящего как минимум из двух подслоев, которые существенно различаются соотношением концентраций кислорода, углерода, никеля и кремния. Модифицированный поверхностный слой с измененным составом не обладает выраженной поверхностью раздела между подслоями, характерной для осажденного слоя (см. фиг.1).
На фиг.1 представлены концентрационные профили распределения основных химических элементов в поверхностных слоях кардиоимплантата из сплава никелида титана. Видно, что максимальное на поверхности содержание кислорода и углерода, 50 ат.% и 20 ат.%, соответственно, понижается по экспоненциальной зависимости в довольно узком наружном слое и уже на глубине 10-20 нм не превышает 5 ат.% каждый. Распределение внедренных ионов кремния описывается кривой с максимумом концентрации кремния 30 ат.%, расположенным в приповерхностной области, как уже было выше отмечено, на глубине 30-35 нм от поверхности.
Наличие углерода в модифицированном слое обусловлено существованием адсорбированного углерода на исходной поверхности кардиоимплантата, на поверхности распыляемого материала (катода из кремния), а также присутствием углерода в остаточной атмосфере технического вакуума, который (углерод) по механизмам атомного перемешивания и диффузии проникает в более глубокие слои обрабатываемого сплава на основе никелида титана.
После ионной модификации увеличилась концентрация кислорода в поверхностном слое, а толщина этого слоя в 2 раза превысила толщину оксидного слоя у кардиоимплантата до ионной обработки. Это связано с тем, что в процессе ионной имплантации помимо атомов основного имплантируемого химического элемента (кремний), как правило, в ионном пучке имеются такие элементы, как кислород, углерод, присутствующие как в остаточной атмосфере рабочей камеры, так и адсорбированные на поверхности облучаемого кардиоимплантата. В процессе ионно-пучкового воздействия, вследствие атомного перемешивания поверхностных и внутренних слоев, а также в результате радиационно-стимулированной диффузии, ионы этих элементов попадают в поверхностный слой и распределяются в нем, участвуя в формировании модифицированного поверхностного слоя.
Особого внимания заслуживают особенности перераспределения атомов никеля в поверхностном модифицированном слое. Из фиг.1 видно, что во внешнем (наружном) подслое толщиной 20 нм атомы никеля практически отсутствуют, затем наблюдается повышение их концентрации до величины, соответствующей его исходной концентрации в сплаве на глубине 80-95 нм от облученной поверхности.
Из результатов коррозионных испытаний следует, что потенциал перепассивации Епп сплава на основе никелида титана в биохимических водных растворах 0.9% NaCl, плазмы крови после модификации поверхности кардиоимплантата в среднем составляет 0.9 В в отличие от его значения Епп≈0.1 В, полученного при испытаниях кардиоимплантата с немодифицированной поверхностью. Повышение коррозионной стойкости поверхности кардиоимплантата из сплава на основе никелида титана с модифицированным ионами кремния поверхностным слоем обусловлено изменением химического состава в поверхностном слое кардиоимплантата после обработки ионным пучком кремния, в результате которой на поверхности кардиоимплантата образовались, как минимум, два высококоррозионностойких к биорастворам подслоя, расположенных один под другим: первый - наружный - на основе окси-карбидов титана (подслой на основе титана, кислорода и углерода); и второй - промежуточный - на основе силицидов титана и никеля; а также тем, что, во-первых, кремний в составе поверхностного слоя не участвует в окислительно-восстановительных процессах и при pH 7.3 не образует растворимых форм, во-вторых, изменение структурного состояния, а именно фрагментация и наноструктурирование приповерхностного слоя, ускоряет процесс перепассивации при коррозионных испытаниях с образованием дополнительного защитного пассивирующего слоя на поверхности кардиоимплантата. В результате потенциостатической выдержки в биохимических растворах при значении анодного потенциала Е, превышающем значение стационарного потенциала Ест для сплава на основе никелида титана, возможно образование малорастворимого соединения Ni2SiO4, что может являться одной из причин стабилизации пассивного состояния поверхностного слоя кардиоимплантата в области положительных потенциалов, повышающего его коррозионную устойчивость.
Из результатов испытаний in vitro на биосовместимость с живыми клетками (были использованы мезенхимальные стволовые клетки (МСК) костного мозга крысы) кардиоимплантата из сплава на основе никелида титана с немодифицированным и модифицированным (кремнием) поверхностным слоем получено, что эффективность пролиферации клеток МСК на поверхности кардиоимплантата после ионной модификации оказалась в ~1,3 раза выше, чем на поверхности кардиоимплантата, которая не подвергалась ионно-пучковой обработке кремнием. Это означает, что после модификации пучками ионов кремния биосовместимость кардиоимплантата повысилась. Повышение эффективности пролиферации МСК клеток обусловлено отмеченными выше физико-химическими свойствами наружного слоя, сформированного при ионно-пучковом воздействии, которые привели к повышению пассивируемости, высокой коррозионной стойкости и биоинертности кардиоимплантата с модифицированным поверхностным слоем.
Изобретение осуществляют следующим образом.
Из трубки сплава на основе никелида титана диаметром 3 мм с помощью аппарата лазерной резки (дискового лазера с диодной накачкой) по специально заданной программе в стенках трубки вырезают отверстия и разрезы нужной геометрии для получения каркасной заготовки.
Осуществляют химическую очистку каркасной заготовки, которая необходима для удаления дефектов лазерной резки типа наплывов, брызг и уменьшения толщины оксидной пленки. Для этого каркасную заготовку обрабатывают смесью азотной и плавиковой кислот при температуре 50°C в течении 5-7 секунд. Проводят мойку каркасной заготовки в ультразвуковой ванне в дистиллированной воде.
Далее каркасной заготовке с помощью формующих шаблонов придают необходимую объемную форму зонтичного устройства. Для этого предварительно охлажденную каркасную заготовку натягивают на охлажденный внутренний формующий шаблон и зажимают охлажденным внешним формующим шаблоном. Операцию выполняют при температуре от минус 15 до плюс 5°C.Зажатую заготовку вместе с формующими шаблонами помещают в расплав смеси неорганических солей при температуре 450-475°C на 15 минут. Проводят закалку заготовки в воду комнатной температуры, и затем объемную заготовку зонтичного устройства (далее в примере кардиоимплантат) освобождают от внешнего шаблона и снимают с внутреннего шаблона.
Далее кардиоимплантат подвергают электрохимической очистке в смеси CH3COOH (97%):HCIO4(70%), взятых в соотношении 3:1 об.ч., при температуре электролита 0°C, время обработки 10-15 секунд при напряжении 30 В. После электрохимической очистки кардиоимплантат промывают в дистиллированной воде в ультразвуковой ванне. Промытый кардиоимплантат подвергают сушке.
Далее проводят обработку поверхности кардиоимплантата ускоренными ионами кремния в вакууме ионно-плазменной установки (далее в примере установка).
Для этого подлежащие обработке аналогичные кардиоимплантаты закрепляют в держателях системы позиционирования, рабочего стола установки. Система позиционирования обеспечивает равномерную обработку внешней и внутренней поверхностей одновременно нескольких (до 10 штук) кардиоимплантатов потоком ионов кремния. Рабочий стол перемещают в рабочую камеру установки. Камеру откачивают до давления не меньше 3·10-3 Па (2·10-5 торр) для уменьшения содержания атомов примеси (кислорода, углерода) в остаточной атмосфере до минимальной их концентрации.
Включают систему прогрева-охлаждения рабочей камеры. Камера должна прогреться до температуры 30-35°C.Устанавливают ускоряющее напряжение 60 кВ, напряжение смещения 1000 В, частоту следования импульсов 50 Гц, включают импульсный ускоритель ионов кремния и систему позиционирования. Ионную модификацию поверхностей кардиоимплантатов проводят с применением импульсных однокомпонентных пучков ионов кремния в условиях безмасляной откачки и высокого вакуума, в режиме высокодозовой ионной имплантации с флюенсом, равным 2×1017 см-2. Обработку ведут в течение от 15 мин. В процессе обработки обеспечивают вращение каждого кардиоимплантата по заданной траектории для достижения равномерного распределения дозы облучения по поверхности обрабатываемого кардиоимплантата. Для выгрузки обработанных кардиоимплантатов в камеру установки напускают воздух, выкатывают стол и вынимают обработанные кардиоимплантаты из держателей. Предложенная ионно-плазменная обработка обеспечивает заявленные свойства модифицированного поверхностного слоя кардиоимплантата.
1. Способ изготовления кардиоимплантата из сплава на основе никелида титана с модифицированным ионно-плазменнной обработкой поверхностным слоем, включающий ионную имплантацию легирующих элементов в поверхностный слой кардиоимплантата с флюенсом (0,5÷6,0)×1017 см-2, отличающийся тем, что сначала изготавливают кардиоимплантат, затем осуществляют химическую и электрохимическую очистку его поверхности, далее проводят обработку поверхности кардиоимплантата потоками ионов кремния, полученных путем распыления кремниевого катода в вакууме, в режиме высокодозовой ионной имплантации с получением поверхностного модифицированного слоя толщиной 80-95 нм, состоящего, по меньшей мере, из двух подслоев:наружный подслой толщиной 20-25 нм содержит кислород, углерод, кремний и титан при следующем соотношении элементов, ат.%:
| кислород | 25-65 |
| углерод | 1-5 |
| кремний | 1-10 |
| титан | остальное; |
| кислород | 5-30 |
| углерод | 1-5 |
| кремний | 10-30 |
| никель | 1-50 |
| титан | остальное, |
2. Способ по п.1, отличающийся тем, что исходный двойной сплав на основе никелида титана имеет следующий состав химических элементов, ат.%:
| Титан | 49.00-49.50 |
| Никель | 50.50-51.00. |
3. Способ по п.2, отличающийся тем, что исходный двойной сплав на основе никелида титана имеет дополнительно примеси внедрения O, N, C и замещения Fe, Co до 0.2 ат.%.
4. Способ по любому из пп.2 или 3, отличающийся тем, что двойной сплав на основе никелида титана имеет температуру завершения обратного мартенситного превращения при его нагреве не более 23°C
5. Способ по любому из пп.2 или 3, отличающийся тем, что двойной сплав на основе никелида титана имеет величину обратимой неупругой деформации не менее 6%.
6. Способ по п.1, отличающийся тем, что кардиоимплантат для закупорки ушка левого предсердия выполнен в виде зонтичного устройства.
7. Способ по любому из пп.1 или 6, отличающийся тем, что химическую очистку кардиоимплантата проводят в смеси азотной и плавиковой кислот при температуре 50°C.
8. Способ по любому из пп.1 или 6, отличающийся тем, что электрохимическую очистку кардиоимплантата проводят в смеси кислот CH3COOH (97%) : HCIO4 (70%), взятых в соотношении 3:1 об.ч.
9. Способ по любому из пп.1 или 6, отличающийся тем, что обработку поверхности кардиоимплантата потоками ионов кремния проводят при ускоряющем напряжении 40-80 кВ, при частоте следования импульсов 50-100 Гц в течение 5-60 минут.