Способ определения индивидуальной чувствительности человека к оксидативному стрессу
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к внутренним болезням. Для определения индивидуальной чувствительности человека к оксидативному стрессу в суспензии нейтрофилов периферической крови конкретного индивидуума регистрируют интенсивность исходной хемилюминесценции (ИХ) и хемилюминесценции (НХ) после их нагревания в пробирках на водяной бане в течение 30-60 секунд при температуре 42°C путем подсчета числа импульсов в минуту. При значении ИХ/НХ менее 3 исследуемого относят к стрессочувствительным. Использование способа повышает эффективность лечения различных патологий в клиниках, способствует своевременному проведению профилактических и реабилитационных мероприятий с предотвращением трудопотерь и отбирает стрессоустойчивых лиц для успешного выполнения наиболее опасных производственных работ. 1 з.п. ф-лы, 5 табл., 5 ил., 3 пр.
Реферат
Изобретение относится к области медицины, более конкретно к разделу внутренних болезней.
В настоящее время большинство исследователей уделяют внимание реализации стресс-реакции на уровне отдельных клеток, способных продуцировать повреждающие организм активные формы кислорода (АФК). К АФК относят атомы кислорода, несущие на внешней оболочке лишний электрон и в связи с чем имеющие отрицательный заряд: супероксид анион ( O 2 − ), гидроксильный радикал (OH-), а также радикал диоксида азота(NO2), перекись водорода (H2O2) и др. Избыточные концентрации АФК повреждают в организме белки, липиды и ДНК, приводя к старению клеток и возникновению так называемых свободно-радикальных заболеваний таких как атеросклероз, эссенциальная гипертония, сенильная деменция типа Альцгеймера, болезнь Паркинсона, рак и др.
Раннее выявление чувствительности индивида к оксидативному стрессу позволит своевременно начать профилактические мероприятия, направленные на предупреждение развития указанных выше заболеваний.
В свою очередь эти заболевания являются для организма стрессорами и еще в большей степени усиливают клеточный оксидативный или окислительный стресс с дальнейшей аггравацией патологического процесса (B. Uttara et al. Oxidative Stress and Neurodegenerative Diseases: A Review of Upstream and Downstream Antioxidant Therapeutic Options. Curr. Neuropharmacology.2009, 7 (1): 65-74).
Как показывают клинические и экспериментальные данные, чувствительность организма к повреждающим стрессорам внешней среды во многом зависит от функции мозгового и коркового слоев надпочечников, находящихся под контролем гипоталамо-гипофизарной системы.
Болезнь Аддисона-Бирмена с недостаточностью функции надпочечников у человека сопровождается весьма высокой чувствительностью к различным стрессорам, включая ряд инфекций, и может реализоваться на уровне фагоцитарных клеток с усилением синтеза АФК. Подобная картина наблюдается у адреналэктомированных животных.
Известен способ оценки уровней психоэмоционального стресса (К.В. Судаков «Социальные и биологические аспекты психоэмоционального стресса: пути защиты от его нежелательных последствий», Вестник международной академии наук, 2006, №1, стр.8-14). Он включает приборную регистрацию наиболее информативных физиологических показателей (частоту сердечных сокращений, частоту дыхания, величины систолического и диастолического кровяного давления, показатели электромиограммы, кожно-гальванической реакции и др.). В представленном способе оценки уровней психоэмоционального стресса не учитывается оксидативный клеточный стресс, приводящий к развитию вышеуказанных патологий у человека.
В качестве прототипа нами выбран способ определения индивидуальной чувствительности к гипербарической оксигенации (авторское свидетельство SU №1246935). Указанный способ включает воздействие на лимфоциты периферической крови человека повышенным парциальным давлением кислорода или гипербарической оксигенацией. Повышенное давление кислорода является для клеток нефизиологическим фактором или стрессором. В результате действия подобного стрессора в лимфоцитах конкретного индивидуума происходят морфологические изменения хромосом (аберрации, делеции), которые отражают индивидуальную чувствительность к стрессу. Прототип обладает следующими недостатками:
- сложностью, поскольку предполагает культивирование лимфоцитов, использование аппаратуры для создания повышенного давления кислорода, оценку изменений структуры хромосом лимфоцитов;
- недостаточной точностью определения индивидуальной чувствительности к стрессовому воздействию, так как лимфоциты не обладают фагоцитарной активностью, не продуцируют экзогенные формы АФК и не могут участвовать непосредственно в развитии оксидативного стресса.
Нами поставлена задача: разработать простой достоверный способ определения индивидуальной чувствительности человека к оксидативному стрессу.
Технический результат заключается в обеспечении простоты и точности определения чувствительности человека к оксидативному стрессу за счет оценки продукции АФК нейтрофилами в реакции хемилюминесценции.
Нами установлено, что регистрация и сравнение интенсивности хемилюминесценции, например, индуцированной опсонизированным зимозаном люминолзависимой хемилюминесценции стрессированных и нестрессированных нейтрофилов периферической крови конкретного индивидуума с оценкой величины коэффициента хемилюминесценции, т.е. соотношения числа импульсов в минуту нестрессированных нейтрофилов к числу импульсов в минуту стрессированных нейтрофилов, позволяет достоверно определять чувствительность исследуемого к оксидативному стрессу.
Сущность изобретения состоит в следующем.
Для определения индивидуальной чувствительности человека к оксидативному стрессу получают суспензию нейтрофилов периферической крови. Регистрируют интенсивности исходной хемилюминесценции (ИХ) нейтрофилов и хемилюминесценции (НХ) после нагревания суспензии нейтрофилов в течение 30-60 секунд при температуре 42°C путем подсчета числа импульсов в минуту. При значении ИХ/НХ менее 3 выявляют чувствительность исследуемого к оксидативному стрессу.
При этом действие на нейтрофилы теплового шока в указанном режиме их нагревания сопровождается продукцией АФК, оценка которой в реакции хемилюминисценции путем подсчета импульсов в минуту позволяет достоверно определить чувствительность к оксидативному стрессу.
В частном случае регистрируют индуцированную опсонизированным зимозаном люминолзависимую хенмилюминесценцию.
Способ осуществляется следующим образом.
Популяцию нейтрофилов получают центрифугированием периферической крови пациентов на двойном градиенте плотности фиколлверографина (плотность нижнего раствора 1.119 г/см3, верхнего раствора - 1.077 г/см3) в течение 40 минут, скорость центрифугирования 400×g. Нейтрофилы удаляют микропипеткой из нижнего интерфазного слоя и отмывают 2 раза физиологическим раствором с последующей ресуспензией в бесцветном растворе Хенкса и подсчетом количества ядерных клеток в суспензии. Суспензия полученных нейтрофилов имеет чистоту 96-98%. Реакцию хемилюминесценции проводят в пластиковых пробирках, которые содержат 20 микролитров бесцветного Хенкса и 150 микролитров люминола (5-амино-2,3-дигидро-1,4-фталазинедион), например, фирмы Serva (Германия) в концентрации 2,5 мкг/мл. Пробирки помещают в барабан хемилюминометра и термостатируют в течение одного часа для достижения температуры 37°C, затем добавляют 100 микролитров суспензии нейтрофилов (2×105 ядерных клеток) и спустя один час стимулируют нейтрофилы опсонизированным зимозаном. Например, фирмы Sigma (США) в объеме 100 микролитров и в концентрации 20 мг/мл. Учитывают индуцированную хемилюминесценцию и динамику продукции активных форм кислорода нейтрофилами в течение 30 минут, с оценкой количества импульсов в минуту. Для стрессирования нейтрофилов применяют тепловой шок - нагревание клеток в пробирках на водяной бане при 42°C в течение 30-60 секунд, т.е. краткосрочный стресс с последующим введением стрессированных и нестрессированных нейтрофилов в реакцию хемилюминесценции.
Математический анализ для сравнения исходной хемилюминесценции и показателей хемилюминесценции нейтрофилов после теплового шока продолжительностью 30 сек., 1 мин. и 3 мин. проводили с использованием биномиального распределения: P ( r ) = C n r p r ( 1 − p ) n − r , где n - число опытов, p - вероятность успеха, r - число успешных опытов,. C n r - число сочетаний из n по r, P(r) - вероятность наблюдать r успехов в n опытах при вероятности успеха P.
Оценка вероятности успеха получается путем максимилизации вероятности наблюдать r успехов при n испытаниях
95% доверительный интервал для вероятности успеха определяется по точным формулам биномиального распределения, приведенным в виде номограмм в статистической литературе (Вентцель Е.С. «Теория вероятностей», 1969 г., «Наука»)
В качестве доказательств возможности реализации заявленного назначения и достижения указанного технического результата приводим следующие данные.
Приводим примеры определения динамики продукции активных форм кислорода в реакции индуцированной опсонизированным зимозаном хемилюминесценции нейтрофилами у 4 из 17 пациентов разного возраста после теплового шока (число импульсов/мин.) (Табл. 1-4).
Пациент М., 88 лет, ж., 31.05.11 (1 - нейтрофилы без шока, 2 - шок 30 сек., 3 - шок 1 мин., 4 - шок 3 мин.) (Таблица 1).
| Таблица 1 | |||||||
| Исходные | 1 мин | 2 мин | 4 мин | 8 мин | 10 мин | 12 мин | 14 мин |
| 1.2254 | 4010 | 7187 | 9149 | 9375 | 9306 | 8538 | 7331 |
| 2. 1007 | 1613 | 3543 | 5015 | 5170 | 5210 | 4720 | 4172 |
| 3. 1176 | 1871 | 4160 | 533,9 | 5685 | 5494 | 4784 | 4008 |
| 4. 347 | 429 | 1194 | 2073 | 2637 | 2454 | 2335 | 1892 |
Пациент X., 86 лет, м, 31.05.11 (1 - нейтрофилы без шока, 2 - шок 30 сек., 3 - шок 1 мин., 4 - шок 3 мин) (Таблица 2).
| Таблица 2 | |||||||
| Исходные | 1 мин | 2 мин | 4 мин | 8 мин | 10 мин | 12 мин | 14 мин |
| 1. 1993 | 2619 | 8536 | 13526 | 15690 | 15824 | 15427 | 14253 |
| 2. 366 | 488 | 1619 | 2941 | 3905 | 4666 | 4700 | 4463 |
| 3.204 | 272 | 729 | 1308 | 1641 | 1828 | 1854 | 1913 |
| 4. 216 | 176 | 416 | 770 | 1036 | 1207 | 1080 | 1146 |
Пациент Ф, 93 года, ж, 23.05.11 (1 - нейтрофилы без шока, 2 - шок 30 сек., 3 - шок 1 мин., 4 - шок 3 мин) (Таблица 3)..
| Таблица 3 | |||||
| Исходные | 2 мин | 4 мин | 6 мин | 10 мин | 12 мин |
| 1. 1022 | 11068 | 14961 | 14825 | 11594 | 8721 |
| 2. 316 | 2965 | 5234 | 5194 | 4562 | 3701 |
| 3. 259 | 2026 | 3845 | 4041 | 3946 | 3133 |
| 4. 131 | 1284 | 2754 | 2801 | 2603 | 1986 |
Пациент В, 26 лет, ж, 23.05.11 (1 - нейтрофилы без шока, 2 - шок 30 сек., 3 - шок 1 мин., 4 - шок 3 мин) (Таблица 4).
| Таблица 4 | |||||
| Исходные | 2 мин | 4 мин | 6 мин | 10 мин | 12 мин |
| 1. 1589 | 8289 | 18524 | 18271 | 16828 | 12784 |
| 2. 343 | 1800 | 3700 | 3953 | 3883 | 2884 |
| 3. 588 | 2767 | 6940 | 6980 | 7063 | 5280 |
| 4. 787 | 2781 | 7120 | 7000 | 7400 | 6107 |
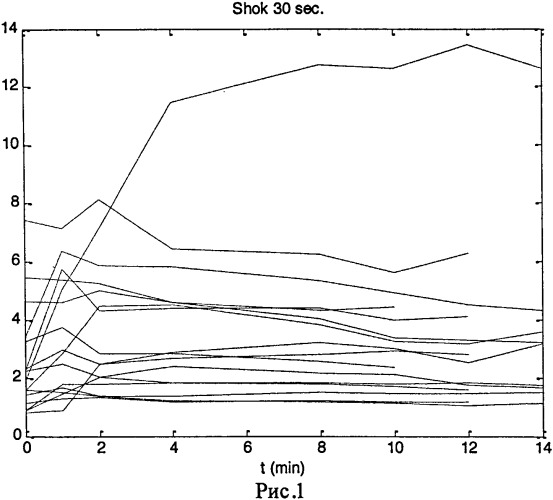
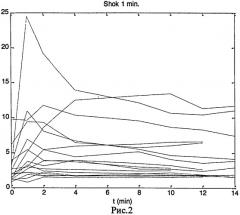
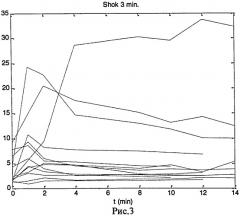
На рисунках 1-3 приведены кривые динамики отношения интенсивности исходной хемилюминесценции нейтрофилов к интенсивности хемилюминесценции нейтрофилов после теплового шока различной длительности для 17 пациентов разного возраста. Вычисляли вероятность того, что отношение интенсивности исходной хемилюминесценции к интенсивности хемилюминесценции после теплового шока достигает максимума в пределах первых 3 минут. Например, по данным хемилюминесценции после теплового шока длительностью 30 секунд, представленным на рис.1, вероятность того, что максимум отношения наступает ранее 3 минут равна 14/17=0.82 при 95% доверительном интервале от 0.59 до 0.84. Результаты расчета для длительности теплового шока 30 сек., 1 мин., 3 мин. представлены в таблице 5.
| Таблица 5 | |||
| Время теплового шока | Вероятность проявления максимальной чувствительности | Нижнее значение 95% доверительного интервала | Верхнее значение 95% доверительного интервала |
| в первые 3 мин | |||
| 30 секунд | 0.82 | 0.59 | 0.84 |
| 1 минута | 0.89 | 0.62 | 0.99 |
| 3 минуты | 0.71 | 0.45 | 0.88 |
Как видно из таблицы большие значения доверительного интервала зарегистрированы при продолжительности теплового шока 30 сек. и 1 мин. Статистически значимое увеличение коэффициента хемилюминесценции нейтрофилов (по оси ординат) для 3 типов стресса зарегистрировано в первую минуту после действия стрессора, что указывает на необходимость определения индивидуальной чувствительности к оксидативному стрессу именно в этот промежуток времени.
Клинические примеры изменения чувствительности пациентов к оксидативному стрессу в результате лечения.
1. Пациентка Р., 84 года
Диагноз: гипертоническая болезнь 3 стадии, ишемическая болезнь сердца (ИБС), кардиосклероз, пневмосклероз, нефроангиосклероз. До госпитализации коэффициент хемилюминесценции нейтрофилов составил 1,75: 7616 импульсов (исходная хемилюминесценция) и 4338 импульсов (после стресса). Через 2 недели лечения амлодипином, предукталом, аспирином, каптоприлом, поливитаминами, преднизолоном коэффициент хемилюминесценции составил 4,56 при исходной хемилюминесценции нейтрофилов 406 импульсов и после действия теплового шока 89 импульсов, т.е. коэффициент увеличился в 2,6 раза.
2. Пациент О., 92 года. Диагноз: перелом шейки бедра. До лечения коэффициент хемилюминесценции составил 2,84 от соотношения исходной хемилюминесценции нейтрофилов 68621 импульс к хемилюминисценции после стресса 24146 импульсов. После лечения 7 сеансами низкоинтенсивной лазерной терапии коэффициент хемилюминесценции равнялся 3,75 от соотношения исходной хемилюминесценции 6484 импульса к хемилюминесценции нейтрофилов после стресса 1725 импульсов, то есть увеличился в 1,3 раза. Низкоинтенсивная лазерная терапия снижает воспаление и синтез АФК фагоцитами.
3. Пациентка В., 98 лет. Диагноз: ИБС, гипофункция щитовидной железы, кахексия. До лечения коэффициент хемилюминесценции составил 0,89 от соотношения исходной хемилюминесценции нейтрофилов 6961 импульс к хемилюминесценции после теплового шока 7741 импульс. Лечение тироксином, аспирином, комплексом витаминов В1, В6, В12, рибоксином, пирацетамом, предукталом в течение 2 недель привело к увеличению коэффициента до 13,8.
Эти примеры показывают, что госпитализация и адекватное лечение заболеваний у пациентов приводят к уменьшению чувствительности к оксидативному стрессу вследствие уменьшения проявлений патологических состояний как стрессоров, а также уменьшения продукции активных форм кислорода фагоцитирующими клетками по причине активации антистрессорных генов антивоспалительными или антиоксидантными свойствами лекарств.
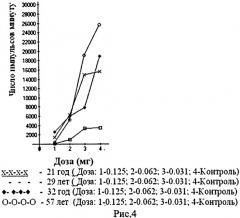
На рисунках 4 и 5 демонстрируется зависимость числа импульсов в минуту (продукция АФК) в нейтрофилах от возраста и дозы (мг) аспирина и индометацина, обладающих стимулирующим действием на антистрессорные гены клеток, антивоспалительным и антиоксидантным эффектами. Уменьшение продукции АФК нейтрофилами у пациентов разного возраста пропорционально дозе используемых препаратов (доза-эффект).
Определяя чувствительность людей к оксидативному стрессу, можно повысить эффективность лечения различных патологий в клиниках, своевременно проводить профилактические и реабилитационные мероприятия с предотвращением трудопотери и отбирать стрессоустойчивых лиц для успешного выполнения наиболее опасных производственных работ.
1. Способ определения индивидуальной чувствительности человека к оксидативному стрессу, отличающийся тем, что получают суспензию нейтрофилов периферической крови, регистрируют интенсивности исходной хемилюминесценции (ИХ) нейтрофилов и хемилюминесценции (НХ) после их нагревания в пробирках на водяной бане в течение 30-60 с при температуре 42°C, путем подсчета числа импульсов в минуту, и при значении ИХ/НХ менее 3 относят исследуемого к стрессочувствительным.
2. Способ по п.1, отличающийся тем, что регистрируют индуцированную опсонизированным зимозаном люминолзависимую хемилюминесценцию.