Пролекарства нестероидных противовоспалительных средств (nsaia) c очень высокой скоростью проникновения через кожу и мембраны и новые медицинские применения указанных пролекарств
Иллюстрации
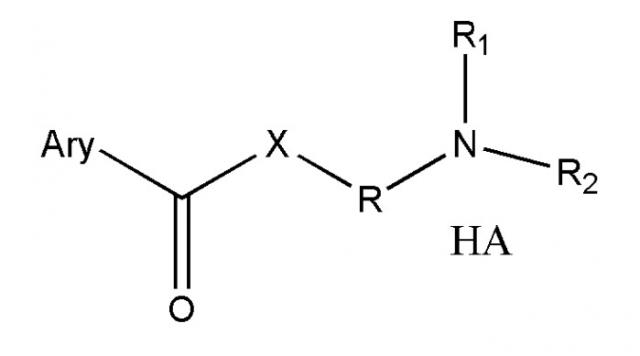
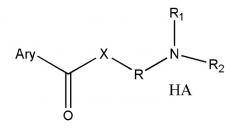
Показать всеИзобретение относится к новым положительно заряженным пролекарствам NSAIA общей формулы (1, 2a, 2b, 2c или 2d) «структуры 1, 2a, 2b, 2c или 2d»
Значение радикалов R, R1, R2, R3, R4, R5, Ary, X представлены в пп.1, 2 формулы. 6 н. и 16 з.п. ф-лы, 14 табл.
Реферат
Область техники
Настоящее изобретение относится к разработке и получению положительно заряженных и водорастворимых пролекарств нестероидных противовоспалительных средств (nonsteroidal anti-inflammatory agents, NSAIA) с очень высокой скоростью проникновения через кожу, для лечения шрамов и преодоления барьера кровь-молоко, гематоэнцефалического барьера и новым медицинским применениям указанных пролекарств для лечения и предотвращения диабета (I и II типа), аномальных уровней глюкозы и липидов в крови, удара, сердечного приступа и других сердечно-сосудистых заболеваний, болезни Альцгеймера, болезни Паркинсона и других нейродегенеративных заболеваний, псориаза, дискоидной красной волчанки, системной красной волчанки (SLE), аутоиммунного гепатита, склеродермии, синдрома Шегрена, ревматоидного артрита, полимиозита, склеродермии, тиреоидита Хашимото, ювенильного сахарного диабета, болезни Аддисона, витилиго, пернициозной анемии, гломерулонефрита и пневмофиброза, рассеянного склероза (MS), болезни Крона и других аутоиммунных заболеваний, бокового амиотрофического склероза (ALS), дистрофии мышц глазного яблока и глотки (OPMD), миотонической дистрофии (MD), мышечной дистрофии Дюшенна (DMD), полимиозита (PM), дерматомиозита (DM), миозита с включенными тельцами (IBM) и других мышечных нарушений, геморроя, воспаленного геморроя, постлучевого проктита, хронического неспецифического язвенного колита, криптита, других воспалительных состояний аноректума, анального зуда, простатита, простатоцистита, варикоза, аутоиммунного воспаления печени, аутоиммунного воспаления почек, воспаления толстой кишки, воспаления кишечника, воспалительных заболеваний вен, воспалительных заболеваний сосудов и других воспалений, раковых заболеваний кожи, рака молочной железы, рака толстой кишки, рака ротовой полости, рака легких и других органов дыхательной системы, рака матки, рака половых органов, раковых заболеваний органов мочевыделения, лейкемии и других раковых заболеваний крови и лимфатических тканей, и других видов раковых заболеваний, шрамов, патологических сосудистых поражений кожи, родимых пятен, родинок (невуса), папиллом, возрастных пятен (печеночных пятен) и других заболеваний кожи. Указанные пролекарства можно вводить трансдермально без помощи веществ, улучшающих проникновение через кожу.
Уровень техники
Нестероидные противовоспалительные средства (NSAIA) применяют для облегчения проявлений и симптомов ревматоидного артрита, остеоартрита и анкилозирующего спондилоартрита. NSAIA применяют отдельно или в качестве вспомогательных средств при лечении печеночных колик, лихорадки и боли при эпизиотомии. Указанные средства также применяют при лечении подагры, острой головной боли, связанной с мигренью, и почечных колик, а также при лечении послеоперационного воспаления у пациентов, которые подверглись удалению катаракты. Для предотвращения сердечных и сосудистых заболеваний применяют аспирин.
Тем не менее, применение NSAIA связано с рядом побочных эффектов, в частности желудочно-кишечных нарушений, таких как диспепсия, гастродуоденальное кровотечение, язва желудка и гастрит. Фишманом (Fishman; Robert, патент США 7052715) было показано, что дополнительная проблема, связанная с применением перорально вводимых лекарственных препаратов, состоит в том, что для эффективного лечения удаленных очагов боли или воспаления необходимо обеспечение значительных концентраций препарата в кровотоке. Указанные уровни концентрации часто намного превышают концентрации, которые были бы необходимы в случае, если бы существовала возможность точечного воздействия на конкретный очаг боли или повреждения. Фишманом и многими другими (Ван Энгеленом с соавторами (Van Engelen et al.), патент США 6416772; Макридсом с соавторами (Macrides et al.), патент США 6346278; Кирби с соавторами (Kirby et al.), патент США 6444234, Пирсоном с соавторами (Pearson et al.), патент США 6528040, и Боткнехтом с соавторами (Botknecht et al.), патент США 5885597) предпринимались попытки создания системы доставки для трансдермального применения путем разработки конкретных составов. Зонг с соавторами (Song et al.) разработали трансдермальную систему доставки лекарственного средства для доставки противовоспалительного болеутоляющего препарата, содержащего диэтиламмониевую соль диклофенака (Song, et al., патент США 6723337). Донати с соавторами (Donati et al.) разработали пластырь для местного применения, содержащий гепарин и диклофенак (Donati, et al., патент США 6592891). Кавайи с соавторами (Kawaji et al.) разработали маслосодержащий пластырь-повязку для наружного применения, содержащий диклофенак натрия (Kawaji et al., патент США 6262121). Эффринг с соавторами (Effing et al.) разработали устройство для трансдермальной доставки диклофенака (Effing et al., патент США 6193996). Однако доставка терапевтически эффективных количеств NSAIA в плазму хозяина за счет обеспечения подходящих составов является очень непростой задачей. Сьюзан Милосович с соавторами (Susan Milosovich et al.) разработали и синтезировали тестостеронил-4-диметиламинобутират.HCl (TSBH), содержащий липофильную часть и третичные аминогруппы, который существует в протонированной форме при физиологических значениях pH. Они обнаружили, что указанное пролекарство (TSBH) диффундирует через кожу человека примерно в 60 раз быстрее, чем сам лекарственный препарат (TS) [Susan Milosovich et al., J. Pharm. Sci., 82, 227(1993)].
Раскрытие изобретения
Техническая задача
NSAIA применяют в медицинских целях в течение более 100 лет. NSAIA показаны к применению для облегчения проявлений и симптомов ревматоидного артрита и остеоартрита, облегчения слабой или средней боли, облегчения лихорадки и лечения дисменореи. Указанные лекарственные препараты являются наиболее широко применяемыми лекарствами в мире.
Тем не менее, применение NSAIA связано с рядом побочных эффектов, в частности желудочно-кишечных нарушений, таких как диспепсия, изжога, рвота, гастродуоденальное кровотечение, язва желудка и гастрит. Гастродуоденальное кровотечение, вызываемое NSAIA, в целом является безболезненным, но может приводить к потере крови с калом и вызывать устойчивую железодефицитную анемию.
Трансдермальные системы доставки помогают избежать непосредственного повреждения желудочно-кишечного тракта и инактивирования лекарственных препаратов, обусловленного “пресистемным метаболизмом” в желудочно-кишечном тракте и печени. Традиционная трансдермальная доставка лекарственного препарата с применением вещества, улучшающего проникновение через кожу, имеет свои ограничения. Во-первых, скорости проникновения являются очень низкими (по шкале мкг/см2/ч). Во-вторых, в тело хозяина будут поступать большие количества вещества, улучшающего проникновение через кожу.
Техническое решение
Трансдермальные системы доставки помогают избежать непосредственного повреждения желудочно-кишечного тракта и инактивирования лекарственных препаратов, обусловленного “пресистемным метаболизмом” в желудочно-кишечном тракте и печени. Традиционная трансдермальная доставка лекарственного препарата с применением вещества, улучшающего проникновение через кожу, имеет свои ограничения. Во-первых, скорости проникновения являются очень низкими (по шкале мкг/см2/ч). Во-вторых, большие количества вещества, улучшающего проникновение через кожу, будут поступать в тело хозяина и могут вызывать дополнительные побочные эффекты. В-третьих, при традиционной трансдермальной доставке лекарственного препарата с применением веществ, улучшающих проникновение через кожу, указанные вещества, содержащиеся в составе в высоких концентрациях, могут способствовать проникновению лекарственного препарата через кожу. Однако после поступления указанных веществ и лекарственного препарата в кожу происходит сильное разбавление веществ, улучшающих проникновение, при этом указанные вещества больше не могут способствовать пересечению молекулой лекарственного препарата дальнейших биологических мембран; соответственно, затем молекулы лекарственного препарата будут накапливаться в жировом слое под кожей, при этом накапливающиеся лекарственные препараты могут вызывать очень серьезные и даже смертельные побочные эффекты.
Биологическую доступность лекарственного препарата определяют путем измерения относительного количества введенного лекарственного препарата, которое достигает общего кровотока. Однако общий кровоток не является “местом действия” для большинства лекарственных препаратов. Даже если молекулы лекарственного препарата поступили в общий кровоток, они должны пересечь дополнительные биологические мембраны, которые могут быть менее проницаемыми, чем желудочно-кишечные мембраны, и взаимодействовать с межклеточными и внутриклеточными жидкостями перед попаданием в труднодостижимую область, называемую “местом действия”; таким образом, большинство лекарственных препаратов будет подвергаться метаболизму на слизистых оболочках желудочно-кишечного тракта, в печени, крови, почках и легких до того, как они достигнут “места действия”. Это обстоятельство не только приводит к очень слабому фармакологическому эффекту, но также является причиной токсической нагрузки на слизистую оболочку кишечника, кровь, печень, почки и легкие. В случае обеспечения возможности увеличения скорости проникновения лекарственных препаратов через различные мембраны фармакологический эффект и клинический ответ лекарственных препаратов будет существенно возрастать, при этом будет требоваться меньшая доза лекарственного препарата и будет возникать меньше побочных эффектов. Трансдермальная доставка пролекарства с очень высокой скоростью проникновения через кожу и мембраны будет очень полезна не только для лечения местных заболеваний, но также для лечения системных заболеваний. Поскольку указанные пролекарства являются в десятки или сотни раз более эффективными, чем исходные лекарственные препараты, потребуется только несколько десятых или сотых долей от обычной дозы лекарственного препарата, при этом будет возникать гораздо меньше побочных эффектов. При этом будет обеспечиваться преимущество не только применительно к трансдермальной доставке лекарственного препарата, но также и к любым другим системам доставки лекарственных препаратов (таким как пероральные, подкожные, внутривенные, ингаляционные и назальные).
Авторами настоящего изобретения было обнаружено, что лекарственные препараты, содержащие липофильную часть и первичную, вторичную или третичную аминогруппу (предпочтительно третичные аминогруппы), которая существует в протонированной форме (гидрофильная часть) при физиологических значениях pH, могут проникать через кожу и преодолевать гематоэнцефалический барьер и барьер «кровь-молоко» с очень высокой скоростью (по шкале мг/см2/ч). Принципы разработки указанных пролекарств NSAIA являются следующими:
1. Пролекарство должно содержать липофильную часть и первичную, вторичную или третичную аминогруппу (предпочтительно, третичные аминогруппы), которая существует в протонированной форме (гидрофильная часть) при физиологических значениях pH.
2. Каждое пролекарство NSAIA должно содержать только одну или две (предпочтительно одну) первичную, вторичную или третичную аминогруппы, которые существуют в протонированной форме (гидрофильная часть) при физиологических значениях pH.
3. Основная роль указанной первичной, вторичной или третичной аминогруппы состоит в том, чтобы способствовать прохождению лекарственного препарата через кожу, шрамы, мембрану, гематоэнцефалический барьер или барьер «кровь-молоко» и другие барьеры. Первичная, вторичная или третичная аминогруппа может представлять собой любую структуру, которая является нетоксичной и не препятствует биологической активности исходных лекарственных препаратов.
В настоящем изобретении предложены некоторые из пролекарств всех NSAIA, которые имеют общую формулу (1) «структуры 1» согласно патентам (международные заявки PCT/IB2006/052732, PCT/IB2006/052318, PCT/IB2006/052815, PCT/IB2006/052563, PCT/IB2006/052575, PCT/IB2006/053741, PCT/IB2006/053091, PCT/IB2006/053090, PCT/IB2006/052549).
Структура 1
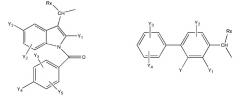
где R представляет собой разветвленную или линейную цепь -(CH2)n-, n=0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12,..., при этом в -(CH2)n- любой CH2 может быть заменен на O, S, NR8, CH=CH, C≡C, CHR8, CR8R9, арильные или гетероарильные остатки или любые другие группы, которые являются фармацевтически приемлемыми; R1 представляет собой H, один из любых алкильных, алкилоксильных, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильные или гетероарильные группы, при этом любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR8, CR8R9, арильные или гетероарильные группы или любые другие группы, которые являются фармацевтически приемлемыми; или R2 представляет собой H, один из любых алкильных, алкилоксильных, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильную или гетероарильную группы, при этом любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR8, CR8R9, арильные или гетероарильные группы или любые другие группы, которые являются фармацевтически приемлемыми; X представляет собой O, NH, NR8, S или отсутствует; R8 представляет собой H, OH, Cl, F, Br, I, один из любых алкильных, алкилоксильных, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильную или гетероарильную группы; R9 представляет собой H, OH, Cl, F, Br, I, один из любых алкильных, алкилоксильных, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильную или гетероарильную группы; HA отсутствует или представляет собой HCl, HBr, HF, HI, HOAc, лимонную кислоту или любые кислоты, которые являются фармацевтически приемлемыми. Все группы R, R1, R2, R8, R9 и -(CH2)n- являются разветвленными или линейными и могут содержать C, H, O, Cl, Br, F, I, P, S, N или любые другие атомы, которые являются фармацевтически приемлемыми, и могут содержать одинарные, двойные и/или тройные связи; все R, R1, R2, R8, R9 или -(CH2)n- группы могут являться ахиральными или хиральными; если группа является хиральной, она может содержать один или более хиральных центров и может представлять собой отдельный (R)- или (S)-энантиомер или смесь (R)- и (S)-энантиомеров; Ary- представляет собой, но не ограничивается ими:
где Rx представляет собой H, CH3, CH3O, OH, CH3CH2, CF3, CHF2, CH2F, Cl, F, Br, F; Ry представляет собой H, один из любых алкильных, алкилоксильных, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильную или гетероарильную группы; X1 или X4 представляет собой CH2, S, O, NH или CO; X2 или X5 представляет собой CH, CR8 или N; X3 представляет собой O, S, NH или NR8; Y, Y1, Y2, Y3, Y4, Y5 или Y6 независимо представляет собой H, HO, CH3COO, RyCOO, HS, NO2, CN, CH3COS, NH2, CH3CONH, RyCONH, CH3, CH3CH2, C3H7, C4H9, CH3O, CH3CH2O, C3H7O, Cl, F, Br, I, CH3S, CHF2O, CF3O, CF3CF2O, C3F7O, CF3, CF3CF2, C3F7, C4F9, CH3SO2, RySO2, CH3SO, RySO, CH3CO, CH3CH2CO; любой Ary- может быть ахиральным или хиральным; Если Ary- является хиральным, он может содержать один или более хиральных центров и может представлять собой отдельный (R)- или (S)-энантиомер или смесь (R)- и (S)-энантиомеров.
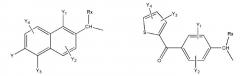
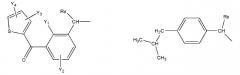
Авторами настоящего изобретения было обнаружено, что основная роль первичной, вторичной или третичной аминогруппы состоит только в том, чтобы способствовать прохождению лекарственного препарата через кожу, мембрану, гематоэнцефалический барьер или барьер «кровь-молоко» и другие барьеры, поэтому первичная, вторичная или третичная аминогруппа может представлять собой структуры любого типа, которые являются нетоксичными и не препятствуют биологической активности исходных лекарственных препаратов. Таким образом, для обеспечения указанного свойства авторами настоящего изобретения были разработаны и получены аминогруппы различных типов. Новые пролекарства NSAIA отвечают общим формулам (2a, 2b, 2c или 2d), «структуры 2a, 2b, 2c или 2d».
| Структура 2a | Структура 2b |
| Структура 2c | Структура 2d |
где R представляет собой разветвленную или линейную цепь, -(CH2)n-, в которой n=0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 …, в -(CH2)n- любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR6R7, арильные или гетероарильные остатки или другие циклические системы; R1 представляет собой разветвленную или линейную цепь, -(CH2)a-, где a=0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10..., в -(CH2)a- любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR6R7, арильные или гетероарильные остатки или другие циклические системы; R2 представляет собой разветвленную или линейную цепь, -(CH2)b-, где b=0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10..., в -(CH2)b- любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR6R7, арильные или гетероарильные остатки или другие циклические системы; R3 представляет собой разветвленную или линейную цепь, -(CH2)c-, где c=0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10..., в -(CH2)c- любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR6R7, арильные или гетероарильные остатки или другие циклические системы; R4 представляет собой H, один из любых алкильных, алкилокси, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильные или гетероарильные группы, при этом, любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR6R7, арильные или гетероарильные группы или другие циклические группы; R5 представляет собой H, один из любых алкильных, алкилокси, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильные или гетероарильные группы, при этом, любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR7R6, арильные или гетероарильные группы или другие циклические группы; R6 представляет собой H, один из любых алкильных, алкилокси, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильные или гетероарильные группы, при этом, любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR7R5, арильные или гетероарильные группы или другие циклические группы, R7 представляет собой H, один из любых алкильных, алкилокси, алкенильных, перфторалкильных, алкилгалогенидных или алкинильных остатков, содержащих от 1 до 12 атомов углерода, арильные или гетероарильные группы, при этом, любой CH2 может быть заменен на O, S, CH=CH, C≡C, CHR6, CR7R5, арильные или гетероарильные группы или другие циклические группы; X отсутствует или представляет собой O, NH, NR6 или S; Ary- в общей формуле (2a, 2b, 2c или 2d) «структуры 2a, 2b, 2c или 2d» имеет то же определение, что и Ary- в общей формуле (1) «структура 1»; HA отсутствует или представляет собой HCl, HBr, HF, HI, HOAc, лимонную кислоту или любые кислоты, которые являются фармацевтически приемлемыми. Все R, R1, R2, R3, R4, R5, R6, R7 или -(CH2)n- группы представляют собой разветвленные или линейные цепи и могут включать C, H, O, Cl, Br, F, I, P, S, N или любые другие атомы, которые являются фармацевтически приемлемыми, и могут содержать одинарные, двойные и/или тройные связи; все R, R1, R2, R3, R4, R5, R6, R7 или -(CH2)n- группы могут являться ахиральными или хиральными; если группа является хиральной, она может содержать один или более хиральных центров и может представлять собой отдельный (R)- или (S)-энантиомер или смесь (R)- и (S)-энантиомеров.
Абсорбция лекарственных препаратов из желудочно-кишечного тракта или других участков требует прохождения лекарственного препарата в молекулярной форме через барьерную мембрану. Прежде всего, лекарственный препарат должен раствориться, и если лекарственный препарат обладает требуемыми биофармацевтическими свойствами, он будет переходить из области высокой концентрации в область низкой концентрации через мембрану в кровь или общий кровоток. Все биологические мембраны содержат в качестве основных компонентов липиды. Все молекулы, которые играют доминирующую роль в формировании мембран, содержат фосфатсодержащие высокополярные головные группы и, в большинстве случаев, два сильногидрофобных углеводородных хвоста. Мембраны являются двухслойными, при этом гидрофильные головные группы с обеих сторон направлены в сторону водных участков. Высокогидрофильные лекарственные препараты не могут пройти через гидрофобный слой мембраны, а высокогидрофобные лекарственные препараты остаются в гидрофобном слое в виде части указанной мембраны вследствие их подобия и не могут эффективно проникать в цитозоль с внутренней стороны.
Одна из задач настоящего изобретения состоит в том, чтобы избежать побочных эффектов NSAIA путем увеличения растворимости NSAIA в желудочном соке, что позволит вводить указанные препараты перорально, а также увеличения скорости проникновения NSAIA через мембрану и кожный барьер, что позволит вводить указанные препараты трансдермально (местное применение). Наиболее важная задача настоящего изобретения заключается в том, чтобы разработать пролекарства NSAIA, способные очень эффективно проникать через кожу, клеточную мембрану, особенно мембраны клеток мозга и нервных клеток, и оставаться в общем кровотоке в течение гораздо меньшего времени, являясь при этом в сотни раз более эффективными, чем исходные лекарственные препараты, при этом будет требоваться лишь несколько десятых или сотых долей от дозы обычного лекарственного средства и будет возникать гораздо меньше побочных эффектов. При этом будет обеспечиваться преимущество не только применительно к трансдермальной доставке лекарственного препарата, но также и к любым другим системам доставки лекарственных препаратов (таким как пероральные, подкожные, внутривенные, ингаляционные и назальные), что позволит лечить многие состояния, которые нельзя лечить с помощью соответствующих исходных лекарственных препаратов. Предложенные новые пролекарства NSAIA в целом имеют две структурные особенности: они содержат липофильную часть и первичную, вторичную или третичную аминогруппу, которая существует в протонированной форме (гидрофильная часть) при физиологических значениях pH. Такой гидрофильно-липофильный баланс необходим для эффективного прохождения через барьер мембраны [Susan Milosovich et al., J. Pharm. Sci., 82, 227(1993)]. Положительно заряженные аминогруппы значительно увеличивают растворимость лекарственных препаратов в воде. Положительный заряд на аминогруппах этих пролекарств будет связываться с отрицательным зарядом на фосфатной головной группе мембраны. Таким образом, локальная концентрация за пределами мембраны или кожи будет очень высокой, что будет способствовать переходу этих пролекарств из области высокой концентрации в область низкой концентрации. Указанное связывание будет немного повреждать мембрану и может создавать некоторое пространство для прохождения липофильной части пролекарства. Когда молекулы мембраны двигаются, мембрана может чуть-чуть “треснуть” вследствие связывания пролекарства. Это позволит пролекарству внедриться в мембрану. При pH 7,4 только примерно 99% аминогрупп являются протонированными. Если аминогруппа не является протонированной, связь между аминогруппой пролекарства и фосфатной головной группой мембраны будет диссоциировать и пролекарство полностью проникнет в мембрану. Когда аминогруппа пролекарства переходит на другую сторону мембраны и, соответственно, становится протонированной, то пролекарство втягивается в цитозоль, полужидкий концентрированный водный раствор или суспензию. Благодаря короткому времени пребывания в желудочно-кишечном тракте указанные пролекарства не вызывают повреждения клеток слизистой оболочки желудка. Скорости проникновения новых пролекарств через человеческую кожу измеряли in vitro с применением модифицированных клеток Франца, которые выделяли из ткани человеческой кожи (360-400 мкм толщиной) передних и задних участков бедра. Принимающую жидкость, которая состояла из 10 мл 2% бычьего сывороточного альбумина в нормальном физиологическом растворе, перемешивали при 600 об./мин. Кумулятивные количества пролекарств и лекарственных препаратов, проникающие через кожу, в зависимости от времени определяли с помощью конкретного способа методом высокоэффективной жидкостной хроматографии. Кажущиеся значения потока пролекарств NSAIA составляли 0,1-50 мг/см2/ч. Полученные результаты свидетельствуют о том, что пролекарство диффундирует через человеческую кожу по меньшей мере в сотни раз быстрее, чем соответствующие исходные лекарственные препараты. Результаты показывают, что положительный заряд на диалкиламиноэтильной группе играет очень важную роль в прохождении лекарственного препарата через барьер мембраны и кожный барьер.
Новые пролекарства NSAIA могут проникать через кожный барьер, гематоэнцефалический барьер и барьер «кровь-молоко». Было проведено сравнение скорости in vivo проникновения пролекарств и соответствующих исходных лекарственных препаратов через кожу интактных крыс. Донор, содержащий 20% пролекарств или соответствующих исходных лекарственных препаратов в 1 мл этанола, наносили на примерно 5 см2 участок на спине крыс (~200 г). Через 4 часа крыс убивали и 5 мл метанола добавляли к 1 мл крови, 1 г печени, 1 г почки или 1 г мозга (печень, почку или мозг промывали буфером с pH 7,2 три раза) и смеси гомогенизировали. Затем пробы центрифугировали в течение 5 мин и анализировали методом ВЭЖХ. Результаты показаны в таблице 1-5.
| Таблица 1Распределение соли диэтиламиноэтилацетилсалицилат.ацетилсалициловой кислоты (P-1) и ее метаболитов в тканях и плазме в организме крыс | ||||
| Пролекарство или метаболиты | Плазма | Печень | Почка | Мозг |
| P-1 | 30±10 мкг/мл | 15±8 мкг/г | 25±6 мкг/г | 15±6 мкг/г |
| Аспирин | 25±8 мкг/мл | 13±8 мкг/г | 20±6 мкг/г | 15±5 мкг/г |
| Салициловая кислота | 80±10 мкг/мл | 30±8 мкг/г | 45±6 мкг/г | 30±6 мкг/г |
| Таблица 2Распределение 1-пиперидинпропил 2[(2,6-дихлорфенил)амино]бензолацетат.AcOH (P-2) и его метаболита в тканях и плазме в организме крыс | ||||
| Пролекарство или метаболиты | Плазма | Печень | Почка | Мозг |
| P-2 | 40±10 мкг/мл | 22±8 мкг/г | 20±6 мкг/г | 25±6 мкг/г |
| Диклофенак | 75±8 мкг/мл | 25±8 мкг/г | 48±6 мкг/г | 40±5 мкг/г |
| Таблица 3Распределение 1-пирролидинпропил-2-(3-бензоилфенил)пропионат.AcOH (P-3) и его метаболита в тканях и плазме в организме крыс | ||||
| Пролекарство или метаболиты | Плазма | Печень | Почка | Мозг |
| P-3 | 35±8 мкг/мл | 22±8 мкг/г | 25±6 мкг/г | 20±6 мкг/г |
| Кетопрофен | 70±8 мкг/мл | 32±8 мкг/г | 45±6 мкг/г | 35±5 мкг/г |
| Таблица 4Распределение 4-пиперидинметил-2-(3-феноксифенил)пропионат.AcOH (P-4) и его метаболита в тканях и плазме в организме крыс | ||||
| Пролекарство или метаболиты | Плазма | Печень | Почка | Мозг |
| P-4 | 32±8 мкг/мл | 20±8 мкг/г | 20±6 мкг/г | 20±6 мкг/г |
| Фенопрофен | 80±8 мкг/мл | 38±8 мкг/г | 48±6 мкг/г | 45±5 мкг/г |
| Таблица 5Распределение 3-пиперидинметил-2-(п-изобутилфенил)пропионат.AcOH (P-5) и его метаболита в тканях и плазме в организме крыс. | ||||
| Пролекарство или метаболиты | Плазма | Печень | Почка | Мозг |
| P-5 | 40±8 мкг/мл | 25±8 мкг/г | 30±6 мкг/г | 25±6 мкг/г |
| Ибупрофен | 70±8 мкг/мл | 35±8 мкг/г | 45±6 мкг/г | 35±5 мкг/г |
Затем 20% аспирина, диклофенака, кетопрофена, фенопрофена или ибупрофена в 1 мл этанола наносили на примерно 5 см2 участок на спине крыс. Через 4 часа крыс убивали и 5 мл метанола добавляли к 1 мл крови, 1 г печени, 1 г почки или 1 г мозга (печень, почку или мозг промывали буфером с pH 7,2 три раза) и смеси гомогенизировали. Ни один из этих лекарственных препаратов не был найден в каких-либо крысиных тканях или плазме. Результаты показали, что пролекарства NSAIA могут проникать через кожный барьер, гематоэнцефалический барьер и другие мембранные барьеры с очень высокой скоростью, а исходные NSAIA не могут проникать через кожный барьер в определяемых количествах.
Для пролекарств общей формулы (1) «структуры 1» была продемонстрирована противовоспалительная, обезболивающая, жаропонижающая и противоревматическая активность согласно полученным патентам (международные заявки PCT/IB2006/052732, PCT/IB2006/052318, PCT/IB2006/052815, PCT/IB2006/052563, PCT/IB2006/052575, PCT/IB2006/053741, PCT/IB2006/053091, PCT/IB2006/053090, PCT/IB2006/052549). Авторами настоящего изобретения было обнаружено, что все пролекарства общей формулы (2a, 2b, 2c или 2d) «структуры 2a, 2b, 2c или 2d», демонстрировали противовоспалительную, обезболивающую, жаропонижающую и противоревматическую активность. Основными задачами настоящего изобретения являются новые медицинские применения пролекарств NSAIA.
Хорошо известна связь между воспалением и раком. Доктор Thea D. Tlsty отметил в своей речи (Keystone Symposia: Inflammation and Cancer, Breckenridge, Colorado, USA, Feb. 27-March 3, 2005), что циклооксигеназа-2 (COX-2) стимулирует активность ароматазы, развитие кровеносных сосудов, пролиферацию, инвазию и синтез простагландина. Увеличение уровней простагландинов приводит к ингибированию апоптоза. Аспирин и другие NSAIA ингибируют COX-1 и COX-2. Совокупный относительный риск развития рака кишечника, рака пищевода, рака яичников или других видов рака уменьшается у людей, принимающих аспирин длительное время. Однако раковые клетки могут изменять структуру своих мембран и удерживать NSAIA от проникновения в раковые клетки. Новые пролекарства, предлагаемые в настоящем изобретении, могут проникать через любые мембранные барьеры и могут быть местно нанесены на наружный участок кожи в месте расположения раковой опухоли, при этом большие количества пролекарств будут проникать в раковые клетки при очень небольшом системном воздействии.
Для оценки противоопухолевой активности пролекарств NSAIA человеческие клетки рака молочной железы (BCAP-37, в случае каждой мыши применяли 2-3 мм3 ткани опухоли) подкожно ксенотрансплантировали «голым» мышам (BALB, 12 групп, 7 мышей в каждой группе). Через 14 дней опухоли вырастали до размеров 50±10 мм3 (0,05 мл). Затем 30 мкл 5% (соответствует 1,5 мг пролекарств) соли диэтиламиноэтилацетилсалицилат.ацетилсалициловой кислоты (P-1, в ацетоне); 1-пиперидинпропил-2[(2,6-дихлорфенил)амино]бензолацетата.AcOH (P-2, в воде), 1-пирролидинпропил-2-(3-бензоилфенил)пропионат.AcOH (P-3, в воде), 4-пиперидинметил-2-(3-феноксифенил)пропионата.AcOH (P-4, в воде), 3-пиперидинметил-2-(п-изобутилфенил)пропионата.AcOH (P-5, в воде), диэтиламиноэтил-1-(п-хлорбензоил)-5-метокси-2-метилиндол-3-ацетата.AcOH (P-11, в воде), 2-(4-морфолинил)этил-(Z)-5-фтор-2-метил-1-[(4-метилсульфинил)фенилметилен]-1H-инден-3-ацетата.AcOH (P-12, в воде), диэтиламиноэтил-2-(2,4-дихлорфенокси)бензолацетата.AcOH (P-19, в воде), диэтиламиноэтил-2-(8-метил-10,11-дигидро-11-оксодибенз(b,f)оксепин-2-ил)пропионата.AcOH (P-37, в воде), 1-пирролидинпропил-2-[[(3-(трифторметил)фенил)амино]бензоата.AcOH (P-48, в воде), 4-N,N-диметиламинобутирилокси-2-метил-N-2-пиридинил-2H,1,2-бензотиазин-3-карбоксамид-1,1-диоксид.HCl (P-51, в ацетоне) каждые 8 часов местно наносили на участок, где были имплантированы человеческие клетки рака молочной железы (около передней лапы). Размеры опухолей на 42 день показаны в таблице 6 и таблице 7.
| Таблица 6Размеры опухолей и массы контрольной группы и групп «голых» мышей, подвергаемых лечению лекарственными препаратами, на 42 день | ||||||
| Пролекарство | Контрольная группа | P-1 | P-2 | P-3 | P-4 | P-5 |
| Размер (мм3) | 800±100 | 150±50 | 180±50 | 200±50 | 180±50 | 190±50 |
| Масса | 22±2 | 22±3 | 22±2 | 21±3 | 22±3 | 23±2 |
| Таблица 7Размеры опухолей и массы групп «голых» мышей, подвергаемых лечению лекарственными препаратами, на 42 день | ||||||
| Пролекарство | Р-11 | Р-12 | Р-19 | Р-37 | Р-48 | Р-51 |
| Размер (мм3) | 210±100 | 250±50 | 280±50 | 250±50 | 290±50 | 390±50 |
| Масса | 21±2 | 23±3 | 21±2 | 23±3 | 22±3 | 23±2 |
Во втором исследовании противоопухолевого действия клетки рака толстой кишки человека (LS174J, в случае каждой мыши применяли 2-3 мм3 ткани опухоли) подкожно ксенотрансплантировали «голым» мышам (BALB). Через 7 дней опухоли вырастали до размеров 55±10 мм3 (0,055 мл). Затем примерно 30 мкл 5% (соответствует 1,5 мг пролекарств) соли диэтиламиноэтилацетилсалицилат.ацетилсалициловой кислоты (P-1, в ацетоне); 1-пиперидинпропил-2[(2,6-дихлорфенил)амино]бензолацетата.AcOH (P-2, в воде), 1-пирролидинпропил-2-(3-бензоилфенил)пропионата.AcOH (P-3, в воде), 4-пиперидинметил-2-(3-феноксифенил)пропионата.AcOH (P-4, в воде), 3-пиперидинметил-2-(п-изобутилфенил) пропионата.AcOH (P-5, в воде), диэтиламиноэтил-1-метил-5-(4-метилбензоил)-1H-пиррол-2-ацетата.AcOH (P-13, в воде), 2-(4-морфолинил)этил-2-амино-3-бензоилбензолацетата.AcOH (P-16, в воде), диэтиламиноэтил-2-(10,11-дигидро-10-оксодибензо(b,f)тиепин-2-ил)пропионата.AcOH (P-36), диэтиламиноэтил-2-[(2,3-диметилфенил)амино]бензоата.AcOH (P-46, в воде), диэтиламиноэтил-2-[(2,6-дихлор-3-метилфенил)амино]бензоата.AcOH (P-47, в воде), N-(2-т