Микрочастицы дикетопиперазина с определенными удельными площадями поверхности
Иллюстрации
Показать всеНастоящее изобретение относится к микрочастицам фумарилдикетопиперазина (ФДКП), которые подходят для доставки в легкие, обладающие удельной площадью поверхности от 15 м2/г до 67 м2/г и диаметром от 0,5 мкм до 10 мкм. Изобретение также относится к сухому порошку, включающему указанные микрочастицы, который также подходит для доставки в легкие, ингаляционной системе, содержащей ингалятор для вдыхания порошка и указанный сухой порошок, а также к способу доставки активного агента, содержащегося в сухом порошке, путем вдыхания указанного сухого порошка. Также раскрываются способы образования микрочастиц ФДКП, первый из которых включает растворение ФДКП в водном растворе аммиака, добавление кислого раствора к раствору аммиака при температуре от 12ºС до 26ºС и сбор осадка, содержащего микрочастицы ФДКП, после промывания деионизированной водой. Второй способ образования микрочастиц ФДКП включает подачу равных масс 10,5 вес.% раствора уксусной кислоты и 2,5 вес.% раствора ФДКП при температуре 14-18ºС через мешалку с большими сдвиговыми усилиями. Изобретение направлено на получение подходящих для введения в легкие микрочастиц ФДКП, которые обладают хорошей аэродинамической характеристикой и обеспечивают улучшенное всасывание лекарственных веществ. 6 н. и 12 з.п. ф-лы, 4 табл., 9 ил., 2 пр.
Реферат
ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Согласно 35 USC §119(e) настоящая заявка притязает на приоритет предварительной американской заявки на патент 61/186773, поданной 12 июня 2009, содержание которой включено в настоящее описание во всей полноте в виде ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0002] Раскрыты микрочастицы дикетопиперазина с удельной площадью поверхности менее чем примерно 67 м2/г. Микрочастицы ФДКП можно использовать в качестве системы доставки лекарственных веществ или активных агентов при лечении заболевания или нарушений, например, эндокринного происхождения, в том числе диабета и ожирения.
УРОВЕНЬ ТЕХНИКИ
[0003] На протяжении многих лет доставка лекарственных веществ была одной из основных проблем, в частности когда доставляемое соединение является нестабильным в условиях, с которыми, до достижения своего целевого местоположения, оно сталкивается в желудочно-кишечном трактате при пероральном введении субъекту. Например, во многих случаях предпочтительным является пероральное введение лекарственных веществ, особенно с точки зрения легкости их введения, соблюдения пациентом режима лечения и более низкой стоимости. Однако многие соединения являются неэффективными или демонстрируют низкую или изменчивую эффективность при пероральном введении. По-видимому, это происходит из-за нестабильности лекарственных веществ в условиях пищеварительного тракта или из-за их неэффективного всасывания.
[0004] Доставка лекарственного вещества в легкие была изучена исходя из проблем, связанных с доставкой лекарственного вещества. Например, лекарственные вещества, доставляемые в легкие, как правило, разрабатывают таким образом, чтобы они воздействовали на легочную ткань, например вазодилятаторы, сурфактанты, химиотерапевтические агенты или вакцины против гриппа или других респираторных заболеваний. Другие лекарственные вещества, в том числе нуклеотидные лекарственные вещества, доставляли в легкие, так как они представляют собой ткань, которая является особенно подходящей для лечения, например, в случае генетической терапии кистозного фиброза, при которой в легкие вводят ретровирусные вектора, экспрессирующие дефектную аденозиндеаминазу.
[0005] В легкие также можно осуществлять доставку лекарственных веществ, которые являются агентами системного действия. Преимущества доставки системных агентов в легкие заключаются в их большой площади поверхности и легкости, с которой происходит всасывание поверхностью слизистой оболочки легкого. Одна из проблем, связанных со всеми формами доставки лекарственных веществ в легкие, заключается в сложности такой доставки, связанной с прохождением лекарственными веществами через все естественные барьеры, такие как реснички, выстилающие трахею, а также с введением постоянного объема и веса лекарственного вещества.
[0006] Следовательно, существует потенциал для усовершенствования доставки лекарственных веществ в легкие.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0007] Настоящее раскрытие относится к системам, микрочастицам и способам, позволяющим улучшить доставку лекарственных веществ в легкие. В раскрытых вариантах осуществления улучшенная доставка достигается путем предоставления микрочастиц дикетопиперазина (ДКП) с удельной площадью поверхности (SSA) в пределах от примерно 35 м2/г до примерно 67 м2/г. Микрочастицы ДКП с удельной площадью поверхности, находящейся в этом диапазоне, демонстрируют характеристики, благоприятные для доставки в легкие, такие как улучшенная аэродинамическая характеристика и улучшенное всасывание лекарственных веществ.
[0008] Один из раскрытых в настоящем описании вариантов осуществления включает микрочастицы дикетопиперазина с удельной площадью поверхности менее чем примерно 67 м2/г. Другой вариант осуществления включает микрочастицы дикетопиперазина с удельной площадью поверхности, находящейся в пределах от примерно 35 м2/г до примерно 67 м2/г. Другой вариант осуществления включает микрочастицы дикетопиперазина, у которых при отсутствии активного агента удельная площадь поверхности больше чем примерно 35 м2/г, но меньше чем примерно 62 м2/г после адсорбции частицами активного агента.
[0009] В другом варианте осуществления микрочастицы фумарилдикетопиперазина (ФДКП) с удельной площадью поверхности в пределах от примерно 35 м2/г до примерно 67 м2/г содержит лекарственное вещество или активный агент, причем указанную SSA определяют до добавления лекарственного вещества к частице. Присоединение активного агента к частице обычно приводит к уменьшению SSA. В различных вариантах осуществления микрочастиц ФДКП лекарственное вещество может представлять собой, например, пептид или белок, в том числе эндокринные гормоны, например инсулин, глюкагон-подобный пептид-1 (GLP-1), глюкагон, эксендин, паратиреоидный гормон, обестатин, кальцитонин, оксинтомодулин и т.п. Другой вариант осуществления микрочастиц ФДКП с удельной площадью поверхности в пределах от примерно 35 м2/г до примерно 67 м2/г может включать содержание лекарственного вещества/пептида, которое может изменяться в зависимости от условий протекания процесса синтеза для получения микрочастиц. В одном из конкретных примеров могут быть получены микрочастицы ФДКП, имеющие содержание лекарственного вещества/пептида, которое может изменяться в зависимости от целевой или доставляемой дозы. Например, в случае, если лекарственное вещество является инсулином, инсулиновый компонент может составлять примерно от 3 Ед/мг до примерно 4 Ед/мг в содержащей микрочастицы порошкообразной лекарственной форме. В некоторых вариантах осуществления лекарственное вещество адсорбируется на поверхности микрочастиц. В других вариантах осуществления таких загруженных лекарственным веществом микрочастицах SSA этих микрочастиц составляет менее чем примерно 62 м2/г.
[0010] Раскрытые здесь варианты осуществления также включают сухие порошки, содержащие микрочастицы. В одном из вариантов осуществления сухие порошки содержат микрочастицы ФДКП с удельной площадью поверхности менее чем примерно 67 м2/г. Другой вариант осуществления включает микрочастицы дикетопиперазина, у которых удельная площадь поверхности находится в пределах от примерно 35 м2/г до примерно 67 м2/г. Другой вариант осуществления включает содержащие лекарственное вещество или активный агент микрочастицы дикетопиперазина с удельной площадью поверхности в пределах от примерно 35 м2/г до примерно 62 м2/г.
[0011] В вариантах осуществления сухих порошков микрочастицы ФДКП содержат лекарственное вещество. В другом варианте осуществления сухих порошков лекарственное вещество представляет собой пептид, у которого размер молекулы и молекулярная масса могут быть различными, включая инсулин, глюкагон-подобный пептид-1, глюкагон, эксендин, паратиреоидный гормон, кальцитонин, оксинтомодулин и т.п. В одном из таких вариантов осуществления сухих порошков, в котором лекарственное вещество представляет собой инсулин, содержание инсулина в микрочастицах ФДКП составляет от примерно 3 Ед/мг до примерно 4 Ед/мг.
[0012] Другие варианты осуществления относятся к системам доставки лекарственного вещества, содержащим ингалятор, контейнер для единичной дозы лекарственного вещества в виде сухого порошка, например картридж, и порошкообразную лекарственную форму, содержащую раскрытые в настоящем описании микрочастицы и активный агент. В одном из вариантов осуществления система доставки лекарственного вещества для использования с сухими порошками включает ингаляционную систему, содержащую ингалятор с высоким сопротивлением, имеющий воздушные каналы, которые оказывают высокое сопротивление воздушному потоку, проходящему через эти каналы, для разрушения агломератов и дозирования порошкообразной лекарственной формы. В одном из вариантов осуществления значение сопротивления в ингаляционной системе составляет, например, от примерно 0,065 (√кПа)/л в мин до примерно 0,200 (√кПа)/л в мин. В некоторых вариантах осуществления сухие порошки могут эффективно подаваться путем вдоха с помощью ингаляционной системы, в которой пиковый дифференциал давления при вдохе может составлять от примерно 2 кПа до примерно 20 кПа и может создавать в результате пиковую скорость потока от примерно 7 до 70 литров в мин. В некоторых вариантах осуществления ингаляционные системы разработаны для предоставления единичной дозы путем выдачи порошка из ингалятора в виде непрерывного потока или в виде одного или нескольких импульсов выдаваемого пациенту порошка. В некоторых раскрытых в настоящем описании вариантах осуществления ингаляционная система для сухих порошков имеет заданный баланс потока массы внутри ингалятора. Например, баланс потока, при котором примерно от 10% до 70% от общего потока, выдаваемого из ингалятора пациенту, доставляется через одно или несколько дозирующих отверстий, которые позволяют потоку воздуха проходить через область, содержащую порошкообразную лекарственную форму, и причем примерно от 30% до 90% воздушного потока генерируется в других каналах ингалятора. Кроме того, обводной поток или поток, не входящий и не выходящий из области размещения порошка, такой как картридж, может снова объединяться с потоком, выходящим через дозирующее порошок отверстие внутри ингалятора, с тем, чтобы разбавлять, ускорять и в конечном счете разрушать агломераты флюидизированного порошка до выхода из мундштука ингалятора. В одном из вариантов осуществления скорости потока в системе ингалятора, находящиеся в пределах от примерно 7 до 70 л в мин, обеспечивают в результате распыление более 75% порошкообразного содержимого контейнера или порошкообразного содержимого картриджа, в порцию весом от 1 до 30 мг. В некоторых вариантах осуществления описанная выше ингаляционная система может выпускать за один вдох вдыхаемую фракцию/порцию, составляющую более 40%, более 50%, более 60% или более 70% от дозы порошка.
[0013] В конкретных вариантах осуществления предоставляется ингаляционная система, содержащая ингалятор для сухих порошков, лекарственную форму в виде сухого порошка, содержащую микрочастицы фумарилдикетопиперазина, причем загруженные микрочастиц ФДКП имеют удельную площадь поверхности менее чем примерно 67 м2/г, и один или несколько активных агентов. В некоторых аспектах этого варианта осуществления ингаляционной системы лекарственная форма в виде сухого порошка предоставляется в картридже для единичной дозы. Альтернативно, лекарственная форма в виде сухого порошка может быть заранее загружена или засыпана в ингалятор. В этом варианте осуществления структурная конфигурация ингаляционной системы позволяет механизму разрушения агломератов в ингаляторе формировать вдыхаемые фракции, превышающие 50%; т.е. более половины от количества порошка, содержавшегося в ингаляторе (картридже), испускается в виде частиц менее чем 5,8 мкм. В одном из вариантов осуществления ингаляторы могут высвобождать во время дозирования более 85% порошкообразного лекарственного вещества, содержащегося внутри контейнера. В некоторых вариантах осуществления ингаляторы могут за один вдох высвобождать более 85% содержащегося порошкообразного лекарственного вещества. В некоторых вариантах осуществления ингаляторы могут высвобождать более 90% содержимого картриджа или содержимого контейнера за менее чем 3 секунды при разнице давлений от 2 кПа до 5 кПа в виде порции весом до 30 мг.
[0014] Раскрытые здесь варианты осуществления также включают способы. В одном из вариантов осуществления предоставляется способ лечения заболевания или расстройства, связанного с нарушениями эндокринной системы, содержащий введение нуждающемуся в этом человеку лекарственной формы в виде сухого порошка, содержащего микрочастицы ФДКП с удельной площадью поверхности менее чем примерно 67 м2/г и лекарственное вещество, подходящее для лечения указанного заболевания или расстройства. Другой вариант осуществления включает микрочастицы дикетопиперазина, у которых удельная площадь поверхности находится в пределах от примерно 35 м2/г до примерно 67 м2/г. Другой вариант осуществления включает содержащие активное вещество микрочастицы дикетопиперазина с удельной площадью поверхности менее чем примерно 62 м2/г. Один из вариантов осуществления включает способ лечения расстройства, связанного с инсулином, содержащий введение сухого порошка, содержащего описанные выше микрочастицы ФДКП нуждающемуся в этом человеку. Способ включает введение субъекту лекарственной формы в виде сухого порошка, содержащей микрочастицы фумарилдикетопиперазина, SSA которых находится в вышеуказанных диапазонах. В различных вариантах осуществления связанное с инсулином расстройство может в частности включать или исключить все или любое из следующих расстройств: предиабет, сахарный диабет типа 1 (фаза “медового месяца” (ремиссии), фаза после медового месяца, или обе), сахарный диабет типа 2, гестационный диабет, гипогликемия, гипергликемия, инсулиновая резистентность, секреторная дисфункция, нарушенная ранняя фаза секреции инсулина, потеря функции панкреатических β-клеток, потеря панкреатических β-клеток и нарушение метаболизма. В одном из вариантов осуществления сухой порошок содержит инсулин. В других вариантах осуществления сухой порошок содержит глюкагон, эксендин или GLP-1.
[0015] Другие раскрытые здесь варианты осуществления включают способы получения подходящих для введения в легкие микрочастиц в виде сухого порошка. В одном из вариантов осуществления способ содержит образование микрочастиц дикетопиперазина с удельной площадью поверхности от примерно 35 м2/г до примерно 67 м2/г в пределах 95%-ого доверительного интервала путем подбора условий изготовления для целевого получения микрочастиц с удельной площадью поверхности примерно 52 м2/г. В другом варианте осуществления подбор условий изготовления включает увеличение или уменьшение температуры или концентрации аммиака, уксусной кислоты и/или дикетопиперазина в подаваемом растворе.
[0016] Другой раскрытый здесь вариант осуществления включает способ изготовления микрочастиц, подходящих для введения в легкие в виде сухого порошка, содержащих дикетопиперазин, такой как ФДКП. В одном из вариантов осуществления микрочастицы содержат синтезирование соединения ФДКП или его композиции, причем микрочастицы имеют удельную площадь поверхности от примерно 35 м2/г до примерно 67 м2/г, и определение площади поверхности микрочастиц ФДКП путем оценки этой площади поверхности в м2/г стандартным анализатором для измерения площади поверхности. В других вариантах осуществления удельную площадь поверхности определяют после адсорбции микрочастицей активного агента вместо или дополнительно к определению площади поверхности до введения активного агента; SSA не превышает примерно 62 м2/г. В одном из вариантов осуществления синтез ФДКП включает: a) растворение композиции ФДКП в растворе с основным pH, получая раствор ФДКП; b) предоставление раствора летучей кислоты и c) смешивание раствора ФДКП с раствором летучей кислоты в смесителе с большими сдвиговыми усилиями для получения микрочастиц.
[0017] В конкретных вариантах осуществления способ получения микрочастиц ФДКП с площадью поверхности в пределах от примерно 35 м2/г до примерно 67 м2/г содержит реакцию омыления и перекристаллизацию. В одном из вариантов осуществления раскрывается способ получения микрочастиц в виде сухого порошка, подходящих для введения в легкие, включающий: a) синтез соединения или композиции ФДКП, b) растворение соединения ФДКП, полученного на стадии а), в растворе с основным pH с получением раствора ФДКП; d) предоставление раствора летучей кислоты и e) смешивание раствора ФДКП с раствором летучей кислоты в смесителе с большими сдвиговыми усилиями для получения микрочастиц. Способ также может содержать определение удельной площади поверхности частиц после их формирования.
[0018] В конкретных вариантах осуществления способ синтеза микрочастиц ФДКП с удельной площадью поверхности, не превышающей примерно 67 м2/г, содержит подачу равных масс примерно 10,5 вес.% раствора уксусной кислоты и примерно 2,5 вес.% раствора ФДКП при температуре от примерно 14°C до примерно 18°C через смеситель с большими сдвиговыми усилиями, такой как Dual-feed SONOLATOR™, под давлением 2000 psi через отверстие площадью 0,001 дюйм2 для получения суспензии. Способ может дополнительно содержать этап осаждения микрочастиц из раствора и сбора микрочастиц, образованных в резервуаре с деионизированной водой, примерно такой же массы и температуры. В этом варианте осуществления суспензия содержит примерно 0,8% твердых микрочастиц. В некоторых вариантах осуществления способ также включает концентрирование суспензии микрочастиц путем промывки микрочастиц, например, в деионизированной воде, используя способ фильтрации с тангенциальным потоком. В этом и других вариантах осуществления осадок может быть сначала сконцентрирован до примерно 4% твердых частиц, а затем промыт деионизированной водой. В некоторых вариантах осуществления суспензию обычно можно концентрировать до примерно 10% твердых частиц из расчета на исходную массу используемой композиции ФДКП. Концентрированную суспензию можно оценить на содержание твердых частиц способом сушки в сушильном шкафу. В раскрытых здесь вариантах осуществления способ дополнительно содержит определение площади поверхности частиц после их сушки.
[0019] В конкретных вариантах осуществления раскрытых в настоящем описании композиций и способов в микрочастицах дикетопиперазина с удельной площадью поверхности менее чем примерно 67 м2/г используется дикетопиперазин формулы 2,5-дикето-3,6-бис(N-X-4-аминобутил)пиперазин, в котором X выбирают из группы, состоящей из фумарила, сукцинила, малеила и глутарила. В приведенном в качестве примера варианте осуществления дикетопиперазин имеет формулу (бис-3,6-(N-фумарил-4-аминобутил)-2,5-дикетопиперазин или 2,5-дикето-3,6-бис(N-фумарил-4-амино-бутил)пиперазин.
[0020] Другой раскрытый здесь вариант осуществления включает способ изготовления микрочастиц ФДКП с удельной площадью поверхности менее чем примерно 67 м2/г , содержащих лекарственное вещество или активный агент, причем указанную удельную площадь поверхности определяют до введения в частицу лекарственного вещества. В этом варианте осуществления способ содержит добавление в суспензию микрочастиц раствора, содержащего активный агент, такой как пептид, в том числе инсулин, глюкагон, глюкагон-подобный пептид-1, оксинтомодулин, пептид YY и т.п.; добавление в суспензию водного раствора аммиака, например, для повышения pH суспензии до 4,5; проведение реакции, мгновенную заморозку полученной суспензии в жидком азоте и лиофилизацию образованных пеллет для получения сухого порошка, содержащего микрочастицы ФДКП с удельной площадью поверхности менее чем примерно 67 м2/г. В аспекте этого варианта осуществления удельная площадь поверхности микрочастиц после адсорбции микрочастицей активного агента не превышает примерно 62 м2/г.
[0021] В одном из вариантов осуществления раскрыт способ доставки инсулина нуждающемуся в этом пациенту, содержащий введение сухого порошка, содержащего микрочастицы дикетопиперазина с удельной площадью поверхности менее чем примерно 62 м2/г (67 м2/г из расчета загруженной микрочастицы), глубоко в легкие путем вдыхания пациентом сухого порошка. В аспектах этого варианта осуществления определены конкретные признаки системы ингалятора.
[0022] Другой раскрытый здесь вариант осуществления содержит способ доставки лекарственного вещества, например инсулина, нуждающемуся в этом пациенту, содержащий введение сухого порошка глубоко в легкие путем вдыхания пациентом сухого порошка; причем сухой порошок содержит микрочастицы дикетопиперазина, содержащие инсулин, где микрочастицы образованы из дикетопиперазина и имеют площадь поверхности в пределах от примерно 35 м2/г до примерно 67 м2/г. В одном из аспектов этого варианта осуществления удельная площадь поверхности микрочастиц после адсорбции на микрочастицу активного агента не превышает 62 м2/г. В аспектах этого варианта осуществления определены конкретные признаки системы ингалятора. Другие варианты осуществления включают способы лечения связанного с инсулином расстройства, содержащие введение сухого порошка, как описано выше, нуждающемуся в этом человеку. В различных вариантах осуществления связанное с инсулином расстройство может в частности включать или исключить все или любое из следующих нарушений: предиабет, сахарный диабет типа 1 (фаза “медового месяца”, фаза после медового месяца, или обе фазы), сахарный диабет типа 2, гестационный диабет, гипогликемия, гипергликемия, инсулиновая резистентность, секреторная дисфункция, нарушенная ранняя фаза секреции инсулина, потеря функции панкреатических β-клеток, потеря панкреатических β-клеток и нарушение метаболизма.
[0023] В одном из вариантов осуществления предоставляется способ лечения заболевания или расстройства, связанного с нарушением эндокринной системы, содержащий введение нуждающемуся в этом человеку лекарственной формы в виде сухого порошка, содержащей микрочастицы ФДКП с удельной площадью поверхности менее чем примерно 67 м2/г, и лекарственное вещество, подходящее для лечения указанного заболевания или расстройства. В одном из аспектов этого варианта осуществления удельная площадь поверхности микрочастиц после адсорбции активного агента на микрочастицу не превышает примерно 62 м2/г. Один из вариантов осуществления включает способ лечения связанного с инсулином расстройства, включающий введение сухого порошка, содержащего микрочастицы ФДКП, как описано выше, нуждающемуся в этом человеку. Способ включает введение субъекту лекарственной формы в виде сухого порошка, содержащей микрочастицы ФДКП с удельной площадью поверхности, не превышающей примерно 67 м2/г, и инсулин. В аспекте этого варианта осуществления удельная площадь поверхности микрочастиц после адсорбции активного агента на микрочастицу не превышает примерно 62 м2/г. В различных вариантах осуществления связанное с инсулином расстройство может, в частности, включать или исключать все или любое из следующих нарушений: предиабет, сахарный диабет типа 1 (фаза “медового месяца”, фаза после медового месяца, или обе фазы), сахарный диабет типа 2, гестационный диабет, гипогликемия, гипергликемия, инсулиновая резистентность, секреторная дисфункция, нарушенная ранняя фаза секреции инсулина, потеря функции панкреатических β-клеток, потеря панкреатических β-клеток и нарушение метаболизма.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0024] Приведенные ниже чертежи являются частью настоящего описания и включены для дополнительной иллюстрации некоторых аспектов раскрытых здесь примеров. Раскрытие может быть лучше понято со ссылкой на один или несколько этих чертежей в комбинации с подробным описанием представленных здесь конкретных вариантов осуществления.
[0025] На Фиг.1A и 1B показаны микрочастицы с высокой и низкой удельной площадью поверхности (SSA) соответственно.
[0026] На Фиг.2 показана микрочастица фумарилдикетопиперазина (ФДКП), имеющая в целом вид сферы.
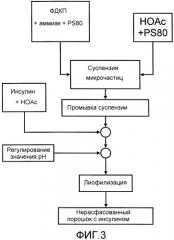
[0027] На Фиг.3 показана блок-схема процесса получения ФДКП.
[0028] На Фиг.4A и 4B показана оцененная и фактическая SSA порошков, состоящих из микрочастиц/инсулина, полученных согласно блок-схеме, приведенной на Фиг.3.
[0029] На Фиг.5A-C показана зависимость между RF/порция, SSA (микрочастиц ФДКП) и температурой подаваемого раствора.
[0030] На Фиг.6A показана зависимость между параметром RF/порция и SSA порошков, состоящих из микрочастиц/инсулина, и показано, что порошки с SSA> примерно 62 м2/г имеют 5% вероятность для значений параметра RF/порция <40%. На Фиг.6B показаны целевые значения для SSA при производстве вследствие неточности прогнозирования SSA на основе подаваемых концентраций.
[0031] На Фиг.7 показан параметр RF/порция как функция SSA порошков, состоящих из микрочастиц/инсулина. Каждая точка представляет отдельную партию порошков, состоящих из микрочастиц/инсулина.
[0032] На Фиг.8A показано влияние SSA порошков, состоящих из микрочастиц/инсулина, на эффективную вязкость суспензии микрочастиц, содержащую примерно 4% твердых частиц. На Фиг.8B показано соотношение между вязкостью суспензии и эффективностью порошка.
[0033] На Фиг.9 показана концентрация инсулина в осадке как функция от SSA микрочастиц ФДКП.
ПОДРОБНОЕ ОПИСАНИЕ
[0034] Как указано выше, доставка лекарственного вещества в легкие имеет много преимуществ. Однако в легкие трудно доставлять постоянный объем и вес лекарственного вещества из-за проблем, связанных с транспортировкой лекарственных веществ через естественные физические барьеры. В настоящем описании раскрыты микрочастицы дикетопиперазина с удельной площадью поверхности менее чем примерно 67 м2/г в качестве агентов доставки лекарственного вещества, способы получения микрочастиц и способы лечения с использованием этих микрочастиц.
[0035] Используемый здесь термин “микрочастица” относится к частице с диаметром от примерно 0,5 мкм до примерно 1000 мкм, независимо от ее точной внешней или внутренней структуры. Микрочастицы, имеющие диаметр от примерно 0,5 мкм до примерно 10 мкм, могут достигать легких, успешно проходя через большинство естественных барьеров. Для прохождения через изгиб в горле требуется диаметр менее чем примерно 10 мкм, а для того чтобы предотвратить выдыхание частиц, требуется диаметр примерно 0,5 мкм или более. Для глубокого проникновения в легкое (или альвеолярную область), где, как предполагается, происходит самое эффективное всасывание, предпочтительно максимизировать долю частиц, содержащихся во “вдыхаемой фракции” (RF), которая согласно общепринятому мнению представляет собой частицы с аэродинамическим диаметром от примерно 0,5 мкм до примерно 5,7 мкм, хотя, согласно некоторым ссылкам, используются несколько другие диапазоны, измеренные стандартными методами, например каскадным импактором Андерсена. Для измерения аэродинамического размера частиц можно использовать другие импакторы, такие как импактор нового поколения NEXT GENERATION IMPACTOR™ (NGI™, корпорация MSP), при этом определенная этим способом вдыхаемая фракция имеет аналогичные аэродинамические размеры, например <6,4 мкм. В некоторых вариантах осуществления для определения размера частиц применяют устройство с использованием дифракции лазерного излучения, например устройство с использованием дифракции лазерного излучения, раскрытое в американской заявке на патент 12/727179 (поданной 18 марта 2010, которая включена в настоящее описание во всей его полноте в части релевантной настоящему описанию), где для оценки эффективности ингаляционной системы измеряли волюметрический средний геометрический диаметр (VMGD) частиц. Например, в различных вариантах осуществления картриджа значение опустошения на ≥80%, 85% или 90% и VMGD испускаемых частиц ≤12,5 мкм, ≤7,0 мкм или ≤4,8 мкм могут указывать на улучшение аэродинамической характеристики. Раскрытые здесь варианты осуществления показывают, что микрочастицы ФДКП с удельной площадью поверхности менее чем примерно 67 м2/г демонстрируют характеристики, благоприятные для доставки лекарственных веществ в легкие, такие как улучшенная аэродинамическая характеристика.
[0036] Вдыхаемая фракция на порцию (RF/порция) представляет процент вылетающих частиц от полной дозы, размер которых является подходящим для доставки в легкие, которая является мерой аэродинамической характеристики микрочастиц. Как описано в настоящем документе, значение RF/порция, равное 40% или превышающее 40%, отражает приемлемые аэродинамические характеристики. В некоторых раскрытых здесь вариантах осуществления вдыхаемая фракция на порцию может превышать 50%. В приведенном в качестве примера варианте осуществления вдыхаемая фракция на порцию может доходить до примерно 80%, где примерно 80% порции вылетающих частиц имеет размер <5,8 мкм согласно измерениям с помощью стандартных методов.
[0037] Используемый здесь термин “сухой порошок” относится к мелкодисперсной композиции, которая не суспендирована и не растворена в пропелленте, носителе или другой жидкости. Это не означает обязательное полное отсутствие молекул воды.
[0038] Следует иметь в виду, что конкретное значение параметра RF/порция может зависеть от ингалятора, используемого для доставки порошка. Порошки, как правило, склонны к образованию агломератов, и кристаллические микрочастицы ДКП образуют особенно когезивные порошки. Одной из функций ингалятора для сухих порошков является разрушение агломератов порошка с тем, чтобы получающиеся в результате частицы содержали вдыхаемую фракцию, подходящую для доставки дозы при вдохе. Однако разрушение агломератов когезивных порошков обычно не бывает полным, поэтому гранулометрический состав частиц, наблюдаемый при измерении вдыхаемой фракции, доставляемой ингалятором, не будет соответствовать гранулометрическому составу первичных частиц, т.е. профиль будет сдвинут в сторону более крупных частиц. Конструкции ингаляторов различаются по своей эффективности разрушения агломератов, и таким образом абсолютное значение RF/порция, наблюдаемое для разных конструкций, также меняется. Однако оптимальное значение параметра RF/порция как функция удельной площади поверхности может быть аналогичным для разных ингаляторов.
[0039] Используемый здесь термин “примерно” применяется для указания того, что значение включает стандартное отклонение измерений, характерное для устройства или способа, используемого для определения данного значения.
[0040] Дикетопиперазины
[0041] Один из классов агентов для доставки лекарственных веществ, который использовался для решения проблемы в области фармацевтики, такой как нестабильность лекарственного вещества и/или слабая всасываемость, представляет собой 2,5-дикетопиперазины. 2,5-дикетопиперазины представлены соединением общей формулы 1, как показано ниже, где E1 и E2 представляют собой независимо N или более точно NH. В других вариантах осуществления E1 и/или E2 представляют собой независимо кислород или азот так, что, когда один из заместителей E1 или E2 является кислородом, а другой азотом, то согласно формуле получается аналог по заместителям дикетоморфолина, или, когда и E1 и E2 представляют собой кислород, то согласно формуле получается аналог по заместителям дикетодиоксана.
Формула 1
[0042] Как было показано, такие 2,5-дикетопиперазины могут использоваться для доставки лекарственного вещества, в частности, те из них, которые имеют кислые группы R1 и R2, как описано, например, в патентах США №№ 5352461 “Self-Assembling Diketopiperazine Drug Delivery System”; 5503852 “Method for Making Self-Assembling Diketopiperazine Drug Delivery System”; 6071497 “Microparticles for Lung Delivery Comprising Diketopiperazine” и 6331318 “Carbon-Substituted Diketopiperazine Delivery System”, каждая из которых включена в настоящее описание в виде ссылки во всей полноте той части, которая относится к дикетопиперазинам и доставке лекарственных веществ с помощью дикетопиперазинов. Дикетопиперазины могут быть сформированы в микрочастицы, которые включают лекарственное вещество, или микрочастицы, на которые может быть адсорбировано лекарственное вещество. Комбинация лекарственного вещества и дикетопиперазина может способствовать улучшению стабильности лекарственного вещества и/или характеристикам абсорбции. Эти микрочастицы могут вводиться различными путями введения. В виде сухих порошков эти микрочастицы можно доставлять с помощью ингаляции в определенные области дыхательной системы, включая легкие.
[0043] Такие микрочастицы обычно получают осаждением свободной кислоты (или основания) в условиях основных pH, что дает самоорганизующиеся микрочастицы, составленные из агрегированных кристаллических пластин. Стабильность частицы может быть увеличена с помощью небольшого количества сурфактанта, такого как полисорбат-80, в растворе ДКП, из которого были осаждены частицы (см., например, заявку на патент США 2007/0059373 “Method of drug formulation based on increasing the affinity of crystalline microparticle surfaces for active agents”, которая включена в настоящее описание во всей полноте в виде ссылки в части, относящейся к формированию и загрузке микрочастиц ДКП и их сухих порошков). В конечном счете растворитель может быть удален для получения сухого порошка. Соответствующие способы удаления растворителя включают лиофилизацию и сушку распылением (см., например, заявку на патент США 2007/0196503 “A method for improving the pharmaceutic properties of microparticles comprising diketopiperazine and an active agen” и патент США 6444226 “Purification and stabilization of peptide and protein pharmaceutical agents”, каждый из которых включен в настоящее описание во всей полноте в виде ссылки в части, относящейся к формированию и загрузке микрочастиц ДКП и их сухих порошков). Описанные здесь микрочастицы отличаются от микрочастиц, составленных из солей ДКП. Такие частицы обычно образуются (в противоположность высушенным) сушкой распылением, формируя сферы и/или деформированные сферы аморфной соли (в противоположность свободной кислоте или основанию) с тем, чтобы они были химически, физически и морфологически отдельными единицами. Настоящее раскрытие относится к ФДКП, которое следует рассматривать как свободную кислоту или растворенный анион.
[0044] Способы синтеза дикетопиперазинов описаны, например, у Katchalski и др., J. Amer. Chem. Soc. 68, 879-880 (1946) и Kopple и др., J. Org. Chem. 33 (2), 862-864 (1968), содержание которых полностью включено в настоящее описание в виде ссылки. 2,5-Дикето-3,6-ди(аминобутил)пиперазин (у Katchalski и др. он назван ангидридом лизина) также может быть получен через циклодимеризацию N-ε-P-L-лизина в расплавленном феноле аналогично способу Коппле (Kopple) с последующим удалением блокирующих (P)-групп с использованием соответствующих реагентов и условий. Например, CBz-защитная группа может быть удалена с помощью 4,3 М HBr в уксусной кислоте. Этот путь может быть предпочтительным, поскольку в нем используется коммерчески доступный исходный материал, реакция протекает в условиях, в которых согласно данным сохраняется стереохимия исходных материалов в продукте, и все стадии могут быть легко увеличены в объеме для использования в промышленном масштабе. Способы синтеза дикетопиперазинов также описаны в патенте США 7709639 “Catalysis of Diketopiperazine Synthesis”, который также включен в настоящее описание в виде ссылки.
[0045] Фумарилдикетопиперазин (бис-3,6-(N-фумарил-4-аминобутил)-2,5-дикето-дикетопиперазин; ФДКП) представляет собой предпочтительный дикетопиперазин для введения в легкие:
[0046] ФДКП обеспечивает благоприятную матрицу микрочастиц благодаря низкой растворимости в кислоте, которая при этом хорошо растворяется в условиях нейтрального или основного pH. Эти свойства позволяют кристаллизовать ФДКП и способствуют самоорганизации кристаллов в микрочастицы в кислых условиях. Частицы легко растворяются в физиологических условиях с нейтральным pH. Как отмечалось выше, микрочастицы, имеющие диаметр от примерно 0,5 до примерно 10 микрон, могут достигать легких, успешно преодолевая большинство естественных барьеров. Частицы такого размера могут быть легко получены из ФДКП.
[0047] Как отмечалось выше, микрочастицы, имеющие диаметр от примерно 0,5 до примерно 10 микрон, могут достигать легких, успешно преодолевая большинство естественных барьеров. Частицы такого размера могут быть легко получены из дикетопиперазинов с кислыми группами, такими как карбоксилатные группы в ФДКП (а также в родственных молекулах, таких как 2,5-дикето-3,6-ди(4-X-аминобутил)пиперазин, где X представляет собой сукцинил, глутарил или малеил). В случае осаждения в кислой среде формируются самоорганизующиеся частицы, составленные из агрегатов кристаллических пластин. Размер этих пластин связан с удельной площадью поверхности частиц, которая в свою очередь влияет на ст