Соединения иттербия с o,n-хелатным гетероциклическим лигандом, люминесцирующие в ик-области, и органический ик-излучающий диод с использованием указанных соединений в качестве эмиссионного слоя
Иллюстрации
Показать всеИзобретение относится к новым химическим соединениям иттербия, люминесцирующим в ближней ИК-области, в частности к соединениям иттербия, содержащим, по меньшей мере, один O,N-хелатный гетероциклический лиганд. Лиганд представляет собой кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов и в орто-положении азольный заместитель с гетероатомом Х (где Х - сера, или кислород, или NH). Соединения имеют общую формулу I
где 1 - кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов; 2 - азольный заместитель с гетероатомом, являющийся 1-бензотиазольным, 1-бензоимидазольным или 1-бензоксазольным фрагментом. Также предложен органический светоизлучающий диод. Изобретение позволяет получить соединения иттербия, проявляющие люминесценцию в ближней ИК-области. 2 н. и 6 з.п. ф-лы, 1 ил., 1 табл., 3 пр.
Реферат
Заявляемое изобретение относится к новым химическим соединениям иттербия, люминесцирующим в ближней ИК-области, в частности к комплексам с O,N-хелатным гетероциклическим лигандом, представляющим собой кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов и в орто-положении азольный заместитель с гетероатомом Х (где Х - сера, или кислород, или NH), общей формулы I
где 1 - кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов; 2 - азольный заместитель с гетероатомом, являющийся 1-бензотиазольным, 1-бензоимидазольным или 1-бензоксазольным фрагментом.
Изобретение относится также к области полупроводниковой оптоэлектроники, а именно к твердотельным источникам ИК-излучения на основе органических светоизлучающих диодов (OLED - Organic Light Emitting Diodes), которые используются для создания экономичных и эффективных источников ИК-излучения.
Спектральный диапазон, эффективность и интенсивность излучения OLED зависят от использованных при их производстве эмиссионных материалов. Особый интерес представляют люминесцентные материалы, излучающие в ИК-области, которые могут быть использованы для создания органических светодиодов, в лазерной технике в качестве источников накачки и активных сред, в медицинской диагностике в качестве люминесцентных меток и других областях. Поэтому задача поиска и исследования новых эффективных и устойчивых ИК-люминесцирующих материалов является одной из приоритетных.
Несмотря на большие успехи, достигнутые в области органических светоизлучающих диодов, задача поиска и исследования новых органических материалов, проявляющих электролюминесцентные свойства в ИК-области, остается в настоящий момент чрезвычайно актуальной. Известно, что соединения иттербия обладают ИК-люминесценцией, которая может генерироваться в результате оптического или других видов возбуждения, например, электротоком (электролюминесценция) (см. М.Н. Бочкарев, А.Г Витухновский, М.А. Каткова. "Органические светоизлучающие диоды (OLED)", Нижний Новгород, 2011, стр.272). Наиболее проблемной областью органических светодиодов, излучающих в ИК-диапазоне, является их недостаточно высокая эффективность. Лучшие на сегодня рабочие характеристики ИК-излучающих диодов на основе органолантаноидных соединений получены на тетрафенилпорфириновых соединениях иттербия (интенсивность 10 мкВт/см2, внешний квантовый выход 0,013% (см. Chem. Mater., 16 (2004) 2938) и трис[2-(1,3-бензоксазол-2-ил)фенолят] иттербия (максимальная интенсивность излучения 286 мкВт/см2, эффективность по мощности при 12 В составляет 1.22 мВт/Вт (см. J. Mater. Chem., 21 (2011) 16611).
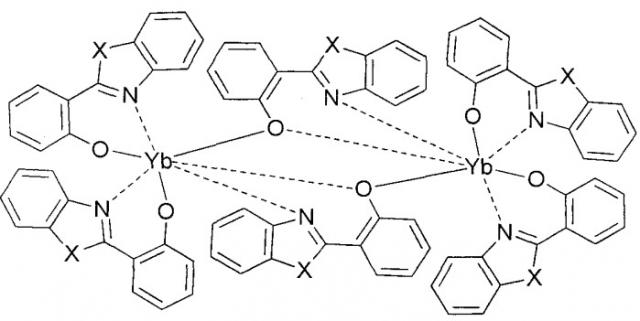
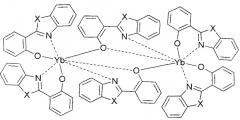
Наиболее близкими по сущности и достигаемому эффекту являются комплексы иттербия состава Yb(ХОМ)3 с димерной структурой Yb2(OON)6 - (2-(2-бензоксазол-2-ил)фенолят), Yb2(SON)6 - (2-(2-бензотиазол-2-ил)фенолят) и Yb2(NON)6 - (2-(2-бензоимидазол-2-ил)фенолят) общей формулы:
где X=О, или S, или NH, которые обладают ИК-люминесценцией (см. J. Mater. Chem., 21 (2011) 16611).
В этом же источнике описан органический светоизлучающий диод конфигурации ITO/TPD/Yb-complex/BATH/Yb (ITO - оксид индия, допированный оловом, TPD - N,N'-бис(3-метилфенил)-N,N'-дифенилбензидин, BATH - 4,7-дифенил-1,10-фенантролин), на котором определяли электролюминесцентные свойства известных упомянутых соединений. Известный органический светоизлучающий диод, на котором получены лучшие характеристики (максимальная интенсивность излучения 286 мкВт/см2, эффективность по мощности при 12 В составляет 1.22 мВт/Вт), содержит несущую основу, выполненную в виде стеклянной подложки с размещенным на ней прозрачным слоем анода ITO (100 нм, 20 Ом/см2), на котором расположен слой органического вещества с дырочной проводимостью TPD (70 нм), затем расположен излучающий (эмиссионный) слой (40 нм) из одного из комплексов иттербия с гетероциклическими лигандами Ln2(XON)6, описанных выше, затем расположен слой дырочно-блокирующего материала BATH, а поверх органических слоев расположен слой катода, выполненный из металлического иттербия (150 нм). Упомянутое устройство взято в качестве прототипа.
Задачей, на решение которой направлено заявляемое изобретение, является расширение арсенала химических соединений, проявляющих люминесценцию в ближней ИК-области, увеличение интенсивности и эффективности ИК-люминесценцирующих материалов, и создание на их основе органических ИК-излучающих диодов с высокими рабочими характеристиками за счет использования нового химического вещества эмиссионного слоя.
Эта задача решается за счет того, что получены новые химические соединения иттербия с O,N-хелатным гетероциклическим лигандом, представляющим собой кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов и в орто-положении азольный заместитель с гетероатомом Х (где Х - сера, или кислород, или NH), общей формулы I.
где 1 - кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов; 2 - азольный заместитель с гетероатомом, являющийся 1-бензотиазольным, 1-бензоимидазольным или 1-бензоксазольным фрагментом.
Лиганд представляет собой кислотный остаток ароматического спирта, замещенного в орто-положении азольным заместителем, таким образом, что в комплексе осуществляется хелатное O,N-связывание с ионом иттербия. При этом ароматическими спиртами, имеющими от 2 до 4 конденсированных шестичленных углеродных циклов, могут быть нафтолы (два конденсированных шестичленных углеродных цикла), или антраценолы или фенантренолы (три конденсированных шестичленных углеродных цикла), или бензантраценолы или пиренолы (четыре конденсированных шестичленных углеродных цикла). При использовании ароматических спиртов с числом конденсированных шестичленных углеродных циклов более 4 возникают технологические сложности при синтезе, связанные с низкой растворимостью исходных соединений. Заместителями в орто-проложении могут быть 1-арилоксазолятные, 1-арилтиазолятные или 1-арилимидазолятные фрагменты.
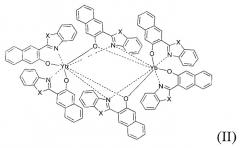
Получены соединения, являющиеся димерными комплексами иттербия с 2-(1,3-бензокс(ти, имид)азол-2-ил)-3-нафтолятными лигандами формулы II
(где Х=О, или S, или NH), в которых ароматический спирт выбран из ряда нафтолов, содержащих 2 конденсированных шестичленных углеродных цикла и является 2-нафтолом, а в opто-положении находится азольный заместитель с гетероатомом, являющийся 1-бензотиазолильным, 1-бензоимидазолильным или 1-бензоксазолильным фрагментом.
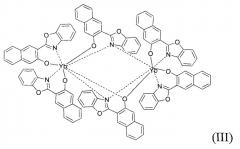
Получено соединение [2-(1,3-бензоксазол-2-ил)-3-нафтолят]иттербия формулы III.
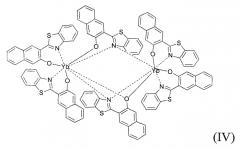
Получено соединение [2-(1,3-бензотиазол-2-ил)-3-нафтолят]иттербия формулы IV.
Получено соединение [2-(1,3-бензимидазол-2-ил)-3-нафтолят]иттербия формулы V
Также могут быть получены соединения, в которых число конденсированных шестичленных углеродных циклов в ароматическом спирте более двух (3 или 4). Заявителем были получены и описаны соединения, содержащие фрагмент формулы I. В этих соединениях тип связывания лиганда с металлом, соответствующий общей формуле I, идентичен. Все они имеют димерную структуру, доказанную методом рентгеноструктурного анализа (см. прототип - J. Mater. Chem., 21 (2011) 16611).
Также могут быть получены соединения, в которых азольными заместителями с гетероатомами, находящимися в орто-положении ароматического спирта, являются нафтотиазолильные нафтоимидазолильные и нафтооксазолильные фрагменты. Заявителем были получены и описаны соединения, содержащие фрагмент формулы I. В этих соединениях тип связывания лиганда с металлом, соответствующий общей формуле I, идентичен. Все они имеют димерную структуру, доказанную методом рентгеноструктурного анализа (см. прототип - J. Mater. Chem., 21 (2011) 16611).
Заявляемые соединения представляют собой комплексы с гетероциклическим лигандом, являющимся кислотным остатком ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов и в орто-положении азольный заместитель с гетероатомом, хелатно (O,N)-связанный с атомом иттербия.
Лиганд состоит из двух фрагментов - ароматического спирта и гетероциклического азольного фрагмента, который в качестве гетероатома содержит кислород, или серу, или NH.
Способ получения соединений заключается во взаимодействии трис-триметилсилиламида иттербия с ароматическим спиртом, в орто-положении которого находится азольный гетероциклический фрагмент.
где Х - кислород, или сера, или NH.
Заявителем были изготовлены органические светоизлучающие диоды, в которых эмиссионный слой выполнен из новых соединений иттербия - димерных трис[2-(1,3-бензоксазол-2-ил)-3-нафтолят]иттербия или трис[2-(1,3-бензотиазол-2-ил)-3-нафтолят]иттербия (см. таблицу ниже).
Задача изобретения также решается за счет того, что изготовлен органический светоизлучающий диод, содержащий несущую основу, выполненную в виде стеклянной подложки с размещенным на ней прозрачным слоем анода, на котором расположен, по меньшей мере, органический излучающий (эмиссионный) слой, содержащий [2-(1,3-бензотиазол-2-ил)-3-нафтолят]иттербия (формула III) или [2-(1,3-бензоксазол-2-ил)-3-нафтолят]иттербия (формула IV), поверх которого расположен металлический катод, выполненный, например, из иттербия.
Предпочтительно наличие в устройстве слоя органического вещества с дырочно-проводящими свойствами, расположенного между эмиссионным слоем и анодом. Роль этого слоя заключается в облегчении инжекции дырок из анода в эмиссионный слой, а также в блокировании электронов в эмиссионном слое. В качестве материала дырочно-транспортного слоя используют соединения, обладающие высокой дырочной проводимостью, например N,N'-бис(3-метилфенил)-N,N'-дифенилбензидин.
Предпочтительно наличие в устройстве слоя органического вещества с электронно-проводящими и дырочно-блокирующими свойствами, расположенного между эмиссионным слоем и катодом. Роль этого слоя заключается в облегчении инжекции электронов из катода в эмиссионный слой, а также в блокировании дырок в эмиссионном слое. В качестве материала электронно-транспортного (дырочно-блокирующего) слоя используют соединения, обладающие хорошей электронной проводимостью, например, 4,7-дифенил-1,10-фенантролин.
В качестве несущей основы могут быть использованы стеклянные или пластмассовые подложки. Стеклянные подложки с размещенным на них слоем анода, материалом которого традиционно является оксид индия, допированный оловом, выпускаются промышленностью. В заявляемом устройстве используются упомянутые подложки. При этом в качестве материала анода могут быть использованы другие соединения, обладающие высокой инжекцией дырок (например, прозрачные оксиды галлия и цинка, нитриды титана и галлия и др.) Электролюминесцентный (эмиссионный) слой является средой, в которой непосредственно происходит соединение инжектированных в него электронов и дырок с образованием электронно-дырочных пар (экситонов). При схлопывании экситонов возникают возбужденные электроны, релаксация из которых (возвращение в основное состояние) может происходить с выбросом кванта света. Толщина эмиссионного слоя составляет 30-50 нм.
Опытным путем было установлено, что использование эмиссионного слоя, выполненного из трис[2-(1,3-бензотиазол-2-ил)-3-нафтолята] иттербия, улучшает рабочие характеристики устройства по сравнению с прототипом.
Заявителем были изготовлены для сравнения органические светоизлучающие диоды, в одном из которых эмиссионный слой выполнен из трис[2-(1,3-бензоксазол-2-ил)-3-нафтолята]иттербия, Yb2(NpOON)6 (см. формулу III), а в другом из трис[2-(1,3-бензотиазол-2-ил)фенолята]иттербия, Yb2(NpSON)6 (см. формулу IV), и определены их технические характеристики (см. таблицу).
| Таблица | ||||
| Комплекс | Квантовая эффективность, % | Эффективность по мощности, (мВт/Вт) | Максимальная интенсивность, мкВт | Рабочее напряжение, В |
| Yb2(NpOON)6 | 1.1 | 0.86 | 632 | 12 |
| Yb2(NpSON)6 | 3.2 | 1.83 | 1777 | 12 |
| Yb2(SON)6 (прототип) | - | 1.22 | 286 | 12 |
Из таблицы видно, что при использовании устройства с эмиссионным слоем, выполненным из трис[2-(1,3-бензотиазол-2-ил)-3-нафтолята] иттербия, в сравнении с прототипом, в котором упомянутый слой выполнен из трис[2-(1,3-бензотиазол-2-ил)фенолята]иттербия, Yb2(SON)6 эффективность по мощности увеличивается с 1.22 до 1.83 мВт/Вт, а максимальная интенсивность ИК-излучения увеличивается с 286 до 1777 мкВт/см2.
Улучшение рабочих характеристик при использовании эмиссионного слоя из новых соединений можно объяснить, по-видимому, внутримолекулярными окислительно-восстановительными процессами, протекающими при пропускании через люминесцентное вещество электрического тока и включающими образование на промежуточных стадиях катионов двухвалентного иттербия. Теоретические подходы не позволяют предсказать обнаруженный эффект, т.е. полученный результат является неочевидным для решения поставленной задачи и явным образом не следует из уровня техники.
Пример 1. Трис[2-(1,3-бензоксазол-2-ил)-3-нафолят] иттербия.
К раствору 1 ммоля трис(триметилсилиламида) иттербия, Yb[N(SiMe3)2]3, в 20 мл тетрагидрофурана прибавляют раствор 3 ммоля 2-(1,3-бензоксазол-2-ил)-3-нафтола в 10 мл тетрагидрофурана при перемешивании в течение 30 минут. Реакционную смесь перемешивают еще 30 минут при комнатной температуре, после чего растворитель и летучие продукты реакции удаляют в вакууме. Образовавшийся твердый остаток промывают толуолом и после перекристаллизации из диметилформамида выделяют целевой продукт в виде светло-желтых кристаллов с Тпл>350°C. Вычислено: C102H60N6O12Yb2: С 64.22, Н 3.17, N 4.41, Yb 18.14. Найдено: С 64.28, Н 3.07, N 4.35, Yb 18.23. ИК-спектр (вазелиновое масло, см-1): 3047 (пл), 1625 (с), 1606 (ср), 1592 (с), 1528 (с), 1489 (сл), 1378 (ср), 1338 (с), 1305 (сл), 1274 (ср), 1258 (сл), 1245 (ср), 1214 (ср), 1174 (с), 1145 (ср), 1033 (с), 918 (сл), 895 (с), 862 (ср), 831 (с), 779 (сл), 760 (с), 631 (ср), 497 (ср).
Пример 2. Трис[2-(1,3-бензотиазол-2-ил)-3-нафтолят] иттербия
К раствору 1 ммоля трис(триметилсилиламида) иттербия Yb[N(SiМе3)2]3 в 20 мл тетрагидрофурана прибавляют 3 ммоля 2-(1,3-бензотиазол-2-ил)-3-нафтола в 10 мл тетрагидрофурана при перемешивании в течение 30 минут. Реакционную смесь перемешивают еще 30 минут при комнатной температуре, после чего растворитель и летучие продукты реакции удаляют в вакууме. Твердый остаток промывают толуолом и после перекристаллизации из диметилформамида выделяют целевой продукт в виде желтых кристаллов с Тпл>350°C. Вычислено: С102Н60N6О6S6Yb2: С 61.13, Н 3.02, N 4.19, Yb 17.26. Найдено: С 61.11, Н 3.02, N 4.20, Yb 17.28. ИК-спектр (вазелиновое масло, см-1): 3053 (пл), 1627 (с), 1590 (с), 1490 (с), 1476 (с), 1345 (с), 1318 (сл), 1275 (ср), 1255 (сл), 1187 (ср), 1144 (ср), 1126 (ср), 1077 (ср), 1014 (ср), 952 (ср), 922 (сл), 861 (ср), 807 (сл), 755 (с), 628 (ср), 567 (сл), 500 (сл).
Пример 3. Трис[2-(1H-бензимидазол-2-ил)-3-нафтолят]иттербия.
К раствору 1 ммоля трис(триметилсилиламида) иттербия Yb[N(SiMe3)2]3 в 20 мл тетрагидрофурана прибавляют 3 ммоля 2-(1H-бензимидазол-2-ил)-3-нафтола в 10 мл тетрагидрофурана при перемешивании в течение 30 минут. Реакционную смесь перемешивают еще 30 минут при комнатной температуре, после чего растворитель и летучие продукты реакции удаляют в вакууме. Твердый остаток промывают толуолом и после перекристаллизации из диметилформамида выделяют целевой продукт в виде бесцветных кристаллов с Тпл>350°С. Вычислено: C102H66N12O6Yb2: С 64.42, Н 3.50, N 8.84, Yb 18.19. Найдено: С 64.39, Н 3.51, N 8.83, Yb 18.20. ИК-спектр (вазелиновое масло, см-1): 3390 (ср), 3286 (ср), 1623 (ср), 1602 (с), 1560 (ср), 1528 (ср), 1317 (с), 1268 (с), 1135 (ср), 1098 (cл), 1040 (ср), 850 (с), 803 (ср), 747 (с).
На чертеже изображен органический светоизлучающий диод, содержащий несущую основу, выполненную в виде стеклянной подложки 1 с размещенным на ней прозрачным слоем анода 2 - источника дырок, выполненным из оксида индия, допированного оловом. На аноде расположен слой органического вещества с дырочной проводимостью 3 -слой проводника дырок, выполненный из N,N'-бис(3-метилфенил-N,N'-дифенилбензидина) толщиной 20 нм. Затем следуют излучающий (эмиссионный) слой 4, выполненный из трис[2-(1,3-бензотиазол-2-ил)-3-нафтолят] иттербия или трис[2-(1,3-бензоксазол-2-ил)-3-нафтолята]иттербия, который является средой, где непосредственно происходит соединение инжектированных в него электронов и дырок и образование квантов света. Затем следует электронно-транспортный слой 5, который одновременно выполняет дырочно-блокирующую функцию, выполненный из 4,7-дифенил-1,10-фенантролина толщиной 20 нм. Поверх органических слоев расположен слой катода 6 - источник электронов, выполненный из иттербия. Толщина эмиссионного и катодного слоев составляет 50 и 200 нм соответственно.
Устройство работает следующим образом. При подаче напряжения минусом к катоду 6, а плюсом к аноду 2 из них инжектируются соответственно электроны и дырки, т.е. отрицательные и положительные заряды. В излучающем слое 4 происходит рекомбинация этих зарядов, что вызывает эффект электролюминесценции (излучение света). В качестве несущей основы 1 устройства использовали выпускаемую промышленностью стеклянную подложку с размещенным на ней прозрачным слоем оксида индия, допированного оловом, выполняющего функцию анода. Для получения органических пленок материалов слоев, входящих в структуру заявляемого OLED и слоя катода, использовали метод термического испарения в вакууме.
Заявляемое устройство с использованием в качестве эмиссионного слоя заявляемых соединений иттербия характеризуется высокими техническими характеристиками: интенсивность излучения 1777 мкВт/см2 при напряжении 19 В, эффективность по мощности составляет 1.83 мВт/Вт. Внешний квантовый выход заявляемого органического светоизлучающего диода составляет 3.2% при плотности тока 30 мА/см2.
Создание нового материала расширяет арсенал химических соединений, проявляющих высокие электролюминесцентные свойства, что позволяет использовать его в качестве эмиссионного слоя в органических ИК-излучающих диодах для улучшения их рабочих характеристик.
1. Соединения иттербия, содержащие, по меньшей мере один O,N-хелатный гетероциклический лиганд, представляющий собой кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов и в орто-положении азольный заместитель с гетероатомом Х (где Х - сера, или кислород, или NH), общей формулы I где 1 - кислотный остаток ароматического спирта, имеющего от 2 до 4 конденсированных шестичленных углеродных циклов; 2 - азольный заместитель с гетероатомом, являющийся 1-бензотиазольным, 1-бензоимидазольным или 1-бензоксазольным фрагментом.
2. Соединения по п.1, которые представляет собой димерные комплексы иттербия с 2-(1,3-бензокс(ти, имид)азол-2-ил)-3-нафтолятными лигандами формулы II где Х=О, или S, или NH, в которых ароматический спирт выбран из ряда нафтолов, содержащих 2 конденсированных шестичленных углеродных цикла и является 2-нафтолом, а в орто-положении находится азольный заместитель с гетероатомом, являющийся 1-бензотиазолильным, или 1-бензоимидазолильным, или 1-бензоксазолильным фрагментом.
3. Соединение по п.2, которое представляет собой димерный комплекс [2-(1,3-бензоксазол-2-ил)-3-нафтолят]иттербия формулы III
4. Соединение по п.2, которое представляет собой димерный комплекс [2-(1,3-бензтиазол-2-ил)-3-нафтолят]иттербия формулы IV
5. Органический светоизлучающий диод, содержащий несущую основу, выполненную в виде подложки с размещенным на ней прозрачным слоем анода, на котором расположен, по меньшей мере, излучающий (эмиссионный) слой, выполненный на основе комплекса иттербия, поверх излучающего слоя расположен катод, выполненный, например из металлического иттербия, отличающийся тем, что в качестве комплекса иттербия используется димеры трис[2-(1,3-бензоксазол-2-ил)-3-нафтолят]иттербия или трис[2-(1,3-бензотиазол-2-ил)-3-нафтолят]иттербия.
6. Органический светоизлучающий диод по п.5, отличающийся тем, что содержит слой органического вещества с дырочной проводимостью (дырочно-транспортный слой), выполненный, например, из N,N'-бис(3-метилфенил)-N,N'-дифенилбензидина, расположенный на слое анода.
7. Органический светоизлучающий диод по п.5, отличающийся тем, что содержит слой органического вещества с низкой дырочной проводимостью (дырочно-блокирующий слой), выполненный, например, из 4,7-дифенил-1,10-фенантролина, расположенный под слоем катода.
8. Органический светоизлучающий диод по п.5, отличающийся тем, что слой анода выполнен из оксида индия, допированного оловом.