Система и способ производства химической потенциальной энергии
Иллюстрации
Показать всеНастоящее изобретение относится к системе и способу производства химической потенциальной энергии и может быть использовано в производстве эффективного топлива, которое можно было бы использовать в чистых энергетических процессах, при которых не образуются и не выделяются парниковые газы и другие загрязнители окружающей среды. Система диссоциации газов включает сепаратор газовых компонентов, источник электронов, выполненный с возможностью испускания электронов, генератор электрического поля, анод и промежуточный электрод. Катод представляет собой термоионный катод. Генератор имеет энергию, достаточную для диссоциации молекул реагирующих газов. Анод расположен от катода на предварительно заданном расстоянии, ограничивающем реакционную газовую камеру. Газовая камера выполнена с возможностью вызывать взаимодействие между электронами и молекулами реагирующего газа. Промежуточный электрод расположен рядом с сепаратором и катодом. Промежуточный электрод выполнен с возможностью диссоциации молекул посредством электролиза на поверхности сепаратора с образованием продуктов. Молекулы реагирующего газа являются по меньшей мере молекулами одного из CO2 и H2O. Продуктами являются O2 и по меньшей мере один из CO и H2. Кроме того, способ диссоциации молекул газа включает подачу молекул реагирующих газов в реактор. Реактор содержит катод, анод и сепаратор между анодом и катодом. По способу создают электрическое поле между анодом и катодом, имеющее энергию, достаточную для диссоциации реагента и для восстановления молекул реагирующих газов с помощью электролиза. Способ также включает нагревание источника электронов, включающего термоионный катод, для высвобождения из него свободных электронов. Затем происходит разделение O2 и молекул других продуктов и выпуск молекул продукта. Молекулы газа являются по меньшей мере молекулами одного из CO2 и H2O. Продукт состоит из O2 и по меньшей мере одного из CO и H2, либо смеси CO и H2. Техническим результатом изобретений является обеспечение низкозатратного высоэффективного цикла, который может быть использован в крупном масштабе для получения топлива без выброса CO2 в окружающую среду. 5 н. и 62 з.п. ф-лы, 9 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение в целом относится к системе и способу производства химической потенциальной энергии.
ССЫЛКИ
Для понимания предпосылок создания настоящего изобретения уместными являются следующие ссылки:
1. Rubin, R., Karni, J. and Yeheskel, J., (2004) “Chemical Kinetics Simulation of High Temperature Hydrocarbons Reforming Using a Solar Reactor (Моделирование химической кинетики высокотемпературного риформинга углеводородов с использованием солнечного реактора),” J. Solar Energy Engineering 126(3), pp.858-866.
2. Fletcher, E.A., (2001) “Solar-thermal Processing: A Review (Солнечная тепловая технология: Обзор),” J. Solar Energy Engineering 123(2), pp 63-74.
3. Steinfeld, A., (2005) “Solar Thermochemical Production of Hydrogen - a Review (Солнечное термохимическое производство водорода - Обзор),” Solar Energy, 78, pp.603-615.
4. Epstein M., Olalde G., Santen S., Steinfeld A., Wieckert C, (2006) “Towards an Industrial Solar Carbothermic Production of Zinc (К вопросу о солнечном карботермическом производстве цинка),” 13th International Symposium on Concentrating Solar Power and Chemical Energy Technologies, Seville, June 2006, ISBN: 84-7834-519-1, paper #FB2-S6.
5. Yoneyama, H., (1997) “Photoreduction of carbon dioxide on quantized semiconductor nanoparticles in solution (Фотовосстановление диоксида углерода на квантуемых полупроводниковых наночастицах в растворе),” Catalysis Today, 39(3), pp.169-175.
6. Kaneco, S., Kurimoto H., Shimizu Y., Ohta K. and and Mizuno Т., (1999) “Photocatalytic reduction of CO2 using TiO2 powders in supercritical fluid CO2 (Фотокаталитическое восстановление CO2 с помощью порошкообразного ТЮз в сверхкритической среде CO2)” Energy, 24(1), pp.21-30.
7. Jun Akikusa, S.U.M.K., (2002) “Photoelectrolysis of water to hydrogen in p-SiC/Pt and p-SiC/n-TiO2 cells (Фотоэлектролиз воды с образованием водорода в р-SiC/Pt и p-SiC/n-TiO2 ячейках),” Int. J. Hydrogen Energy 27, pp.863-870.
8. G.В. Stevens, T. Reda, В. Raguse, (2002) “Energy storage by the electro chemical reduction of CO2 to CO at a porous Au film (Накопление энергии путем химического восстановления CO2 до CO на пористой Au пленке)”, Journal of Electrochemical Chemistry, 526, pp.125-133.
9. Hori Y., Ito H., Okano K., Nagasu K. and Sato S, (2003) “Silver-coated ion exchange membrane electrode applied to electrochemical reduction of carbon dioxide (Электрод с ионообменной мембраной с серебряным покрытием для электрохимического восстановления диоксида углерода)”, Electrochimica Acta, 48, pp.2651-2657.
10. Dey G. R., Belapurkar A.D. and Kishore K., (2004) “Photo-catalytic reduction of carbon dioxide to methane using TiO2 as suspension in water (Фотокаталитическое восстановление диоксида углерода до метана с использованием TiO2 в виде водной суспензии)”, Journal of Photochemistry and Photobiology A: chemistry, 163, pp.503-508.
11. Eguchi K., Hochino T. and Fujihara, (1995) “Performance Analysis of FGM-Based Direct Energy Conversion System for Space Power Applications (Анализ характеристик системы прямого преобразования энергии на основе FGM (функционально-градиентного материала) для применений в области космической энергетики),” Proceedings of FGM '94, edited by В. llschner and N. Cherradi (Polytechnic University Romandes Press, Lausanne, Switzerland, 1995), pp.619-625.
12. Naito H., KohsakaY., Cooke D. and Arashi H., (1996) “Development of a Solar Receiver for a High-Efficiency Thermionic/Thermoelectric Conversion System (Усовершенствование приемника солнечного излучения для высокоэффективной системы термоионного/термоэлектрического преобразования),” Solar Energy, 58, No. 4-6, pp.191-195.
13. Ibragimova L.В., Smekhov G.D., Shatalov O.P., Eremin A.V. and Shumova V.V., (2000) “Dissociation of CO2 Molecules in a Wide Temperature Range (Диссоциация молекул CO2 в широком диапазоне температур),” High Temperature, Vol.38, No.1, pp 33-36.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Широкомасштабное низкозатратное производство эффективного топлива, которое можно было бы использовать в по сути чистых энергетических процессах, то есть процессах, при которых не образуются и не выделяются парниковые газы и другие загрязнители окружающей среды, является сложной задачей.
Для получения водорода из углеводородов широко используют паровой риформинг. Паровой риформинг природного газа с водяным паром, иногда называемый паровым риформингом метана (SMR), является наиболее общим способом получения основной массы промышленного водорода, а также водорода, используемого для промышленного синтеза аммиака.
Паровой риформинг метана и других углеводородов (реакция 1, ниже) сопровождается, как правило, реакцией конверсии водяного пара с конверсией CO в H2. Синтез-газ (то есть синтетическая смесь водорода и окиси углерода), образующийся при риформинг-процессе, может использоваться в качестве обогащенного газового топлива либо может быть превращен в жидкое топливо, такое как метанол. Метан СН4 может быть преобразован под действием водяного пара либо диоксида углерода с образованием смеси окиси углерода и водорода (синтез-газа) следующим образом:
C H 4 + H 2 O ⇔ C O + 3 H 2 Δ H = 206 ,2 кДж/моль (1)
C H 4 + C O 2 ⇔ 2 C O + 2 H 2 Δ H = 247 ,3 кДж/моль (2)
где ΔН - энтальпия реакции. При высоких температурах (700-1100°C) и в присутствии катализатора на основе металла водяной пар реагирует с метаном с образованием окиси углерода и водорода.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Одним из способов производства чистого топлива является широко изучаемый солнечный риформинг метана [1]. Для получения энергии по требованию приведенная выше реакция (2) может быть реверсирована для работы в замкнутом цикле и, таким образом, для обеспечения средства для хранения и транспортировки солнечной энергии. Реакции с твердыми веществами, такими как оксиды металлов и углерод, при высокой температуре [2-4] обеспечивают другие солнечные термохимические циклы, позволяющие получать топливо без выделения в окружающую среду CO2.
Другой пример - простым способом производства экологически чистого топлива (водорода) является электролиз воды. Однако этот способ имеет низкий КПД вследствие необходимости использования электричества. Недавно Stoots, С.М., O′Brien, J.Е., Herring, J.S., Condie, K.G. and Hartvigsen, J.J. “Idaho National Laboratory Experimental Research in High Temperature Electrolysis for Hydrogen and Syngas Production (Национальная лаборатория экспериментальных исследований в области высокотемпературного электролиза для производства водорода и синтез-газа, Айдахо),” Proceedings of the 4th International Topical Meeting on High Temperature Reactor Technology (Материалы 4-ой Международной специализированной конференции по высокотемпературным реакторным технологиям) HTR2008, September 28 - October 1 (28 сентября - 1 октября), 2008, Washington, DC USA, предложили проведение высокотемпературного электролиза по возможности с использованием чистого источника энергии, такого как солнечное излучение. Более высокая температура снижает количество электричества, требующееся для проведения процесса.
Еще одним альтернативным способом является термолиз - нагревание вещества до температуры, при которой свободная энергия равна или больше нуля, и оно самопроизвольно диссоциирует [2]. Хотя для термолиза воды/водяного пара или диоксида углерода не требуется электрической энергии, при этом требуется создание очень высоких температур - выше 3000K и 2500K, соответственно.
Еще одним способом получения чистой энергии является фотокаталитический процесс, при котором не требуется использования ни электричества, ни высокой температуры. Согласно этому способу, фотон высокой энергии инициирует эндотермическую реакцию, при которой образуется топливо. Однако КПД такого способа является очень низким (около 1%) [5-7].
Многостадийные термохимические процессы не требуют использования электрической энергии и имеют удобные рабочие температуры. Например, общая эффективность преобразования тепла в водород при некоторых термохимических способах разложения воды может достигать 50% при диапазоне рабочих температур от средних до высоких (Т<1000°C). Однако эти процессы являются сложными и требуют работы с редкими, дорогостоящими и/или коррозионными материалами. Другие многостадийные термохимические процессы, протекающие при более высокой температуре, например, с помощью восстановления оксидов металлов, предложены авторами работы [4] и позднее Diver, R.В., Siegel, N.Р., Miller, J.E., Moss, T.A., Stuecker, J.N. и James, D.L., “Development of a Cr5 Solar Thermochemical Heat Engine Prototype (Развитие прототипа солнечного термохимического теплового двигателя Cr5),” Concentrated Solar Symposium (Симпозиум по концентрированной солнечной энергии), март 2008, Las Vegas, Nevada.
При электролизе CO2 могут использоваться различные металлические электроды, а также жидкие или твердые полимерные электролиты, как показано авторами работы [8] и позднее Stoots, С.М., O′Brien, J.E., Herring, J.S., Condie, K.G. и Hartvigsen, J.J. в Proceedings of the 4th International Topical Meeting on High Temperature Reactor Technology (Материалах 4-й Международной специализированной конференции по высокотемпературным реакторным технологиям) HTR2008, 28 сентября - 1 октября, 2008, Washington, DC USA. Максимальная эффективность не загрязняющей окружающую среду электролитической системы зависит от эффективности чистого источника электричества, например, фотоэлектрической системы. Во время электролиза на электродах может осаждаться углерод, что снижает их эффективность и в конечном итоге останавливает процесс.
Stevens et. al. [8] показали текущее восстановление 40% в течение 100 минут во время электрохимического восстановления CO2. В соответствии с их опытами максимальная эффективность накопления энергии газообразного CO (в качестве топлива) составила 35%.
Фотокаталитическое восстановление до CO под высоким давлением изучалось Hori et al. [9], а прямое восстановление CO2 до газообразного метана изучалось Dey et al. [10]. Эти процессы имеют низкую скорость восстановления и требуют использования дорогостоящих и/или коррозионных материалов.
В данной области техники существует необходимость в новом подходе, позволяющем обеспечить правильное решение для эффективного высокоскоростного способа производства экологически чистого и недорогого синтетического топлива.
Таким образом, согласно широкому аспекту изобретения, предложена система для получения одного или нескольких соединений с высокой химической потенциальной энергией, при этом система включает в себя: источник электронов, содержащий катод и выполненный с возможностью испускания электронов с помощью, например, термоионного (TI) эффекта; генератор электрического поля, генерирующий электрическое поле, достаточное для диссоциации молекул реагирующих газов CO2 и/или H2O; и анод, расположенный от катода на предварительно заданном расстоянии, ограничивающем реакционную газовую камеру, выполненную с возможностью вызывать взаимодействие между электронами и молекулами газов CO2 и/или H2O по механизму диссоциативного прилипания электронов (DEA) внутри камеры, такое, что электроны, имеющие требуемую энергию, разлагают молекулы газов CO2 и/или H2O до CO и/или H2 и O2. Молекулами реагирующих газов являются, таким образом, по меньшей мере молекулы одного из CO2 и H2O, а получаемыми соединениями являются O2 и по меньшей мере одно из CO и H2.
Согласно некоторым вариантам осуществления, генератор электрического поля подвергается воздействию тепловой энергии, излучаемой по меньшей мере одним из следующих источников: источником электронов или источником тепловой энергии.
Согласно некоторым вариантам осуществления изобретения, система включает в себя источник тепловой энергии (источник тепла), выполненный с возможностью подвода тепловой энергии (излучения) к источнику электронов, тем самым повышая температуру источника электронов и вызывая термоионную (TI) эмиссию электронов, и/или к генератору электрического поля (например, к одному или нескольким термоэлектрическим элементам и/или их каскадам, или к одному или нескольким двигателям Стирлинга) для создания электрического поля.
Таким образом, согласно некоторым вариантам осуществления, генератор электрического поля включает в себя по меньшей мере один термоэлектрический элемент и/или каскад термоэлектрических элементов и работает за счет использования разницы температур, создаваемой источником тепловой энергии. Или же генератор электрического поля включает в себя по меньшей мере один двигатель Стирлинга, работающий за счет использования разницы температур, создаваемой источником тепловой энергии.
Согласно некоторым вариантам осуществления изобретения, вместо непосредственно анода, описанного выше, система включает в себя промежуточный электрод расположенный рядом с сепаратором газовых компонентов (например, мембраной), причем оба они находятся между анодом и катодом. Такая конфигурация обеспечивает (a) дополнительное средство диссоциации CO2 или H2O посредством электролиза, и (b) средство для разделения образующихся CO и H2 с одной стороны, и O2 с другой стороны. Таким образом, промежуточный электрод выполнен с возможностью диссоциации молекул реагирующих газов посредством электролиза на поверхности сепаратора, при этом сепаратор газовых компонентов выполнен с возможностью разделения O2 и других образующихся соединений.
Входящим реагирующим газом является CO2 или H2O, или они оба. CO2 и H2O могут вводиться в процесс с одной сторону разделительной мембраны или с противоположных ее сторон. Продуктами, покидающими реакционную камеру, являются CO или H2, или их смесь. Ионами, проходящими через мембрану, являются отрицательно заряженные ионы кислорода или протоны (H+), или те и другие. Молекулы кислорода покидают систему со стороны анода.
Настоящее изобретение объединяет фото-, термические, электрические и химические (РТЕС) процессы для усовершенствования нового способа, максимального увеличения эффективности и коэффициента преобразования теплового излучения в химический потенциал в форме восстановления CO2 до CO и O2 и восстановления H2O до H2 и O2 в одной системе. Диссоциация CO2 и H2O может протекать в одной системе одновременно, или же любой из этих процессов может происходить один. Соотношение CO и H2 регулируют во время процесса, при этом смесь окиси углерода и водорода может использоваться непосредственно в качестве синтез-газа, газообразного топлива (например, на силовых или химических установках) или же может быть превращена в метанол либо другие углеводороды, которые могут быть использованы, например, в качестве транспортного топлива. CO2 и вода, образующиеся при сгорании такого топлива, могут улавливаться, возвращаться на силовую установку и снова подвергаться восстановлению. Такой способ позволяет получать экологически чистое топливо в широких масштабах везде, где доступна тепловая энергия.
Согласно некоторым вариантам осуществления, система включает в себя сепаратор газовых компонентов, выполненный с возможностью разделения ионов кислорода и молекул CO и/или H2, образующимися при диссоциации CO2 и/или H2O. Сепаратор может включать в себя мембрану, позволяющую только определенному газовому компоненту, такому как ионы кислорода (O-), проходить через нее (например, пропуская отрицательно заряженные ионы кислорода). Такие мембраны могут быть изготовлены из керамического материала, такого как, например, оксид циркония, стабилизированный оксидом иттрия (YSZ). Их поверхность, обращенная к камере, содержащей CO2, содержит катод, а другая поверхность содержит анод для извлечения электронов из ионов кислорода, прикрепленный к средству для переноса этих электронов обратно к катоду.
Согласно некоторым вариантам осуществления изобретения, CO2 и H2O подают в систему на катодную сторону мембраны. В этом случае сепаратор используют для отделения ионов O- от H2 и CO; он проводит ионы O- от катода к аноду. Коэффициенты диссоциации CO2 и H2O регулируют с помощью температурного режима и величины расхода CO2 и H2O, поступающих на катодную сторону.
Согласно еще одному варианту осуществления, CO2 подают в систему на катодную сторону мембраны, a H2O подают в систему на анодную сторону мембраны. В этом случае сепаратор может использоваться для отделения ионов H+ (протонов) от OH-. Этот же сепаратор может использоваться для проведения одновременно ионов O- с катодной стороны на анодную, а ионов H+ - с анодной стороны на катодную. Эта ионная проводимость может осуществляться в обоих направлениях одновременно, или же в каждом направлении по отдельности. Коэффициенты ионной проводимости O- и H+ регулируют с помощью температурного режима и величины расхода CO2 на катодной стороне и H2O - на анодной стороне.
Согласно еще одному варианту осуществления, система включает в себя источник тепловой энергии (источник тепла), выполненный с возможностью подачи тепловой энергии (например, концентрированного солнечного света) на нагревающие элементы по меньшей мере одного двигателя Стирлинга, генерирующего электрическое поле с относительно высокой эффективностью.
Согласно еще одному варианту осуществления, система включает в себя отдельное устройство для создания электрического поля (например, отдельную солнечную электрогенерирующую систему).
Термический (тепловой) источник может включать в себя коллектор солнечной энергии, который может, например, содержать набор отражателей, выполненных с возможностью накапливать солнечное излучение, концентрировать его и отражать его в сторону источника электронов.
Согласно некоторым вариантам осуществления изобретения, источник электронов включает в себя термоионный катод или фотокатод. Термоионный катод может быть связан с генератором электрического поля или отдельным генератором электрического поля, выполненным с возможностью переносить электрический потенциал на источник электронов, снижая потенциальный барьер катода и увеличивая число испущенных электронов.
Согласно некоторым вариантам осуществления, на термоионный катод наносят защитное покрытие для защиты его от воздействия газовой среды, содержащей CO2, CO, O- и O2. Защитное покрытие может включать в себя слой оксидов металлов и может быть выполнено с возможностью облегчать электронную трансмиссию при туннелировании путем снижения работа выхода материала катода.
Согласно некоторым вариантам осуществления изобретения, система включает в себя источник магнитного поля, выполненный с возможностью регулирования движения электронов, максимально увеличивая вероятность реакции диссоциативного прилипания электрон - CO2.
Согласно некоторым вариантам осуществления изобретения, газообразный CO2 перед входом в реакционную камеру предварительно нагревают с помощью газов и/или с помощью горячей стороны стенок реактора.
Согласно некоторым вариантам осуществления изобретения, газообразный CO2 возбуждают воздействием по меньшей мере одного из следующих излучений: электронного пучка (например, из лазерного источника), магнитного поля и электрического поля, что увеличивает его энергию колебаний по мере того, как он поступает в реакционную камеру. Это улучшает возможность реакции диссоциативного прилипания электрон - CO2.
Предпочтительно, чтобы система включала в себя коллектор электронов, выполненный с возможностью сбора испущенных электронов, не объединяющихся с молекулами CO2.
Система согласно изобретению работает с высокой эффективностью преобразования тепловой энергии в химический потенциал, оцениваемой выше 40%, и может использоваться при температурах в диапазоне приблизительно 600°C-1500°C.
Согласно некоторым вариантам осуществления, источник электронов, генератор электрического поля, реакционная газовая камера и мембрана объединены в единый модуль (например, ячейку).
Согласно другому широкому аспекту настоящего изобретения, также предложена система для получения одного или нескольких соединений с высокой химической потенциальной энергией. Система включает в себя источник электронов, содержащий катод и выполненный с возможностью испускания электронов; генератор электрического поля, создающий электрическое поле; анод, расположенный на расстоянии от катода; промежуточный электрод и сепаратор газовых компонентов, причем оба они расположены между анодом и катодом; промежуточный электрод, выполненный с возможностью разложения молекул реагирующих газов посредством электролиза на поверхности сепаратора; при этом молекулы реагирующих газов являются по меньшей мере молекулами одного из CO2 и H2O, образующимися соединениями являются O2 и по меньшей мере одно из CO и H2, соответственно.
Следует отметить, что система согласно настоящему изобретению обеспечивает один или несколько продуктов, имеющих относительно высокую энергию образования из одного или нескольких химических соединений, имеющих относительно низкую энергию образования. Химическая потенциальная энергия продуктов может быть трансформирована в другие формы энергии, такие как тепло, работа или электрическая энергия, при помощи химической реакции.
Согласно другому широкому аспекту настоящего изобретения, представлен способ получения одного или нескольких соединений с высокой химической потенциальной энергией. Способ включает в себя подачу молекул реагирующих газов CO2 (например, путем отделения его от других газообразных продуктов сгорания) и/или H2O в реактор, включающий в себя катод, анод и сепаратор между анодом и катодом; создание между анодом и катодом электрического поля, имеющего энергию, достаточную для диссоциации молекул реагирующих газов по механизму диссоциативного прилипания электронов (DEA) и/или восстановления молекул реагирующих газов с помощью электролиза; разделение O2 и молекул других продуктов; и выпуск молекул продуктов.
Диссоциацию/восстановление CO2 до CO и O2 и H2O до H2 и O2 можно выполнять следующим образом: источник электронов, включающий в себя термоионный катод, нагревают с помощью источника тепла для высвобождения из него свободных электронов; электроны испускаются из термоэлектронного катода за счет термоионного (TI) эффекта; создают электрическое поле, чтобы обеспечить энергетического поле, достаточное для диссоциации молекул газа за счет эффекта диссоциативного прилипания; вводят электроны и молекулы газа в реактор (например, в реакционную камеру), где электроны вызывают диссоциацию газовых молекул с образованием молекул продуктов.
Нагревание источника электронов предпочтительно включает в себя подачу тепловой энергии (например, солнечного излучения) на источник электронов, тем самым увеличивая температуру источника электронов и генерируя эмиссию термоэлектронов с термоионного катода. Создание электрического поля может включать в себя концентрирование тепловой энергии и направление ее на генератор электрического поля.
Термоионный (TI) эффект и создание электрического поля могут быть активированы с помощью того же источника тепловой энергии, например, концентратора солнечной энергии. Последний может включать в себя накопление солнечного излучения, концентрирование его и отражение в сторону источника электронов.
Согласно некоторым вариантам осуществления изобретения, молекулы газа могут быть предварительно нагреты перед введением их в реакционную камеру. Предварительный нагрев молекул газа может осуществляться с помощью того же источника тепловой энергии, выполненного с возможностью активировать термоионный (TI) эффект и создание электрического поля, например, с помощью по меньшей мере одного теплообменника.
Число испущенных электронов может быть увеличено путем приложения электрического поля к источнику электронов.
Отрицательно заряженные ионы кислорода могут проводиться через мембрану по направлению к коллектору электронов; избыток электронов, высвободившихся с помощью ионов кислорода, может объединяться с образованием молекул O2; при этом электроны могут быть рециклизованы обратно в источник электронов. Кроме того, электроны, не взаимодействующие с молекулами газа, также могут быть рециклизованы.
Согласно некоторым вариантам осуществления, электрическое поле может использоваться для осуществления электролиза газа (CO2 и/или H2O) на поверхности мембраны после или независимо от процесса диссоциативного прилипания. После электролиза ионы кислорода проводят через мембрану.
Способ включает в себя подачу молекул газообразных CO2 и H2O по одну сторону сепаратора или с противоположных сторон сепаратора.
Согласно некоторым вариантам осуществления, CO2 вводят с катодной стороны мембраны, тогда как Н2О вводят с анодной стороны мембраны. В этом случае диссоциация CO2 и H2O происходит с противоположных сторон мембраны, и мембрана проводит ионы кислорода от катода к аноду, а протоны (H+) от анода к катоду.
Согласно некоторым вариантам осуществления, способ включает в себя улавливание CO2 путем отделения CO2 от других газообразных продуктов сгорания и рециклизацию.
Способ может включать в себя нанесение покрытия на по меньшей мере часть термоионого катода для обеспечения возможности электронной трансмиссии посредством туннелирования.
Согласно другим вариантам осуществления, способ включает в себя воздействие на молекулы газа излучения или пучка электронов, магнитного либо электрического поля (например, флуктуации поля при различной ориентации) для увеличения энергии колебаний молекул газа.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
С целью понимания изобретения, а также чтобы представить, каким образом возможно его осуществление на практике, далее будут описаны варианты осуществления, исключительно в качестве неограничивающего примера, со ссылкой на прилагаемые графические материалы, где:
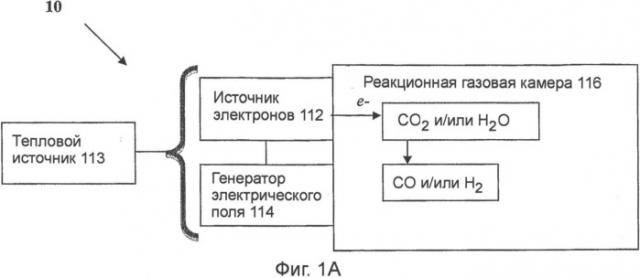
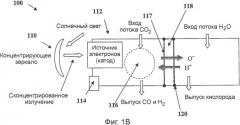
Фиг.1A и 1B схематически иллюстрируют блок-схему системы в соответствии с одним из вариантов осуществления настоящего изобретения;
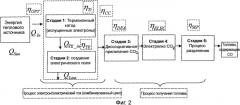
Фиг.2 схематически иллюстрирует схему технологических потоков предложенного способа согласно другому варианту осуществления настоящего изобретения;
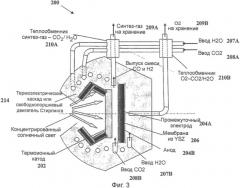
Фиг.3 схематически иллюстрирует пример конфигурации модуля системы настоящего изобретения;
Фиг.4 схематически иллюстрирует один из примеров использования газообразного СО для получения электричества с помощью замкнутого цикла CO2→CO→CO2.
На Фиг.5 представлены графики I-V (ток-напряжение) при разных температурах для электролитической ячейки, обеспечивающей диссоциацию O2;
На Фиг.6A и 6B показана термоионная эмиссия электронов в газообразном CO2 при температуре 1150°C (6A) и при температуре 1320°C (6B); и
Фиг.7 иллюстрирует концентрацию CO и H2 во время опытов с CO2 на катодной стороне и концентрацию влажного воздуха на анодной стороне при температуре ячейки приблизительно 650°C.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Фиг.1A представляет собой блок-схему основных функциональных элементов системы настоящего изобретения. Система 10 включает в себя источник 112 электронов, выполненный с возможностью испускания электронов, источник 112 электронов находится под воздействием источника 113 тепловой энергии, повышающего температуру источника 112 электронов; генератор 114 электрического поля, создающий электрическое поле, обеспечивающее энергетическое поле, достаточное для диссоциации молекул газа (CO2 и/или H2O), при этом генератор электрического поля находится под воздействием потока тепловой энергии от источника 113 тепловой энергии или от источника 112 электронов, или от них обоих; главную реакционную газовую камеру 116, выполненную с возможностью осуществлять взаимодействие между электронами и молекулами газов CO2 и/или H2O; так что электроны диссоциируют CO2 и/или H2O до CO и H2, соответственно, и отрицательно заряженных ионов кислорода посредством диссоциативного прилипания электронов (DEA) внутри камеры и/или путем электролиза.
Система и способ настоящего изобретения обеспечивают низкозатратный высокоэффективный цикл, который может быть использован в крупном масштабе для получения топлива без выброса CO2 в окружающую среду. Способ включает в себя улавливание CO2 → восстановление CO2 до CO в ходе чистого процесса → расходование непосредственно CO либо превращение его в другие виды топлива (например, метанол) и их расходование → улавливание CO2 и рециклизацию.
Способ согласно изобретению использует концентрированное тепловое излучение (например, солнечное излучение или другой источник тепла) для восстановления CO2 до CO и H2O до H2 методом диссоциативного прилипания электронов (DEA) и электролизом, используя серию взаимосвязанных стадий преобразования энергии, включающую (i) термоионную (TI) эмиссию электронов, (ii) создание разности потенциалов для обеспечения требуемого энергетического поля, используя при этом средства, преобразующие тепловое излучение в разность потенциалов, например, термоэлектрический (ТЕ) элемент, двигатель Стирлинга и так далее, (iii) восстановление CO2 и/или H2O с помощью диссоциативного прилипания электронов,
C O 2 + e − ⇒ C O 2 − ⇒ C O + O − ( 3 a ) ,
H 2 O + e − ⇒ H 2 O − ⇒ H 2 + O − ( 3 b ) ,
(iv) диссоциацию CO2 и/или H2O посредством электролиза, (v) разделение CO и кислорода, и (vi) рекомбинацию ионов кислорода и рециклизацию их электронов.
Согласно некоторым вариантам осуществления, при этом водяной пар, находящийся на анодной стороне мембраны, диссоциирует, и ионы H+ проводятся от анода к катоду, в то время как ионы O- проводятся от катода к аноду.
На Фиг.1B представлена более подробная блок-схема примера системы, в целом обозначенной как 100, имеющей конфигурацию и работающей в соответствии с изобретением. Система 100 включает в себя устройство 112, являющееся источником свободных заряженных частиц (электронов), подвергаемое воздействию солнечной энергии, предпочтительно, при посредстве коллектора 110 солнечной энергии; генератор 114 электрического поля; главную реакционную камеру 116; промежуточный катод 117; сепаратор 118 и анод 120, на котором электроны накапливаются и возвращаются в источник 112 электронов. Компоненты системы объединены в компактную ячейку. Благодаря взаимосвязи способов преобразования энергии система согласно настоящему изобретению использует практически всю входящую энергию (за вычетом потерь на обратное излучение) при любом механизме ее преобразования - термическом, электрическом или химическом.
Коллектор 110 солнечной энергии может включать в себя один или несколько отражателей (например, зеркал), которые накапливают и концентрируют солнечный свет и отражают его в сторону источника 112 электронов для повышения его температуры. Как показано в примере на Фиг.1B, коллектор 110 солнечной энергии может включать в себя одно зеркало, выполненное в форме параболического зеркала. Следует понимать, что вместо солнечного излучения может быть использован любой другой источник тепла, способный обеспечивать требуемую температуру и поток энергии к источнику электронов.
Источник электронов может быть высокоэффективным источником электронов, использующим термоионный эффект, функционирующим в газовой среде CO2/CO/O2/O-. Термоионный эффект относится к термоионной эмиссии потока заряженных электронов с нагретой поверхности, вызванной тепловой колебательной энергией, превосходящей электростатические силы, удерживающие электроны у поверхности. Источник электронов может быть образован с помощью термоионного катода, связанного с соответствующим электрическим полем, увеличивающим эмиссию электронов. Требуемые температуры могут достигаться за счет концентрирования солнечного излучения в сторону катода.
Срок службы некоторых таких катодов может составлять тысячи часов, однако в некоторых случаях предпочтительно, чтобы они были защищены (например, с помощью покрытия) от воздействия газовой среды. Некоторые из таких катодных материалов, предназначенные для эксплуатации при сильных токах, чувствительны к воздействию диоксида углерода, окиси углерода, кислорода и водорода. Вследствие этого катод может быть покрыт тонким слоем оксидов толщиной в несколько нанометров для защиты его поверхности от атомной и ионной бомбардировки. Кроме того, покрытие может обеспечивать возможность электронной трансмиссии посредством туннелирования, обеспечивая уменьшение эффективной работы выхода, в то же время защищая термоионный материал от газов, присутствующих в реакционной камере, а именно, CO2, CO, O- и O2. Могут использоваться некоторые комбинации металлов и их оксидов; такие как комбинации Al/оксид алюминия/Au или Al, комбинация Та/оксид тантала/Pt, титан/оксид титана, скандий/оксид скандия, цирконий/оксид циркония, вольфрам/оксид вольфрама и гафний/оксид гафния. Возможны и другие комбинации, такие как вольфрам/оксид скандия и гексаборид лантана /оксид лантана. В качестве термоионных источников электронов (катодов) также могут быть использованы карбиды, нитриды и другие материалы.
Следует отметить, что количество испущенных электронов увеличивается при возрастании электрического поля, например, между катодом 112 и промежуточным электродом 117. Электрическое поле снижает потенциальный барьер поверхности катода, и большее количество электронов может покинуть поверхность катода. Приложенное напряжение определяет энергию электронов. Характеристики барьера после приложения электрического поля зависят от интенсивности поля, расстояния между катодом и анодом, толщины покрытия и диэлектрической проницаемости. Расстояние туннелирования также зависит от энергии электронов. Количество электронов, проходящих через этот слой оксидов металлов путем туннелирования, зависит от ширины оксидного (изоляционного) слоя и от электрического поля, приложенного к слою. При увеличении температуры изменяется распределение энергии Ферми, увеличивая энергию электронов, что повышает вероятность их туннелирования. Расстояние катод-анод должно позволять создавать сильное электрическое поле внутри изоляционного материала, но поле при этом не должно превышать величину пробоя. Требуемое электрическое поле может быть получено за счет изменения напряжения возбуждения и расстояния катод-анод.
Следует отметить, что могут быть использованы различные комбинации термоионный катод/покрытие, имеющие разные электронноэмиссионные свойства в зависимости от температуры, приложенного напряжения, интенсивности электрического поля и прилежащей среды (вакуум, инертный газ, газообразный CO2). Рабочие температуры могут составлять приблизительно 600°C-1500°C. Каждая из таких комбинаций термоионный катод/покрытие имеет разный потенциальный барьер, приводящий к разной вероятности туннелировния электронов для данного приложенного электрического поля. Для максимальной вероятности диссоциации в случае молекулы CO2 электрон должен иметь энергию приблизительно 4,4 эВ. После высвобождения электронов, если приложенное напряжение превышает необходимое (4,4 В), для достижения требуемой энергии электрона может быть приложена другая совокупность тормозящих электрических полей.
Поскольку система работает при высоких температурах (600°C-1500°C), генератор электрического поля (например, термоэлектрический элемент или двигатель Стирлинга) может создавать электрическое поле, необходимое для термо-полевой (T-F) эмиссии (то есть суммарного эффекта от термоэмиссии и эмиссии под действием электрического поля). Использование термоэлектрического элемента или двигателя Стирлинга в комбинации с термоионным катодом обеспечивает возможность: (i) работы при высокой температуре и (ii) использования избытка тепловой энергии, получаемой с термоионного катода, для на