Полипептиды, обладающие антимикробной активновностью, и полинуклеотиды, кодирующие их
Иллюстрации
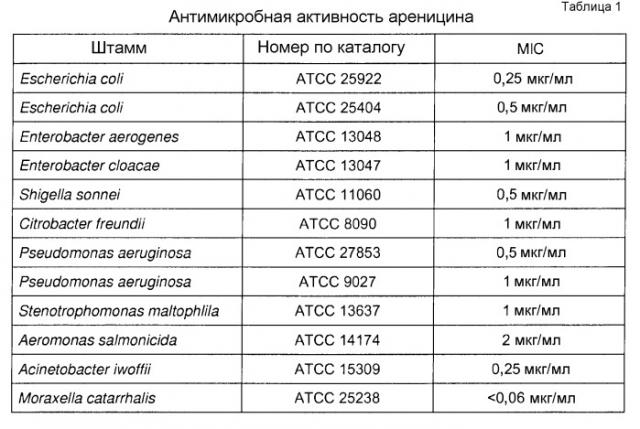
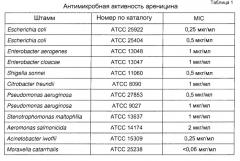
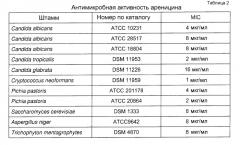
Показать всеИзобретение относится к биохимии и представляет собой полипептид, обладающий антимикробной активностью, включающий аминокислотную последовательность, которая имеет, по меньшей мере, 70% идентичности с аминокислотной последовательностью, соответствующей положениям 1-21 SEQ ID NO:2. Изобретение также относится к конструкциям нуклеиновых кислот, векторам и клеткам-хозяевам, включающим полинуклеотид, кодирующий полипептид согласно изобретению, а также к способу получения такого полипептида, а также к применению полипептида для уничтожения микробных клеток. Изобретение позволяет расширить ассортимент антимикробных полипептидов. 10 н. и 8 з.п.ф-лы, 2 табл., 2 пр.
Реферат
Список последовательностей
Настоящее изобретение включает список последовательностей.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к выделенным полипептидам, обладающим антимикробной активностью, и к выделенным полинуклеотидам, кодирующим полипептиды. Изобретение также относится к конструкциям нуклеиновых кислот, векторам и клеткам-хозяевам, включающим полинуклеотиды, а также к способам получения и применения полипептидов.
УРОВЕНЬ ТЕХНИКИ
Целью настоящего изобретения является предложение полипептидов, обладающих антимикробной активностью, и полинуклеотидов, кодирующих полипептиды.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к выделенным полипептидам, обладающим антимикробной активностью, выбранным из группы, состоящей из:
(a) полипептида, имеющего аминокислотную последовательность, которая имеет, по меньшей мере, 60% идентичности с аминокислотной последовательностью, соответствующей положениям 1-21 из SEQ ID NO:2;
(b) полипептида, который кодируется нуклеотидной последовательностью, которая гибридизуется, по меньшей мере, при условиях средней жесткости с (i) нуклеотидной последовательностью, соответствующей положениям 496-558 из SEQ ID NO:1, (ii) с кДНК-последовательностью, содержащейся в нуклеотидной последовательности, соответствующей положениям 1-558 из SEQ ID NO:1, или (iii) с комплементарной цепью (i) или (ii);
(c) варианта, включающего консервативную замену, делецию и/или вставку одной или более аминокислоты аминокислотной последовательности, соответствующей положениям 1-21 из SEQ ID NO:2; и
(d) фрагмента (a) или (b), который обладает антимикробной активностью.
Настоящее изобретение также относится к выделенным полинуклеотидам, кодирующим полипептиды, обладающие антимикробной активностью, выбранные из группы, состоящей из:
(a) полинуклеотида, кодирующего полипептид, имеющий аминокислотную последовательность, которая имеет, по меньшей мере, 60% идентичности с аминокислотной последовательностью, соответствующей положениям 1-21 из SEQ ID NO:2;
(b) полинуклеотида, имеющего, по меньшей мере, 60% идентичности с нуклеотидной последовательностью, соответствующей положениям 496-558 из SEQ ID NO:1; и
(c) полинуклеотида, который гибридизуется, по меньшей мере, при условиях средней жесткости с (i) нуклеотидной последовательностью, соответствующей положениям 496-558 из SEQ ID NO:1, (ii) с кДНК-последовательностью, содержащейся в нуклеотидной последовательности, соответствующей положениям 1-558 из SEQ ID NO:1, или (iii) с комплементарной цепью (i) или (ii).
Настоящее изобретение также относится к конструкциям нуклеиновых кислот, рекомбинантным экспрессирующим векторам и рекомбинантным клеткам-хозяевам, включающим полинуклеотиды.
Настоящее изобретение также относится к способам получения таких полипептидов, обладающих антимикробной активностью, включающим (a) культивирование рекомбинантной клетки-хозяина, включающей полинуклеотид, кодирующий полипептид, при условиях, подходящих для получения полипептида; и (b) получение полипептида.
Настоящее изобретение также относится к способам применения полипептидов и полинуклеотидов по изобретению.
ОПРЕДЕЛЕНИЯ
Антимикробная активность: Термин "антимикробная активность" определяется здесь как активность, которая способна уничтожать микробные клетки или ингибировать их рост. В контексте настоящего изобретения подразумевается, что термин "антимикробный" обозначает, что существует бактерицидный, и/или бактериостатический, и/или фунгицидный эффект, и/или фунгистатический эффект, и/или вируцидный эффект, где термин "бактерицидный" следует понимать, как «способный уничтожать бактериальные клетки». Термин "бактериостатический" следует понимать как «способный ингибировать бактериальный рост», т.е. ингибировать растущие бактериальные клетки. Термин "фунгицидный" следует понимать, как «способный уничтожать грибковые клетки». Термин "фунгистатический" следует понимать, как «способный ингибировать грибковый рост», т.е. ингибировать растущие грибковые клетки. Термин "вируцидный" следует понимать как «способный инактивировать вирус». Термин "микробные клетки" обозначает бактериальные или грибковые клетки (включая дрожжи). В контексте настоящего изобретения подразумевается, что термин "ингибирование роста микробных клеток" обозначает, что клетки не находятся в фазе роста, т.е. что они не способны размножаться.
Для целей настоящего изобретения антимикробную активность можно определить согласно процедуре, описанной Lehrer et al., Journal of Immunological Methods, Vol. 137 (2), p. 167-174 (1991). В качестве альтернативы, антимикробную активность можно определить согласно NCCLS-руководству из CLSI (Института клинических и лабораторных стандартов; широко известного как Национальный комитет клинических и лабораторных стандартов).
Полипептиды, обладающие антимикробной активностью, могут иметь способность уменьшать количество живых клеток Escherichia coli (DSM 1576) до 1/100 через 24 часа (предпочтительно, после 12 часов, более предпочтительно, через 8 часов, более предпочтительно, через 4 часа, более предпочтительно, через 2 часа, наиболее предпочтительно через 1 час, и в особенности через 30 минут) инкубирования при 20°C в 25%(масс./масс.) водном растворе полипептидов, обладающих антимикробной активностью; предпочтительно, в 10% (масс./масс.) водном растворе; более предпочтительно, в 5% (масс./масс.) водном растворе; еще более предпочтительно в 1% (масс./масс.) водном растворе; наиболее предпочтительно, в 0,5% (масс./масс.) водном растворе; и в особенности в 0,1% (масс./масс.) водном растворе полипептидов, обладающих антимикробной активностью.
Полипептиды, обладающие антимикробной активностью, также могут быть способны к ингибированию повышенного роста Escherichia coli (DSM 1576) в течение 24 часов при 25°C в субстрате микробного роста, при добавлении в концентрации 1000 м.д.; предпочтительно, при добавлении в концентрации 500 м.д.; более предпочтительно, при добавлении в концентрации 250 м.д.; еще более предпочтительно, при добавлении в концентрации 100 м.д.; наиболее предпочтительно, при добавлении в концентрации 50 м.д.; и в особенности, при добавлении в концентрации 25 м.д.
Полипептиды, обладающие антимикробной активностью, могут быть способны к уменьшению количества живых клеток Bacillus subtilis (ATCC 6633) до 1/100 через 24 часа (предпочтительно, через 12 часов, более предпочтительно, через 8 часов, более предпочтительно, через 4 часа, более предпочтительно, через 2 часа, наиболее предпочтительно, через 1 час, и в особенности, через 30 минут) инкубирования при 20°C в 25% (масс./масс.) водном растворе полипептидов, обладающих антимикробной активностью; предпочтительно, в 10% (масс./масс.) водном растворе; более предпочтительно, в 5% (масс./масс.) водном растворе; еще более предпочтительно в 1% (масс./масс.) водном растворе; наиболее предпочтительно, в 0,5% (масс./масс.) водном растворе; и в особенности в 0,1% (масс./масс.) водном растворе полипептидов, обладающих антимикробной активностью.
Полипептиды, обладающие антимикробной активностью, также могут быть способны к ингибированию повышенного роста Bacillus subtilis (ATCC 6633) в течение 24 часов при 25°C в субстрате микробного роста, при добавлении в концентрации 1000 м.д.; предпочтительно, при добавлении в концентрации 500 м.д.; более предпочтительно, при добавлении в концентрации 250 м.д.; еще более предпочтительно, при добавлении в концентрации 100 м.д.; наиболее предпочтительно, при добавлении в концентрации 50 м.д.; и в особенности, при добавлении в концентрации 25 м.д.
Полипептиды по настоящему изобретению имеют, по меньшей мере, 20%, предпочтительно, по меньшей мере, 40%, более предпочтительно, по меньшей мере, 50%, более предпочтительно, по меньшей мере, 60%, более предпочтительно, по меньшей мере, 70%, более предпочтительно, по меньшей мере, 80%, еще более предпочтительно, по меньшей мере, 90%, наиболее предпочтительно, по меньшей мере, 95%, и в наибольшей степени предпочтительно, по меньшей мере, 100% антимикробной активности полипептида, состоящего из аминокислотной последовательности, показанной в виде аминокислотной последовательности, соответствующей положениям 1-21 из SEQ ID NO:2.
Выделенный полипептид: Термин "выделенный полипептид", как он применяется здесь, обозначает полипептид, который является чистым, по меньшей мере, на 20%, предпочтительно, по меньшей мере, на 40% чистым, более предпочтительно, по меньшей мере, на 60% чистым, еще более предпочтительно, по меньшей мере, на 80% чистым, наиболее предпочтительно, по меньшей мере, на 90% чистым, и в наибольшей степени предпочтительно, по меньшей мере, на 95% чистым, как определено с помощью SDS-PAGE.
По существу чистый полипептид: Термин "по существу чистый полипептид" обозначает здесь препарат полипептида, который содержит по большей части 10%, предпочтительно, по большей части 8%, более предпочтительно, по большей части 6%, более предпочтительно, по большей части 5%, более предпочтительно, по большей части 4%, по большей части 3%, еще более предпочтительно, по большей части 2%, наиболее предпочтительно, по большей части 1 %, и в наибольшей степени предпочтительно, по большей части 0,5% по массе другого полипептидного вещества, с которым он естественно ассоциирован. Таким образом, является предпочтительным, что по существу чистый полипептид является, по меньшей мере, на 94% чистым, более предпочтительно, по меньшей мере, на 95% чистым, более предпочтительно, по меньшей мере, на 96% чистым, более предпочтительно, по меньшей мере, на 96% чистым, более предпочтительно, по меньшей мере, на 97% чистым, более предпочтительно, по меньшей мере, на 98% чистым, еще более предпочтительно, по меньшей мере, на 99%, наиболее предпочтительно, по меньшей мере, на 99,5% чистым, и в наибольшей степени предпочтительно на 100% чистым по массе от общего полипептидного вещества, присутствующего в препарате.
Полипептиды по настоящему изобретению представлены, предпочтительно, в, по существу, чистой форме. В особенности является предпочтительным, чтобы пептиды были представлены в "по существу чистой форме", т.е. чтобы препарат полипептида был по существу свободен от другого полипептидного вещества, с которым он естественно ассоциирован. Это можно осуществить, например, путем получения пептида посредством хорошо известных рекомбинантных способов или с помощью классических способов очистки.
Здесь термин "по существу чистый полипептид" является синонимом терминов "выделенный полипептид" и "полипептид в выделенной форме".
Идентичность: Родство между двумя аминокислотными последовательностями или между двумя нуклеотидными последовательностями описывают параметром "идентичность".
Для целей настоящего изобретения степень идентичности между двумя аминокислотными последовательностями определяют с помощью программы FASTA, включенной в версию 2.Ox программного пакета FASTA (смотри W. R. Pearson and D. J. Lipman (1988), "Improved Tools for Biological Sequence Analysis", PNAS 85:2444-2448; and W. R. Pearson (1990) "Rapid and Sensitive Sequence Comparison with FASTP and FASTA", Methods in Enzymology 183:63-98). Применяемой выравнивающей матрицей является BLOSUM50, штраф на введение делеции составляет -12, и штраф на продолжение делеции составляет -2. Степень идентичности между двумя нуклеотидными последовательностями определяют с помощью того же алгоритма и пакета программного обеспечения, как описано выше. Применяемой выравнивающей матрицей является матрица идентичности, штраф на введение делеции составляет -16, и штраф на продолжение делеции составляет -4. В качестве альтернативы сравнение двух аминокислотных последовательностей определяют с помощью программы Needle из программного пакета EMBOSS (http://emboss.org) версии 2.8.0. Программа Needle применяет общий алгоритм сравнения, описанный в Needleman, S. B. и Wunsch, C. D. (1970) J. MoI. Biol. 48, 443-453. Применяемой замещающей матрицей является BLOSUM62, штраф на внесение делеции в выравнивание составляет 10, и штраф на продолжение делеции составляет 0,5. Степень идентичности между аминокислотной последовательностью по настоящему изобретению (такой, как аминокислотная последовательность, соответствующая положениям 1-43 из SEQ ID NO:2) и другой аминокислотной последовательностью рассчитывают как количество точных соответствий при сравнении двух последовательностей, деленное на длину (количество аминокислотных остатков) последовательности по настоящему изобретению; или в качестве альтернативы выходное устройство Needle "наибольшая идентичность" применяют как процент идентичности и рассчитывают следующим образом: (идентичные остатки × 100)/(длина сравнения - количество делеций при сравнении). Результат выражается как процент идентичности.
Полипептидный фрагмент: Термин "полипептидный фрагмент" определяется здесь как полипептид, имеющий одну или более аминокислот, делетированных из амино и/или карбоксильного конца SEQ ID NO:2 или ее гомологичной последовательности, где фрагмент обладает антимикробной активностью. В частном воплощении фрагмент включает, по меньшей мере, 15, предпочтительно, по меньшей мере, 16, более предпочтительно, по меньшей мере, 17, еще более предпочтительно, по меньшей мере, 18, наиболее предпочтительно, по меньшей мере, 19 и в особенности, по меньшей мере, 20 расположенных друг за другом аминокислот из SEQ ID NO:2.
Фрагмент последовательности: Термин "фрагмент последовательности" определяется здесь как нуклеотидная последовательность, имеющая один или более нуклеотидов, делетированных из 5' и/или 3' конца SEQ ID NO:1, или ее гомологичная последовательность, где фрагмент последовательности кодирует полипептидный фрагмент, имеющий антимикробную активность.
Аллельный вариант: Термин "аллельный вариант" обозначает здесь одну из двух или более альтернативных форм гена, занимающего один и тот же хромосомный локус. Аллельная вариация возникает естественно посредством мутации и может в результате привести к полиморфизму внутри популяций. Генные мутации могут быть молчащими (без изменений в кодируемом полипептиде) или могут кодировать полипептиды, имеющие альтернативные аминокислотные последовательности. Аллельный вариант полипептида представляет собой полипептид, кодируемый аллельным вариантом гена.
По существу чистый полинуклеотид: Термин "по существу чистый полинуклеотид", как он применяется здесь, обозначает полинуклеотидный препарат, свободный от других посторонних или не желательных полинуклеотидов и представленный в форме, подходящей для применения в системах получения белков методами генной инженерии. Таким образом, по существу чистый полинуклеотид содержит по большей части 10%, предпочтительно, по большей части 8%, более предпочтительно, по большей части 6%, более предпочтительно, по большей части 5%, более предпочтительно, по большей части 4%, более предпочтительно, по большей части 3%, еще более предпочтительно, по большей части 2%, наиболее предпочтительно, по большей части 1%, и в наибольшей степени предпочтительно, по большей части 0,5% по массе другого полинуклеотидного вещества, с которым он естественно ассоциирован. Однако по существу чистый полинуклеотид может включать природные 5' и 3' нетранслируемые участки, такие как промоторы и терминаторы. Является предпочтительным, чтобы по существу чистый полинуклеотид являлся, по меньшей мере, на 90% чистым, предпочтительно, по меньшей мере, на 92% чистым, более предпочтительно, по меньшей мере, на 94% чистым, более предпочтительно, по меньшей мере, 95% чистым, более предпочтительно, по меньшей мере, на 96% чистым, более предпочтительно, по меньшей мере, на 97% чистым, еще более предпочтительно, по меньшей мере, на 98% чистым, наиболее предпочтительно, по меньшей мере, на 99%, и в наибольшей степени предпочтительно, по меньшей мере, на 99,5% чистым по массе. Полинуклеотиды по настоящему изобретению представлены предпочтительно в по существу чистой форме. В особенности является предпочтительным, чтобы полинуклеотиды, описанные здесь, были представлены в "по существу чистой форме", т.е. чтобы препарат полинуклеотида являлся по существу свободным от другого полинуклеотидного вещества, с которым он естественно ассоциирован. Здесь, термин "по существу чистый полинуклеотид" является синонимом терминов "выделенный полинуклеотид" и "полинуклеотид в выделенной форме". Полинуклеотиды могут иметь геномное, кДНК-, РНК-, полусинтетическое, синтетическое происхождение или любые их комбинации.
кДНК: Термин "кДНК" определяется здесь как молекула ДНК, которую можно получить с помощью обратной транскрипции из матричной сплайсированной молекулы мРНК, полученной из эукариотической клетки. кДНК лишена интронных последовательностей, которые обычно присутствуют в соответствующей геномной ДНК. Инициирующий, первичный РНК транскрипт является предшественником мРНК, которая процессируется через ряд стадий пока не появится в виде матричной сплайсированной мРНК. Эти стадии включают удаление интронных последовательностей с помощью процесса, называемого сплайсинг. кДНК, выделенная из мРНК, таким образом, лишена любых интронных последовательностей.
Конструкция нуклеиновой кислоты: Термин "конструкция нуклеиновой кислоты", как он применяется здесь, обозначает молекулу нуклеиновой кислоты, или одноцепочечную, или двухцепочечную, которая выделена из природного гена либо которую модифицировали с получением сегментов нуклеиновых кислот таким образом, что иначе они не могли бы существовать в природе. Термин конструкция нуклеиновой кислоты является синонимом термина "экспрессирующая кассета", когда конструкция нуклеиновой кислоты содержит контрольные последовательности, требующиеся для экспрессии кодирующей последовательности по настоящему изобретению.
Контрольная последовательность: Термин "контрольные последовательности" определяется здесь, чтобы включить все компоненты, которые необходимы или полезны для экспрессии полинуклеотида, кодирующего полипептид по настоящему изобретению. Каждая контрольная последовательность может быть нативной или чужеродной по отношению к нуклеотидной последовательности, кодирующей полипептид. Такие контрольные последовательности включают, но не ограничены ими, лидер, последовательность полиаденилирования, пропептидную последовательность, промотор, последовательность сигнального пептида и терминатор транскрипции. Как минимум, контрольные последовательности включают промотор и стоп-сигналы транскрипции и трансляции. Контрольные последовательности могут обеспечиваться линкерами с целью введения специфических сайтов рестрикции, облегчающих лигирование контрольных последовательностей с кодирующим участком нуклеотидной последовательности, кодирующей полипептид.
Функционально связанный: Термин "функционально связанный" обозначает здесь конфигурацию, в которой контрольная последовательность размещена в подходящем положении по отношению к кодирующей последовательности полинуклеотидной последовательности, так что контрольная последовательность направляет экспрессию кодирующей последовательности полипептида.
Кодирующая последовательность: При использовании здесь, термин "кодирующая последовательность" обозначает нуклеотидную последовательность, которая непосредственно определяет аминокислотную последовательность ее белкового продукта. Границы кодирующей последовательности в основном определяются открытой рамкой считывания, которая обычно начинается с ATG-старт-кодона или альтернативных старт-кодонов, таких как GTG и TTG. Кодирующей последовательностью может быть ДНК, кДНК или рекомбинантная нуклеотидная последовательность.
Экспрессия: Термин "экспрессия" включает любую стадию, вовлеченную в продукцию полипептида, включающую, но не ограниченную ими, транскрипцию, пост-транскрипционную модификацию, трансляцию, пост-трансляционную модификацию и секрецию.
Экспрессирующий вектор: Термин "экспрессирующий вектор" определяется здесь как линейная или циклическая молекула ДНК, которая включает полинуклеотид, кодирующий полипептид по изобретению, и который функционально связан с дополнительными нуклеотидами, которые обеспечиваются для его экспрессирования.
Клетка-хозяин: Термин "клетка-хозяин", как он применяется здесь, включает любой тип клетки, который является восприимчивым к трансформации, трансфекции, трансдукции и подобным конструкции нуклеиновой кислоты, включающей полинуклеотид по настоящему изобретению.
Модификация: Термин "модификация" обозначает здесь любую химическую модификацию полипептида, состоящего из аминокислотной последовательности, соответствующей положениям 1-21 из SEQ ID NO:2, а также обозначает генетическую манипуляцию с ДНК, кодирующей полипептид. Модификация(и) может представлять собой замену(ы), делецию(и) и/или вставку(и) аминокислоты(аминокислот), а также замену(ы) аминокислотной боковой цепи(ей); или может представлять собой применение не природных аминокислот с подобными характеристиками аминокислотной последовательности. В особенности, модификация(и) может представлять собой амидирования, такие как амидирование C-конца.
Искусственный вариант: При использовании здесь, термин "искусственный вариант" обозначает полипептид, обладающий антимикробной активностью, полученный с помощью организма, экспрессирующего модифицированную нуклеотидную последовательность SEQ ID NO:1. Модифицированную нуклеотидную последовательность получают посредством вмешательства человека с помощью модификации нуклеотидной последовательности, описанной в SEQ ID NO:1.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Полипептиды, обладающие антимикробной активностью
В первом аспекте настоящее изобретение относится к выделенным полипептидам, имеющим аминокислотную последовательность, которая имеет степень идентичности с аминокислотной последовательностью, соответствующей положениям 1-21 из SEQ ID NO:2 (т.е. зрелый полипептид), по меньшей мере, 60%, предпочтительно, по меньшей мере, 65%, более предпочтительно, по меньшей мере, 70%, более предпочтительно, по меньшей мере, 75%, более предпочтительно, по меньшей мере, 80%, более предпочтительно, по меньшей мере, 85%, еще более предпочтительно, по меньшей мере, 90%, наиболее предпочтительно, по меньшей мере, 95%, и в наибольшей степени предпочтительно, по меньшей мере, 97%, и которые имеют антимикробную активность (здесь и далее "гомологичные полипептиды"). В предпочтительном аспекте гомологичные полипептиды имеют аминокислотную последовательность, которая отличается десятью аминокислотами, предпочтительно, пятью аминокислотами, более предпочтительно, четырьмя аминокислотами, еще более предпочтительно тремя аминокислотами, наиболее предпочтительно, двумя аминокислотами, и в наибольшей степени предпочтительно, одной аминокислотой от аминокислотной последовательности, соответствующей положениям 1-21 из SEQ ID NO:2.
Полипептид по настоящему изобретению предпочтительно включает аминокислотную последовательность из SEQ ID NO:2 или ее аллельный вариант; или ее фрагмент, который обладает антимикробной активностью. В предпочтительном аспекте, полипептид включает аминокислотную последовательность из SEQ ID NO:2. В другом предпочтительном аспекте, полипептид включает аминокислотную последовательность, соответствующую положениям 1-21 из SEQ ID NO:2, или ее аллельный вариант; или ее фрагмент, который обладает антимикробной активностью. В другом предпочтительном аспекте, полипептид включает аминокислотную последовательность, соответствующую положениям 1-21 из SEQ ID NO:2. В другом предпочтительном аспекте, полипептид состоит из аминокислотной последовательности из SEQ ID NO:2 или ее аллельный вариант; или ее фрагмент, который обладает антимикробной активностью. В другом предпочтительном аспекте, полипептид состоит из аминокислотной последовательности из SEQ ID NO:2. В другом предпочтительном аспекте, полипептид состоит из аминокислотной последовательности, соответствующей положениям 1-21 из SEQ ID NO:2 или ее аллельного варианта; или ее фрагмента, который обладает антимикробной активностью. В другом предпочтительном аспекте, полипептид состоит из аминокислотной последовательности, соответствующей положениям 1-21 из SEQ ID NO:2.
Во втором аспекте, настоящее изобретение относится к выделенным полипептидам, обладающим антимикробной активностью, которые кодируются полинуклеотидами, которые гибридизуются при условиях очень низкой жесткости, предпочтительно, при условиях низкой жесткости, более предпочтительно, при условиях средней жесткости, более предпочтительно, при условиях средневысокой жесткости, еще более предпочтительно, при условиях высокой жесткости, и наиболее предпочтительно, при условиях очень высокой жесткости с (i) нуклеотидной последовательностью, соответствующей положениям 496-558 из SEQ ID NO:1, (ii) с кДНК-последовательностью, содержащейся в нуклеотидной последовательности, соответствующей положениям 1-558 из SEQ ID NO:1, (iii) с фрагментом последовательности (i) или (ii), или (iv) с комплементарной цепью (i), (ii), или (iii) (J. Sambrook, E. F. Fritsch, and T. Maniatus, 1989, Molecular Cloning, A Laboratory Manual, 2d edition, Cold Spring Harbor, New York). Фрагмент последовательности SEQ ID NO:1 содержит, по меньшей мере, 100 расположенных друг за другом нуклеотидов или предпочтительно, по меньшей мере, 200 расположенных друг за другом нуклеотидов. Кроме того, фрагмент последовательности может кодировать полипептидный фрагмент, который обладает антимикробной активностью.
Нуклеотидная последовательность SEQ ID NO:1 или ее фрагмент, а также аминокислотная последовательность SEQ ID NO:2 или ее фрагмент могут применяться для создания зонда нуклеиновой кислоты для идентификации и клонирования ДНК, кодирующей полипептиды, обладающие антимикробной активностью, из штаммов или видов различного происхождения согласно методам, хорошо известным из уровня техники. В особенности, такие зонды могут применяться для гибридизации с геномной или кДНК интересующего рода или вида, с последующими стандартными процедурами блоттинга по Саузерну для того, чтобы идентифицировать и выделить там соответствующий ген. Такие зонды предположительно могут быть короче, чем целая последовательность, но должны быть длиной, по меньшей мере, 14, предпочтительно, по меньшей мере, 25, более предпочтительно, по меньшей мере, 35, и наиболее предпочтительно, длиной, по меньшей мере, 70 нуклеотидов. Однако является предпочтительным, чтобы длина зонда нуклеиновой кислоты составляла, по меньшей мере, 100 нуклеотидов. Например, зонд нуклеиновой кислоты может быть длиной, по меньшей мере, 200 нуклеотидов, предпочтительно, по меньшей мере, 270 нуклеотидов. Могут применяться оба зонда ДНК и РНК. Зонды обычно метят для обнаружения соответствующего гена (например, с помощью 32P, 3H, 35S, биотина или авидина). Такие зонды охвачены настоящим изобретением.
Библиотека геномной ДНК или кДНК, полученная из каких-то других организмов, может быть, таким образом, проскринирована с ДНК, которая гибридизуется с зондами, описанными выше, и которая кодирует полипептид, обладающий антимикробной активностью. Геномная или другая ДНК из каких-то других организмов может быть разделена с помощью электрофореза на агарозном или полиакриламидном геле или с помощью других методов разделения. ДНК из библиотек или разделенная ДНК может быть перенесена и иммобилизована на нитроцеллюлозу или другую подходящую подложку. Для того чтобы идентифицировать клон или ДНК, которая является гомологичной с SEQ ID NO:1 или с ее фрагментом, в блоттинге по Саузерну применяется подложка.
Для целей настоящего изобретения гибридизация выявляет, что нуклеотидная последовательность гибридизуется с меченым зондом нуклеиновой кислоты, соответствующим нуклеотидной последовательности, представленной в SEQ ID NO:1, ее комплементарной цепью или фрагментом ее последовательности при условиях от очень низкой до очень высокой жесткости. Молекулы, с которыми при этих условиях гибридизуется зонд нуклеиновой кислоты, можно обнаруживать, используя рентгеновскую пленку.
В предпочтительном аспекте, зонд нуклеиновой кислоты представляет собой полинуклеотидную последовательность, которая кодирует полипептид из SEQ ID NO:2, или фрагмент его последовательности. В другом предпочтительном аспекте, зонд нуклеиновой кислоты представляет собой SEQ ID NO:1. В другом предпочтительном аспекте, зонд нуклеиновой кислоты представляет собой участок из SEQ ID NO:1, кодирующий зрелый полипептид.
Для длинных зондов длиной, по меньшей мере, 100 нуклеотидов определяют условия предгибридизации и гибридизации от условий очень низкой до очень высокой жесткости при 42°C в 5X SSPE, 0,3% SDS, 200 мкг/мл порезанной и денатурированной ДНК спермы лосося, и или 25% формамид для условий очень низкой и низкой жесткости, 35% формамид для условий средней и средневысокой жесткости, или 50% формамид для условий высокой и очень высокой жесткости, с последующими стандартными процедурами блоттинга по Саузерну оптимально в течение 12-24 часов.
Для длинных зондов длиной, по меньшей мере, 100 нуклеотидов, подложку в конце отмывают три раза каждый по 15 минут с применением 2X SSC, 0,2% SDS предпочтительно, по меньшей мере, при 45°C (очень низкая жесткость), более предпочтительно, по меньшей мере, при 50°C (низкая жесткость), более предпочтительно, по меньшей мере, при 55°C (средняя жесткость), более предпочтительно, по меньшей мере, при 60°C (средневысокая жесткость), еще более предпочтительно, по меньшей мере, при 65°C (высокая жесткость), и наиболее предпочтительно, по меньшей мере, при 70°C (очень высокая жесткость).
Для коротких зондов, длина которых составляет примерно от 15 нуклеотидов до примерно 70 нуклеотидов, условия жесткости определяют как предгибридизацию, гибридизацию и отмывку после гибридизации при температуре ниже рассчетной Tm, рассчитанной согласно Bolton и McCarthy (1962, Proceedings of the National Academy of Sciences USA 48:1390) примерно на 5°C-10°C в 0,9 M NaCl, 0,09 M Tris-HCl pH 7,6, 6 мМ EDTA, 0,5% NP-40, 1X растворе Денхардта, 1 мМ пирофосфате натрия, 1 мМ монофосфате натрия, 0,1 мМ ATP и 0,2 мг дрожжевой РНК на мл раствора с последующими стандартными процедурами блоттинга по Саузерну.
Для коротких зондов, длина которых составляет примерно от 15 нуклеотидов до примерно 70 нуклеотидов, подложку отмывают один раз в 6X SCC плюс 0,1% SDS в течение 15 минут с применением 6X SSC при температуре ниже рассчитанной Tm примерно на 5°C-10°C.
В третьем аспекте настоящее изобретение относится к искусственным вариантам, включающим консервативную замену, делецию и/или вставку одной или более аминокислот из SEQ ID NO:2 или ее зрелого полипептида. Предпочтительно, аминокислотные замены имеют минорную природу, то есть это консервативные аминокислотные замены или вставки, которые не оказывают значительного влияния на сборку и/или активность белка; короткие делеции, обычно от одной до примерно 10 аминокислот; короткие амино- или карбоксиконцевые удлинения, такие, как аминоконцевой остаток метионина; короткий линкерный пептид до примерно 20-25 остатков; или короткое удлинение, такое как полигистидиновый тракт, антигенный эпитоп или связывающий домен, которое облегчает очистку с помощью изменения результирующего заряда или другой функции.
Примеры консервативных замен представлены в группе основных аминокислот (аргинина, лизина и гистидина), кислых аминокислот (глутаминовой кислоты и аспарагиновой кислоты), полярных аминокислот (глутамина и аспарагина), гидрофобных аминокислот (лейцина, изолейцина и валина), ароматических аминокислот (фенилаланина, триптофана и тирозина) и коротких аминокислот (глицина, аланина, серина, треонина и метионина). Аминокислотные замены, которые в основном не изменяют специфической активности, известны из уровня техники и описаны, например, в H. Neurath and R. L. Hill, 1979, In, The Proteins, Academic Press, New York. Наиболее часто встречающиеся замены представляют собой Ala/Ser, Val/lle, Asp/Glu, Thr/Ser, Ala/Gly, Ala/Thr, Ser/Asn, Ala/Val, Ser/Gly, Tyr/Phe, Ala/Pro, Lys/Arg, Asp/Asn, Leu/lle, Leu/Val, Ala/Glu и Asp/Gly.
В дополнение к 20 стандартным аминокислотам, нестандартные аминокислоты (такие как 4-гидроксипролин, 6-N-метиллизин, 2-аминоизомасляная кислота, изовалин и альфа-метилсерин) могут быть заменены на аминокислотные остатки полипептидов дикого типа. Ограниченное количество неконсервативных аминокислот, аминокислоты, которые не кодируются генетическим кодом, и не природные аминокислоты могут быть заменены аминокислотными остатками. "Неприродные аминокислоты" были модифицированы после белкового синтеза и/или имеют химическую структуру в своей боковой цепи(ях), отличную от той, что имеют стандартные аминокислоты. Неприродные аминокислоты могут быть химически синтезированы и, предпочтительно, являются коммерчески доступными и включают пиперидин-N-карбоновую кислоту, тиазолидин-карбоксильную кислоту, дегидропролин, 3- и 4-метилпролин и 3,3-диметилпролин.
В качестве альтернативы, аминокислотные замены имеют такую природу, что физико-химические свойства полипептидов изменяются. Например, аминокислотные замены могут улучшать термостабильность полипептида, изменять специфичность к субстрату, изменять оптимальное значение pH и подобные.
Незаменимые аминокислоты в родительском полипептиде можно идентифицировать согласно процедурам, известным из уровня техники, таким как сайт-направленный мутагенез или аланин-сканирующий мутагенез (Cunningham and Wells, 1989, Science 244: 1081-1085). В последнем методе единичные мутации аланина вводят в каждый остаток молекулы, и полученные в результате мутантные молекулы тестируют на биологическую активность (т.е. на антимикробную активность) для идентификации аминокислотных остатков, которые являются критическими для активности молекулы. Смотри также, Hilton et al., 1996, J. Biol. Chem. 271: 4699-4708. Биологическое взаимодействие можно также определить с помощью физического анализа структуры, как определяют такими методами, как ядерный магнитный резонанс, кристаллография, электронная дифракция или фотоафинное мечение совместно с мутацией предполагаемого сайта контакта аминокислот. Смотри, например, de Vos et al., 1992, Science 255: 306-312; Smith et al., 1992, J. MoI. Biol. 224: 899-904; Wlodaver et al., 1992, FEBS Lett. 309:59-64. Идентичности незаменимых аминокислот можно также получить из анализа идентичности с полипептидами, которые относятся к полипептидам согласно изобретению.
Единичные или множественные аминокислотные замены могут быть произведены и протестированы с использованием известных методов мутагенеза, рекомбинации и/или перетасовки, с последующей существенной процедурой скрининга, такими как те, что описаны в Reidhaar-Olson and Sauer, 1988, Science 241: 53-57; Bowie and Sauer, 1989, Proc. Natl. Acad. Sci. USA 86: 2152-2156; WO 95/17413; or WO 95/22625. Другие методы, которые могут применяться, включают подверженный ошибкам ПЦР, фаговый дисплей (например, Lowman et al., 1991, Biochem. 30:10832-10837; U.S. Patent No. 5,223,409; WO 92/06204), сайт-направленный мутагенез (Derbyshire et al., 1986, Gene 46:145; Ner et al., 1988, DNA 7:127).
Методы мутагенеза/перетасовки могут быть объединены с высоко производительными, автоматическими способами скрининга для обнаружения активности клонированных, подвергнутых мутагенезу полипептидов, экспрессирующихся клетками-хозяевами. Подвергнутые мутагенезу молекулы ДНК, которые кодируют активные полипептиды, можно получить из клеток-хозяев, и их последовательность можно быстро определить с использованием стандартных методов, известных из уровня техники. Эти методы дают возможность быстрого определения важности индивидуальных аминокислотных остатков в интересующем полипептиде и могут применяться к полипептидам неизвестной структуры.
Общее количество аминокислотных замен, делеций и/или вставок аминокислотной последовательности, соответствующей положениям 1-21 из SEQ ID NO:2, составляет 10, предпочтительно 9, более предпочтительно 8, более предпочтительно 7, более предпочтительно по большей части 6, более предпочтительно по большей части 5, более предпочтительно 4, еще более предпочтительно 3, наиболее предпочтительно 2 и в наибольшей степени предпочтительно 1.
В отдельном воплощении пептиды по изобретению включают, по меньшей мере, 4 цистеиновых остатка, предпочтительно, полипептиды включают ровно 4 цистеиновых остатка. В другом воплощении, полипептиды являются циклическими полипептидами.
N-концевое продолжение
N-концевое продолжение полипептидов по изобретению соответственно может состоять из 1-50 аминокислот, предпочтительно, из 2-20 аминокислот, особенно из 3-15 аминокислот. В одном воплощении N-концевое продолжение пептида не содержит Arg (R). В другом воплощении N-концевое продолжение включает kex2 или kex2-подобные сайты расщепления, как дополнительно определено ниже. В предпочтительном воплощении, N-к