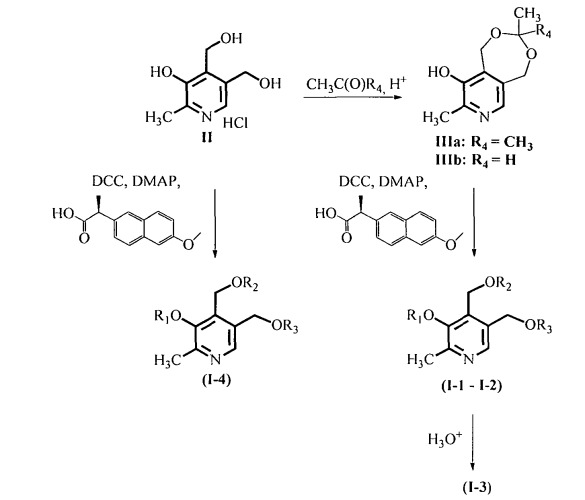
Нестероидные противовоспалительные средства на основе производных пиридоксина
Иллюстрации
Показать всеИзобретение относится к производным пиридоксина общей формулы (I),
где: при R2+R3=-C(CH3)2- или -CH(CH3)-;
при R1=H; R2=H;
при R1=H; R3=H;
Технический результат - производные пиридоксина, обладающие высокой противовоспалительной активностью и низкой токсичностью. 1 з.п. ф-лы, 1 сх., 1 ил., 6 пр.
Реферат
Изобретение относится к новым производным пиридоксина формулы (I), которые обладают высокой противовоспалительной активностью и низкой токсичностью и могут найти применение в медицине и ветеринарии.
где:
при R2+R3=-C(CH3)2- или -CH(CH3)-; R1=
при R1=H; R3=H; R2=
R1=R2=R3=
Заболевания опорно-двигательного аппарата являются одним из наиболее массовых типов заболеваний, лечение которых представляет собой сложную проблему для здравоохранения. Для лечения воспалительных заболеваний наиболее часто используются нестероидные противовоспалительные средства (НПВС).
За последние 30 лет количество НПВС значительно возросло и в настоящее время данная группа насчитывает большое число препаратов, отличающихся по длительности действия и способам применения. Главным элементом механизма действия НПВС является угнетение синтеза воспалительных медиаторов - простагландинов. В процессе альтерации (1 стадии воспаления) из клеточной мембраны высвобождаются фосфолипиды, которые под действием фермента фосфолипазы A2 метаболизируются до арахидоновой кислоты. Арахидоновая кислота, в свою очередь, метаболизируется двумя путями: циклооксигеназным (ЦОГ) и липооксигеназным (ЛОГ). НПВС подавляют только ЦОГ, поэтому они блокируют развитие только второй стадии воспаления.
Существует 2 изофермента ЦОГ: ЦОГ-1 (конститутивный, существующий в норме) - контролирует выработку простаноидов, регулирующих физиологические функции желудка, сосудов и почек, ЦОГ-2 (индуцированный) - участвует в синтезе простагландинов при воспалении. ЦОГ-2 в норме отсутствует и образуется под действием тканевых факторов, индуцирующих воспалительную реакцию (цитокины и др.). Противовоспалительное действие НПВС обусловлено ингибированием ЦОГ-2, а побочные эффекты возникают в результате ингибирования ЦОГ-1.
Наиболее известными (применяемыми) НПВС являются кетопрофен (3-бензоил-альфа-метилбензолуксусная кислота), ибупрофен ((RS)-2-(4-изобутилфенил)пропионовая кислота), диклофенак (2-[(2,6-дихлорфенил)амино] бензол уксусная кислота), индометацин (1-(4-хлорбензоил)-5-метокси-2-метил-1H-индол-3-уксусная кислота) и напроксен ((S)-6-метокси-α-метил-2-нафталинуксусная кислота).
К наиболее частым и опасным побочным эффектам НПВС относятся поражения желудочно-кишечного тракта (ЖКТ), которые могут проявляться диспепсией (тошнотой, рвотой), эрозиями желудка, пептическими язвами и желудочно-кишечным кровотечением. Язвенные заболевания в значительной степени связаны с собственной кислотностью НПВС, которая в сочетании с кислотностью содержимого желудка приводит к нарушению проницаемости клеток слизистой оболочки и становится непосредственной причиной образования язвенных процессов.
Кровотечение также связывают со способностью данных препаратов подавлять синтез простагландинов и тромбоксанов, в норме способствующих сохранению целостности слизистого слоя.
Защита карбоксильной группы является одним из основных способов снижения токсичности НПВС. Наиболее часто для этого применяют сложноэфирную защиту. Сложные эфиры НПВС являются типичными пролекарствами, которые в ЖКТ подвергаются ферментативному гидролизу с постепенным высвобождением НПВС, тем самым обеспечивая пролонгированный эффект лекарственного препарата. Помимо этого они лучше проникают через цитоплазматические мембраны клеток, благодаря чему оказывают меньшее раздражающее действие на слизистую оболочку ЖКТ.
В международной заявке [WO 2008101064 A1. Method of treating arthritis, pain or inflammation with naproxen 2-(methanesulfonyl)ethyl ester and an h2 receptor antagonist/logical therapeutics inc - Опубл. - 21.08.2008] предложено использовать 2-(метансульфонил)этиловый эфир напроксена в лечении артрита и воспалительных процессов.
В американском патенте [US 4851426. Ethoxycarbonyloxy ethyl esters of non-steroidal anti-inflammatory carboxylic acids and pharmaceutical compositions thereof / Teva pharma. Ind. - Опубл. - 12.09.1989] описаны этоксикарбонилоксиэтиловые эфиры различных НПВС, обладающие высокой противовоспалительной и анальгетической активностью, наряду с низкой гастротоксичностью.
Предложены морфолинокарбонилоксиэтиловые эфиры НПВС, существенно менее гастротоксичные по сравнению с исходными НПВС [US 2005004118. Prodrugs of non-steroidal anti-inflammatory and carboxylic acid containing compounds / Jilani Jamal A. - Опубл. - 19.12.2000].
Получен ряд сложных эфиров N-замещенных гликоламидов напроксена. Данные соединения обладают эквивалентной напроксену противовоспалительной активностью, при этом in vivo будучи значительно более безопасными [Ranatunge R.R., Augustyniak M.E., Dhawan V. и другие. Synthesis and anti-inflammatory activity of a series of N-substituted naproxen glycolamides: nitric oxide-donor naproxen prodrugs // Bioorg. Med. Chem. - 2006. - V.14. - P.2589-2599].
В качестве аналогов к заявленному техническому решению могут также рассматриваться и сложные эфиры напроксена и пиридоксина по гидроксиметильной группе в 5 положении, описанные в американском патенте [US 4260613. Pyridoxine derivatives / Crinos Industria Farmacobiologica. - Опубл. - 07.04.1981]. У указанных соединений выявлена способность ингибировать воспалительные процессы, вызванные моделью каррагенинового отека на крысах.
Задачей изобретения являются новые малотоксичные соединения, обладающие высокой противовоспалительной активностью, расширяющие арсенал известных средств указанного назначения.
Техническим результатом заявленного изобретения является получение новых соединений общей формулы (I), содержащих в своем составе как фрагмент природного соединения (пиридоксина, входящего в группу витамина B6), так и фрагмент нестероидного противовоспалительного препарата напроксена.
Задача решается, и указанный технический результат достигается получением заявляемых новых производных пиридоксина формулы (I)
согласно нижеприведенной схеме в одну, две или три стадии:
| R1 | R2 | R3 | |
| I-1 | R2+R3=-C(CH3)2- | ||
| I-2 | R2+R3=-CH(CH3)- | ||
| I-3 | H | H | |
| I-4 |
Характеристики новых соединений приведены в примерах конкретного выполнения. Структуры полученных соединений подтверждены методами масс-спектрометрии, 1H и 13C ЯМР-спектроскопии. Спектры ЯМР регистрировали на приборе Bruker AVANCE-400. Химический сдвиг определялся относительно сигналов остаточных протонов дейтерированных растворителей (1H и 13C). Контроль за ходом реакций и чистотой соединений проводили методом ТСХ на пластинах Sorbfil Plates.
Масс-спектры MALDI регистрировались на приборе Ultraflex III компании Bruker, оборудованном твердотельным лазером и время-пролетным анализатором масс. Ускоряющее напряжение 25 кВ. Образцы наносили на мишень Anchor Chip. Запись спектров производили в режиме положительных ионов. Результирующий спектр представлял собой сумму 300 спектров, полученных в разных точках образца. В качестве матриц применяли 2,5-дигидроксибензойную кислоту (DHB) (Acros, 99%) и n-нитроанилин (PNA). Для приготовления матриц использовали хлороформ. Нанесение образцов на мишень проводили методом «высушенных капель».
Примеры конкретного выполнения заявленного технического решения
Пример 1
3,3,8-Триметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ол (IIIa)
Через суспензию 20 г (97.3 ммоль) пиридоксингидрохлорида (II) в 300 мл ацетона, при охлаждении до 3-5°C и перемешивании пропускают 22 г (603 ммоль) хлористого водорода. Полученную реакционную смесь перемешивают в течение 20 ч. Осадок отфильтровывают, промывают эфиром и нейтрализуют водным раствором поташа. Продукт отфильтровывают и перекристаллизовывают из этилового спирта. Выход 19.1 г (94%), бесцветные кристаллы. Т.пл. 184.5-186°C (184-185°C [Korytnyk W. A seven-membered cyclic ketal of pyridoxol // J. Org. Chem. - 1962. - V.27, N. 10. - P.3724-3726]).
Пример 2
3,8-Диметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ол (IIIb)
Синтезируют и разрабатывают аналогично соединению (IIIa) из 20 г (0.096 моль) пиридоксингидрохлорида, 300 мл ацетальдегида и 22 г (603 ммоль) хлороводорода. Выход 65%, бесцветные кристаллы. Т.пл. 186-186.5°C (лит. 186-186.5°C [Fedorenko V.Yu., Lodochnikova O.A., Petukhov A.S., Kataeva O.N., Litvinov I.A., Shtyrlin Yu.G., Klimovitskii, E.N. Crystal structure of seven-member ed acetals with furan and pyridine planar fragments // J. Mol. Struct. - 2003. - V. 644, N 1-3 - P.89-96].
Пример 3
3,3,8-Триметил-4H-[1,3]диоксепино[5,6-c]пиридин-9-ол (2S)-(6-метоксинафталин-2-ил)пропионат (I-1)
К 0,3 г (1,44 ммоль) соединения (IIIa) при 20°C добавляли 0,4 г (1,95 ммоль) дициклогексилкарбодиимида (DCC), 0,2 г (1,64 ммоль) 4-(диметиламино)пиридина (DMAP) и 0,33 г (1,44 ммоль) напроксена. Через 20 минут осадок отфильтровывали, фильтрат концентрировали в вакууме и очищали с помощью колоночной хроматографии (элюент этилацетат-петролейный эфир 1:1). Выход 0,48 г (79%), бесцветные кристаллы. Т.пл. 136-137°C. [α]24 D=+54,21° (c=2.50, CH2Cl2). Спектр ЯМР 1H (400 МГц, CDCl3) δ, м.д.: 1.36 с (3H, CH3), 1.39 с (3H, CH3), 1.73 д (3H, 2JHH=-7.1 Гц, CH3), 2.10 уш (3H, CH3), 3.87 с (3H, OCH3), 4.14 к (1H, 2JHH=-7.1 Гц, CH), 4.44 уш (2H, CH2), 4.77 с (2H, CH2), 7.14-7.78 м (2H, ар), 8.05 с (1H, CH). ЯМР 13C {Н} (100 МГц, CDCl3) δ, м.д.: 18.20, 18.99, 23.60, 23.70, 45.48, 55.44, 58.99, 61.65, 102.73, 105.77, 119.45, 126.14, 126.50, 127.63, 129.05, 129.41, 133.39, 134.14, 134.31, 139.93, 142.42, 144.04, 150.24, 158.02, 171.92. Масс-спектр: Найдено [M+H]+ 408. C24H25NO5. Вычислено М 407.
Пример 4
3,8-Диметил-1,5-дигидро-[1,3]диоксепино[5,6-c]пиридин-9-ол (2S)-(6-метоксинафталин-2-ил)пропионат (I-2)
Синтезируют и разрабатывают аналогично соединению (I-1) из 0,3 г (1,54 ммоль) соединения (IIIb), 0,43 г (2,08 ммоль) дициклогексилкарбодиимида (DCC), 0,22 г (1,80 ммоль) 4-(диметиламино)пиридина (DMAP) и 0,35 г (1,54 ммоль) напроксена. Выход 0,46 г (75%), бесцветные кристаллы. Т.пл. 119,5-121,5°С. Спектр ЯМР 1H (400 МГц, CD2Cl2:CS2=1:1) (смесь двух диастереомеров 1:1) δ, м.д.: 1.28 уш (3H, CH3), 1.72 д (1.5H, 2JHH=-3 Гц, CH3), 1.73 д (1.5H, 2JHH=-3 Гц, CH3), 2.07 уш (3H, CH3), 3.90 с (3H, OCH3), 4.131 к (0.5H, 2JHH=-7 Гц, CH), 4.130 к (0.5H, 2JHH=-7 Гц, CH) 4.32, 4.53 уш (2H, CH2), 4.64, 4.84 (AB, 2JHH=-11.6 Гц, CH2), 4.96 уш (1H, CH), 7.12-7.75 м (6H, ар), 8.04 с (1H, CH). ЯМР 13C {H} (100 МГц, CDCl3) (смесь двух диастереомеров 1:1) δ, м.д.: 18.22, 19.11, 19.16, 19.72, 45.44, 55.40, 65.57, 65.78, 105.74, 119.43, 126.04, 126.08, 126.49, 127.63, 129.02, 129.40, 133.57, 134.11, 134.16, 134.23, 140.26, 142.28, 142.40, 144.35, 150.84 158.00, 172.10. Масс-спектр: Найдено [M+H]+ 408. C24H25NO5. Вычислено M 407.
Пример 5
(3-Гидрокси-5-гидроксиметил-2-метилпиридин-4-ил)метил (2S)-(6-метоксинафталин-2-ил)пропионат (I-3)
Раствор 0,25 г (0,59 ммоль) соединения (I-1) в 15 мл воды, 5 мл этанола и 0,2 мл конц. HCl перемешивали 12 ч при 20°C, после чего раствор нейтрализовывали до pH=7 раствором NaHCO3. Растворитель отгоняли в вакууме, остаток экстрагировали этанолом и очищали с помощью колоночной хроматографии (элюент этилацетат-этанол 8:1). Выход 0,067 г (30%), бесцветные кристаллы. Т.пл. 140-142°C. [α]24 D=-12,93° (c=0.58, CH2Cl2). Спектр ЯМР 1H (400 МГц, CDCl3) δ, м.д.: 1.73 д (3H, 3JHH=7.1 Гц, CH3), 2.56 с (3H, CH3), 4.00 к (1H, 3JHH=7.1, CH), 4.08 с (3H, CH3), 4.83 с (2H, CH2), 5.09, 5.14 (AB, 2JHH=-12.4 Гц, CH2), 6.29 уш (2H, 2OH), 7.29-7.84 м (6H, ар), 7.95 с (1H, CH). ЯМР 13C {H} (100 МГц, CDCl3) δ, м.д.: 18.23, 18.33, 45.47, 55.46, 60.34, 62.03, 105.75, 119.33, 126.03, 126.14, 127.38, 128.93, 129.27, 130.15, 130.91, 133.80, 135.33, 139.31, 148.36, 151.88, 157.86, 174.14. Масс-спектр: Найдено [M]+ 382. C22H23NO5. Вычислено M 381.5.
Пример 6
(5-{[(2S)-2-(6-Метоксинафталин-2-ил)пропаноил]окси}-4-({[(2S)-2-(6-метоксинафталин-2-ил)пропаноил]окси}метил)-6-метилпиридин-3-ол)метил (2S)-2-(6-метоксинафталин-2-ил)пропионат (I-4)
Синтезируют и разрабатывают аналогично соединению (I-1) из 0,3 г (1,46 ммоль) пиридоксин гидрохлорида (II), 1,31 г (6,36 ммоль) дициклогексилкарбодиимида (DCC), 0,53 г (4,38 ммоль) 4-(диметиламино)пиридина (DMAP) и 1,01 г (4,38 ммоль) напроксена. Выход 0,82 г (70%), бесцветные кристаллы. Т.пл. 125°C. [α]24 D=+5,93° (c=8.10, CH2Cl2). Спектр ЯМР 1H (400 МГц, CDCl3) δ, м.д.: 1.46 д (3H, 3JHH=6.2 Гц, CH3), 1.53 д (3H, 3JHH=7.1 Гц, CH3). 1.63 д (3H, 3JHH=7.1 Гц, CH3), 2.04 уш (3H, CH3), 3.6 уш (1H, CH), 3.79 к (1H, 3JHH=7.1 Гц, CH), 3.91 с (3H, CH3), 3.92 с (3H, CH3), 3.94 с (3H, CH3), 3.96 к (1H, 3JHH=7.1 Гц, CH), 4.67 уш (1H, CH3), 4.92 уш (1H, CH2), 5.08, 5.17 (AB, 2JHH=-12.8 Гц, CH2), 7.10-7.71 м (6H, ар), 8.29 с (1H, CH). ЯМР 13C {H} (100 МГц, CDCl3) δ, м.д.: 17.99, 18.41, 18.52, 19.33, 45.04, 45.36, 45.44, 55.37, 57.16, 61.69, 105.69, 105.76, 119.11, 119.15, 119.35, 125.94, 126.08, 126.16, 126.56, 127.27, 127.34, 129.37, 133.79, 133.82, 134.05, 134.21, 135.25, 135.65, 144.66, 147.59, 152.91, 157.77, 157.81, 157.97, 171.97, 173.98. Масс-спектр: Найдено [M]+ 806. C50H47NO9. Вычислено M 805.9.
Исследование острой токсичности полученных соединений
Исследования токсичности проводили на аутбредных мышах линии CD-I SPF-категории (питомник лабораторных животных «Пущино»). Мыши содержались согласно Правилам содержания животных в пластиковых вентилируемых боксах, на подстилке из бумаги, при условиях постоянной температуры 22-25°C и влажности, в нормальном световом режиме и свободном доступе к пище и воде. Животным предоставлялся зерновой корм, специализированные корма. За сутки до введения препарата у животных изымался корм, а за 5 часов - вода.
После введения препарата наблюдали за поведением мышей и за проявлением симптомов, регистрировали время наступления смерти, оставшихся в живых животных эвтаназировали с помощью усыпления углекислым газом. При этом регистрировали имевшиеся по сравнению с контролем патологии, которые могли быть связаны с повреждающим действием вещества.
Для выявления острой токсичности полученные соединения в виде суспензии в минеральном масле вводили перорально с помощью канюли однократно в следующих дозах: 1343 мг/кг, 2686 мг/кг, 4060 мг/кг. Согласно результатам исследования острой токсичности все мыши в опытных группах выжили, поэтому вычислить дозы ЛД50 и ЛД10 не представлялось возможным. Очевидно, что ЛД50 заявляемых соединений больше 4060 мг/кг, что соответствует категории «относительно безвредных» (VI класс токсичности) [Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном введении (Справочник). - М.: Медицина, 1977. - 197 с] или умеренно опасных [согласно ГОСТ 12.1.007-76] и более чем в 3 раза превышает значение ЛД50 для напроксена [http://www.drugs.com/pro/naproxen.html].
По данным вскрытия и патологоанатомического исследования патологий в строении органов животных не обнаружено. Шерсть была блестящей, опрятного вида. Выделения из естественных отверстий отсутствовали. Передние и задние конечности сохранились в неизмененном виде. Деформации конечностей не наблюдалось. Зубы были сохранены. Видимые слизистые оболочки были бледными, блестящими, гладкими.
При осмотре грудной и брюшной полостей нарушений в положении внутренних органов не отмечалось.
Листки плевры, перикарда и брюшины были тонкими, блестящими, гладкими.
Тимус имел треугольную форму, беловатый цвет и умеренно плотную консистенцию.
Диаметр аорты был равномерным на всем протяжении. Интима аорты была гладкой, блестящей, беловатой окраски. Величина и форма сердца изменений не представляли.
Мышца сердца была умеренно плотной, равномерно коричневатой окраски. Клапаны сердца были тонкими, гладкими, блестящими. В полостях сердца содержалось небольшое количество жидкой крови.
Легкие спадались при вскрытии грудной клетки. Величина и форма их изменений не представляли. Поверхность легких имела однородную бледно-розовую окраску. Просвет трахеи и крупных бронхов был широким. Слизистая оболочка - блестящей, бледно-розовой, гладкой.
Слизистая пищевода была блестящей, гладкой, бледного цвета. Величина и форма желудка изменений не представляли. Его просвет был заполнен пищевым содержимым.
Просвет 12-перстной кишки изменений не представлял, слизистая кишки была блестящей, гладкой, бледно-розовой. Слизистая оболочка тонкой кишки была также бледно-розовой, блестящей, гладкой. Слизистая оболочка толстой кишки имела слегка сероватый оттенок, была гладкой, блестящей.
Форма и величина печени изменений не представляли. Поверхность печени была гладкой, однородной темно-красной окраски. Ткань печени на разрезе была темно-красной. Капсула печени была тонкой, прозрачной. Консистенция печени имела обычную плотность.
Форма поджелудочной железы изменений не представляла. Железа имела дольчатое строение, бледно-розовую окраску и умеренно плотную консистенцию.
Размеры и форма селезенки изменений не представляли. Поверхность селезенки имела однородную темно-вишневую окраску, была гладкой.
Консистенция селезенки была умеренно плотной. На разрезе органа выделялись сероватые мелкоклеточные фолликулы.
Величина и форма почек также не представляли изменений. Капсула почек легко снималась. Поверхность была гладкой, однородно коричневато-сероватого цвета. На разрезе органа были хорошо различимы корковое и мозговое вещество. Консистенция почек была умеренно плотной.
Надпочечники имели округлую форму, беловато-желтую окраску и умеренно плотную консистенцию. На разрезе отчетливо выделялось темно-коричневое мозговое вещество.
Мочевой пузырь был заполнен прозрачной, светлой мочой. Слизистая оболочка мочевого пузыря была гладкой, блестящей, бледной окраски.
Оболочки головного мозга были тонкими, прозрачными. Вещество головного мозга было чуть плотноватым на ощупь, поверхность мозга была гладкой. На фронтальных размерах расширения желудочков не наблюдалось.
Противовоспалительная активность полученных соединений
Мыши CD-1 были разделены на несколько групп по 5 голов в каждой в соответствии с количеством тестируемых соединений.
Индукцию формалинового отека проводили по следующей схеме: 50 мкл 1%-ного раствора формалина вводили мышам в субплантарный апоневроз задней правой лапки [Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М.: Медицина, 2005. - 832 с.]. Через 2 часа и через 5 часов после введения формалина замеряли следующие показатели: размеры лапки (высота, ширина, длина) с помощью онкометра.
На следующие сутки начинали противовоспалительную терапию. Препараты вводили внутрижелудочно с помощью канюли 1 раз в сутки в течение 7 дней. Доза вводимых препаратов составляла соответственно 26,5-27,5 мг/кг.
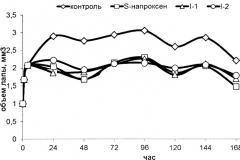
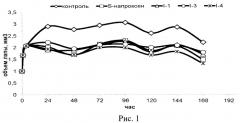
Рисунок 1. Типичная зависимость степени воспалительного процесса на модели формалинового отека у мышей от времени при введении соединений I-1 и I-2.
На рис.1 представлены данные по противовоспалительной активности наиболее активных соединений. Результаты проведенных исследований показали, что данные соединения в пределах экспериментальной ошибки определения обладают одинаковой с напроксеном противовоспалительной активностью (рис.1).
Таким образом, использование эфиров НПВС на основе производных пиридоксина представляет интерес при разработке новых малотоксичных НПВС.
1. Производные пиридоксина общей формулы (I) где:при R2+R3=-C(CH3)2- или -CH(CH3)-; R1= при R1=H; R3=H; R2= R1=R2=R3=
2. Производные пиридоксина по п.1, обладающие противовоспалительной активностью.