Способ получения водорастворимой неагломератной фуллереновой иммуностимулирующей наночастицы и водорастворимая неагломератная фуллереновая иммуностимулирующая наночастица
Иллюстрации
Показать всеИзобретение относится к водорастворимой неагломератной фуллереновой иммуностимулирующей наночастицы, состоящей из гидрофобного фуллеренового ядра, ковалентно соединенного с капрониловым лигандом посредством пиперазинового спейсера (1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновая кислота) и к способу ее получения, который заключается в синтезе очищенной 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты в четыре этапа, на первом из которых получают 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазин, на втором этапе получают 6-(пиперазин-1-ил)-капроновой кислоты этиловый эфир путем растворения 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазина в 2Н НСl и упаривания полученного раствора, рН остатка которого доводят до значения 10,0, экстрагируют этилацетатом с просушкой органического слоя, на третьем этапе получают этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновую кислоту путем смешения и перемешивания до растворения фуллерена-С60 и толуола с добавлением после растворения Ср2TiCl2 и этилового эфира 6-(пиперазин-1-ил)-капроновой кислоты и последующим элюированием смесью гексан:хлороформ, а очищенную 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновую кислоту в виде готового продукта получают растворением этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты в этиловом спирте с добавлением раствора NaOH и нагреванием смеси при перемешивании до полной гомогенизации. Затем доводят рН реакционной смеси до нейтрального рН и выпавшую в осадок кислоту отделяют микрофильтрацией на фильтрах для последующего смывания осадков наночастиц и упаривания стокового осадка, состоящего из водорастворимой неагломератной фуллереновой иммуностимулирующей наночастицы, состоящей из гидрофобного фуллеренового ядра, ковалентно соединенного с капрониловым лигандом посредством пиперазинового спейсера. 2 н. и 2 з.п. ф-лы, 4 ил., 1 табл.
Реферат
Настоящее изобретение относится к биотехнологии, в частности к использованию пиперазилкапрониловых производных фуллерена С60 в качестве стимуляторов иммунного ответа - адъювантов, и может быть использовано в биологической промышленности при разработке и производстве вакцин.
Фуллерен С60 - молекула, состоящая из 60 атомов углерода (и ничего больше), расположенных так же, как вершины футбольного мяча, является третьей (после алмаза и графита) аллотропной формой углерода, обладающей крайне низкой токсичностью (Mori Т. et al. (2006). Preclinical studies on safety of fullerene upon acute oral administration and evaluation for no mutagenesis. Toxicology 225, 48-54; Szwarc H, Moussa F. (2011). Toxicity of 60fullerene: confusion in the scientific literature. J. Nanosci. Lett. 1, 61-62).
Фуллерен и его производные можно использовать:
- для защиты организма от радиации и ультрафиолетового излучения (Theriot С.А., Casey R.C., Moore V.C., Mitchell L., Reynolds J.O., Burgoyne M., et al. (2010). Dendro[C60]fullerene DF-1 provides radioprotection to radiosensitive mammalian cells. Radiat. Environ. Biophys. 49, 437-445; Andrievsky G.V., Bruskov V.I., Tykhomyrov A.A., Gudkov S.V. (2009). Peculiarities of the antioxidant and radioprotective effects of hydrated С60 fullerene nanostructures in vitro and in vivo. Free Radic. Biol. Med. 47, 786-793);
- для защиты от вирусов (Mashino Т., Shimotohno К., Ikegami N.. et al. (2005). Human immunodeficiency virus-reverse transcriptase inhibition and hepatitis С virus RNA-dependent RNA polymerase inhibition activities of fullerene derivatives. Bioorg. Med. Chem. Lett. 15, 1107-1109) и бактерий (Lu Z.S., Dai Т.Н., Huang L.Y., et al. (2010). Photodynamic therapy with a cationic functionalized fullerene rescues mice from fatal wound infections. Nanomedicine 5, 1525-1533);
- для защиты от аллергии. Так, в экспериментах in vivo введение производных фуллерена ингибирует анафилаксию у мышей, и при этом токсического эффекта не наблюдается;
- как вещество, стимулирующее иммунитет (Xu Y.Y., Zhu J.D., Xiang К., Li Y.K., Sun R.H., Ma J., et al. (2011). Synthesis and immunomodulatory acdvity of 60fuUerene-tuftsin conjugates. Biomaterials 32, 9940-9949);
- как мощный антиоксидант, поскольку он является активным акцептором радикалов. Антиоксидантная активность фуллерена сопоставима с действием антиоксидантов класса SkQ («ионов Скулачева») и в 100-1000 раз превышает действие обычных антиоксидантов, таких как витамин Е, бутилгидрокситолуол, β-каротин;
- как лекарственные препараты для борьбы с раковыми заболеваниями (Chen Z., Ma L., Liu Y., Chen С.(2012). Applications of Functionalized Fullerenes in Tumor Theranostics. Theranostics 2, 238-250; Jiao F., Liu Y., Qu Y. et al. (2010). Studies on anti-tumor and antimetastatic activities of fullerenol in a mouse breast cancer model. Carbon 48, 2231-2243);
- для ингибирования ангиогенеза, для защиты мозга от алкоголя, для стимуляции роста нервов, для стимуляции процессов регенерации кожи (фуллерен является важным компонентом косметических омолаживающих средств GRS и CEFINE), для стимуляции роста волос и как лекарство с антиамилоидным действием.
Помимо этого фуллерен может использоваться для доставки в клетку различных лекарственных веществ и невирусной доставки в клеточное ядро генетических векторов (Montellano A., Da Ros Т., Bianco A., Prato M. (2011). Fullerene C(60) as a multifunctional system for drug and gene delivery. Nanoscale 3, 4035-4041; Кузнецова С.А., Орецкая Т.С. (2010). Нанотранспортные системы адресной доставки нуклеиновых кислот в клетки. Российские нанотехнологии, 5 (№9-10), 40-52).
Механизмы взаимодействия фуллеренов с клетками пока не ясны, но результаты его применения дают представление о возможно новом направлении в медицине (Пиотровский Л.Б. (2010). Наномедицина как часть нанотехнологии. Вестник РАМН 3, 41-46).
Из данных научной литературы известно, что бутирил- и капронил-производные фуллерена С60 обладают выраженными иммуностимулирующими свойствами (активация пролиферации макрофагов, ускорение фагоцитарных реакций, увеличение удельной выработки гамма-глобулинов клетками лимфоидной ткани), а включение в состав лиганд-формирующего «хвоста» азотсодержащих гетероциклов (пиррола, пирролидина, пиримидина, оксиметилпуринов) способно усиливать прогнозируемый иммуностимулирующий эффект. Этот вывод убедительно обоснован в аналитическом обзоре Devenji & Lakatos (2011).
Этот вывод говорит в пользу того, что применение ранее не использовавшегося при конструировании фуллереновых НЧ азот-содержащего гетероцикла пиперазина в сочетании с капронил-функционализацией фуллеренового ядра способно привести к созданию нанотехнологичного продукта, пригодного для эффективного применения в качестве адъюванта при производстве вакцин. Этот продукт, впервые синтезированный по нашей методике, отвечает специфическим критериям нанотехнологичности, предъявляемым к наночастицам медицинского назначения экспертным сообществом РОСНАНО и ряда европейских стран (Нано - Россия, 2011, Издательство РОСНАНО - Медиа Стратегия, М., 2011).
Среди аналогов можно выделить ряд экспериментальных исследований, не ставивших прикладных задач, но содержащих тщательное описание клеточных и молекулярных механизмов иммуностимулирующих эффектов ряда производных фуллерена С60. Так, Кайдашев и соавт. описали увеличение функциональной активности фагоцитарных клеток под влиянием самого ядра С60 (Кайдашев И.П. и соавт. (2011), Экспер. Клин. Фармакол, №6: 26-29). Иммунногенные свойства фуллереновых нанокомпозитов охарактеризовали Вентерович и соавторы (Вентерович Н.Г. и соавт. (2011), Иммунология, 12(1); 24-29). В работе Шимановского проанализирован синергизм противовирусного и иммуностимулирующего эффектов аминокислотных и пептидных ковалентных комплексов с фуллереном С60 (Shimanovsky N.S. (2009) Internat. Med. J., 1: 131-136).
Интересен также анализ Bakry и соавт., выявивший общие тенденции и перспективы фармакологического и биотехнологического применения наночастиц на основе фуллерена С60, указывающий, в частности, на возрастающее внимание к перспективам возможного адъювантного использования алифатизированных С60-сфер (Bakiy R., et al. (2007), Internat. J. Nanomed, 2(4): 639-649). Механизм аффинного докинг-распознавания в системе триггер-активации синтеза антител в присутствии пептидил-фуллеренов и обсуждение перспектив использование данного вида НЧ в качестве адьювантов при создании вакцин составили предмет исследования Xu и соавт (Xu Y., et al. (2011), Biomaterialas, 32: 9940-9949).
Выявлены немногочисленные патенты (1997-2009), защищающие права на синтез, структуру и способ применения в качестве адъювантов ряда водорастворимых аддуктов фуллерена С60. Ни один из зарегистрированных на данный момент патентов не защищает права на класс (тип, группу, семейство) соединений, но только на ту или иную конкретную структуру (RU 2124022 - гликопептид-С60, RU 2129436 - аминокислотные и пептидные аддукты С60, RU 2184566 - аминокислотные и пептидные аддукты С60, RU 2184669 - аминокислотный (сериновый) аддукт С60, RU 2348416 - порфириновый аддукт С60 и US 2009/0197951 - оксидендример-фуллереновый комплекс).
Например, известно применение в качестве адъювантов фуллереновых производных аминокислот и дипептидов общей формулы С60-Х, где С60 - фуллереновое ядро, Х=NH-CHR-СООН, NH-(СН2)nCOOH, NH-CHR-СО-NH-CHR-СООН; n = от 2 до 6; R - боковой радикал природной аминокислоты (RU 2129436, А61К 38/05, опубл. 27.04.1999). Данное решение выбрано в качестве прототипа для водорастворимой наночастицы.
А из RU 2213048, С01В 31/02, С07С 229/06, опубл. 27.09.2003, известен например, способ получения водорастворимых солей аминокислотных производных фуллерена общей формулы HC60NH(CH2)nCOOM, где С60 - фуллереновое ядро, М - щелочной металл, n=1, 3, 5, включающий взаимодействие фуллерена с солью аминокислоты в среде органического растворителя при нагревании и последующего выделения целевого продукта, при этом взаимодействие осуществляют в присутствии низкомолекулярного полиалкиленоксида мол. массы 150-400. Данное решение выбрано в качестве прототипа для способа получения водорастворимой наночастицы.
Не найдено ни одного патента, который содержал бы описание фуллеренового наноадьюванта с точным указанием на вид нозологии, для профилактики и/или лечения которой должна создаваться вакцина, содержащая этот наноадъювант. Каждый из найденных патентов просто предлагает неспецифический способ увеличения активности реакций клеточного и гуморального иммунитета, сочетая в экспериментах на животных описываемый наноадъювант и антиген, представленный суспензией клеток убитых условно-патогенных микроорганизмов (и даже их произвольных смесей) - таких как Е. coli, Azotobacter vinilandii, Clostridium pasteurianum, Hehcobacter pilori, Streptococcus carnaei, и др.
Настоящее изобретение направлено на достижение технического результата, заключающегося в создании нового способа получения водорастворимой неагломератной фуллереновой наночастицы (НЧ), обладающей иммуномодулирующими свойствами.
Указанный технический результат достигается тем, что водорастворимая неагломератная фуллереновая иммуностимулирующая наночастица состоит из гидрофобного фуллеренового ядра, ковалентно соединенного с капрониловым лигандом посредством пиперазинового спейсера.
Указанный технический результат достигается тем, что способ получения водорастворимой неагломератной фуллереновой иммуностимулирующей наночастицы заключается в синтезе очищенной 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты в четыре этапа, на первом из которых получают 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазин, на втором этапе получают 6-(пиперазин-1-ил)-капроновой кислоты этиловый эфир путем растворения 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазина в 2Н HCl и упаривания полученного раствора, рН остатка которого доводят до значения 10,0, экстрагируют этилацетатом с просушкой органического слоя, на третьем этапе получают этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновую кислоту путем смешения и перемешивания до растворения фуллерена-С60 и толуола с добавлением после растворения Cp2TiCl2 и этилового эфира 6-(пиперазин-1-ил)-капроновой кислоты и последующим элюированием смесью гексан:хлороформ, а очищенную 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновую кислоту в виде готового продукта получают растворением этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты в этиловом спирте с добавлением раствора NaOH и нагреванием смеси при перемешивании до полной гомогенизации. Затем доводят рН реакционной смеси до нейтрального рН и выпавшую в осадок кислоту отделяют микрофильтрацией на фильтрах для последующего смывания осадков наночастиц и упаривания стокового осадка.
Указанные признаки являются существенными и взаимосвязаны с образованием устойчивой совокупности существенных признаков, достаточной для получения требуемого технического результата.
Настоящее изобретение поясняется иллюстрациями, где на рис.1 приведены схемы реакций, структуры интермедиатов и продукта.
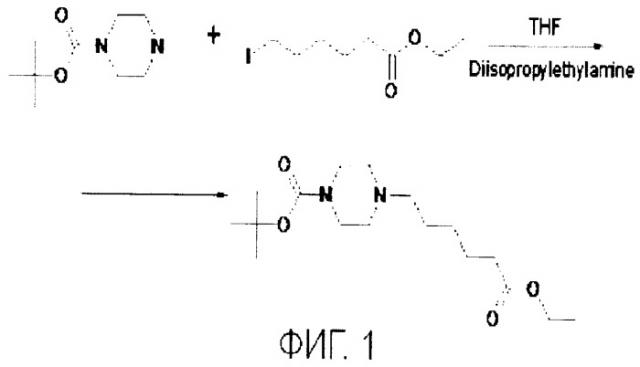
На фиг.1 - схема получения 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазина;
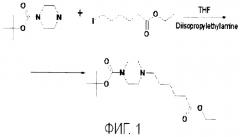
фиг.2 - схема получения 6-(пиперазин-1-ил)-капроновой кислоты этилового эфира;
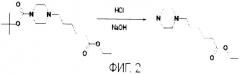
фиг.3 - схема получения этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты;
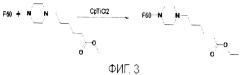
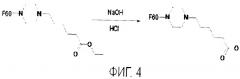
фиг.4 - схема получения 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты.
Основу разработанного авторами способа, поэтапно описанного ниже, составила функционализация фуллереновой С60-сферы с помощью использования реакции нуклеофильного циклоприсоединения Диес-Алдера в модификации авторов настоящего изобретения.
Целевым продуктом описываемого способа является водорастворимая неагломератная наночастица (размером 0,8-1,2 нм), состоящая из гидрофобного фуллеренового ядра, ковалентно соединенного с капрониловым лигандом посредством пиперазинового спейсера (лиганд - интерфейса).
Данная нанотопология НЧ уникальна и создана авторами впервые с учетом известных сведений о выраженных иммуностимулирующих свойствах бутирил- и капронил-аддуктов фуллерена-С60, с одной стороны, и учитывая прогнозы о возможном увеличении иммуностимулирующего эффекта фуллереновых НЧ при их функционализации азот-содержащими гетероциклами, с другой [Devenji I. & Lakatos S. (2011) A regressive prediction model for fullerene based nanostructures in the immunomimetic approach to vaccination enhancement, pp.207-238, In: Nanopharmaceuticals and Nanodevices for Contemporary Medicine (Waugh R.N. & Bielka H., Eds.), Szeged University Press: Szeged].
Предлагаемый способ состоит из четырех последовательных этапов синтеза интермедиатов и целевого продукта. Способ показан на примере получения 250 мг очищенной 1,2-дигидрофуллерен-1-(6-пиперазин- 1-ил)-капроновой кислоты)
Этапы способа
1. Получение 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазина (фиг.1)
24.3 г (90 мМоль) этилового эфира 6-Иодкапроновой кислоты и 16.79 г 1-Вос-пиперазина растворяли в 75 мл ТГФ, к раствору добавляли 16.95 мл (99 мМоль) диизопропилэтиламина. Реакционную смесь кипятили 6 часов. Затем растворитель упаривали в вакууме, остаток растворяли в этилацетате, органический слой 3 раза промывали раствором гидрокарбоната натрия и 1 раз водой, затем сушили над сульфатом магния и отгоняли растворитель. Полученное масло очищали хроматографически на колонке 80×400 мм с силикагелем SL200, растворитель/элюент - этилацетат. Выход: 27.6 г 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазина (93%).
2. Получение 6-(пиперазин-1-ил)-капроновой кислоты этиловый эфир (фиг.2).
26.3 г (80 мМоль) 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазина растворяли в 150 мл 2Н НС1 и раствор упаривали на роторном испарителе при 50°С под вакуумом. рН остатка доводили до значения 10,0 15%-ным раствором гидроксида натрия. Продукт экстрагировали этилацетатом, органический слой сушили над сульфатом магния и упаривали. Выход: 12 г 6-(пиперазин-1-ил)-капроновой кислоты этиловый эфир (66%).
3. Получение этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты (фиг.3)
В стеклянный реактор объемом 100 мл, установленный на магнитной мешалке, помещали 0.056 мМоль фуллерена-С60 в 50 мл толуола, перемешивали до полного растворения, вводили 0.0112 мМоль Cp2TiCl2 и 0.056 мМоль этилового эфира 6-(пиперазин-1-ил)-капроновой кислоты. Перемешивали при комнатной температуре. Реакционную массу пропускали через колонку, заполненную силикагелем марки L (100×250 мм). Продукт выделяли элюированием смесью гексан:хлороформ (6:1). Выход: 2,8 г этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты (21%).
4. Получение 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты (фиг.4).
Этиловый эфир 1,2-дигидрофуллерен-1 -(6-пиперазин-1 -ил)-капроновой кислоты растворяли в этиловом спирте и добавляли 33% раствор NaOH, смесь нагревали при перемешивании до полной гомогенизации. Реакционную смесь доводили до нейтрального рН, выпавшую в осадок кислоту отделяли микрофильтрацией на фиберглассовых фильтрах Millipore RX7M и затем тщательно отмывали преципитантным раствором этанол -NaOH (pH 7,0), пропуская не менее 70 мл его через 1,0 см2 поверхности фильтра. Выход: 62,5 мг 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты (2,3%).
Содержащие итоговый продукт фиберглассовые фильтры тщательно высушивали при комнатной температуре (аэрация феном), после чего находящиеся на них осадки наночастиц (наноадъювант) смывали 100-кратным объемом деминерализованной воды и упаривали в роторном испарителе до объема 2,5-3,0 мл. Полученные таким образом порции стокового раствора продукта объединяли и использовали для качественного анализа состава, идентификации структуры и количественного определения НЧ.
Проведенный синтез наноадъюванта выбранной структуры позволил получить итоговый продукт в количестве 250 мг, что достаточно для обеспечения необходимого тестирования по программе доклинических испытаний компонентов вакцины. Авторами не найдено ни одного патента, описывающего конкретную структуру полученного авторами целевого продукта. Пиперазиновый спейсер - иммунопровокатор, присутствующий в полученном продукте - фактор абсолютной патентной новизны.
Количественное определение интермедиатов и продукта в растворах проводили рефрактометрически с использованием калибровки по пиперазиновому вкладу. IR-VIS дифференциальную спектрофотометрию в диапазонах длин волн 280-330/520-770 нм и 1450-1970 нм дополнительно использовали для точного определения микрограммовых и миллиграммовых количеств целевого продукта в разбавленных водных растворах. Анализ проводили на двухлучевом сканирующем спектрофотометре Perkm Elmer Lambda 1050. В качестве калибровочных стандартов при этом использовали диглютамиласпарагил-фуллерен и чистый пиперазин. Расчет определяемых концентраций автоматизирован пакетом программного обеспечения LabRun 6A и осуществлен на аналитическом модуле НР4100 - 09 (Hewlett Packard).
Стоковый раствор продукта, юстированный до концентрации 25 мг/мл, стерилизовали ультрафильтрацией на мембранах Diaflo Y5.0 (Amicon QS400 UF System, 800 p.s.i.) и затем разливали в условиях стерильности (УФ-манипулятор) в автоклавированные герметически укупориваемые полиалломерные пробирки для последующего использования.
Для идентификации структур интермедиатов и целевого продукта использовали технологию LC-MS, в которой ЖХВД-система Shimadzu HPLC 600 TGS System соединена он-лайн с МАЛДИ-масс-спектрометром Shimadzu Prizm Analyser JS2200. Хроматографический модуль включал колонку 20×250 мм «Buckyclutcher-1» со стационарной фазой 5-ПББ (5-пентабромбензол), подвижная фаза - CS2, 16 мл/мин, 2000 p.s.i., 20-22 С. Масс-спектрометрический времяпролетный модуль включал анализатор, основанный на лазерной электроспрей-десорбции/ионизации испаряемого ЖХВД-элюата. Программа идентификации структуры включала аналитический пакет и библиотеку данных ERCO 2010 (NC Research Triangle) и была процессирована в модуле Shimadzu LMMC 440 XS Analyser.
Оценку степени аналитической чистоты (наличие и содержание примесей) осуществляли с помощью рутинной рентген-флуоресцентной спектрометрии водных растворов целевого продукта в аналитической системе Finnigan Matt RC708.
Определение размеров полученных наночастиц проводили с помощью стандартного метода АСМ-визуализации (NanoFinder AFM Orion - 302).
Использовали также метод седиментационного шлирен-оптического мониторинга при аналитическом равновесном ультрацентрифугировании стокового раствора НЧ. Образец такого раствора наносили на стандартный сведберговский линейный градиент плотности хлорида цезия (300000 g, +4°C, 18 часов, Sorvall M77 Analytical Ultracentrifuge). Калибровочными стандартами служили высокоочищенные препараты фуллерена С60, 0,7 нм, растворенные в толуоле, а также препараты РМС16, 1,8-2,0 нм, и пептидил-фуллерен ASK27, 4,8-5,2 нм, растворенные в воде.
Полученные данные качественного анализа целевого продукта (НЧ - наноадъювант пиперазинкапронил - фуллереновой структуры) приведены в таблице 1.
| Таблица 1 | ||
| Параметр, ед. измерения | Величина Параметра | |
| Заданная по НД | Установленная аналитически | |
| Мол. масса, а.е.м. | 920 | 920 |
| Количество, мг | не менее 250 | 267,7 |
| Хим. чистота, % | не менее 95 | 98,4 |
| Размер НЧ, нм | не более 2,0 | 0,8-1,2*** |
| Физ. гомогенность, % | не менее 90 | 94,6 |
| *** ПРИМЕЧАНИЕ: 0,8 нм - по данным АСМ; 1,2 нм - по данным седиментационного анализа. |
Исходя из данных, представленных в патентах и в изученной научной литературе, мы рекомендуем для проведения тестов на биологическую активность и безопасность продукта in vivo дозовый интервал 2,5-10 мг/кг при внутривенном введении крысам.
1. Водорастворимая неагломератная фуллереновая иммуностимулирующая наночастица, состоящая из гидрофобного фуллеренового ядра, ковалентно соединенного с капрониловым лигандом посредством пиперазинового спейсера.
2. Водорастворимая неагломератная фуллереновая иммуностимулирующая наночастица по п.1, отличающаяся тем, что имеет размер 0,8-1,2 нм.
3. Способ получения водорастворимой неагломератной фуллереновой иммуностимулирующей наночастицы, заключающийся в синтезе очищенной 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты в четыре этапа, на первом из которых получают 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазин, на втором этапе получают 6-(пиперазин-1-ил)-капроновой кислоты этиловый эфир путем растворения 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазина в 2Н НСl и упаривания полученного раствора, рН остатка которого доводят до значения 10,0, экстрагируют этилацетатом с просушкой органического слоя, на третьем этапе получают этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновую кислоту путем смешения и перемешивания до растворения фуллерена-С60 и толуола с добавлением после растворения Ср2TiСl2 и этилового эфира 6-(пиперазин-1-ил)-капроновой кислоты и последующим элюированием смесью гексан:хлороформ, а очищенную 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновую кислоту в виде готового продукта получают растворением этилового эфира 1,2-дигидрофуллерен-1-(6-пиперазин-1-ил)-капроновой кислоты в этиловом спирте с добавлением раствора NaOH и нагреванием смеси при перемешивании до полной гомогенизации, затем доводят рН реакционной смеси до нейтрального рН и выпавшую в осадок кислоту отделяют микрофильтрацией на фильтрах для последующего смывания осадков наночастиц и упаривания стокового осадка.
4. Способ по п.3, отличающийся тем, что 4-Вос-1-(5-этоксикарбонил-пентил)-пиперазин получают путем растворения этилового эфира 6-Иодкапроновой кислоты и 1-Вос-пиперазина в ТГФ с добавлением к раствору диизопропилэтиламина, последующим кипячением раствора и упариванием для получения остатка, который растворяют в этилацетате и промывают раствором гидрокарбоната натрия и водой, а затем высушивают с отгонкой растворителя.