Иммуноглобулин с двойными вариабельными доменами и его применения
Иллюстрации
Показать всеНастоящее изобретение относится к иммунологии и биотехнологии. Предложен связывающий белок для связывания одной или более мишеней, содержащий четыре полипептидные цепи, которые образуют четыре функциональных антигенсвязывающих сайта. Две полипептидные цепи содержат VD1-(X1)n-VD2-С-(Х2)n. VD1 означает первый вариабельный домен тяжелой цепи, VD2 означает второй вариабельный домен тяжелой цепи, С означает СН1 домен, X1 означает полипептидный линкер, при условии, что он не является константным доменом, и Х2 означает Fc-область, а n равно 0 или 1. Две полипептидные цепи содержат VD1-(X1)n-VD2-С. VD1 означает первый вариабельный домен легкой цепи, VD2 означает второй вариабельный домен легкой цепи, С означает CL домен, X1 означает линкер, при условии, что он не является константным доменом; и n равно 0 или 1. Описан конъюгат связывающего белка с визуализирующим, детектирующим, цитотоксическим или терапевтическим агентом. Раскрыты нуклеиновые кислоты (НК), кодирующие полипептидные цепи, а также: экспрессирующие вектора, вектора для репликации, клетки-хозяина их содержащие и способ получения антитела, использующий клетки. Описана фармацевтическая композиция для лечения или предупреждения связанного с мишенью заболевания или нарушения на основе связывающего белка. Раскрыт способ лечения путем введения связывающего белка. Использование изобретения обеспечивает новый формат (DVD-Ig) антигенсвязывающих молекул, которые при той же дозировке обладают большей активностью в отношении мишени, чем соответствующие полноразмерные антитела, что может найти применение в медицине для профилактики, лечения различных заболеваний. 13 н. и 52 з.п. ф-лы, 27 табл., 5 пр.
Реферат
Перекрестная ссылка на родственную заявку
В настоящей заявке заявляется приоритет по предварительной заявке США №60/709911, поданной 19 августа 2005 года, и предварительной заявке США №60/732892, поданной 2 ноября 2005 года.
Область техники, к которой относится изобретение
Данное изобретение относится к мультивалентным и мультиспецифическим связывающим белкам, способам получения и, в частности, к их применениям в предупреждении и/или лечении острых и хронических воспалительных, раковых и других заболеваний.
Уровень техники
Сконструированные белки, такие как мультиспецифические антитела, способные связывать два или более антигенов, известны в данной области. Такие мультиспецифические связывающие белки могут быть получены путем слияния клеток, химической конъюгации или способами рекомбинантных ДНК.
Биспецифические антитела получали с использованием технологии квадром (см. Milstein, С. and А.С.Cuello, Nature, 1983. 305(5934): p.537-40), основанной на соматическом слиянии двух разных гибридомных клеточных линий, экспрессирующих мышиные моноклональные антитела с желаемой специфичностью биспецифического антитела. Вследствие случайного спаривания двух разных тяжелых и легких цепей Ig в полученной гибрид-гибридомной (или квадромной) клеточной линии получали до десяти разных видов иммуноглобулинов, из которых только один является функциональным биспецифическим антителом. Присутствие ошибочно спаренных побочных продуктов и значимо уменьшенные выходы означают, что необходимы сложные методы очистки.
Биспецифические антитела могут быть получены химической конъюгацией двух разных mAb (см. Staerz, U.D., et al., Nature, 1985. 314(6012): p. 628-31). Этот подход не приводит к гомогенному препарату. В других подходах использовали химическую конъюгацию двух разных моноклональных антител или меньших фрагментов антител (см. Brennan, M., et al., Science, 1985. 229(4708): p. 81-3). Другим способом является связывание двух исходных антител с гетеро-бифункциональным сшивающим агентом, но полученные препараты биспецифических антител имели недостаток, заключающийся в существенной молекулярной гетерогенности, так как реакция сшивающего агента с исходными антителами не является сайт-направленной. Для получения более гомогенных препаратов биспецифических антител два разных Fab-фрагмента химически сшивали в их остатках цистеинов сайт-направленным образом (см. Glennie, M.J., et al., J Immunol, 1987. 139(7): p. 2367-75). Но этот способ приводит к F(ab')2-фрагментам, а не к полной молекуле IgG.
В последнее время было разработано широкое разнообразие других форматов рекомбинантных биспецифических антител (см. Kriangkum, J., et al., Biomol Eng, 2001. 18(2): p. 31-40). Среди них наиболее широко используемыми форматами для конструирования рекомбинантных биспецифических антител являются тандемные одноцепочечные Fv-молекулы и диатела и их различные производные. По стандартной методике конструирование этих молекул начинается с двух одноцепочечных Fv (scFv)-фрагментов, которые распознают различные антигены (см. Economides, A.N., et al., Nat Med, 2003. 9(1): p. 47-52). Тандемные молекулы scFv (taFv) представляют прямой формат, прямо соединяющий две молекулы scFv дополнительным пептидным линкером. Два scFv-фрагмента, присутствующие в этих тандемных молекулах scFv, образуют отдельные элементы укладки (фолдинга). Могут быть использованы разные линкеры для соединения двух scFv-фрагментов и линкеры с длиной до 63 остатков (см. Nakanishi, K., et al., Annu Rev Immunol, 2001. 19: p. 423-74). Хотя исходные scFv-фрагменты могут обычно экспрессироваться в растворимой форме в бактериях, часто наблюдается, что тандемные молекулы scFv образуют нерастворимые агрегаты в бактериях. Таким образом, протоколы рефолдинга или применения систем экспрессии млекопитающих используют обычным путем для получения тандемных молекул scFv. В недавнем исследовании сообщалось об экспрессии in vivo трансгенными кроликами и крупным рогатым скотом тандемного scFv, направленного против CD28 и ассоциированного с меланомой протеогликана (см. Gracie, J.A., et al., J Clin Invest, 1999. 104(10): p. 1393-401). В этой конструкции две молекулы scFv соединяли CH1-линкером и обнаруживали сывороточные концентрации биспецифического антитела до 100 мг/л. Для получения растворимой экспрессии в бактериях использовали различные стратегии, включая варьирования порядка доменов или использование средних линкеров варьируемой длины или гибкости. В настоящее время в нескольких исследованиях сообщалось об экспрессии растворимых тандемных молекул scFv в бактериях (см. Leung, B.P., et al., J Immunol, 2000. 164(12): p. 6495-502; Ito, A., et al., J Immunol, 2003. 170(9): p. 4802-9; Karni, A., et al., J Neuroimmunol, 2002. 125(1-2): p. 134-40) с использованием либо очень короткого линкера Ala3, либо длинных богатых глицином/серином линкеров. В недавнем исследовании использовали фаговый дисплей тандемного scFv-репертуара, содержащего рандомизированные средние линкеры длиной из 3 или 6 остатков, для обогащения в отношении молекул, которые продуцируются в растворимой и активной форме в бактериях. Этот подход приводил к выделению предпочтительной тандемной молекулы scFv с линкером из 6 аминокислотных остатков (см. Arndt, M. and J. Krauss, Methods Mol Biol, 2003. 207: p. 305-21). Неясно, представляет ли эта линкерная последовательность общее решение растворимой экспрессии тандемных молекул scFv. Тем не менее, данное исследование продемонстрировало, что фаговый дисплей тандемных молекул scFv в комбинации с направленным мутагенезом является мощным инструментом для обогащения этими молекулами, которые могут быть экспрессированы в бактериях в активной форме.
В биспецифических диателах (Db) для экспрессии используется димерный формат. Диатела получают из scFv-фрагментов уменьшением длины линкера, соединяющего VH- and VL-домен, до приблизительно 5 остатков (см. Peipp, M. and T. Valerius, Biochem Soc Trans, 2002. 30(4): p. 507-11). Уменьшение размера линкера облегчает димеризацию двух полипептидных цепей кроссоверным спариванием VH- и VL-доменов. Биспецифические диатела получают экспрессией двух полипептидных цепей либо со структурой VHA-VLB и VHB-VLA (конфигурацией VH-VL), либо со структурой VLA-VHB и VLB-VHA (конфигурацией VL-VH) в одной и той же клетке. В прошлом было получено большое разнообразие различных биспецифических диател, и большинство из них могут быть экспрессированы в растворимой форме в бактериях. Однако недавнее сравнительное исследование демонстрирует, что ориентация вариабельных доменов может влиять на экспрессию и образование активных связывающих сайтов (см. Mack, M., G. Riethmuller, and P. Kufer, Proc Natl Acad Sci U S A, 1995. 92(15): p. 7021-5). Тем не менее, растворимая экспрессия в бактериях представляет важное преимущество по сравнению с тандемными молекулами scFv. Однако поскольку две различные полипептидные цепи экспрессируются в одной клетке, вместе с активными гетеродимерами могут быть получены неактивные гомодимеры. Это создает необходимость введения дополнительных стадий очистки для получения гомогенных препаратов биспецифических диател. Одним из подходов для ускорения генерирования биспецифических диател является получение диател типа knob-into-hole (выпуклость-в-углубление) (см. Holliger, P., T. Prospero, and G. Winter, Proc Natl Acad Sci U S A, 1993. 90(14): p. 6444-8.18). Это было продемонстрировано для биспецифического диатела, направленного против HER2 и CD3. Большую «выпуклость» вводили в VH-домен заменой Val37 на Phe и Leu45 на Trp, а комплементарное «углубление» получали в VL-домене мутацией Phe98 в Met и Tyr87 в Ala в вариабельных доменах либо анти-HER2, либо анти-CD3. Используя такой подход, продуцирование биспецифических диател удалось увеличить с 72% исходного диатела до более 90% с использованием knob-into-hole диатела. Важно то, что выходы только слегка уменьшались в результате мутаций. Однако уменьшение антигенсвязывающей активности наблюдали для нескольких анализируемых конструкций. Таким образом, этот довольно сложный подход требует анализа многочисленных конструкций для идентификации мутаций, которые дают гетеродимерную молекулу с неизмененной связывающей активностью. Кроме того, такой подход требует мутационной модификации последовательности иммуноглобулина в константной области, что создает ненативную и неприродную форму последовательности антитела, что может приводить к увеличенной иммуногенности, плохой стабильности in vivo, а также нежелательной фармакокинетике.
Одноцепочечные диатела (scDb) представляют альтернативную стратегию для улучшения образования биспецифических диателоподобных молекул (см. Holliger, P. and G. Winter, Cancer Immunol Immunother, 1997. 45(3-4): p. 128-30; Wu, A.M., et al., Immunotechnology, 1996. 2(1): p. 21-36). Биспецифические одноцепочечные диатела получают соединением двух диателообразующих полипептидных цепей с дополнительным помещенным в середине линкером с длиной приблизительно 15 аминокислотных остатков. Таким образом, все молекулы с молекулярной массой, соответствующей мономерным одноцепочечным диателам (50-60 кДа), являются биспецифическими. Несколько исследований продемонстрировали, что биспецифические одноцепочечные диатела экспрессируются в бактериях в растворимой и активной форме, причем большинство очищенных молекул присутствуют в виде мономеров (см. Holliger, P. and G. Winter, Cancer Immunol Immunother, 1997. 45(3-4): p. 128-30; Wu, A.M., et al., Immunotechnology, 1996. 2(1): p. 21-36; Pluckthun, A. and P. Pack, Immunotechnology, 1997. 3(2): p. 83-105; Ridgway, J.B., et al., Protein Eng, 1996. 9(7): p. 617-21). Таким образом, одноцепочечные диатела объединяют преимущества тандемных scFvs (все мономеры являются биспецифическими) и диател (растворимая экспрессия в бактериях).
Позже диатело было слито с Fc для генерирования более Ig-подобных молекул, названных ди-диателом (см. Lu, D., et al., J Biol Chem, 2004. 279(4): p. 2856-65). Кроме того, была описана мультивалентная конструкция антитела, содержащая два Fab-повтора в тяжелой цепи IgG и способная связывать четыре молекулы антигена (см. WO 0177342A1, and Miller, K., et al., J Immunol, 2003. 170(9): p. 4854-61).
В данной области существует потребность в улучшенных мультивалентных связывающих белках, способных связывать два или более антигенов. Данное изобретение обеспечивает новое семейство связывающих белков, способных связывать два или более антигенов с высокой аффинностью.
Сущность изобретения
Данное изобретение относится к мультивалентным связывающим белкам, способным связывать два или более антигенов. Изобретение обеспечивает новое семейство связывающих белков, способных связывать два или более антигенов с высокой аффинностью.
В одном из вариантов осуществления данное изобретение обеспечивает связывающий белок, содержащий полипептидную цепь, причем указанная полипептидная цепь содержит VD1-(X1)n-VD2-C-(X2)n, где VD1 означает первый вариабельный домен, VD2 означает второй вариабельный домен, C означает константный домен, X1 представляет аминокислоту или полипептид, X2 представляет Fc-район и n равно 0 или 1. В предпочтительном варианте осуществления VD1 и VD2 в связывающем белке означают вариабельные домены тяжелой цепи. Более предпочтительно вариабельный домен тяжелой цепи выбран из группы, состоящей из мышиного вариабельного домена тяжелой цепи, вариабельного домена тяжелой цепи человека, CDR-трансплантированного вариабельного домена тяжелой цепи и гуманизированного вариабельного домена тяжелой цепи. В предпочтительном варианте осуществления VD1 и VD2 способны связывать один и тот же антиген. В другом варианте осуществления VD1 и VD2 способны связывать различные антигены. Предпочтительно С означает константный домен тяжелой цепи. Более предпочтительно X1 означает линкер при условии, что X1 не является CH1. Наиболее предпочтительно X1 означает линкер, выбранный из группы, состоящей из AKTTPKLEEGEFSEAR; AKTTPKLEEGEFSEARV; AKTTPKLGG; SAKTTPKLGG; AKTTPKLEEGEFSEARV; SAKTTP; SAKTTPKLGG; RADAAP; RADAAPTVS; RADAAAAGGPGS; RADAAAA(G4S)4; SAKTTP; SAKTTPKLGG; SAKTTPKLEEGEFSEARV; ADAAP; ADAAPTVSIFPP; TVAAP; TVAAPSVFIFPP; QPKAAP; QPKAAPSVTLFPP; AKTTPP; AKTTPPSVTPLAP; AKTTAP; AKTTAPSVYPLAP; ASTKGP; ASTKGPSVFPLAP, GGGGSGGGGSGGGGS; GENKVEYAPALMALS; GPAKELTPLKEAKVS и GHEAAAVMQVQYPAS. Предпочтительно X2 означает Fc-район. Более предпочтительно X2 является вариантным Fc-районом.
В предпочтительном варианте осуществления связывающий белок, описанный выше, содержит полипептидную цепь, причем указанная полипептидная цепь содержит VD1-(X1)n-VD2-C-(X2)n, где VD1 означает первый вариабельный домен тяжелой цепи, VD2 означает второй вариабельный домен тяжелой цепи, C означает константный домен тяжелой цепи, X1 означает линкер при условии, что он не является CH1 и X2 не является Fc-районом.
В другом варианте осуществления VD1 и VD2 в связывающем белке являются вариабельными доменами легкой цепи. Предпочтительно вариабельный домен легкой цепи выбран из группы, состоящей из мышиного вариабельного домена легкой цепи, вариабельного домена легкой цепи человека, CDR-трансплантированного вариабельного домена легкой цепи и гуманизированного вариабельного домена легкой цепи. В одном варианте осуществления VD1 и VD2 способны связывать один и тот же антиген. В другом варианте осуществления VD1 и VD2 способны связывать различные антигены. Предпочтительно С означает константный домен легкой цепи. Более предпочтительно X1 означает линкер при условии, что X1 не является CL1. Предпочтительно X1 является линкером, выбранным из группы, состоящей из AKTTPKLEEGEFSEAR; AKTTPKLEEGEFSEARV; AKTTPKLGG; SAKTTPKLGG; AKTTPKLEEGEFSEARV; SAKTTP; SAKTTPKLGG; RADAAP; RADAAPTVS; RADAAAAGGPGS; RADAAAA(G4S)4; SAKTTP; SAKTTPKLGG; SAKTTPKLEEGEFSEARV; ADAAP; ADAAPTVSIFPP; TVAAP; TVAAPSVFIFPP; QPKAAP; QPKAAPSVTLFPP; AKTTPP; AKTTPPSVTPLAP; AKTTAP; AKTTAPSVYPLAP; ASTKGP и ASTKGPSVFPLAP. Предпочтительно связывающий белок не содержит X2.
В предпочтительном варианте осуществления описанный выше связывающий белок содержит полипептидную цепь, причем указанная полипептидная цепь содержит VD1-(X1)n-VD2-C-(X2)n, где VD1 означает первый вариабельный домен легкой цепи, VD2 означает второй вариабельный домен легкой цепи, C означает константный домен легкой цепи, X1 означает линкер при условии, что он не является CH1 и X2 не содержит Fc-район.
В другом предпочтительном варианте осуществления данное изобретение обеспечивает связывающий белок, содержащий две полипептидные цепи, причем указанная первая полипептидная цепь содержит VD1-(X1)n-VD2-C-(X2)n, где VD1 означает первый вариабельный домен тяжелой цепи, VD2 означает второй вариабельный домен тяжелой цепи, C означает константный домен тяжелой цепи, X1 означает линкер при условии, что он не является CH1 и X2 не является Fc-районом; и указанная вторая полипептидная цепь содержит VD1-(X1)n-VD2-C-(X2)n, где VD1 означает первый вариабельный домен легкой цепи, VD2 означает второй вариабельный домен легкой цепи, C означает константный домен легкой цепи, X1 означает линкер при условии, что он не является CH1 и X2 не содержит Fc-район. Наиболее предпочтительно связывающий белок с двойными вариабельными доменами (DVD) содержит четыре полипептидные цепи, причем первые две полипептидные цепи содержат VD1-(X1)n-VD2-C-(X2)n, соответственно, где VD1 означает первый вариабельный домен тяжелой цепи, VD2 означает второй вариабельный домен тяжелой цепи, C означает константный домен тяжелой цепи, X1 означает линкер при условии, что он не является CH1 и X2 является Fc-районом; и вторые две полипептидные цепи содержат VD1-(X1)n-VD2-C-(X2)n, соответственно, где VD1 означает первый вариабельный домен легкой цепи, VD2 означает второй вариабельный домен легкой цепи, C означает константный домен легкой цепи, X1 означает линкер при условии, что он не является CH1 и X2 не содержит Fc-район. Такой белок с двойными вариабельными доменами (DVD) имеет четыре антигенсвязывающих сайта.
В другом предпочтительном варианте осуществления описанные выше связывающие белки способны связывать одну или несколько мишеней. Предпочтительно мишень выбрана из группы, состоящей из цитокинов, белков клеточной поверхности, ферментов и рецепторов. Предпочтительно связывающий белок способен модулировать биологическую функцию одной или нескольких мишеней. Более предпочтительно связывающий белок способен нейтрализовать одну или несколько мишеней. Связывающий белок согласно изобретению способен связывать цитокины, выбранные из группы, состоящей из лимфокинов, монокинов и полипептидных гормонов. В конкретном варианте осуществления связывающий белок способен связывать пары цитокинов, выбранные из группы, состоящей из IL-1α и IL-1β; IL-12 и IL-18, TNFα и IL-23, TNFα и IL-13; TNF и IL-18; TNF и IL-12; TNF и IL-1β; TNF и MIF; TNF и IL-17; и TNF и IL-15; TNF и VEGF; VEGFR и EGFR; IL-13 и IL-9; IL-13 и IL-4; IL-13 и IL-5; IL-13 и IL-25; IL-13 и TARC; IL-13 и MDC; IL-13 и MIF; IL-13 и TGF-β; IL-13 и агониста LHR; IL-13 и CL25; IL-13 и SPRR2a; IL-13 и SPRR2b; IL-13 и ADAM8; и TNFα и PGE4, IL-13 и PED2, TNF и PEG2. В другом варианте осуществления связывающий белок согласно изобретению способен связывать пары мишеней, выбранные из группы, состоящей из CD138 и CD20; CD138 и CD40; CD19 и CD20; CD20 и CD3; CD38 и CD138; CD38 и CD20; CD38 и CD40; CD40 и CD20; CD-8 и IL-6; CSPG и RGM A; CTLA-4 и BTNO2; IGF1 и IGF2; IGF1/2 и Erb2B; IL-12 и TWEAK; IL-13 и IL-1β; MAG и RGM A; NgR и RGM A; NogoA и RGM A; OMGp и RGM A; PDL-1 и CTLA-4; RGM A и RGM B; Te38 и TNFα; TNFα и Blys; TNFα и CD-22; TNFα и CTLA-4; TNFα и GP130; TNFα и IL-12p40; и TNFα и лиганда RANK.
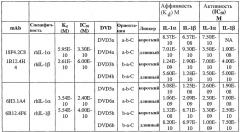
В одном варианте осуществления связывающий белок, способный связывать IL-1α человека и IL-1β человека, содержит аминокислотную последовательность тяжелой цепи DVD, выбранную из группы, состоящей из SEQ ID NO. 33, SEQ ID NO. 37, SEQ ID NO. 41, SEQ ID NO. 45, SEQ ID NO. 47, SEQ ID NO. 51, SEQ ID NO. 53, SEQ ID NO. 55, SEQ ID NO. 57 и SEQ ID NO. 59; и аминокислотную последовательность легкой цепи DVD, выбранную из группы, состоящей из SEQ ID NO. 35, SEQ ID NO. 39, SEQ ID NO. 43, SEQ ID NO. 46, SEQ ID NO. 49, SEQ ID NO. 52, SEQ ID NO. 54, SEQ ID NO. 56, SEQ ID NO. 58 и SEQ ID NO. 60. В другом варианте осуществления связывающий белок, способный связывать мышиный IL-1α и мышиный IL-1β, содержит аминокислотную последовательность тяжелой цепи DVD SEQ ID NO. 105 и аминокислотную последовательность легкой цепи DVD SEQ ID NO. 109.
В одном варианте осуществления связывающий белок, способный связывать IL-12 и IL-18, содержит аминокислотную последовательность тяжелой цепи DVD, выбранную из группы, состоящей из SEQ ID NO. 83, SEQ ID NO. 90, SEQ ID NO. 93, SEQ ID NO. 95 и SEQ ID NO. 114; и аминокислотную последовательность легкой цепи DVD, выбранную из группы, состоящей из SEQ ID NO. 86, SEQ ID NO. 91, SEQ ID NO. 94, SEQ ID NO. 46, SEQ ID NO. 96 и SEQ ID NO. 116.
В одном варианте осуществления связывающий белок, способный связывать CD20 и CD3, содержит аминокислотную последовательность тяжелой цепи DVD SEQ ID NO. 97 и аминокислотную последовательность легкой цепи DVD SEQ ID NO. 101.
В другом варианте осуществления связывающий белок согласно изобретению способен связывать один, два или более цитокинов, цитокин-родственных белков и рецепторов цитокинов, выбранных из группы, состоящей из BMP1, BMP2, BMP3B (GDF10), BMP4, BMP6, BMP8, CSF1 (M-CSF), CSF2 (GM-CSF), CSF3 (G-CSF), EPO, FGF1 (aFGF), FGF2 (bFGF), FGF3 (int-2), FGF4 (HST), FGF5, FGF6 (HST-2), FGF7 (KGF), FGF9, FGF10, FGF11, FGF12, FGF12B, FGF14, FGF16, FGF17, FGF19, FGF20, FGF21, FGF23, IGF1, IGF2, IFNA1, IFNA2, IFNA4, IFNA5, IFNA6, IFNA7, IFNB1, IFNG, IFNW1, FIL1, FIL1 (EPSILON), FIL1 (ZETA), IL1A, IL1B, IL2, IL3, IL4, IL5, IL6, IL7, IL8, IL9, IL10, IL11, IL12A, IL12B, IL13, IL14, IL15, IL16, IL17, IL17B, IL18, IL19, IL20, IL22, IL23, IL24, IL25, IL26, IL27, IL28A, IL28B, IL29, IL30, PDGFA, PDGFB, TGFA, TGFB1, TGFB2, TGFB3, LTA (TNF-b), LTB, TNF (TNF-a), TNFSF4 (лиганда OX40), TNFSF5 (лиганда CD40), TNFSF6 (FasL), TNFSF7 (лиганда СD27), TNFSF8 (лиганда CD30), TNFSF9 (лиганда 4-1BB), TNFSF10 (TRAIL), TNFSF11 (TRANCE), TNFSF12 (APO3L), TNFSF13 (April), TNFSF13B, TNFSF14 (HVEM-L), TNFSF15 (VEGI), TNFSF18, FIGF (VEGFD), VEGF, VEGFB, VEGFC, IL1R1, IL1R2, IL1RL1, IL1RL2, IL2RA, IL2RB, IL2RG, IL3RA, IL4R, IL5RA, IL6R, IL7R, IL8RA, IL8RB, IL9R, IL10RA, IL10RB, IL11RA, IL12RB1, IL12RB2, IL13RA1, IL13RA2, IL15RA, IL17R, IL18R1, IL20RA, IL21R, IL22R, IL1HY1, IL1RAP, IL1RAPL1, IL1RAPL2, IL1RN, IL6ST, IL18BP, IL18RAP, IL22RA2, AIF1, HGF, LEP (лептина), PTN и THPO.
Связывающий белок согласно изобретению способен связывать один или несколько хемокинов, рецепторов хемокинов и хемокин-родственных белков, выбранных из группы, состоящей из CCL1 (I-309), CCL2 (MCP-1/MCAF), CCL3 (MIP-1a), CCL4 (MIP-1b), CCL5 (RANTES), CCL7 (MCP-3), CCL8 (mcp-2), CCL11 (эотаксина), CCL13 (MCP-4), CCL15 (MIP-1d), CCL16 (HCC-4), CCL17 (TARC), CCL18 (PARC), CCL19 (MIP-3b), CCL20 (MIP-3a), CCL21 (SLC/эксодуса-2), CCL22 (MDC/STC-1), CCL23 (MPIF-1), CCL24 (MPIF-2/эотаксин-2), CCL25 (TECK), CCL26 (эотаксин-3), CCL27 (CTACK/ILC), CCL28, CXCL1 (GRO1), CXCL2 (GRO2), CXCL3 (GRO3), CXCL5 (ENA-78), CXCL6 (GCP-2), CXCL9 (MIG), CXCL10 (IP 10), CXCL11 (I-TAC), CXCL12 (SDF1), CXCL13, CXCL14, CXCL16, PF4 (CXCL4), PPBP (CXCL7), CX3CL1 (SCYD1), SCYE1, XCL1 (лимфотактина), XCL2 (SCM-1b), BLR1 (MDR15), CCBP2 (D6/JAB61), CCR1 (CKR1/HM145), CCR2 (mcp-1RB/RA), CCR3 (CKR3/CMKBR3), CCR4, CCR5 (CMKBR5/ChemR13), CCR6 (CMKBR6/CKR-L3/STRL22/DRY6), CCR7 (CKR7/EBI1), CCR8 (CMKBR8/TER1/CKR-L1), CCR9 (GPR-9-6), CCRL1 (VSHK1), CCRL2 (L-CCR), XCR1 (GPR5/CCXCR1), CMKLR1, CMKOR1 (RDC1), CX3CR1 (V28), CXCR4, GPR2 (CCR10), GPR31, GPR81 (FKSG80), CXCR3 (GPR9/CKR-L2), CXCR6 (TYMSTR/STRL33/Bonzo), HM74, IL8RA (IL8Ra), IL8RB (IL8Rb), LTB4R (GPR16), TCP10, CKLFSF2, CKLFSF3, CKLFSF4, CKLFSF5, CKLFSF6, CKLFSF7, CKLFSF8, BDNF, C5R1, CSF3, GRCC10 (C10), EPO, FY (DARC), GDF5, HIF1A, IL8, PRL, RGS3, RGS13, SDF2, SLIT2, TLR2, TLR4, TREM1, TREM2 и VHL. Связывающий белок согласно изобретению способен связывать белок клеточной поверхности, выбранный из группы, состоящей из интегринов. Связывающий белок согласно изобретению способен связывать фермент, выбранный из группы, состоящей из киназ и протеаз. Связывающий белок согласно изобретению способен связывать рецептор, выбранный из группы, состоящей из рецептора лимфокина, рецептора монокина и рецептора полипептидного гормона.
В предпочтительном варианте осуществления связывающий белок является мультивалентным. Более предпочтительно связывающий белок является мультиспецифическим. Мультивалентные и/или мультиспецифические связывающие белки, описанные выше, обладают желаемыми свойствами, в частности, с терапевтической точки зрения. Например, мультивалентный и/или мультиспецифический связывающий белок может (1) быть интернализован (и/или катаболизирован) быстрее, чем бивалентное антитело, клеткой, экспрессирующей антиген, с которым антитела связываются; (2) быть антителом-агонистом; и/или (3) индуцировать смерть клетки и/или апоптоз клетки, экспрессирующей антиген, с которым мультивалентное антитело может связываться. «Исходное антитело», которое обеспечивает по меньшей мере одну антигенсвязывающую специфичность мультивалентных и/или мультиспецифических связывающих белков, может быть антителом, которое интернализуется (и/или катаболизируется) клеткой, экспрессирующей антиген, с которым связывается антитело); и/или может быть агонистом, индуцирующим смерть клетки и/или индуцирующим апоптоз, и описанный здесь мультивалентный и/или мультиспецифический связывающий белок может проявлять улучшение (улучшения) в одном или нескольких из указанных свойств. Кроме того, исходное антитело может быть лишено любого одного или нескольких из этих свойств, но может быть наделено ими при конструировании в виде описанного здесь мультивалентного связывающего белка.
В другом варианте осуществления связывающий белок согласно изобретению имеет константу скорости ассоциации (Kon) в отношении одной или нескольких мишеней, выбранную из группы, состоящей из значений указанной константы, составляющих по меньшей мере приблизительно 102M-1с-1; по меньшей мере приблизительно 103M-1с-1; по меньшей мере приблизительно 104M-1с-1; по меньшей мере приблизительно 105M-1с-1; и по меньшей мере приблизительно 106M-1с-1, как измерено с использованием резонанса поверхностного плазмона. Предпочтительно связывающий белок согласно изобретению имеет константу скорости ассоциации (Kon) в отношении одной или нескольких мишеней, составляющую от 102M-1с-1 до 103M-1с1; от 103M-1с1 до 104M-1с1; от 104M-1с-1 до 105M-1с-1 или от 105M-1с-1 до 106M-1с-1, как измерено с использованием резонанса поверхностного плазмона.
В другом варианте осуществления связывающий белок имеет константу скорости диссоциации (Koff) в отношении одной или нескольких мишеней, выбранную из группы, состоящей из значений указанной константы, составляющих самое большее приблизительно 10-3с-1; самое большее приблизительно 10-4с-1; самое большее приблизительно 10-5с-1; и самое большее приблизительно 10-6с-1, как измерено с использованием резонанса поверхностного плазмона. Предпочтительно связывающий белок согласно изобретению имеет константу скорости диссоциации (Koff) по отношению к одной или нескольким мишеням, составляющую от 10-3с-1до 10-4с-1; от 10-4с-1 до 10-5с-1; или от 10-5с-1 до 10-6с-1, как измерено с использованием резонанса поверхностного плазмона.
В другом варианте осуществления связывающий белок имеет константу диссоциации (KD) в отношении одной или нескольких мишеней, выбранную из группы, состоящей из значений указанной константы, составляющих самое большее приблизительно 10-7 M; самое большее приблизительно 10-8 M; самое большее приблизительно 10-9 M; самое большее приблизительно 10-10 M; самое большее приблизительно 10-11 M; самое большее приблизительно 10-12 M; и самое большее 10-13 M. Предпочтительно связывающий белок согласно изобретению имеет константу диссоциации (KD) в отношении IL-12 или IL-23, составляющую от 10-7 M до 10-8 M; от 10-8 M до 10-9 M; от 10-9 M до 10-10 M; от 10-10 до 10-11 M; от 10-11 M до 10-12 M; или от 10-12 до M 10-13 M.
В другом варианте осуществления описанный выше связывающий белок является конъюгатом, дополнительно содержащим агент, выбранный из группы, состоящей из молекулы иммуноадгезии, агента визуализации, терапевтического агента и цитотоксического агента. Предпочтительно агент визуализации выбран из группы, состоящей из радиоизотопной метки, фермента, флуоресцентной метки, люминесцентной метки, биолюминесцентной метки, магнитной метки и биотина. Более предпочтительно агентом визуализации является радиоизотопная метка, выбранная из группы, состоящей из 3H, 14C, 35S, 90Y, 99Tc, 111In, 125I, 131I, 177Lu, 166Ho и 153Sm. Предпочтительно терапевтический или цитотоксический агент выбран из группы, состоящей из антиметаболита, алкилирующего агента, антибиотика, фактора роста, цитокина, антиангиогенного агента, антимитотического агента, антрациклина, токсина и апоптотического агента.
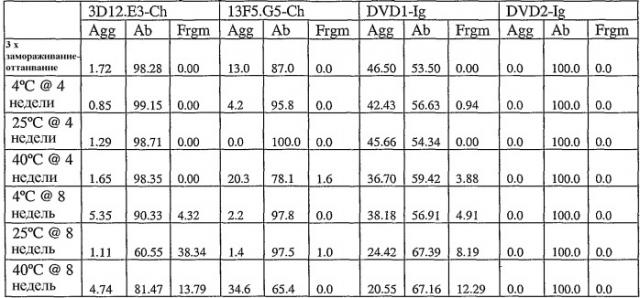
В другом варианте осуществления описанный выше связывающий белок является кристаллизованным связывающим белком и существует в виде кристалла. Предпочтительно этот кристалл является не содержащим носитель фармацевтическим кристаллом регулируемого высвобождения. Более предпочтительно кристаллизованный связывающий белок имеет больший период полу-жизни in vivo, чем растворимый аналог указанного связывающего белка. Наиболее предпочтительно кристаллизованный связывающий белок сохраняет биологическую активность.
В другом варианте осуществления описанный выше связывающий белок является гликозилированным. Предпочтительно гликозилирование является гликозилированием, характерным для человека.
Один из аспектов данного изобретения относится к выделенной нуклеиновой кислоте, кодирующей любой из описанных выше связывающих белков. Дополнительный вариант осуществления обеспечивает вектор, содержащий описанную выше нуклеиновую кислоту, причем указанный вектор выбран из группы, состоящей из pcDNA; pTT (Durocher et al., Nucleic Acids Research 2002, Vol 30, No.2); pTT3 (pTT с дополнительным сайтом множественного клонирования; pEFBOS (Mizushima, S. and Nagata, S., (1990) Nucleic acids Research Vol 18, No. 17); pBV; pJV; pcDNA3.1 TOPO, pEF6 TOPO и pBJ.
В другом аспекте клетку-хозяина трансформируют описанным выше вектором. Предпочтительно клеткой-хозяином является прокариотическая клетка. Более предпочтительно клеткой-хозяином является E.coli. В родственном варианте осуществления клеткой-хозяином является эукариотическая клетка. Предпочтительно эукариотическая клетка выбрана из группы, состоящей из клетки протиста, клетки животного, клетки растения и грибковой клетки. Более предпочтительно клеткой-хозяином является клетка млекопитающего, включая, но не ограничиваясь ими, СНО и COS; или грибковая клетка, такая как Saccharomyces cerevisiae; или клетка насекомого, такая как Sf9.
В другом аспекте данного изобретения предусмотрен способ получения описанного выше связывающего белка, включающий культивирование любой из клеток-хозяев, также описанных выше, в культуральной среде в условиях, достаточных для продуцирования связывающего белка. Предпочтительно 50%-75% связывающего белка, полученного указанным способом, являются четырехвалентным связывающим белком с двойной специфичностью. Более предпочтительно 75%-90% связывающего белка, полученного указанным способом, являются четырехвалентным белком с двойной специфичностью. Наиболее предпочтительно 90%-95% получаемого связывающего белка являются четырехвалентным связывающим белком с двойной специфичностью.
Другой вариант осуществления обеспечивает связывающий белок, полученный в соответствии с описанным выше способом.
Один из вариантов осуществления обеспечивает композицию для высвобождения связывающего белка, где композиция содержит готовую форму, которая, в свою очередь, содержит описанный выше кристаллизованный связывающий белок и ингредиент; и по меньшей мере один полимерный носитель. Предпочтительно полимерным носителем является полимер, выбранный из одной или нескольких групп, состоящих из поли(акриловой кислоты), поли(цианоакрилатов), поли(аминокислот), поли(ангидридов), поли(депсипептидов), поли(сложных эфиров), поли(молочной кислоты), сополимера молочной и гликолевой кислот или PLGA, поли(β-гидроксибутирата), поли(капролактона), поли(диоксанона); поли(этиленгликоля), поли(гидроксипропил)метакриламида, поли[(органо)фосфацена], поли(сложных ортоэфиров), поли(винилового спирта), поли(винилпирролидона), сополимеров малеинового ангидрида и алкилвинилового эфира, полиолов плуроников, альбумина, альгината, целлюлозы и производных целлюлозы, коллагена, фибрина, желатина, гиалуроновой кислоты, олигосахаридов, гликаминогликанов, сульфатированных полисахаридов, их смесей и сополимеров. Предпочтительно ингредиент выбран из группы, состоящей из альбумина, сахарозы, трегалозы, лактита, желатина, гидроксипропил-β-циклодекстрина, метоксиполиэтиленгликоля и полиэтиленгликоля. В другом варианте осуществления представлен способ лечения млекопитающего, включающий стадию введения млекопитающему эффективного количества описанной выше композиции.
Данное изобретение обеспечивает также фармацевтическую композицию, содержащую описанный выше связывающий белок и фармацевтически приемлемый носитель. В следующем варианте осуществления фармацевтическая композиция содержит по меньшей мере один дополнительный терапевтический агент для лечения нарушения. Предпочтительно дополнительный агент выбран из группы, состоящей из терапевтического агента, агента визуализации, цитотоксического агента, ингибиторов ангиогенеза (включая, но не ограничиваясь ими, анти-VEGF-антитела или VEGF-trap); ингибиторов киназ (включая, но не ограничиваясь ими, ингибиторы KDR и TIE-2); блокаторов молекул костимуляции (включая, но не ограничиваясь ими, анти-B7.1, анти-B7.2, CTLA4-Ig, анти-CD20); блокаторов молекул адгезии (включая, но не ограничиваясь ими, анти-LFA-1-Ab, анти-E/L селектин-Ab, ингибиторы с малой молекулой); анти-цитокин-антитела или его функционального фрагмента (включая, но не ограничиваясь ими, анти-IL-18, анти-TNF, антитела против IL-6/рецептора цитокина); метотрексата; циклоспорина; рапамицина; FK506; детектируемой метки или репортера; антагониста TNF; противоревматического агента; миорелаксанта, наркотического агента, нестероидного противовоспалительного лекарственного средства (NSAID), аналгезирующего агента, анестезирующего агента, седативного средства, местного анестезирующего средства, нервно-мышечного блокатора, противомикробного агента, антипсориатического агента, кортикостероида, анаболического стероида, эритропоэтина, иммунизации, иммуноглобулина, иммунодепрессанта, гормона роста, замещающего гормон лекарственного средства, радиофармацевтического средства, антидепрессанта, антипсихотического средства, стимулятора, противоастматического средства, бета-агониста, ингалируемого стероида, эпинефрина или его аналога, цитокина и антагониста цитокина.
В другом аспекте данное изобретение обеспечивает способ лечения субъекта-человека, страдающего от нарушения, в котором мишень или мишени, способные связываться описанным выше связывающим белком, является (являются) вредными, предусматривающий введение этому субъекту-человеку описанного выше связывающего белка так, чтобы ингибировать активность мишени или мишеней у субъекта-человека и добиться лечения. Предпочтительно нарушение выбрано из группы, состоящей из артрита, остеоартрита, хронического ювенильного артрита, септического артрита, артрита Лайма, псориатического артрита, реактивного артрита, спондилоартропатии, системной красной волчанки, болезни Крона, язвенного колита, воспалительного заболевания кишечника, инсулинзависимого сахарного диабета, тиреоидита, астмы, аллергических заболеваний, псориаза, дерматита, склеродермии, болезни трансплантат против хозяина, отторжения трансплантатов органов, острого или хронического иммунного заболевания, ассоциированного с трансплантацией органов, саркоидоза, атеросклероза, диссеминированного внутрисосудистого свертывания, болезни Кавасаки, болезни Грейвса, нефротического синдрома, синдрома хронической усталости, гранулематоза Вегенера, пурпуры Геноха-Шенлейна, микроскопического васкулита почек, хронического активного гепатита, увеита, септического шока, синдрома токсического шока, синдрома сепсиса, кахексии, инфекционных заболеваний, паразитарных заболеваний, синдрома приобретенного иммунодефицита, острого поперечного миелита, хореи Гентингтона, болезни Паркинсона, болезни Альцгеймера, инсульта, первичного билиарного цирроза, гемолитической анемии, злокачественных заболеваний, сердечной недостаточности, инфаркта миокарда, болезни Аддисона, спорадической плюригландулярной недостаточности типа I и плюригландулярной недостаточности типа II, синдрома Шмидта, (острого) респираторного дистресс-синдрома взрослых, алопеции, гнездной (очаговой) алопеции, сероотрицательной артропатии, артропатии, болезни Рейтера, псориатической артропатии, артропатии язвенного колита, энтеропатического синовита, ассоциированной с Chlamydia, Yersinia и Salmonella артропатии, спондилоартропатии, атероматозного заболевания/артериосклероза, атопической аллергии, аутоиммунного буллезного заболевания, пузырчатки обыкновенной, листовидной пузырчатки, пемфигоида, линейного IgA-заболевания, аутоиммунной гемолитической анемии, положительной гемолитической анемии Кумбса, приобретенной пернициозной анемии, ювенильной пернициозной анемии, миалгического энцефалита/британского миалгического энцефалита, хронического кожно-слизистого кандидоза, гигантоклеточного артериита, первичного склерозирующего гепатита, криптогенного аутоиммунного гепатита, синдрома приобретенного иммунодефицита, заболеваний, родственных приобретенному иммунодефициту, гепатита В, гепатита С, общего транзиторного иммунодефицита (общей транзиторной гипогаммаглобулинемии), дилатационной кардиомиопатии, женского бесплодия, угасания функции яичников, преждевременного угасания функции яичников, фибротического заболевания легких, криптогенного фиброзирующего альвеолита, послевоспалительного интерстициального заболевания легких, интерстициального пневмонита, ассоциированной с болезнью соединительной ткани интерстициальной болезни легких, ассоциированной с болезнью смешанной соединительной ткани болезни легких, ассоциированной с системным склерозом интерстициальной болезни легких, ассоциированной с ревматоидным артритом интерстициальной болезни легких, ассоциированной с системной красной волчанкой болезни легких, ассоциированной с дерматомиозитом/полимиозитом болезни легких, ассоциированной с болезнью Шегрена болезни легких, ассоциированной с анкилозирующим спондилитом болезни легких, васкулитной диффузной болезни легких, ассоциированной с гемосидерозом болезни легких, индуцированной лекарственным средством интерстициальной болезни легких, фиброза, лучевого фиброза, облитерирующего бронхиолита, хронической эозинофильной пневмонии, лимфоцитарного инфильтративного заболевания легких, постинфекционного интерстициального заболевания легких, подагрического артрита, аутоиммунного гепатита, аутоиммунного гепатита типа-1 (классического аутоиммунного или люпоидного гепатита), аутоиммунного гепатита типа-2 (гепатита с анти-LKM-антителами), аутоиммунно опосредованной гипогликемии, инсулинорезистентности типа В с папиллярно-пигментной дистрофией кожи (acanthosis nigricans), гипопаратиреоза, острого иммунного заболевания, ассоциированного с трансплантацией органа, хронического иммунного заболевания, ассоциированного с трансплантацией органа, остеоартроза, первичного склерозирующего холангита, псориаза типа 1, псориаза типа 2, идиопатической лейкопении, аутоиммунной нейтропении, почечного заболевания NOS (БДУ), гломерулонефрита, микроскопического васкулита почек, болезни Лайма, дискоидной красной волчанки, мужского бесплодия идиопатического или NOS (БДУ), аутоиммунности спермы, рассеянного склероза (всех подтипов), симпатической офтальмии, легочной гипертензии, вторичной относительно заболевания соединительной ткани, синдрома Гудпасчера, легочной манифестации нодозн