Способ разделения акриловой кислоты, содержащейся в качестве основного компонента и глиоксаля, содержащегося в качестве побочного продукта в газообразной смеси продуктов частичного гетерогенно катализируемого парофазного окисления соединения-предшественника акриловой кислоты, содержащего 3 атома углерода
Иллюстрации
Показать всеИзобретение относится к способу разделения акриловой кислоты, содержащейся в качестве основного продукта, и глиоксаля, содержащегося в качестве побочного продукта, в смеси продуктов частичного гетерогенно катализируемого парофазного окисления соединения-предшественника акриловой кислоты, содержащего 3 атома углерода, при котором получают жидкую фазу Р, которая по меньшей мере на 70% от своей массы состоит из акриловой кислоты, а также, в пересчете на молярное количество содержащейся в ней акриловой кислоты, содержит по меньшей мере 200 мол. м.д. глиоксаля, при котором это отделение глиоксаля от акриловой кислоты осуществляется путем кристаллизации из жидкой фазы Р. Способ позволяет предотвратить нежелательную полимеризацию акриловой кислоты. 24 з.п. ф-лы.
Реферат
Данное изобретение касается способа разделения акриловой кислоты, содержащейся в качестве основного продукта, и глиоксаля, содержащегося в качестве побочного продукта в газообразной смеси продуктов частичного гетерогенно катализируемого парофазного окисления соединения-предшественника акриловой кислоты, содержащего 3 атома углерода, при котором получают жидкую фазу Р, которая по меньшей мере на 70% от своей массы состоит из акриловой кислоты, а также, в пересчете на молярное количество содержащейся в ней акриловой кислоты, содержит по меньшей мере 200 мол. м.д. глиоксаля.
Акриловая кислота представляет собой важнейший мономер, который находит применение как таковой и/или в форме его сложных алкиловых эфиров для производства полимеров, используемых в области гигиены (например, суперабсорбирующих воду) (смотри, например, международные заявки WO 02/055469 и WO 03/078378).
Получение акриловой кислоты может осуществляться, например, путем гетерогенно катализируемого частичного окисления в газовой фазе соединения-предшественника, содержащего 3 атома углерода (например, пропилена, пропана, акролеина, пропионового альдегида, пропионовой кислоты, пропанола и/или глицерина), (смотри, например, европейскую заявку на патент ЕР-А 990 636, заявку на патент США US-A 5,198,578, европейские заявки на патент ЕР-А 1 015 410, ЕР-А 1 484 303, ЕР-А 1 484 308, ЕР-А 1 484 309, заявку на патент США US-A 2004/0242826 и международную заявку WO 2006/136336).
Как правило, в рамках такого гетерогенно-катализируемого частичного парофазного окисления получается не чистая акриловая кислота, а лишь газообразная смесь продуктов, содержащая акриловую кислоту, которая помимо этой акриловой кислоты также содержит компоненты, отличающиеся от акриловой кислоты, от которых эта акриловая кислота должна быть отделена.
Как на вид, так и на количественное содержание в газообразной смеси продуктов компонентов, отличающихся от акриловой кислоты, среди прочего, могут влиять чистота используемого в качестве исходного сырья соединения-предшественника, содержащего 3 атома углерода, а также условия реакции, при которых проводится это гетерогенно-катализируемое частичное парофазное окисление (сравни, например, немецкие заявки на патент DE-A 101 31 297 и DE-A 10 2005 052 917).
Из европейской заявки ЕР-А 770 592 известно, что газообразная смесь продуктов такого гетерогенно-катализируемого частичного парофазного окисления, среди прочего, может содержать в качестве отличающихся от акриловой кислоты компонентов различные альдегиды. Кроме того, из европейской заявки ЕР-А 770 592 известно, что самые незначительные количества альдегидных примесей, остающихся в акриловой кислоте, могут оказывать значительное отрицательное влияние на свойства акриловой кислоты. Так, в соответствии с техническим решением европейской заявки на патент ЕР-А 770 592, отдельные количества альдегида в акриловой кислоте должны были находиться в области менее 1 м.д., чтобы в рамках применения такой акриловой кислоты, прежде всего, в радикальных реакциях полимеризации, например, для получения суперабсорбирующих полимеров или полимеров, эффективных в качестве диспергирующих средств для буровых растворов на основе углеводородов или в качестве коагулянтов, достичь оптимальных характеристик продукции. Чтобы достичь такой степени разделения, в европейской заявке на патент ЕР-А 770 592 предлагают совместное применение акцепторов альдегидов. Однако их дополнительный расход одновременно обусловливает недостатки способа, предлагаемого в этой европейской заявке на патент ЕР-А 770 592.
Из европейской заявки на патент ЕР-А 1 298 120 известно, что в качестве возможного побочного продукта гетерогенно-катализируемого частичного парофазного окисления соединений-предшественников с 3 атомами углерода до акриловой кислоты при определенных условиях также может образовываться альдегид глиоксаль. Среди прочего, также и из-за того, что глиоксаль способствует нежелательной радикальной полимеризации акриловой кислоты, в европейской заявке на патент ЕР-А 1 298 120 рекомендуется таким образом проектировать получение акриловой кислоты, что образование глиоксаля как побочного продукта минимизируется (в качестве возможного источника образования глиоксаля в качестве побочного продукта в рамках гетерогенно-катализируемого частичного парофазного окисления соединений-предшественников акриловой кислоты, содержащих 3 атома углерода, в европейской заявке ЕР-А 1 298 120, среди прочих, установлена случайно содержащаяся в соединении-предшественнике с 3 атомами углерода примесь этилена, содержащая 2 атома углерода).
При дополнительном использовании способа разделения обратным осмосом согласно европейской заявке на патент ЕР-А 1 298 120 можно получить газообразную смесь продуктов, из которой акриловая кислота, также при циркуляции абсорбирующего агента, может быть переведена в жидкую фазу, которая содержит менее 100 масс. м.д. глиоксаля. Из жидкой фазы такого рода акриловая кислота, в соответствии с техническим решением европейской заявки на патент ЕР-А 1 298 120, далее сравнительно беспроблемно может отделяться при помощи способа разделения перегонкой. Недостатком этого способа действий, тем не менее, является необходимость обратного осмоса, который снижает объемную производительность.
В европейской заявке на патент ЕР-А 1 396 484 предлагается способ действий для разделения акриловой кислоты, содержащейся в качестве основного продукта, и глиоксаля, содержащегося в качестве побочного продукта в газообразной смеси продуктов частичного гетерогенно-катализируемого парофазного окисления соединений-предшественников акриловой кислоты, содержащих 3 атома углерода, отличающийся от способа действий, рекомендуемого в европейской заявке на патент ЕР-А 1 298 120, который допускает более высокое содержание глиоксаля как побочного продукта (среди прочего, это является преимуществом в том отношении, что допускает использование экономически более привлекательных, имеющих повышенное содержание примесей соединений-предшественников с 3 атомами углерода).
Он отличается тем, что акриловая кислота и глиоксаль сначала абсорбируются из газообразной смеси продуктов водным раствором. А затем вода из этого раствора отделяется путем азеотропной отгонки (ректификации). При этом, чтобы в значительной степени подавлять нежелательное образование полимера, следует действовать так, чтобы поток флегмы имел определенное содержание воды, а флегмовое число не было меньше определенной величины. Кроме того, следует поддерживать определенные температурные соотношения.
При этих условиях применимости глиоксаль в форме высококипящих гидратов накапливается в нижней части колонны вместе с акриловой кислотой.
Из указанной выше кубовой жидкости акриловая кислота после этого может быть отделена от гидратов глиоксаля перегонкой, причем эти гидраты глиоксаля, совершенно очевидно, больше не обладают свойством мономерного глиоксаля вызывать нежелательную радикальную полимеризацию акриловой кислоты или, во всяком случае, обладают этим свойством в значительно меньшем масштабе.
Собственные исследования фирмы-заявителя показали, что способность глиоксаля в качестве примеси в акриловой кислоте вызывать склонность акриловой кислоты к нежелательной радикальной полимеризации выражена значительно сильнее, по сравнению с другими возможными альдегидами из побочных реакций при гетерогенно катализируемом частичном парофазном окислении соединений-предшественников, содержащих 3 атома углерода (таких как, например, ацетальдегид, формальдегид, пропиональдегид, бензальдегид, бутиральдегид, акролеин), в пересчете на одинаковое молярное содержание примесей. По всей вероятности, это объясняется тем, что, как оказалось по результатам квантово-механических расчетов энергий диссоциации, с одной стороны, термические затраты на расщепление мономерного глиоксаля на два формильных радикала являются особенно незначительными, а, с другой стороны, получающиеся в результате этого формильные радикалы намного реакционноспособнее, чем, например, радикал водорода или метильный радикал (метод расчета CCSD(T) (метод связанных кластеров с одно-, двух- (и трехкратными) возбуждениями, англ. Coupled Cluster including Single, Double (and Triple) excitations)).
Эксперименты в совокупности с обзорами в литературе (например, L'actualite chimique, Mai 1982, страницы с 23 по 31, а также цитируемая в этой публикации литература) показали, что гидраты глиоксаля уже не обладают указанным выше выраженным действием мономерного (молекулярного) глиоксаля, вызывающим полимеризацию.
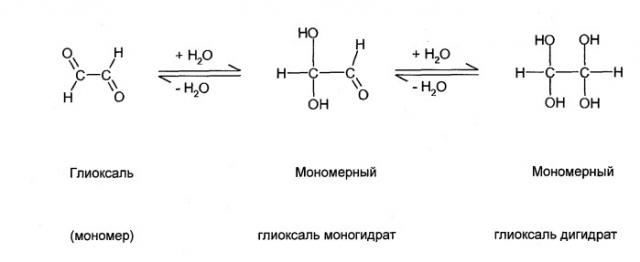
При этом глиоксаль гидраты образуют две группы разновидностей гидратов. Первая группа состоит из мономерного глиоксаль моногидрата и из мономерного глиоксаль дигидрата:
Оба вышеназванных глиоксаль гидрата образуются уже при сравнительно мягких условиях (низкие температуры, ограниченное содержание воды являются достаточными).
Однако реакция образования как мономерного глиоксаль моногидрата, так и мономерного глиоксаль дигидрата является ярко выраженной обратимой реакцией. То есть, хотя каждый из обоих вышеназванных гидратов более не обладает выраженной способностью мономерного глиоксаля вызывать полимеризацию, тем не менее, из обоих этих гидратов, например, при небольшом повышении температуры, может снова образовываться мономерный глиоксаль, который потом в состоянии известным образом способствовать нежелательной радикальной полимеризации акриловой кислоты. Таким образом, в дальнейшем, а также вообще во всей данной публикации (за исключением ее вводной части), стоящий отдельно термин «глиоксаль» все время должен включать общее количество, состоящее из мономерного глиоксаля, мономерного глиоксаль моногидрата, а также мономерного глиоксаль дигидрата.
Следовательно, на фоне вышесказанного, для успешного исполнения технического решения, приведенного в европейской заявке на патент ЕР-А 1 396484, образование мономерного глиоксаль моногидрата и/или мономерного глиоксаль дигидрата в ректификационной колонне при азеотропной перегонке является недостаточным, раз эти гидраты также, как правило, имеют повышенную температуру кипения и в обычном режиме накапливаются вместе с акриловой кислотой в нижней части колонны.
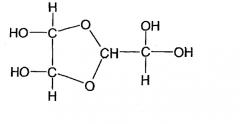
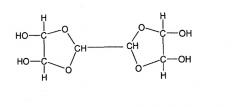
Более того, для успешного осуществления способа проведения процесса, рекомендованного в европейской заявке на патент ЕР-А 1 396 484, в соответствии с собственными исследованиями, необходимо образование гидратов «полиглиоксаля» или «олигоглиоксаля». Они образуют вторую группу глиоксаль гидратов. В качестве примеров следует привести диглиоксаль гидрат и триглиоксаль гидрат:
или
Диглиоксаль гидрат
или
Триглиоксаль гидрат
Предположительно образование полиглиоксаль гидратов протекает через промежуточную стадию глиоксаль дигидрата.
В отличие от образования мономерного глиоксаль гидрата, образование полиглиоксаль гидратов требует повышенных температур (как правило, их образование в значительном объеме протекает только при температурах выше 50°С) и/или более длительного протекания реакции. Также как и мономерные глиоксаль гидраты, полиглиоксаль гидраты больше не обладают обычным для мономерного глиоксаля эффектом в отношении акриловой кислоты - вызывать полимеризацию или, во всяком случае, обладают этим свойством в значительно меньшем масштабе, чем он. Однако в отличие от образования мономерных глиоксаль гидратов, образование полиглиоксаль гидратов протекает в значительной мере необратимо (по крайней мере, при тех же условиях, которые обычно применяются для отделения акриловой кислоты от смеси продуктов гетерогенно катализируемого частичного парофазного окисления соединений-предшественников акриловой кислоты, содержащих 3 атома углерода).
Таким образом, успешное применение методики, рекомендованной в европейской заявке на патент ЕР-А 1 396484, является воспроизводимым только на основании образования полиглиоксаль гидратов. Однако это же требует, что является недостатком способа, как повышенных температур, так и увеличенного времени взаимодействия.
Таким образом, задача данного изобретения состояла в том, чтобы предоставить улучшенный по отношению к процессу, являющемуся ближайшим аналогом из уровня техники, способ разделения акриловой кислоты, содержащейся в качестве главного продукта в газообразной смеси продуктов частичного гетерогенно катализируемого парофазного окисления соединений-предшественников акриловой кислоты, содержащих 3 атома углерода, а также глиоксаля, содержащегося в качестве побочного продукта, который, в основном, больше не имеет описанных недостатков способов из уровня техники и, в частности, не требует образования полиглиоксаль гидратов.
Соответственно этому предлагается способ разделения акриловой кислоты, содержащейся в качестве основного продукта в газообразной смеси продуктов частичного гетерогенно катализируемого парофазного окисления соединения-предшественника акриловой кислоты, содержащего 3 атома углерода, и глиоксаля, содержащегося в качестве побочного продукта, при котором получают жидкую фазу Р, которая по меньшей мере на 70% от своей массы состоит из акриловой кислоты, а также, в пересчете на количество содержащейся в ней акриловой кислоты, содержит по меньшей мере 200 мол. м.д. глиоксаля (под этим в данной публикации, как уже было сказано, понимают общее количество, состоящее из мономерного глиоксаля, мономерного глиоксаль моногидрата и мономерного глиоксаль дигидрата), который отличается тем, что это отделение глиоксаля от акриловой кислоты из жидкой фазы Р осуществляется путем кристаллизации, причем акриловая кислота накапливается в образующемся продукте кристаллизации, а глиоксаль в маточном растворе, остающемся при кристаллизации.
Преимущество способа согласно изобретению, с одной стороны, обосновано тем, что он не требует или соответственно не предполагает ограничений по количеству образования глиоксаля как побочного продукта, а, с другой стороны, тем, что он не требует образования гидратов полиглиоксалей.
Кроме того, неожиданно оказалось, что коэффициент обогащения для глиоксаля АGly, сопровождающий кристаллическое разделение согласно изобретению, как правило, достигает величины, превышающей десять тысяч (>>10000).
Под коэффициентом обогащения А, как правило, понимают соотношение количества примеси, остающейся в маточном растворе, и примеси, остающейся в продукте кристаллизации (соответственно, выраженное как % масс. в пересчете на общее количество маточного раствора или соответственно общее количество продукта кристаллизации; например, при помощи центрифугирования или при помощи центрифугирования и/или промывки маточный раствор и продукт кристаллизации можно в основном полностью отделить друг от друга, а путем последующего анализа определить коэффициент обогащения А; для этого, как правило, достаточным является отделение маточного раствора более чем на 90% масс., предпочтительно более чем на 95 или 97, или 98, или 99% масс. от его общего количества).
В рамках соответствующего кристаллизационного разделения никакой другой нежелательный возможный побочный продукт гетерогенно катализируемого частично окислительного получения в газовой фазе акриловой кислоты из ее соединений-предшественников, содержащих 3 атома углерода, не достигает величины А сравнимого порядка.
Это обстоятельство тем более примечательно, что величина АGly охватывает не только кристаллизационное отделение мономерного глиоксаля, но и кристаллизационное отделение мономерного глиоксаля, мономерного глиоксаль моногидрата и мономерного глиоксаль дигидрата (сравни с определением стоящего отдельно термина «глиоксаль»).
Вышеназванные результаты экспериментов открывают возможность отделения из жидкой фазы Р в процессе получения, например, подходящей для суперабсорбирующих целей чистой акриловой кислоты, препятствующих такому использованию глиоксальных примесей удовлетворительным образом за одну стадию разделения, в одной стадии кристаллизации.
Единицу измерения «мол. м.д.» (мольные миллионные доли) следует понимать таким образом, что если определенное количество жидкой фазы Р содержит, например, 1 моль акриловой кислоты, и то же самое количество жидкой фазы Р одновременно содержит 10·10-6 моль глиоксаля, то в этом количестве жидкой фазы Р, в пересчете на содержащееся в ней молярное количество акриловой кислоты, содержатся 10 мол. м.д. глиоксаля.
То есть, способ согласно изобретению также может быть применен с успехом в том случае, если жидкая фаза Р, которая по меньшей мере на 70% от своей массы состоит из акриловой кислоты, в пересчете на содержащееся в ней молярное количество акриловой кислоты, содержит ≥ 250 мол. м.д. или ≥ 300 мол. м.д., или ≥ 400 мол. м.д., или ≥ 500 мол. м.д., или ≥ 750 мол. м.д., или ≥ 1000 мол. м.д., или ≥ 1250 мол. м.д., или ≥ 1500 мол. м.д. глиоксаля (который в данной публикации представляет собой общее количество, состоящее из мономерного глиоксаля, мономерного глиоксаль моногидрата и мономерного глиоксаль дигидрата).
Как правило, жидкая фаза Р, которая по меньшей мере на 70% от своей массы состоит из акриловой кислоты, в пересчете на содержащееся в ней молярное количество акриловой кислоты, содержит ≤ 5% мол., часто ≤ 2% мол. или ≤ 1% мол. глиоксаля. Само собой разумеется, что способ согласно изобретению также может быть успешно использован еще и в случае вышеприведенного содержания глиоксаля.
Но способ согласно изобретению также может быть успешно использован для всех (то есть, каждого в отдельности, также названных выше) индивидуально указанных в этой публикации содержаний глиоксаля в жидкой фазе Р (соответственно приведенных в мол. м.д. в пересчете на молярное количество акриловой кислоты, содержащееся в этой жидкой фазе Р), если эта жидкая фаза Р состоит из акриловой кислоты на величину ≥ 75% масс. или ≥ 80% масс., или ≥ 85% масс., или ≥ 90% масс., или ≥ 95% масс., или ≥ 96% масс., или ≥ 97% масс., или ≥ 98% масс., или ≥ 99% масс. (соответственно от массы этой жидкой фазы Р).
Содержание глиоксаля в жидкой фазе Р, которую следует обрабатывать согласно изобретению (или в другой жидкой фазе), (то есть, общее содержание в жидкой фазе Р мономерного глиоксаля, мономерного глиоксаль моногидрата и мономерного глиоксаль дигидрата) в рамках данной публикации определяется следующим образом:
Сначала готовят раствор для получения производного D. Для этого 2,0 г 50%-ного раствора 2,4-динитрофенилгидразина (изготовитель: фирма Aldrich, чистота: ≥ 97%) при температуре 25°С растворяют в 62 мл водной соляной кислоты с концентрацией 37% масс. (изготовитель: Aldrich, чистота: ≥ 99,999%). Получающийся в результате раствор затем (также при температуре 25°С) при перемешивании добавляют к 335 г дистиллированной воды. После перемешивания в течение 1 часа при 25°С при помощи фильтрования получают в виде образовавшегося фильтрата раствор для получения производного D.
Для определения содержания глиоксаля в жидкой фазе Р 1 г раствора для получения производного D (при необходимости это количество может быть соответствующим образом увеличено) отвешивают в стеклянную банку с навинчивающейся крышкой, вместимость которой составляет 10 мл. Затем в наполненную таким образом стеклянную банку с навинчивающейся крышкой дополнительно отвешивают образец жидкой фазы Р, количество которой лежит в интервале от 0,15 до 2,0 г.
Затем при помощи встряхивания все содержимое этой стеклянной банки с навинчивающейся крышкой перемешивают и далее оставляют стоять без вмешательства при температуре 25°С в течение времени, составляющего 10 минут. В течение этого времени из мономерного глиоксаля, содержащегося в этой стеклянной банке с навинчивающейся крышкой, путем химической реакции с 2,4-динитрофенилгидразином образуется соответствующий гидразон мономерного глиоксаля Н. Однако во время этого 2,4-динитрофенилгидразин также в форме гидразона Н извлекает из мономерных глиоксаль моногидрата и глиоксаль дигидрата, содержащихся в этой стеклянной банке с навинчивающейся крышкой, связанный в них мономерный глиоксаль (и наоборот, соответствующего извлечения мономерного глиоксаля из гидратов полиглиоксалей, содержащихся в этой стеклянной банке с навинчивающейся крышкой, не происходит).
Затем путем добавления в эту стеклянную банку с навинчивающейся крышкой 0,5 г ледяной уксусной кислоты (изготовитель: Aldrich, чистота: ≥ 99,8%) произошедшее образование гидразона замораживается. Если добавление ледяной уксусной кислоты сопровождается образованием твердого осадка, то понемногу добавляют еще ледяной уксусной кислоты, чтобы снова растворить этот образовавшийся осадок (однако общее количество добавляемой ледяной уксусной кислоты не может превышать 1 г). Если образовавшийся осадок не перешел в раствор и при достижении самой верхней границы (1,0 г) допустимого общего количества добавляемой ледяной уксусной кислоты, то добавляют 0,5 г диметилфталата. Если это также не помогает растворить образовавшийся осадок, то добавляемое количество диметилфталата постепенно увеличивают, чтобы способствовать этому растворению (однако общее количество добавляемого диметилфталата не может превышать 1 г). Если образовавшийся осадок также не перешел в раствор при достижении самой верхней границы (1,0 г) допустимого общего количества добавляемого диметилфталата, то добавляют 2 г смеси G, состоящей из 9 г ацетонитрила и 1 г диметилфталата. Если это добавление также не помогает растворить осадок, то добавляемое количество смеси G постепенно увеличивают, чтобы способствовать этому растворению. Обычно общее количество добавляемой смеси G, чтобы достичь растворения осадка, не превышает 5 г (все вышеперечисленные эксперименты по растворению проводятся при 25°С).
После этого раствор гидразона Н, полученный, как описано, в стеклянной банке с навинчивающейся крышкой, исследуют на содержание в нем гидразона с помощью метода ВЭЖХ (высокоэффективной жидкостной хроматографии при высоком давлении, англ. HPLC (High Pressure Liquid Chromatography)) при указанных ниже рабочих условиях (из его молярного количества непосредственно получается молярное количество глиоксаля, содержащегося в жидкой фазе Р):
| применяемая хроматографическая колонка: | Waters Symmetry C18, 150×4,6 мм, |
| 5 мкм | |
| (фирмы Waters Associates, Мил-форд, Массачусетс, США); |
| Впрыскиваемый объем раствора, | |
| подлежащего анализу: | 50 мкл (момент времени t=0); |
| Температура: | 40°С; |
| Расход элюента: | 1,5 мл/мин; |
| Продолжительность анализа: | 17 мин; |
| Время установления равновесия: | 8 мин; |
| Элюент: | на отрезке времени от t>0 мин до 15 мин смесь из 30% масс. ацетонитрила, 50% масс. воды и20% масс. тетрагидрофурана (соответственно квалификации «для ВЭЖХ»); |
| на отрезке времени от > 15 мин до 17 мин смесь из 65% масс. ацетонитрила, 30% масс. воды и 5% масс. тетрагидрофурана; | |
| на отрезке времени от > 17 мин до 25 мин смесь из 30% масс. ацетонитрила, 50% масс. воды и 20% масс. тетрагидрофурана (затем в колонке устанавливается равновесие, и она опять готова для проведения следующего анализа). |
Время удерживания глиоксаля в форме гидразона Н при названных условиях составляет 7,613 мин.
Этот анализ осуществляется с помощью монохроматического излучения с длиной волны 365 нм. В качестве метода анализа применяется абсорбционная спектроскопия. Изменение элюента на протяжении процесса элюирования обеспечивает повышенную эффективность разделения (как правило, жидкая фаза Р, помимо глиоксаля, содержит еще и другие побочные альдегидные продукты и/или побочные продукты - кетоны, которые в каждом случае образуют соответствующие гидразоны с 2,4-динитрофенилгидразином).
Для калибровки в способе ВЭЖХ в прикладных целях целесообразно использовать раствор мономерного глиоксаля в метаноле, который содержит 50 мол. м.д. мономерного глиоксаля.
Для этой цели он, как описано выше, обрабатывается с помощью раствора для получения производного D, а затем подвергается указанному анализу методом ВЭЖХ.
Способ согласно изобретению, среди прочего, располагает к себе тем, что, как уже было сказано, он обходится без использования имеющих высокую степень чистоты соединений-предшественников акриловой кислоты, содержащих 3 атома углерода, для гетерогенно-катализируемого частичного парофазного окисления для получения этой акриловой кислоты.
Например, для этого гетерогенно-катализируемого частичного парофазного окисления для получения акриловой кислоты может применяться исходная газообразная реакционная смесь, которая, в пересчете на содержащееся в ней молярное количество используемых соединений-предшественников с 3 атомами углерода (например, пропана, пропилена, акролеина, пропионовой кислоты, пропиональдегида, пропанола и/или глицерина), содержит суммарное молярное количество соединений, имеющих 2 атома углерода (например, этана, этилена, ацетилена, ацетальдегида, уксусной кислоты и/или этанола), равное ≥ 200 мол. м.д. или ≥ 250 мол. м.д., или ≥ 300 мол. м.д., или ≥ 400 мол. м.д., или ≥ 500 мол. м.д., или ≥ 750 мол. м.д., или ≥ 1000 мол. м.д., ил ≥ 1250 мол. м.д., или ≥ 1500 мол. м.д.
При этом исходная газообразная реакционная смесь представляет собой ту же газообразную смесь, которая подается через слой катализатора с целью частичного окисления до акриловой кислоты содержащегося в ней соединения-предшественника с 3 атомами углерода. Помимо соединения предшественника, содержащего 3 атома углерода, нежелательных примесей, а также молекулярного кислорода в качестве окислителя, эта исходная газообразная реакционная смесь, как правило, еще содержит инертные газы-разбавители, такие как, например, N2, CO2, Н2O, благородный газ, молекулярный водород и т.д. Каждый инертный разбавялющий газ обычно имеет такие свойства, что в процессе прохождения этого гетерогенно катализируемого частичного окисления он сохраняется в неизменном виде по меньшей мере на 95% мол. от своего исходного количества.
Доля соединения предшественника, содержащего 3 атома углерода, в исходной газообразной реакционной смеси может находиться в пределах, например, от 4 до 20% об. или от 5 до 15% об., или от 6 до 12% об.
Обычно эта исходная газообразная реакционная смесь, в пересчете на стехиометрию реакции частичного окисления соединения-предшественника, содержащего 3 атома углерода, до акриловой кислоты, содержит избыток молекулярного кислорода, для того, чтобы снова подвергнуть повторному оксилению, как правило, оксидные катализаторы.
Этот избыток в случае последующего применения способа осуществления согласно изобретению может выбираться особенно большим, поскольку при увеличивающемся избытке кислорода, как правило, также одновременно происходит увеличение нежелательного образования побочного продукта - глиоксаля.
Аналогичным образом, при гетерогенно-катализируемом частичном парофазном окислении соединения-предшественника акриловой кислоты, содержащего 3 атома углерода, может быть выбрана сравнительно высокая максимальная температура, имеющаяся в слое катализатора, если по окончании этого частичного окисления применяется способ согласно изобретению. Среди прочего, это объясняется тем, что при возрастающей максимальной температуре, как правило, также одновременно происходит увеличение нежелательного образования побочного продукта - глиоксаля. Однако применение повышенных максимальных температур, как правило, позволяет использование катализаторов с более низкой активностью, что открывает возможность увеличенного ресурса работы катализатора. Правда, при применении катализаторов с пониженной активностью при возрастающей степени превращения соединения-предшественника, содержащего 3 атома углерода, в увеличивающемся объеме часто также происходит его нежелательное полное окисление. При этом при необходимости в качестве промежуточного продукта также может образовываться глиоксаль.
Аналогичным образом, в соответствии со способом согласно изобретению также можно вести процесс в широком диапазоне в отношении выбора нагрузки на слой катализатора по соединению-предшественнику, содержащему 3 атома углерода. Кроме того, оказалось, что образованию побочного продукта - глиоксаля способствует повышенное содержание в реакционной газовой смеси водяного пара. Поэтому способ согласно изобретению не в последнюю очередь является важным в том случае, когда исходная газообразная реакционная смесь, используемая для гетерогенно катализируемого частичного парофазного окисления соединения-предшественника, содержащего 3 атома углерода, включает ≥ 1% масс. или ≥ 2% масс., или ≥ 3% масс., или ≥ 4% масс., или ≥ 5% масс., или ≥ 7% масс., или ≥ 9% масс., или ≥ 15% масс., или ≥ 20% масс. водяного пара. Как правило, однако, содержание водяного пара в исходной газообразной реакционной смеси составляет не более 40% масс., часто не более 30% масс.
В остальном, процесс гетерогенно-катализируемого частичного парофазного окисления для получения акриловой кислоты может осуществляться по известным способам так, как описано в уровне техники.
Если в случае соединений-предшественников с 3 атомами углерода речь идет, например, о пропилене и/или акролеине, то это гетерогенно катализируемое частичное парофазное окисление может проводиться, как описано, например, в таких публикациях, как международные заявки на патент WO 2005/042459, WO 2005/047224 и WO 2005/047226.
Если соединение-предшественник с 3 атомами углерода представляет собой, например, пропан, то гетерогенно катализируемое частичное парофазное окисление для получения акриловой кислоты может проводиться, как описано, например, в таких публикациях, как европейская заявка ЕР-А 608 838, немецкие заявки на патент DE-A 198 35 247, DE-A 102 45 585 и DE-A10246119.
Если соединение-предшественник с 3 атомами углерода представляет собой, например, глицерин, то гетерогенно катализируемое частичное парофазное окисление для получения акриловой кислоты может проводиться, как описано, например, в таких публикациях, как международные заявки на патент WO 2007/090991, WO 2006/114506, WO 2005/073160, WO 2006/114506, WO 2006/092272 или WO 2005/073160.
Также уже было предложено, чтобы получать пропилен в качестве соединения-предшественника с 3 атомами углерода путем проводимого перед частичным парофазным оксилением предварительного частичного дегидрирования и/или оксидегидрирования пропана (например, как в международных заявках WO 076370, WO 01/96271, европейской заявке на патент ЕР-А 117146, международных заявках WO 03/011804 и WO 01/96270).
Для отделения акриловой кислоты из газообразной смеси продуктов гетерогенно-катализируемого частичного парофазного окисления соединений-предшественников с 3 атомами углерода обычно используется комбинация различных способов разделения, чтобы как можно более экономически целесообразным способом добиться чистоты акриловой кислоты, соответствующей целям ее дальнейшего использования. При этом комбинация, использованная в конкретном случае, не в последнюю очередь зависит от вида и количества отличающихся от акриловой кислоты различных компонентов, которые содержатся в газообразной смеси продуктов. Таким образом, получение жидкой фазы Р, которую можно обрабатывать согласно изобретению, может осуществляться самыми различными путями.
Важной составляющей такой комбинации способов разделения являются обычно не кристаллизационные термические способы разделения. Эти не кристаллизационные термические способы разделения представляют собой такие способы, при которых в разделяющих колоннах, содержащих внутренние элементы, способствующие разделению, подаются противотоком газообразные (восходящие) и жидкие (нисходящие) потоки веществ или соответственно два потока жидких веществ, причем вследствие возникающих между потоками веществ градиентов происходит тепло- и массообмен, который, в конечном счете, и обусловливает заданное разделение в этой разделительной колонне.
Примерами таких не кристаллизационных термических способов разделения являются (частичная) конденсация, фракционная конденсация (смотри немецкую заявку на патент DE-A 199 24 532), а также ректификация.
Результирующее разделяющее действие в данном случае основывается, прежде всего, на различии температур кипения акриловой кислоты и побочных компонентов, отличающихся от акриловой кислоты. Другой пример составляет абсорбция. В данном случае разделяющее действие основано, прежде всего, на различной растворимости в абсорбирующей жидкости акриловой кислоты и побочных компонентов, отличающихся от акриловой кислоты. Вышеназванное также относится к не кристаллизационному термическому способу разделения отгонкой (удаляемый газ захватывает из жидкости компоненты с различным сродством, содержащиеся в ней в растворенном виде), а также к десорбции (процесс, обратный абсорбции; вещество, растворенное в жидкой фазе, отделяется при помощи понижения парциального давления). Однако термин «термические способы разделения» включает также азеотропную перегонку или ректификацию (они используют по-разному выраженные склонности к образованию азеотропов с добавленными агентами, образующими азеотропы, в случае акриловой кислоты и в случае побочных компонентов (компонентов в газообразной реакционной смеси, отличающихся от акриловой кислоты). Кроме того, термин «термические способы разделения» включает экстракцию.
Отличительным признаком, в основном, являющимся общим для всех возможных комбинаций термических способов отделения акриловой кислоты от газообразной смеси продуктов гетерогенно катализируемого частичного парофазного окисления соединений-предшественников с 3 атомами углерода, является то, что, при необходимости, после прямого и/или непрямого охлаждения вышеназванной газообразной смеси продуктов, акриловая кислота, содержащаяся в газообразной смеси продуктов, на основной стадии разделения переводится в конденсированную (в частности, жидкую) фазу (из которой, в рамках этого основного разделения, остаточный газ, оставшийся газообразным, с точки зрения технической целесообразности, по меньшей мере частично подается обратно в процесс частичного гетерогенно катализируемого парофазного окисления соединения-предшественника с 3 атомами углерода (например, в исходную газообразную реакционную смесь для этого окисления) в качестве «циркуляционного газа» («режим с рециклизацией газа»); как правило, этот остаточный газ (циркуляционный газ) в значительной мере состоит из инертных газов-разбавителей, применяемых совместно при частичном гетерогенно-катализируемом парофазном окислении соединения-предшественника с 3 атомами углерода, а также из водяного пара, обычно образующегося в качестве побочного продукта при этом частичном окислении, и побочных продуктов, образующихся путем нежелательного полного окисления соединения-предшественника с 3 атомами углерода (например, диоксид углерода), которые также могут содержать глиоксаль; если основная стадия разделения представляет собой абсорбцию, то этот циркуляционный газ также может содержать абсорбент; частично он еще содержит незначительные количества неизрасходовавшегося при частичном окислении молекулярного кислорода (остаточного кислорода) и/или непрореагировавшее органическое соединение-предшественник с 3 атомами углерода (смотри, например, международную заявку WO 2004/007405, а также немецкую заявку на патент DE-A 102007019597)).
Это может осуществляться, например, при помощи абсорбции подходящим растворителем (например, водой, высококипящим органическим растворителем, водными растворами) и/или с помощью частичной или преимущественно полной конденсации (например, фракционой конденсации) (для этого смотри, например, публикации европейских заявок на патент ЕР-А 13 88 533, ЕР-А 13 88 532, немецкую заявку на патент DE-A 102 35 847, европейскую заявку ЕР-А 79 2