Способ получения сахарного раствора
Иллюстрации
Показать всеИзобретение относится к химии сахаров. Способ включает стадию гидролиза целлюлозосодержащей биомассы с получением водного сахарного раствора. Затем полученный водный сахарный раствор фильтруют через нанофильтрационную мембрану и/или обратноосмотическую мембрану. Очищенный сахарный раствор собирают со стороны впуска и удаляют ингибирующие ферментацию вещества со стороны фильтрата. Указанные ингибирующие ферментацию вещества представляют собой одно или более соединений из органических кислот, соединений фурана и фенольных соединений. Изобретение позволяет получить очищенный от ингибирующих ферментацию соединений сахарный сироп простым способом и повысить эффективность ферментационного получения различных химических продуктов. 2 н. и 11 з.п. ф-лы, 7 ил., 49 табл., 24 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения сахарного раствора из биомассы, содержащей целлюлозу.
Уровень техники
Процесс ферментационного получения химических продуктов при использовании сахаров в качестве сырья применяли для производства различных промышленных материалов. В настоящее время в качестве сахаров, используемых в качестве исходного сырья для ферментации, в промышленности используют сахара, полученные из пищевых материалов, таких как сахарный тростник, крахмал и сахарная свекла. Впрочем, ввиду того, что в будущем из-за увеличения мирового населения ожидается рост цен на пищевую продукцию, или по этическим соображениям, ввиду того, что сахара в качестве промышленных материалов могут конкурировать с сахаром как пищевым продуктом, необходимо разработать способ эффективного производства сахарного раствора из возобновляемого непищевого ресурса, то есть целлюлозосодержащей биомассы, или способ эффективной переработки полученного сахарного раствора как исходного сырья для ферментации в промышленный материал.
Примеры раскрытых способов получения сахарного раствора из целлюлозосодержащей биомассы включают способы получения сахарных растворов с применением серной кислоты, такие как способы получения сахарных растворов с помощью кислотного гидролиза целлюлозы и гемицеллюлозы при использовании концентрированной серной кислоты (Патентные документы 1 и 2), и способ, в котором целлюлозосодержащую биомассу подвергают гидролизной обработке с использованием разбавленной серной кислоты, а затем энзиматически обрабатывают целлюлазой и т.п. с получением сахарного раствора (Непатентный документ 1).
Кроме того, примеры раскрытых способов, в которых не используются кислоты, включают способ, в котором для получения сахарного раствора целлюлозосодержащую биомассу гидролизуют, используя воду в докритических условиях при температуре приблизительно 250-500°C (Патентный документ 3), способ, в котором целлюлозосодержащую биомассу подвергают обработке водой в докритических условиях с последующей ферментной обработкой, с получением сахарного раствора (Патентный документ 4), и способ, в котором целлюлозосодержащую биомассу подвергают гидролизной обработке под давлением водой, нагретой до 240°C-280°C, а затем обработке ферментами с получением сахарного раствора (Патентный документ 5).
Однако во время гидролиза целлюлозосодержащей биомассы, одновременно с разложением целлюлозного или гемицеллюлозного компонента или подобного, протекают реакции разложения образующихся сахаров, таких как глюкоза и ксилоза, при этом образуются такие побочные продукты, как соединения фурана, включая фурфурол и гидроксиметилфурфурол (ГМФ), а также органические кислоты, включая муравьиную кислоту, уксусную кислоту и левулиновую кислоту, которые представляют собой проблему. Кроме того, поскольку целлюлозосодержащая биомасса содержит лигниновые компоненты, которые являются ароматическими полимерами, лигниновые компоненты расщепляются в стадии кислотной обработки с образованием низкомолекулярных ароматических соединений, таких как фенолы, также являющиеся побочными продуктами. Указанные соединения оказывают ингибирующее действие в ходе стадии ферментации с использованием микроорганизмов и вызывают ингибирование роста микроорганизмов, что приводит к уменьшению выхода продукта ферментации. Таким образом, указанные соединения называются веществами, ингибирующими ферментацию, и представляют серьезную проблему при использовании сахарного раствора, полученного из целлюлозосодержащей биомассы, в качестве исходного сырья для ферментации.
Примеры раскрытого способа удаления подобных ингибирующих ферментацию веществ в ходе процесса производства сахарного раствора включают способ избыточной обработки известью (Непатентный документ 2). В данном способе, в ходе стадии нейтрализации целлюлозы, обработанной кислотой, или осахаренной жидкости с помощью добавления извести, жидкость выдерживают при нагревании до приблизительно 60°C в течение некоторого периода, с целью удаления ингибирующих ферментацию веществ, таких как фурфурол и ГМФ, вместе с образующимся сульфатом кальция. Однако избыточная обработка известью дает слабый эффект при удалении органических кислот, таких как муравьиная кислота, уксусная кислота и левулиновая кислота, которые являются проблематичными.
Далее, в качестве другого способа удаления веществ, ингибирующих ферментацию, был раскрыт способ, в котором в сахарный раствор, полученный из целлюлозосодержащей биомассы, пропускают водяной пар для удаления ингибирующих ферментацию веществ выпариванием (Патентный документ 6). Впрочем, поскольку такой способ удаления выпариванием зависит от температуры кипения ингибирующих ферментацию веществ, эффективность удаления ингибирующих ферментацию веществ, таких как органические кислоты, имеющие низкую температуру кипения, крайне низка, при этом для получения достаточной эффективности удаления требуется большое количество энергии, что является проблематичным.
Также существует способ, в котором вещества, ингибирующие ферментацию, удаляют посредством ионного обмена (Патентный документ 7), однако данный способ сложен ввиду высокой стоимости. Кроме того, существует способ, в котором проводят адсорбционное удаление при использовании древесного карбида, то есть активированного угля или подобного материала, однако удаляемые вещества ограничены гидрофобными соединениями, что является проблематичным (Патентный документ 8).
Документы из предшествующего уровня техники
Патентные документы
[Патентный документ 1] опубликованная японская переведенная заявка на патент PCT 11-506934
[Патентный документ 2] JP 2005-229821 A
[Патентный документ 3] JP 2003-212888 A
[Патентный документ 4] JP 2001-95597 A
[Патентный документ 5] JP 3041380 B
[Патентный документ 6] JP 2004-187650 A
[Патентный документ 7] опубликованная японская переведенная заявка на патент PCT 2001-511418
[Патентный документ 8] JP 2005-270056 A
Непатентные документы
[Непатентный документ 1] А A. Aden et al., "Lignocellulosic Biomass to Ethanol Process Design and Economics Utilizing Co-Current Dilute Acid Prehydrolysis and Enzymatic Hydrolysis for Corn Stover" NREL Technical Report (2002)
[Непатентный документ 1] M. Alfred et al., "Effect of pH, time and temperature of overliming on detoxification of dilute-acid hydrolyzates for fermentation by Saccaromyces cerevisiase" Process Biochemistry, 38, 515-522 (2002)
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задачи, решаемые изобретением
В настоящем изобретении предложены способы решения вышеуказанных проблем, а именно способ, в котором ингибирующие ферментацию вещества, образующиеся в стадии получения сахара из целлюлозосодержащей биомассы, удаляются в ходе стадии получения сахарного раствора, а также способ получения очищенного сахарного раствора, содержащего очень малое количество ингибирующих ферментацию веществ.
Способы решения задач
Авторы настоящего изобретения тщательно изучали вышеуказанные проблемы с целью их решения и обнаружили, что при пропускании сахарного раствора через нанофильтрационную мембрану и/или обратноосмотическую мембрану в ходе стадии получения сахара из целлюлозосодержащей биомассы, сахар, который будет использоваться в качестве исходного сырья для ферментации, и ингибирующие ферментацию вещества могут быть разделены, при этом ингибирующие ферментацию вещества могут быть удалены из сахарного раствора. Таким образом, настоящее изобретение составлено следующими пунктами [1]-[14].
[1] Способ получения сахарного раствора с применением в качестве сырья целлюлозосодержащей биомассы, включающий:
(1) стадию гидролиза целлюлозосодержащей биомассы с получением водного сахарного раствора; и
(2) стадию пропускания полученного водного сахарного раствора через нанофильтрационную мембрану и/или обратноосмотическую мембрану со сбором очищенного сахарного раствора со стороны впуска и удалением ингибирующих ферментацию веществ со стороны фильтрата.
[2] Способ получения сахарного раствора согласно [1], где pH водного сахарного раствора в Стадии (2) доведен до 1-5.
[3] Способ получения сахарного раствора согласно [1] или [2], где ингибирующие ферментацию вещества включают одно или несколько веществ, выбранных из группы, состоящей из органических кислот, соединений фурана и фенольных соединений.
[4] Способ получения сахарного раствора согласно [3], где органическая кислота является муравьиной кислотой или уксусной кислотой.
[5] Способ получения сахарного раствора согласно [3], где соединение фурана является гидроксиметилфурфуролом или фурфуролом.
[6] Способ получения сахарного раствора согласно [3], где фенольное соединение является ванилином, ацетованилином или сиреневой кислотой.
[7] Способ получения сахарного раствора согласно любому из [1]-[6], где очищенный сахарный раствор в Стадии (2) является сахарным раствором, содержащим моносахарид в качестве основного компонента.
[8] Способ получения сахарного раствора согласно любому из [1]-[7], где водный сахарный раствор, полученный в Стадии (1), пропускают через микрофильтрационную мембрану и/или ультрафильтрационную мембрану для удаления мелких частиц и макромолекулярных компонентов перед обработкой в Стадии (2).
[9] Способ получения сахарного раствора согласно любому из [1]-[8], где температуру водного сахарного раствора в Стадии (2) доводят до 1-15°C и фильтруют раствор через нанофильтрационную мембрану.
[10] Способ получения сахарного раствора согласно любому из [1]-[8], где температуру водного сахарного раствора в Стадии (2) доводят до 40°C-80°C и фильтруют раствор через обратноосмотическую мембрану.
[11] Способ получения сахарного раствора согласно любому из [1]-[10], где Стадия (2) является стадией фильтрования водного сахарного раствора через нанофильтрационную мембрану и фильтрования полученного фильтрата через обратноосмотическую мембрану.
[12] Способ получения сахарного раствора согласно любому из [1]-[11], где функциональный слой (слои) нанофильтрационной мембраны и/или обратноосмотической мембраны в Стадии (2) представляет собой полиамид.
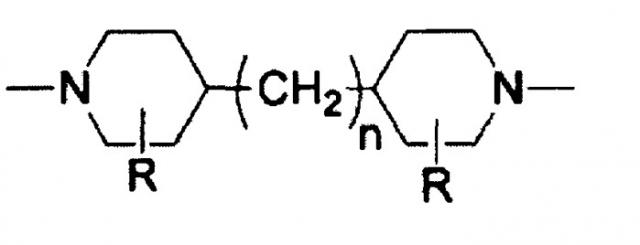
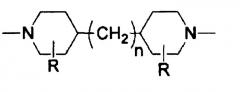
[13] Способ получения сахарного раствора согласно любому из [1]-[12], где функциональный слой нанофильтрационной мембраны в Стадии (2) включает сшитый пиперазин полиамид в качестве основного компонента и дополнительно включает составной компонент, представленный Химической формулой 1:
Химическая формула 1
(в которой R обозначает -H или -CH3, а n обозначает целое число от 0 до 3).
[14] Способ получения химического продукта, где в способе в качестве исходного сырья для ферментации применяется сахарный раствор, полученный с помощью способа получения сахарного раствора согласно любому из [1]-[13].
Технический результат изобретения
В соответствии с настоящим изобретением, соединения фурана, такие как фурфурол и ГМФ; органические кислоты, такие как уксусная кислота, муравьиная кислота и левулиновая кислота; и фенольные соединения, такие как ванилин; которые являются веществами, ингибирующими ферментацию, могут быть полностью удалены из водного сахарного раствора, полученного из целлюлозосодержащей биомассы, и в то же время сахара, такие как глюкоза и ксилоза, могут быть получены с высокой чистотой и высоким выходом. В результате, с применением очищенного сахарного раствора, полученного согласно настоящему изобретению, в качестве исходного сырья для ферментации, может быть повышена эффективность ферментационного получения различных химических продуктов.
Краткое описание фигур
На фиг. 1 показан общий вид фильтрационного устройства, в котором применяется нанофильтрационная мембрана/обратноосмотическая мембрана.
На фиг. 2 показано схематическое изображение камеры из нержавеющей стали, которую использовали в тесте с плоской мембраной.
Фиг. 3 представляет собой график, на котором показано сравнение величины потока при различных pH в процессе фильтрации сахарного раствора через нанофильтрационную мембрану.
Фиг. 4 представляет собой график, на котором показано сравнение величины потока посредством способа, в котором сахарный раствор фильтруют через микрофильтрационную мембрану или ультрафильтрационную мембрану перед фильтрацией сахарного раствора через нанофильтрационную мембрану.
На фиг. 5 показаны фотографии поверхности мембраны до и после фильтрации гидротермически обработанной жидкости через микрофильтрационную мембрану, которые были сделаны с помощью растрового электронного микроскопа.
На фиг. 6 показаны результаты измерения распределения элементов при наблюдении растрово-электронных микрофотографий, показанных на фиг. 5, выполненного с помощью рентгеноспектрального анализатора на основе метода энергетической дисперсии, присоединенного к растровому электронному микроскопу.
Фиг. 7 представляет собой диаграмму, на которой показана схема дрожжевого вектора экспрессии pTRS11.
Наилучший вариант осуществления изобретения
Далее настоящее изобретение будет описано более подробно.
Примеры целлюлозосодержащей биомассы, используемой в способе получения сахарного раствора по настоящему изобретению, включают травяные биомассы, такие как выжимки сахарного тростника, просо прутьевидное, кукурузная солома, рисовая солома и пшеничная солома; а также древесную биомассу, такую как древесина и строительные отходы. Указанные целлюлозосодержащие биомассы содержат целлюлозу или гемицеллюлозу, которые являются полисахаридами, образующимися при конденсации и дегидратации сахаров. При гидролизе таких полисахаридов могут быть получены сахарные растворы, которые могут применяться в качестве исходного сырья для ферментации.
Сахарный раствор в настоящем изобретении означает водный сахарный раствор, полученный путем гидролиза целлюлозосодержащей биомассы. Сахара обычно классифицируют, с учетом степени полимеризации моносахаридов, на моносахариды, такие как глюкоза и ксилоза, олигосахариды, образованные при конденсации с дегидратацией 2-9 моносахаридов, и полисахариды, образованные при конденсации с дегидратацией не менее чем 10 моносахаридов. Сахарный раствор по настоящему изобретению означает сахарный раствор, содержащий моносахарид(ы) в качестве основного компонента (компонентов), и более конкретно, сахарный раствор по настоящему изобретению содержит глюкозу или ксилозу в качестве основного компонента. Кроме того, сахарный раствор по настоящему изобретению также содержит олигосахариды, такие как целлобиоза; и моносахариды, такие как арабиноза и манноза, хотя их количество является небольшим. В данном случае термин "содержит моносахарид в качестве основного компонента" означает, что моносахарид(ы) составляет(ют) не менее 80% по весу от общей массы сахаров, таких как моносахариды, олигосахариды и полисахариды, растворенных в воде. Конкретные примеры способа анализа моносахаридов, олигосахаридов и полисахаридов, растворенных в воде, включают количественный анализ ВЭЖХ, основанный на сравнении со стандартным образцом. Конкретные условия ВЭЖХ: реакционный раствор не используется; используется колонка Luna NH2 (производства Phenomenex, Inc.); подвижная фаза, вода сверхвысокой очистки:ацетонитрил = 25:75; скорость потока 0,6 мл/мин; время измерения 45 мин; способ детектирования, RI (дифференциальный показатель преломления); температура 30°C.
Далее будет описана Стадия (1), которая является стадией гидролиза целлюлозосодержащей биомассы в способе получения сахарного раствора по настоящему изобретению.
Когда целлюлозосодержащую биомассу подвергают гидролизу, целлюлозосодержащая биомасса может использоваться без дополнительной обработки или может быть подвергнута известной обработке, такой как обработка паром, измельчение или истирание. С помощью такой обработки эффективность гидролиза может быть повышена.
Стадия гидролиза целлюлозосодержащей биомассы не ограничивается, и ее конкретные примеры главным образом включают 6 методов, то есть методику A: метод, в котором используют только кислоту; методику B: метод, в котором проводят обработку кислотой с последующим использованием фермента; методику C: метод, в котором используют только гидротермическую обработку; методику D: метод, в котором проводят гидротермическую обработку с последующим использованием фермента; методику E: метод, в котором проводят обработку щелочью с последующим использованием фермента; и методику F: метод, в котором проводят обработку аммиаком с последующим использованием фермента.
В методике A для гидролиза целлюлозосодержащей биомассы используется кислота. Примеры используемой кислоты включают серную кислоту, азотную кислоту и соляную кислоту, при этом предпочтительно используется серная кислота.
Концентрация кислоты не ограничивается, при этом может использоваться кислота с концентрацией 0,1-99% по весу. В случаях, когда концентрация кислоты составляет 0,1-15% по весу, предпочтительно 0,5-5% по весу, температуру реакции устанавливают в пределах диапазона 100-300°C, предпочтительно 120-250°C, а время реакции устанавливают в пределах диапазона от 1 секунды до 60 минут. Количество циклов обработки не ограничивается, при этом вышеописанная обработка может быть выполнена 1 или более раз. В частности, в тех случаях, когда вышеописанную обработку выполняют 2 или более раз, условия при первой обработке могут отличаться от условий при второй и последующих обработках.
Кроме того, в случаях, когда концентрация кислоты составляет 15-95% по весу, предпочтительно 60-90% по весу, температуру реакции устанавливают в пределах диапазона 10-100°C, а время реакции устанавливают в пределах диапазона от 1 секунды до 60 минут.
Количество циклов обработки кислотой не ограничивается, при этом вышеописанная обработка может быть выполнена 1 или более раз. В частности, в тех случаях, когда вышеописанную обработку выполняют 2 или более раз, условия при первой обработке могут отличаться от условий при второй и последующих обработках.
Поскольку гидролизат, полученный после обработки кислотой, содержит кислоты, такие как серная кислота, его нужно нейтрализовать, чтобы он мог применяться в качестве исходного сырья для ферментации. Нейтрализация может быть выполнена либо в случае водного раствора кислоты, полученного при удалении твердых компонентов из гидролизата, или в состоянии, в котором содержатся твердые компоненты. Щелочной реагент, используемый для нейтрализации, не ограничивается и предпочтительно представляет собой одновалентный щелочной реагент. В случаях, когда кислотные и щелочные компоненты являются солями, имеющими валентность 2 или выше, во время стадии (2) они не проходят через нанофильтрационную мембрану, при этом соли осаждаются в жидкости в процессе концентрирования жидкости, что может вызвать забивание мембраны.
В случаях, когда используется одновалентная щелочь, примеры щелочи включают, помимо прочего, аммиак, гидроксид натрия и гидроксид калия.
В случаях, когда используется щелочной реагент, имеющий валентность 2 или выше, необходимо снижать количество кислоты и щелочи или использовать механизм для удаления осадков в ходе Стадии (2), чтобы избежать осаждения солей во время Стадии (2). В случаях, когда используется щелочь, имеющая валентность 2 или выше, щелочью предпочтительно является гидроксид кальция с учетом его низкой стоимости. Поскольку в тех случаях, когда используется гидроксид кальция, при нейтрализации образуется сульфат кальция, его нужно удалять разделением твердой и жидкой фаз. Примеры способа разделения твердой и жидкой фаз включают, помимо прочих, центрифугирование и разделение с помощью мембраны, при этом сульфат кальция также может быть удален с помощью нескольких типов стадий разделения.
Как правило, при гидролизе с использованием кислоты, сначала протекает гидролиз гемицеллюлозного компонента, имеющего низкую кристалличность, после чего протекает гидролиз целлюлозного компонента, имеющего высокую кристалличность. Поэтому при использовании кислоты можно получить жидкость, содержащую большое количество ксилозы, образующейся из гемицеллюлозы. Кроме того, при обработке кислотой, если после обработки подвергать биомассу, содержащую твердую фазу, реакции при более высоком давлении и более высокой температуре, чем при вышеуказанной обработке, целлюлозный компонент, имеющий более высокую кристалличность, может расщепляться с получением раствора, содержащего большое количество глюкозы, полученной из целлюлозы. Устанавливая двухэтапную стадию гидролиза, могут быть подобраны такие условия гидролиза, которые подходят для гемицеллюлозы и целлюлозы, при этом могут быть повышены эффективность разложения и выход сахара. Кроме того, при хранении сахарного раствора, полученного при первых условиях разложения, и сахарного раствора, полученного при вторых условиях разложениях, отдельно друг от друга, могут быть получены два типа сахарных растворов с различными отношениями моносахаридов, содержащихся в гидролизатах. Таким образом, также можно отделить сахарный раствор, полученный при первых условиях разложения, как сахарный раствор, содержащий в качестве основного компонента ксилозу, и сахарный раствор, полученный при вторых условиях разложения, как сахарный раствор, содержащий в качестве основного компонента глюкозу. Посредством разделения моносахаридных компонентов, содержащихся в сахарном растворе, как описано выше, ферментация может быть выполнена отдельно как ферментация, в которой в качестве исходного сырья для ферментации используется ксилоза в сахарном растворе, и как ферментация, в которой в качестве исходного сырья для ферментации используется глюкоза в сахарном растворе, где для соответствующих типов ферментации могут быть подобраны и применены наиболее подходящие виды микроорганизмов. Следует отметить, что сахар, полученный из обоих компонентов, также может быть получен сразу, без разделения гемицеллюлозного компонента/целлюлозного компонента, выполнением высокотемпературной обработки кислотой при высоком давлении в течение длительного времени.
В методике B обработанный раствор, полученный в методике A, дополнительно подвергают ферментативному гидролизу целлюлозосодержащей биомассы. Концентрация кислоты, которая используется в методике B, предпочтительно составляет 0,1-15% по весу, более предпочтительно 0,5-5% по весу. Температура реакции может быть установлена в пределах диапазона 100-300°C, предпочтительно 120-250°C. Время реакции может быть установлено в пределах диапазона от 1 секунды до 60 минут. Количество циклов обработки не ограничено, при этом вышеописанная обработка может быть выполнена 1 или более раз. В частности, в тех случаях, когда вышеописанную обработку выполняют 2 или более раз, условия при первой обработке могут отличаться от условий при второй и последующих обработках.
Поскольку гидролизат, полученный при обработке кислотой, содержит кислоты, такие как серную кислоту, он должен быть нейтрализован, чтобы его можно было далее подвергнуть реакции гидролиза ферментом или использовать в качестве исходного сырья для ферментации. Нейтрализация может быть выполнена аналогичным образом, как и нейтрализация в методике A.
Фермент не ограничивается, при условии, что он является ферментом, обладающим целлюлозорасщепляющей активностью, при этом могут применяться стандартно используемые целлюлазы. Фермент предпочтительно является целлюлазой, включающей целлюлазу экзо-типа или целлюлазу эндо-типа, которая обладает способностью расщеплять кристаллическую целлюлозу. В качестве подобной целлюлазы предпочтительна целлюлаза, продуцируемая микроорганизмом, принадлежащим к роду Trichoderma. Род Trichoderma включает микроорганизмы, относящиеся к нитчатым грибам, которые секретируют большое количество различных целлюлаз внеклеточно. Целлюлаза, используемая в настоящем изобретении, предпочтительно является целлюлазой из Trichoderma reesei. Кроме того, в качестве фермента, используемого для гидролиза, β-глюкозидаза, которая является ферментом, расщепляющим целлобиозу, может быть добавлена для повышения эффективности производства глюкозы, при этом β-глюкозидаза может также использоваться вместе с вышеуказанной целлюлазой для гидролиза. β-глюкозидаза не ограничивается, но предпочтительно происходит из рода Aspergillus. Реакцию гидролиза с использованием таких ферментов предпочтительно проводят при pH приблизительно 3-7, более предпочтительно при pH приблизительно 5. Температура реакции предпочтительно составляет 40-70°C. Кроме того, после завершения ферментативного гидролиза предпочтительно проводить разделение твердой и жидкой фаз, чтобы удалить твердые компоненты, которые не были расщеплены. Примеры способа удаления твердых компонентов включают центрифугирование и разделение с помощью мембран, впрочем, данный способ не ограничивается этим. Кроме того, такие способы разделения твердой и жидкой фаз могут применяться в виде комбинации нескольких способов.
В случаях, когда обработка кислотой сопровождается ферментативным гидролизом целлюлозосодержащей биомассы, предпочтительно проводить гидролиз гемицеллюлозы, имеющей низкую кристалличность, путем обработки кислотой при первом гидролизе, с последующим проведением гидролиза целлюлозы, имеющей высокую кристалличность, при использовании фермента во втором гидролизе. При использовании фермента во втором гидролизе стадию гидролиза целлюлозосодержащей биомассы можно провести более эффективно. Более конкретно, при первом гидролизе кислотой главным образом протекает гидролиз гемицеллюлозного компонента, содержащегося в целлюлозосодержащей биомассе, и частичное разложение лигнина, при этом получаемый в результате гидролизат разделяется на раствор кислоты и твердые компоненты, содержащие целлюлозу. Затем твердые компоненты, содержащие целлюлозу, гидролизуют при добавлении фермента. Поскольку разделенный/выделенный раствор в разбавленной серной кислоте в качестве основного компонента содержит ксилозу, которая является пентозой, водный сахарный раствор может быть выделен при нейтрализации кислотного раствора. Кроме того, из продукта реакции гидролиза твердых компонентов, содержащих целлюлозу, могут быть получены моносахаридные компоненты, содержащие глюкозу в качестве основного компонента. Водный сахарный раствор, полученный в результате нейтрализации, может быть смешан с твердыми компонентами, с последующим добавлением к полученной смеси фермента и проведением гидролиза.
В методике C, в частности, не добавляют кислоту, а воду добавляют таким образом, чтобы концентрация целлюлозосодержащей биомассы составляла 0,1-50% по весу, с последующей обработкой при температуре 100-400°C в течение от 1 секунды до 60 минут. При выполнении обработки в таких температурных условиях происходит гидролиз целлюлозы и гемицеллюлозы. Количество циклов обработки не ограничивается, при этом обработка может быть выполнена 1 или более раз. В частности, в случаях, когда вышеописанную обработку выполняют 2 или более раз, условия при первой обработке могут отличаться от условий при второй и последующих обработках.
Как правило, при гидролизе, в котором используют гидротермическую обработку, сначала протекает гидролиз гемицеллюлозного компонента, имеющего низкую кристалличность, с последующим разложением целлюлозного компонента, имеющего высокую кристалличность. Таким образом, при использовании гидротермической обработки можно получить раствор, содержащий большое количество ксилозы, полученной из гемицеллюлозы. Кроме того, при гидротермической обработке, подвергая после обработки твердые компоненты биомассы реакции при более высоком давлении и более высокой температуре, чем при вышеуказанной обработке, может быть расщеплен целлюлозный компонент, имеющий более высокую кристалличность, с получением раствора, содержащего большое количество глюкозы, полученной из целлюлозы. При введении двухэтапной стадии гидролиза могут быть подобраны условия гидролиза, подходящие для гемицеллюлозы и целлюлозы, при этом могут быть повышены эффективность разложения и выход сахара. Кроме того, при хранении сахарного раствора, полученного при первых условиях разложения, и сахарного раствора, полученного при вторых условиях разложения, отдельно друг от друга, могут быть получены два типа сахарных растворов с различными соотношениями моносахаридов, содержащихся в гидролизатах. Таким образом, также можно разделить сахарный раствор, полученный при первых условиях разложения, как сахарный раствор, содержащий в качестве основного компонента ксилозу, и сахарный раствор, полученный при вторых условиях разложения, как сахарный раствор, содержащий в качестве основного компонента глюкозу. Посредством разделения моносахаридных компонентов, содержащихся в сахарном растворе, как описано выше, ферментация может быть выполнена отдельно, как ферментация, в которой в качестве исходного сырья для ферментации используется ксилоза в сахарном растворе, и как ферментация, в которой в качестве исходного сырья для ферментации используется глюкоза в сахарном растворе, где могут быть подобраны и применены виды микроорганизмов, которые являются наиболее подходящими для соответствующих типов ферментации.
В методике D обработанную жидкость, полученную в методике C, дополнительно подвергают ферментативному гидролизу целлюлозосодержащей биомассы.
Используемый фермент может быть таким же, как фермент, используемый в методике B. Условия ферментной обработки также могут быть такими же, как соответствующие условия в методике B.
В тех случаях, когда гидротермическая обработка сопровождается гидролизом целлюлозосодержащей биомассы с использованием фермента, предпочтительно проводить гидролиз гемицеллюлозы, имеющей низкую кристалличность, с помощью гидротермической обработки при первом гидролизе, с последующим проведением гидролиза целлюлозы, имеющей высокую кристалличность, с использованием фермента при втором гидролизе. При использовании фермента во втором гидролизе стадию гидролиза целлюлозосодержащей биомассы можно провести более эффективно. Более конкретно, при первом гидролизе с помощью гидротермической обработки главным образом протекает гидролиз гемицеллюлозного компонента, содержащегося в целлюлозосодержащей биомассе, и частичное разложение лигнина, при этом получаемый в результате гидролизат разделяется на водный раствор и твердые компоненты, содержащие целлюлозу. Затем твердые компоненты, содержащие целлюлозу, гидролизуют при добавлении фермента. Разделенный/выделенный водный раствор в качестве основного компонента содержит ксилозу, которая является пентозой. Кроме того, из продукта реакции гидролиза твердых компонентов, содержащих целлюлозу, могут быть получены моносахаридные компоненты, содержащие в качестве основного компонента глюкозу. Водный раствор, полученный в результате гидротермической обработки, может быть смешан с твердыми компонентами, с последующим добавлением к полученной смеси фермента и проведением гидролиза.
В методике E используемая щелочь более предпочтительно является гидроксидом натрия или гидроксидом кальция. Указанные щелочи добавляют к целлюлозосодержащей биомассе таким образом, чтобы их концентрации находились в пределах диапазона 0,1-60% по весу, при этом обработка может быть выполнена при температуре в пределах диапазона 100-200°C, предпочтительно 110-180°C. Количество циклов обработки не ограничивается, при этом вышеописанная обработка может быть выполнена 1 или более раз. В частности, в тех случаях, когда вышеописанную обработку выполняют 2 или более раз, условия при первой обработке могут отличаться от условий при второй и последующих обработках.
Поскольку обработанный продукт, полученный в результате обработки щелочью, содержит такие щелочи, как гидроксид натрия, его необходимо нейтрализовать, чтобы его можно было подвергнуть далее реакции гидролиза с использованием фермента. Нейтрализация может быть выполнена либо для водного щелочного раствора, полученного в результате удаления твердых компонентов из гидролизата при разделении твердой и жидкой фаз, или в состоянии, в котором содержатся твердые компоненты. Кислотный реагент, используемый для нейтрализации, не ограничивается и предпочтительно является одновалентным кислотным реагентом. В случаях, когда и кислотные, и щелочные компоненты являются солями, имеющими валентность 2 или выше, в ходе Стадии (2) они не проходят через нанофильтрационную мембрану, при этом соли осаждаются в жидкости в ходе процесса концентрирования жидкости, что может вызвать забивание мембраны.
В случаях, когда используется одновалентная кислота, примеры кислоты включают, помимо прочих, азотную кислоту и соляную кислоту.
В случаях, когда используется кислотный реагент, имеющий валентность 2 или выше, необходимо снижать количества кислоты и щелочи или использовать механизм для удаления осадков в ходе Стадии (2), чтобы избежать осаждения солей во время Стадии (2). В случаях, когда используется кислота, имеющая валентность 2 или выше, кислота предпочтительно является серной кислотой или фосфорной кислотой. Поскольку в тех случаях, когда используется гидроксид кальция, в результате нейтрализации образуется сульфат кальция, сульфат кальция необходимо удалять путем разделения твердой и жидкой фаз. Примеры способа разделения твердой и жидкой фаз включают, помимо прочего, центрифугирование и разделение с помощью мембран, при этом сульфат кальция может быть также удален при выполнении нескольких типов стадий разделения.
Используемый фермент может быть таким же, как фермент, используемый в методике B. Условия ферментной обработки также могут быть такими же, как условия в методике B.
В случаях, когда после обработки щелочью целлюлозосодержащую биомассу гидролизуют с использованием фермента, лигниновый компонент вокруг гемицеллюлозного и целлюлозного компонентов удаляется путем смешивания целлюлозосодержащей биомассы с водным раствором, содержащим щелочь, и нагревания полученной смеси, что переводит, таким образом, гемицеллюлозный и целлюлозный компоненты в активное состояние, с последующим проведением ферментативного гидролиза гемицеллюлозы, имеющей низкую кристалличность, и целлюлозы, имеющей высокую кристалличность, которые не были расщеплены в гидротермическом процессе во время обработки щелочью. Более конкретно, при обработке щелочью главным образом протекает гидролиз части гемицеллюлозного компонента, содержащегося в целлюлозосодержащей биомассе, и частичное разложение лигнина, при этом получаемый в результате гидролизат разделяется на щелочной раствор и твердые компоненты, содержащие целлюлозу. Затем твердые компоненты, содержащие целлюлозу, после доведения pH гидролизуют при добавлении к ним фермента. В случаях, когда концентрация в щелочном растворе низкая, гидролиз может быть проведен сразу, при добавлении фермента после нейтрализации, без выделения твердых компонентов. Из продукта реакции гидролиза твердых компонентов, содержащих целлюлозу, могут быть получены моносахаридные компоненты, содержащие в качестве основного компонента глюкозу и ксилозу. Поскольку разделенный/выделенный щелочной раствор в качестве основного компонента содержит в дополнение к лигнину ксилозу, которая является пентозой, водный сахарный раствор может быть выделен при нейтрализации щелочного раствора. Водный сахарный раствор, полученный в результате нейтрализации, может быть смешан с твердыми компонентами, с последующим добавлением к полученной смеси фермента и проведением гидролиза.
Условия для обработки аммиаком в методике F основаны на JP 2008-161125 A и JP 2008-535664 A. Например, концентрация аммиака, добавляемого к целлюлозосодержащей биомассе, находится в пределах 0,1-15% по весу относительно целлюлозосодержащей биомассы, при этом обработку проводят при температуре 4-200°C, предпочтительно 90-150°C. Добавляемый аммиак может находиться в жидком или газообразном состоянии. Кроме того, до