Способ лечения ларвального эхинококкоза лабораторных животных
Иллюстрации
Показать всеИзобретение относится к области ветеринарии и предназначено для лечения ларвальных эхинококкозов лабораторных животных. Нокодазол вводят подкожно в количестве, не вызывающем образования соединительнотканной капсулы вокруг препарата, по 10 инъекций в сутки в суточной дозе 11-200 мг/кг, с интервалом в 3-4 дня, в точки, расположенные на дорзальной и вентральной поверхностях тела животного. Способ высокоэффективен для лечения цистного и альвеолярного ларвальных эхинококкозов и других тканевых паразитозов лабораторных животных. 3 табл., 1 пр.
Реферат
Изобретение относится к медицине и ветеринарии и может найти применение для лечения ларвальных цистного и альвеолярного эхинококкозов человека и животных.
Цистный и альвеолярный эхинококкозы - хронически протекающие гельминтозы вызываемые ларвальной стадией цестод Echinococcus granulosus и E.multilocularis, относятся к наиболее тяжелым и опасным паразитарным заболеваниям. Альвеолярный эхинококкоз (альвеококкоз) является заболеванием человека, а цистным эхинококкозом болеют человек и сельскохозяйственные животные. Ввиду широкого распространения и огромного экономического ущерба здравоохранению и животноводству, исчисляемого сотнями миллионов долларов в год, эти заболевания представляют серьезную социальную и экономическую проблему для многих стран мира, в том числе и России [8].
Единственным радикальным методом лечения эхинококкозов является хирургический, малоэффективный в запущенных случаях заболевания и при множественной инвазии.
Применяемые для химиотерапии эхинококкозов препараты группы карбаматбензимидазолов (мебендазол и альбендазол) не обеспечивают радикальный терапевтический эффект и не гарантируют излечение больного на протяжении всей его жизни, ввиду того что они обладают слабым паразитоцидным действием и вызывают преимущественно паразитостатический эффект [5, 7, 9].
Нокодазол - серосодержащее гетероциклическое органическое соединение, относящееся к группе карбаматбензимидазолов, вызывает деполимеризацию микротрубочек и применяется при экспериментальной химиотерапии злокачественных новообразований [4, 6, 10, 11]. Однако при парентеральном введении нокодазол, как и другие препараты группы карбаматбензимидазолов, не проявил способности подвергаться резорбции из места инъекции. В местах инъекции нокодазола вокруг введенного препарата в результате клеточной реакции организма формируется постепенно утолщающаяся соединительнотканная капсула. В брюшной полости формирование такой капсулы вокруг конгломератов препарата сопровождается выраженным спаечным процессом и петрификацией.
Паразитоцидное действие на ларвальный альвеококк обнаружено у нокодазола лишь при парентеральном применении [1].
При внутримышечном введении вокруг введенного препарата образуется зона некроза распространяющаяся на мышечную ткань, сосуды и нервные волокна, что исключает возможность парентерального применения нокодазола в клинических условиях для химиотерапии ларвальных эхинококкозов.
В качестве прототипа избрана работа [1], в которой приведены результаты испытания внутрибрюшных инъекций нокодазола при лечении экспериментального альвеококкоза хлопковых крыс.
Недостатками прототипа являются:
1. низкая эффективность препарата (отсутствие губительного действия на большинство ларвоцист альвеококка у животного);
2. применение высоких доз препарата сопряжено с высокой его токсичностью и последующими осложнениями вплоть до гибели животного;
3. высокая стоимость препарата, связанная с нерациональным использованием большей части дорогостоящего препарата (50 мг препарата стоят 68,2 $), которая исключается из лечебного процесса из-за формирования соединительнотканной капсулы, препятствующей резорбции нокодазола.
Ввиду этих недостатков исключается возможность применения способа прототипа в медицине и ветеринарии в качестве противоэхинококкового средства системного действия.
Задачей изобретения является создание способа лечения ларвального эхинококкоза на основе нокодазола, обеспечивающего повышение эффективности терапии при низкой лечебной дозе препарата, отсутствие токсичности, а также снижение риска осложнений.
Поставленная задача решается способом лечения ларвального эхинококкоза лабораторных животных нокодазолом, отличающимся тем, что препарат вводят подкожно в количестве, не вызывающем образования соединительнотканной капсулы вокруг препарата, по 10 инъекций в сутки в суточной дозе 11-200 мг/кг, с интервалом в 3-4 дня, в точки, расположенные на дорзальной и вентральной поверхностях тела животного.
Изобретение основано на использовании впервые выявленного феномена полной резорбции из места инъекции введенной подкожно субстанции нокодазола в количестве, не вызывающем образования соединительнотканной капсулы вокруг препарата.
Практически способ осуществляется следующим образом. Экспериментально зараженному животному вводят подкожно водную суспензию нокодазола путем множественных точечных инъекций в точки, расположенные на дорзальной и вентральной поверхностях тела животного. Выполняют 10 инъекций в сутки два раза в неделю с интервалом в 3-4 дня, при суточной дозе, равной 11-200 мг/кг, которая наряду с продолжительностью лечения зависит от видов животных и возбудителей инвазии (у мышей, зараженных Е. granulosus - от 11 мг/кг, у хлопковых крыс, зараженных Е. multilocularis - 200 мг/кг).
Все инъекции проводят на расстоянии друг от друга, предотвращающем увеличение концентрации ДВ в месте инъекций и слияние соседних подкожных диффузий, способствующих формированию соединительнотканной капсулы вокруг препарата, которая препятствует постоянному и непрерывному поступлению ДВ в кровь животного.
Ввиду существенных отличительных признаков, приведенных в таблице 1, заявляемый способ имеет следующие преимущества перед способом прототипа:
- радикальный терапевтический эффект - паразитоцидное действие (деструкция герминативного слоя и зародышевых элементов паразита выявлена у 100% леченых животных) достигается при низких лечебных дозах препарата;
- не происходит накопление препарата в местах инъекций, в результате чего соединительнотканная капсула не образуется, создаются условия для полной резорбции нокодазола из множественных микродепо, что обеспечивает постоянное, непрерывное и продолжительное поступление препарата в кровь животного и весь введенный препарат участвует в лечебном процессе;
- применение низких лечебных доз нокодазола исключает токсическое действие препарата;
- отсутствует побочное действие препарата (спаечный процесс и петрификация);
- возможное применение препарата в клинических условиях благодаря высокой эффективности ДВ (оказывающего паразитоцидное действие на герминативные клетки паразита) и отсутствию побочного и токсического действий препарата в лечебных суточных дозах.
Эффективность предлагаемого способа иллюстрируют следующие примеры.
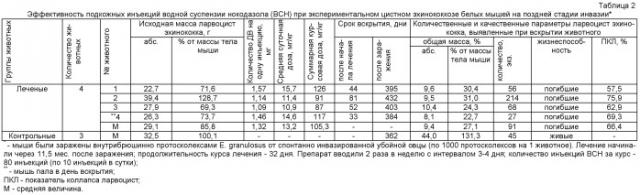
Пример 1. Терапевтическую активность нокодазола (Aldrich Chemical Company, Inc., США), испытанного в виде суспензии в физиологическом растворе, оценивали при экспериментальном цистном эхинококкозе белых мышей на поздней стадии инвазии. 7 аутбредных мышей в возрасте 1 мес (самки) заражали внутрибрюшинно протосколексами Е. granulosus, выделенными из эхинококковых пузырей от убойной спонтанно инвазированной овцы по ранее описанному методу [2]. Каждое животное получило по 1000 зрелых протосколесов. Через 7,5 мес после заражения мыши были разделены на 2 группы: экспериментальную и контрольную. 4 мышей экспериментальной группы начинали лечить подкожными инъекциями водной суспензии нокодазола (ВСН) через 11,5 мес после заражения; остальные 3 мыши служили контролем. Препарат вводили 2 раза в неделю с интервалами в 3-4 дня. Продолжительность курса лечения составила 32 дня; всего за курс лечения животные получили 80 инъекций (по 10 инъекций в сутки) в точки, расположенные на дорзальной и вентральной поверхностях тела животного, в суммарной курсовой дозе 87-126 мг/кг (при минимальной суточной дозе - 11 мг/кг; средняя суточная доза составила - 13,2 мг/кг; количество ДВ на одну инъекцию в среднем - 1,3 мг). Взвешивание каждого леченого и контрольного животного начинали через 11,5 мес после заражения и проводили ежедневно в течение всего опыта. Исходную массу ларвоцист эхинококка (ИМЛ) у каждой леченой мыши определяли по формуле:
ИМЛ=МТи-МТпл+МЛпл,
где МТи, МТпл и МЛпл - масса тела животного исходная (в начале лечения), после лечения и масса ларвоцист после лечения соответственно. Всех мышей сравниваемых групп вскрывали через 12-14 мес после заражения, у каждой леченой мыши определяли показатель коллапса ларвоцист (ПКЛ), количество и жизнеспособность ларвоцист. ПКЛ вычисляли в процентах по формуле:
ПКЛ=МЛпл·100/МТи-МТпл,
где МТи и МТпл - массы тела животного исходная и после лечения соответственно.
У каждой леченой мыши отмечали наличие субстанции нокодазола в подкожной клетчатке после сепарирования участков кожи в местах инъекций ВСН на дорзальной и вентральной поверхностях тела животного.
Результаты вскрытия животных показали, что ВСН проявила высокую терапевтическую активность в сравнительно низких дозах ДВ на поздних стадиях инвазии (табл.2). У всех леченых мышей, вскрытых через 33-81 день после начала лечения установлена гибель всех выявленных в брюшной полости ларвоцист эхинококка.
Число погибших ларвоцист на 1 животное составляло 27-214 экземпляров, а их масса колебалась в пределах 8,1-10,4 г (22,7-31,0% от массы тела хозяина). Все выявленные ларвоцисты были спавшимися и содержали разрушенную герминативную оболочку. Губительное действие нокодазола сопровождалось высоким значением ПКЛ (57,5-75,9%) у всех излеченных животных. При исследовании подкожной клетчатки следов введенного нокодазола не обнаружено, что свидетельствовало о полной резорбции препарата из депо.
У контрольных мышей, павших от интенсивного эхинококкоза через 11,5-12 мес после заражения, масса паразитов на 1 животное составляла 34,0-54,0 г (76,7-186,6% от массы тела хозяина), а количество ларвоцист колебалось от 18 до 71 экземпляра.
Пример 2. Эффективность подкожных инъекций ВСН определяли при экспериментальном ларвальном альвеококкозе хлопковых крыс (Sigmodon hispidus). 11 хлопковых крыс обоего пола в возрасте 1-1,5 мес заражали внутрибрюшинно микроскопическими ацефалоцистами диаметром 100-300 мкм, выделенными из ларвоцист E.multilocularis от экспериментально зараженной хлопковой крысы - донора. Каждому животному вводили внутрибрюшинно по 200 ацефалоцист альвеококка, выделенных по ранее описанному методу [3]. Животных разделили на 2 группы. 3 хлопковые крысы экспериментальной группы получали ВСН подкожно в точки, расположенные на дорзальной и вентральной поверхностях тела животного, в суточной дозе 200 мг/кг. Вторая группа (8 животных) была контрольной. Лечение 3 животных экспериментальной группы начинали на 38 день после заражения при средней исходной массе ларвоцист альвеококка (СИМЛ), равной 3,25 г и составлявшей 2,2% от средней массы тела хозяина (СМТХ). ВСН вводили подкожно всего 8 дней (2 раза в неделю с интервалом 3-4 дня, в течение 4-х недель) по 10 инъекций в день в суточной дозе ДВ 200 мг/кг (количество ДВ на одну инъекцию - 2,4 мг) в точки, расположенные на дорзальной и вентральной поверхностях тела животного. Всего за весь курс животные получили 80 инъекций. Леченых и контрольных хлопковых крыс вскрывали на 82 день после заражения. При вскрытии определяли жизнеспособность, степень зрелости и массу всех выявленных ларвоцист альвеококка у каждого животного. Показателем зрелости ларвоцист служило наличие зрелых протосколексов. В экспериментальных и контрольных группах определяли среднюю массу ларвоцист на 1 животное (СМЛ) в граммах, ее отношение к СМТХ в процентах и индекс торможения роста паразитарных ларвоцист (ИТРПЛ) в процентах у леченых животных по сравнению с контрольными по формуле:
ИТПРЛ=(Мк-Мл)/(Мк-Ми)·100,
где Ми, Мк и Мл - средние значения массы ларвоцист эхинококка на 1 животное: исходной, у контрольных и леченых животных соответственно (3).
При вскрытии леченых и контрольных хлопковых крыс установлена гибель всех ларвоцист альвеококка у всех леченых животных. СМЛ у животных экспериментальной группы не превышала СИМЛ и составляла 2,84 г (2,1% от СМТХ). ИТПРЛ составлял 100% (табл.3). К этому сроку у контрольных животных все ларвоцисты были живыми, зрелыми; СМЛ была равна 87,84 г и составляла 77,2% от СМТХ. У всех леченых животных в подкожной клетчатке следов введенного нокодазола не обнаружено, что свидетельствовало о полной резорбции введенного препарата из депо в подкожной клетчатке.
Таким образом, заявляемый способ обеспечивает повышение эффективности нокодазола при низкой лечебной дозе препарата, а также профилактику осложнений.
При низком содержании в месте инъекции под кожей субстанция нокодазола обладает способностью подвергаться полной резорбции благодаря предотвращению тканевой реакции организма на препарат, проявляющейся в образовании соединительнотканной капсулы вокруг препарата.
Избежание попадания препарата в одну и ту же точку предотвращает увеличение концентрации ДВ в месте инъекции и обеспечивает рациональное использование препарата, профилактику формирования соединительной капсулы вокруг препарата в месте инъекции и связанных с этим осложнений.
Множественность инъекций препарата в день обеспечивает создание серии подкожных микродепо, что создает условия для постоянного, непрерывного и продолжительного поступления нокодазола в кровь животного и обеспечивает повышение эффективности лечения.
| Таблица 1 | ||
| Сравнение отличительных признаков способов лечения ларвальных эхинококкозов лабораторных животных заявляемого и прототипа | ||
| Отличительный признак | Способы | |
| прототипа | заявляемый | |
| Способ парентерального введения препарата | внутрибрюшинный | подкожный |
| Повторность введения препарата | однократное | многократное |
| Общее число инъекций на весь курс лечения | 1 | 80 |
| Масса действующего вещества на одну инъекцию, мг | 60 | 1,1-2,4 |
| Минимальные лечебные суточные дозы, мг/кг | 500 | 11-200 |
| Эффективность способа при экспериментальном альвеококкозе хлопковых крыс | неэффективен (ввиду паразитостатического действия на герминативные клетки паразита) | эффективен (ввиду паразитоцидного действия на герминативные клетки паразита) |
| Деструкция герминативного слоя и зародышевых элементов паразита | отсутствует | выявлена у 100% леченых животных |
| Значение индекса торможения роста паразитарных ларвоцист (ИТРПЛ) | ИТРПЛ=91,0% | ИТРПЛ=100% |
| Степень резорбции препарата из места инъекции | частичная (из-за использования большой массы ДВ на одну инъекцию, вследствие чего формируется соединительнотканная капсула вокруг конгломератов препарата, большая часть которого исключается из лечебного процесса) | полная (благодаря применению малого количества ДВ на одну инъекцию формирование соединительнотканной капсулы не происходит, и весь введенный препарат участвует в лечебном процессе) |
| Условия для эффективной химиотерапии | отсутствуют (ограниченное и прекращающееся со временем поступление ДВ в кровь животного из крупных конгломератов внутрибрюшинного депо) | создаются (постоянное, непрерывное и продолжительное поступление ДВ в кровь животного из множественных подкожных микродепо) |
| Побочное действие | присутствует (в результате использования высоких доз ДВ и внутрибрюшинного способа введения происходит формирование соединительнотканной капсулы вокруг препарата, сопровождающееся выраженным спаечным процессом и петрификацией) | отсутствует (ввиду применения низких суточных доз ДВ) |
| Токсическое действие | выраженное острое (применение нокодазола в дозе 250 мг/кг проявляется картиной острого отравления и гибелью животных на 2-4 сутки) | исключено (ввиду использования низких разовых доз ДВ) |
| Возможность применения в клинических условиях | исключена (ввиду низкой эффективности препарата и применения высоких токсических доз ДВ, вызывающих осложнения) | имеется (благодаря высокой эффективности ДВ, оказывающего паразитоцидное действие на герминативные клетки паразита и отсутствие побочного и токсического действий препарата в лечебных суточных дозах) |
Источники информации
1. Джабарова В.И., Кротов А.И., Колосова М.О. и другие. Экспериментальная химиотерапия альвеококкоза. Сообщение VIII. Сравнительная эффективность и токсичность нокодазола и мебендазола. Медицинская паразитология и паразитарные болезни. 1983, №5, 96, 65-68.
2. Коваленко Ф.П., Кротов А.И., Буданова И.С., Разаков Ш.А. Экспериментальная терапия эхинококкоза. Сообщение I. Лабораторная модель эхинококкоза и влияние на развитие ларвоцист Echinococcus granulosus сарколизинакридина, левамизола и мебендазола. Медицинская паразитология и паразитарные болезни 1976, №5, 546-551.
3. Коваленко Ф.П. Экспериментальные модели эхинококкоза: оптимизация и применения в разработке новых методов диагностики профилактики и лечения эхинококкозов человека и животных. Дисс. …д.м.н., 1998, 59 с.
4. Hong F.D., Chen J., Donovan S. et al. Taxol, vincristine or nocodazole induces lethality in Gj-checkpoint- defective human astrocytoma U373MG cells by triggering hyperploid progression. Carcinogenesis 1999, vol.20, nol.7, pp.1161-1168.
5. Horton R.J. Albendazole in treatment of human cystic echinococcosis: 12 years of experience. Acta Trop., 1997, 64:79-93.
6. Hye Joung Choi, Masayuki Fukui, Bao Ting Zhu. Role of Cyclin B1/Cdc2 Up-Regulation in the Development of Mitotic Prometaphase Arrest in Human Breast Cancer Cells Treated with Nocodazole. PloS ONE 2011, 6 (8): e24312. doi:10.1371/jornal.pone.0024312.
7. Morris D.L., Dykes P.W., Dickson B., Marriner S.E., Bogan J.A., Burrows F.G. Albendazole in hydatid disease. Br Med J (Clin Res Ed) 1983, 286:103-104.
8. Torgerson P.R, Keller K., Magnotta M., Ragland N. The global burden of alveolar echinococcosis. PLoS Negl Dis 2010, 4(6): e722. doi: 10.1371/jourenal.pntd.0000722.
9. Stojkovic M., Zwahlen M., Teggi A. et al. Treatment Response of Cystic Echinococcosis to Benzimidazoles: A Systematic Review. PLoS Negl Trop Dis(2009, Sep 29;3(9):e524.
10.Yuan-Soon Ho, Jiing-Shium, Jiiang-Huei et al. Griseofulvin potentiates anti-tumorigenesis effects of nocodazole through induction of apoptosis and G2/M cell cycle arrest in human colorectal cancer cells. J Cancer - 2001, 91, 393-401.
11. Wang Y.J., Jeng J.H., Chen R.J., et al. Ketoconazole potentiates the antitumor effects of nocodazole: In vivo therapy for human tumor xenografts in nude mice. // Molecular Carcinogenesis 2002, 34(4): 199-210.
Способ лечения ларвального эхинококкоза лабораторных животных нокодазолом, отличающийся тем, что препарат вводят подкожно в количестве, не вызывающем образования соединительнотканной капсулы вокруг препарата, по 10 инъекций в сутки в суточной дозе 11-200 мг/кг, с интервалом в 3-4 дня, в точки, расположенные на дорзальной и вентральной поверхностях тела животного.