Композиция на основе диацетата бетулина
Иллюстрации
Показать всеИзобретение относится к фармацевтической промышленности, в частности к композиции производного бетулина с биосовместимым носителем. Композиция, содержащая диацетат бетулина с арабиногалактаном, при определенном соотношении компонентов. Вышеописанная композиция обладает улучшенной растворимостью и проявляет противоопухолевые свойства. 3 з. п. ф-лы, 3 ил., 3 табл., 5 пр.
Реферат
Изобретение относится к химико-фармацевтической промышленности, в частности, к производству композиций фармакологически активных веществ.
Диацетат бетулина (C34H54O4, 3β,28-диацетокси-луп 20(29)-ен), сложный эфир уксусной кислоты и бетулина, получают из бересты березы. Диацетат бетулина (ДАБ) проявляет гепатопротекторные, гиполипидемические, желчегонные, антиоксидантные свойства и является перспективным препаратом для фармации [Патент РФ №2324700. Опубл. 20.05.2008; Патент РФ №2436791. Опубл. 20.12.2011].
Основным препятствием для использования диацетата бетулина в качестве лечебного средства для внутреннего и наружного применения является низкая биологическая доступность, связанная с его плохой растворимостью.
Известны разные способы увеличения растворимости и повышения биологической доступности бетулина, одним из которых является создание композиций с водорастворимыми носителями.
Известно фунгицидное средство, включающее в качестве активного ингредиента тебуконазол и природные или синтетические водорастворимые полимеры в массовом соотношении тебуконазол: водорастворимые полимеры 1:0-5) соответственно, при этом его получают путем механохимического взаимодействия тебуконазола с водорастворимыми полимерами [Патент РФ №2469536. Опубл. 20.12.2012 г.].
Известно лекарственное средство, представляющее собой комплекс нифедипина с арабиногалактаном при весовом соотношении компонентов нифедипин: арабиногалактан, равном 1:(10-40), полученное механической обработкой в планетарной мельнице при ускорении 60 g [Патент РФ №2391980. Опубл. 20.06.2010 г.].
Недостатком данных композиций является их узкая направленность (фунгицидное и кардиотропное средства).
Наиболее близкой к предолагаемому изобретению является композиция бетулина с биосовместимыми носителями - полиэтиленгликолем и поливинилпирролидоном, при следующем соотношении компонентов: бетулин (активное вещество) - 10-25%, полимерный носитель - 75-90%, полученная механической активацией в мельнице-активаторе в течение 10-30 мин при нагрузке на мелющие тела не более 20 g и в соотношении массы смеси к массе мелющих тел 1:30 [Патент РФ №2401118. Опубл. 10.10.2010].
Недостатком данной композиции является использование в качестве носителей синтетических полимеров.
Задача настоящего изобретения состоит в создании новой композиции на основе диацетата бетулина (ДАБ) и природного полимерного носителя с улучшенной растворимостью и проявляющей противоопухолевые свойства.
Поставленная задача решается тем, что в композиции производного бетулина с биосовместимым носителем, согласно изобретению, в качестве производного бетулина используют диацетат бетулина, а в качестве биосовместимого носителя - арабиногалактан при соотношении компонентов, масс.%: диацетат бетулина - 10%, арабиногалактан - остальное, при этом ее получают механохимической активацией диацетата бетулина с арабиногалактаном либо растворением смеси исходных или механоактивированных компонентов в воде с последующим выпариванием раствора.
Композиция представляет собой либо порошок белого цвета с желтоватым оттенком, либо прозрачные пленки, легко растворимые в воде. Полученная композиция проявляет противоопухолевые свойства.
Авторами было показано, что при механохимической обработке диацетата бетулина с водорастворимыми полимерами полиэтиленгликолем и поливинилпирролидоном не удалось повысить растворимость диацетата бетулина, что связано с тем, что диацетат бетулина не образует молекулярных комплексов с данными полимерами [Михайленко М.А., Шахтшнейдер Т.П., Дребущак В.А., Кузнецова С.А., Скворцова Г.П., Болдырев В.В. Влияние механической обработки на свойства бетулина и их смеси с водорастворимыми полимерами // Химия природных соединений. 2011. №2. С.211-214].
Арабиногалактан (АГ) - водорастворимый природный дешевый, доступный и нетоксичный полисахарид, выделяемый из древесины лиственницы, обладающий комплексом уникальных свойств. Арабиногалактан безвреден, разрешен для применения в качестве добавок к продуктам питания и в биологически активные добавки. Он имеет низкую среднечисленную молекулярную массу, гарантирующую повышенную водорастворимость создаваемых композиций. Макромолекула АГ имеет разветвленное строение, что способствует прочному удерживанию ДАБ в боковой цепи арабиногалактана.
Данную композицию получают следующим образом.
Исходные компоненты - диацетат бетулина и арабиногалактан - получают по оригинальным методикам [Патент РФ №2436791 и патент РФ №2273646], хотя можно использовать ДАБ и АГ, полученные другими способами, но с чистотой не менее 95%. Композицию получают путем растворения смеси исходных или механоактивированных компонентов в воде с последующим выпариванием раствора либо совместной механохимической обработкой исходных компонентов, не приводящей к их деструкции, в мельнице-активаторе в течение 10-30 минут при нагрузке не мелющие тела не более 10 g и соотношении массы смеси к массе мелющих тел 1:30. Для предотвращения деструкции исходных компонентов, могут быть использованы высокоэнергонапряженные мельницы-активаторы с охлаждаемыми реакторами, причем плотность материала реактора и мелющих тел не должна превышать плотность стали, или аппараты с пониженной нагрузкой на мелющие тела. Одним из таких аппаратов является мельница SPEX 8000 (CertiPrep Corp., США).
Растворение АГ и его смесей с ДАБ в воде проводили в тестере растворимости Varian 705 DS. В сосуд с водой помещали 200 мг АГ или 180 мг АГ и 20 мг ДАБ и выдерживали при постоянном перемешивании при 37°C в течение 2 суток. После чего раствор отфильтровывали с помощью фильтров с диаметром пор 0.2 мкм. Фильтраты подвергали выпариванию при пониженном давлении и температуре 35-40°C (ротационный испаритель ИР-1М, Россия). Полученные прозрачные пленки исследовали рентгендифракционными, хроматографическими и спектроскопическими методами.
Рентгенофазовый анализ (РФА) проводили с использованием дифрактометра D8 DISCOVER с двухкоординатным детектором (Bruker), CuKα-излучение, 2θ=5÷40. ИК-спектры получали методом нарушенного полного внутреннего отражения (НПВО) в диапазоне частот 4000-500 см-1 на Фурье ИК-спектрометре Digilab Excalibur 3100 (Varian) без прессования образцов. Молекулярно-массовое распределение (ММР) образцов исследовали методом гель-проникающей хроматографии на хроматографе Agilent 1200 с рефрактометрическим детектором 1260 Infinity (колонка PL aquagel-OH 40 300*7.5 мм, температура колонки 30°C, элюент 0,1 М LiNO3 1 мл/мин). Калибровка колонки осуществлялась с помощью стандартных образцов декстранов (SIGMA-ALDRICH) с молекулярными массами 10600, 20000, 41272, 70000. Хроматограммы отнормированы на максимум поглощения рефрактометрического детектора. Электронномикроскопические наблюдения осуществляли с помощью электронного микроскопа ТМ-100 (Hitachi, Япония). Для определения содержания ДАБ навеску образца 9-10 мг подвергали трехкратной экстракции 1 мл хлороформа. Полученный экстракт выпаривали и проводили растворение в 1 мл этанола. Содержание ДАБ определяли хроматографически с помощью хроматографа Милихром А-02 (ЗАО «ЭкоНова», Россия). Условия хроматографирования: колонка N2301 2.0*75 мм, сорбент ProntoSIL 120-5C18 AQ, размер частиц 5.0 мкм, подвижная фаза Н2О (А)-CH3CN (В), градиентный режим 80-100-100% В. Скорость потока 100 мкл/мин, Т=35°C. Содержание ДАБ определяли на длине волны 200 и 210 нм.
Путем выпаривания в ротационном испарителе водных растворов смесей АГ с ДАБ получены слабоокрашенные (желтоватые) прозрачные пленки, легко подвергавшиеся повторному растворению в гораздо меньших объемах воды, нежели было использовано для их получения, с образованием вязкого раствора. Поверхность пленок достаточно гладкая, а на электронно-микроскопическом изображении пленки видна неупорядоченная внутренняя структура. Толщина пленок составляла около 10 мкм. Рентгенофазовый анализ показал, что пленки являются аморфными и стабильны по отношению к кристаллизации (аморфное состояние пленок сохранялось в течение 1 года).
Изобретение поясняется конкретными примерами.
Пример 1. Смесь, состоящую из 0,02 г диацетата бетулина и 0,18 г АГ, без проведения механоактивации растворяли в 250 мл дистиллированной воды при 37°C в течение 24 часов. Затем проводили центрифугирование и фильтрование полученного раствора. Фильтрат подвергали испарению с помощью ротационного испарителя, после удаления воды получали слабоокрашенные прозрачные пленки, которые исследовали методом ВЭЖХ. Растворимость пленки в воде - 100% (см. табл.1).
Пример 2. Смесь, состоящую из 0,2 г диацетата бетулина и 1,8 г АГ, активировали в мельнице SPEX 8000 (CertiPrep Corp., США) в стальном барабане объемом 40 мл с мелющими телами в виде стальных шаров диаметром 6 мм и ускорением мелющих тел 8-10 g, загрузка 30 г. Механическую обработку проводили в течение 10 минут, после чего смесь растворяли в 250 мл дистиллированной воды при 37°C в течение 24 часов. Затем проводили центрифугирование и фильтрование полученного раствора. Фильтрат подвергали испарению с помощью ротационного испарителя, после удаления воды получали слабоокрашенные прозрачные пленки, которые исследовали методом ВЭЖХ. Растворимость пленки в воде - 100% (см. табл.1).
Пример 3. Смесь, состоящую из 0.2 г диацетата бетулина и 1.8 г АГ, активировали в мельнице SPEX 8000 (CertiPrep Corp., США) в стальном барабане объемом 40 мл с мелющими телами в виде стальных шаров диаметром 6 мм и ускорением мелющих тел 8-10 g, загрузка 30 г. Механическую обработку проводили в течение 30 минут, после чего смесь растворяли в 250 мл дистиллированной воды при 37°C в течение 24 часов. Затем проводили центрифугирование и фильтрование полученного раствора. Фильтрат подвергали испарению с помощью ротационного испарителя, после удаления воды получали слабоокрашенные прозрачные пленки, которые исследовали методом ВЭЖХ. Растворимость пленки в воде - 100%. (см. табл.1).
Пример 4. Смесь, состоящую из 0,2 г диацетата бетулина и 1,8 г АГ, активировали в мельнице SPEX 8000 (CertiPrep Corp., США) в стальном барабане объемом 40 мл с мелющими телами в виде стальных шаров диаметром 6 мм и ускорением мелющих тел 8-10 g, загрузка 30 г, в течение 10 минут. Получали образцы в виде порошка, которые исследовали методом ВЭЖХ. Растворимость порошка в воде - 20-25% (см. табл.1).
Пример 5. Смесь, состоящую из 0,2 г диацетата бетулина и 1,8 г АГ, активировали в мельнице SPEX 8000 (CertiPrep Corp., США) в стальном барабане объемом 40 мл с мелющими телами в виде стальных шаров диаметром 6 мм и ускорением мелющих тел 8-10 g, загрузка 30 г, в течение 30 минут. Получали образцы в виде порошка, которые исследовали методом ВЭЖХ. Растворимость порошка в воде - 20-25% (см. табл.1).
В таблице 1 представлены данные по растворимости в воде смесей ДАБ-АГ.
| Таблица 1 | ||||
| № п/п | Смеси (композиции) ДАБ-АГ (1:9, масс.) | Внешний вид | Продолжительность механо-активации (мин) | Растворимость смеси в воде, % |
| Физическая смесь | ||||
| 1 | Пленка | 0 | 100 | |
| 2 | Механоактивированная смесь | Пленка | 10 | 100 |
| 3 | Механоактивированная смесь | Пленка | 30 | 100 |
| 10 | ||||
| 4 | Механоактивированная смесь | Порошок | 20-25 | |
| 5 | Механоактивированная смесь | Порошок | 30 | 20-25 |
Из таблицы следует, что как физическая, так и механоактивированные смеси ДАБ и АГ в виде пленок растворяются полностью, а механоактивированные (МА) смеси в виде порошка растворяются частично.
Следует отметить, что содержание ДАБ в пленках, полученных выпариванием водных растворов физических смесей ДАБ-АГ, определенное с помощью ВЭЖХ анализа экстрактов в хлороформе, составляет 2-2,5% от массы пленки. При растворении пленки в воде были получены растворы с концентрацией ДАБ 0,15-0,18 мг/мл, в то время как чистый ДАБ в воде практически нерастворим (~10-2-10-3 мг/мл).
В таблице 2 приведены данные по молекулярным массам и степени полидисперсности композиций АГ-ДАБ (9:1, масс.) в виде пленок, полученных выпариванием водного раствора, в зависимости от продолжительности механической активации. Для сравнения в знаменателе дроби приведены значения для чистого АГ.
| Таблица 2 | ||||
| № п/п | Продолжительность механо-активации (мин) | Средневесовая молекулярная масса Mw | Среднечисловая молекулярная масса Mn | |
| Mw/Mn | ||||
| 1 | 0 | 15680/17210 | 11260/11890 | 1,39/1,45 |
| 2 | 10 | 17030/14650 | 10680/10270 | 1,5/1,43 |
| 3 | 30 | 14560/15260 | 10430/10710 | 1,40/1,43 |
Обнаружено, что ДАБ не извлекается из водного раствора смеси ДАБ с АГ экстракцией гексаном. Это говорит о том, что в водном растворе, по-видимому, образуется прочный межмолекулярный комплекс АГ с ДАБ. Аналогично, в случае пленок, полученных выпариванием водных растворов смесей АГ с ДАБ, экстракции диацетата бетулина этиловым спиртом, в котором АГ не растворим, не происходит.
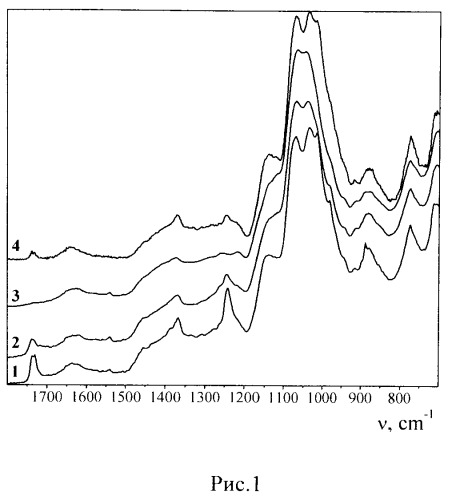
На рис. 1 представлены ИК-спектры смесей ДАБ-АГ: 1 - физическая смесь 1:9 (масс.) в виде порошка, 2 - механоактивированная смесь 1:9 (масс.) в виде порошка, 3 - механоактивированный АГ, 4 - пленка, полученная выпариванием водного раствора физической смеси.
В ИК-спектрах пленок, полученных выпариванием фильтратов, присутствуют полосы поглощения, относящиеся к ДАБ. При этом не наблюдается существенного сдвига полос в ИК-спектрах, что говорит о том, что водородные связи между компонентами, по-видимому, не образуются. Молекулы ДАБ, вероятно, находятся внутри полисахаридной оболочки и связаны с молекулами АГ за счет Ван-дер-Ваальсовых взаимодействий.
Учитывая линейные размеры молекулы ДАБ и сопоставляя молекулярную массу ДАБ с молекулярной массой комплекса, можно предположить, что ДАБ может взаимодействовать с несколькими макромолекулами АГ.
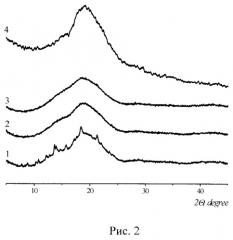
На рис.2 представлены дифрактограммы механоактивированных композиций ДАБ с АГ 1: 9 (по массе): 1 - после 5 мин механической активации, 2 - после 15 мин механической активации, 3 - после 30 мин механической активации. Исчезновение рефлексов ДАБ на рентгенограммах механоактивированных смесей подтверждает распределение тонко диспергированного вещества в матрице носителя с образованием механокомпозита. Согласно данным рентгенофазового анализа смесей ДАБ с АГ можно утверждать, что механоактивированные композиции ДАБ с АГ являются рентгеноаморфными.
В ИК-спектрах механоактивированных смесей не наблюдается сдвига максимумов полос, относящихся к колебаниям ν(C=O) и (С-O), по сравнению с физической смесью компонентов, что может свидетельствовать о распределении ДАБ в матрице АГ без образования межмолекулярных водородных связей. Возможно образование комплекса за счет Ван-дер-Ваальсовых взаимодействий.
Содержание ДАБ в пленке, полученной выпариванием водного раствора механически активированной смеси, практически не отличалось от содержания ДАБ в пленках, полученных в случае физических смесей аналогичного состава. Следовательно, как в случае механоактивированных, так и в случае физических смесей, можно получить ДАБ в виде комплекса с АГ путем растворения смесей в воде и испарения растворителя. Учитывая, что полученные пленки легко подвергаются растворению в гораздо меньших объемах воды, чем было использовано для их получения, исследование фармакологической активности таких материалов в дальнейших экспериментах может представлять интерес для использования их в медицине. Использование пленок, благодаря их полному растворению, позволит избежать избыточных количеств ДАБ при приготовлении препаратов.
Токсикологическое исследование.
Проведенное токсикологическое исследование показало, что полученные механокомпозиты диацетата бетулина с арабиногалактаном, так же как и индивидуальные вещества, в дозе 2000 мг/кг не являются ядовитыми и, согласно международной токсикологической классификации, их можно отнести к 4 классу малотоксичных веществ. Исследование фармакологической активности полученных комплексов в дальнейших экспериментах может представлять интерес для использования их в медицине.
Изучение противоопухолевой активности комплекса диацетата бетулина с арабиногалактаном на клетках асцитной аденокарциномы Эрлиха в экспериментах in vitro.
Противоопухолевую активность МА композитов ДАБ с АГ в сравнении с чистыми ДАБ и АГ определяли по данным ионного гомеостаза и доли апоптотических и некротических асцитных клеток асцитной аденокарциномы Эрлиха через 24 ч после воздействия препаратов.
Оценку ионного гомеостаза проводили с учетом концентрации ионов натрия, калия, кальция через 3 ч после добавления препаратов. Для определения влияния исследуемых веществ на параметры ионного гомеостаза отмытые асцитные клетки инкубировали в готовой среде для культивирования с концентрацией исследуемых веществ 0,5 мг/мл, в течение 3-х ч при температуре 37°C, 5% СО2 и влажности 6%. Для определения уровня внутриклеточного кальция использовали флуоресцентный зонд GreenCa2+ натрия - SBFI-AM, калия - PBFI-AM. Отмытые бесцветным раствором Хенкса клетки инкубировали с зондом в конечной концентрации 0,05 мг/мл в течение 30 мин при 37°C, после чего их отмывали от избытка красителя. Интенсивность флуоресценции измеряли на проточном цитометре Beckman Coulter FC500. Собственную флуоресценцию клеток без красителя принимали за нулевую.
Для определения доли апоптотических и некротических клеток отмытые асцитные клетки инкубировали в растворе Хенкса, содержащем флуоресцентные красители - Hoechst 33342 (1 мг/мл) и Propidium iodide (1 мг/мл), 10-15 мин при комнатной температуре. Количество апоптотических (ярко голубых), некротических (красных и красно-голубых) и слабо светящихся голубым живых клеток подсчитывали в режиме флуоресценции, общее количество клеток - в световом режиме в том же поле зрения. Рассчитывали процентное соотношение всех трех фракций клеток.
На рис.3 показано изменение концентрации катионов кальция (А), натрия (Б) и калия (В) в клетках АКЭ под влиянием механокомпозита ДАБ с АГ (2), ДАБ (3) и АГ (4) в сравнении с контролем (1).
Согласно данных ионного гомеостаза (Рис.3), все исследуемые вещества уменьшали долю клеток с высокой концентрацией кальция, что являлось косвенным свидетельством подавления уровня пролиферации клеток асцитной карциномы Эрлиха (АКЭ). Все исследуемые вещества снижали также концентрацию внутриклеточного калия и натрия, однако в большей степени содержание катионов калия в клетке снижалось под воздействием МА композиции ДАБ с АГ. Поскольку известно, что синхронное уменьшение содержания натрия, калия и кальция приводит к индукции апоптоза, следовательно, МА композиция ДАБ с АГ в большей степени стимулирует процесс элиминации клеток асцитной аденокарциномы Эрлиха.
Подтверждением этого являются данные по влиянию исходных веществ ДАБ и АГ и их МА композиции на уровень элиминации клеток АКЭ, которые представлены в таблице 3.
| Таблица 3 | ||||
| Показатели выживаемости клеток АКЭ | Образец | |||
| АГ | ДАБ | Механокомпозит ДАБ+АГ | Контроль | |
| Некроз, % | 6,6±0,8 | 5,0±0,6 | 6,6±0,9 | 7,3±0,5 |
| Апоптоз, % | 16,7±1,8* | 23±2,5* | 36±3,8* | 3,1±2,8 |
| Общая доля элиминирующихся клеток | 23,3±2,8 | 28,0±3,0 | 42,6±5,8 | 10,4±1,3 |
| Примечание: * - достоверность отличий от контроля, Р<0,05. |
Согласно представленным данным, под влиянием всех исследуемых веществ увеличилась доля клеток АКЭ в состоянии апоптоза: в присутствии АГ более чем в 5 раз, в присутствии ДАБ более чем в 7 раз, в присутствии МА композиции ДАБ с АГ - почти в 12 раз. На основании данных ионного гомеостаза и определения уровня апоптоза и некроза клеток АКЭ можно утверждать, что композиция диацетата бетулина с арабиногалактаном проявляет противоопухолевые свойства.
Таким образом, получены новые композиции диацетата бетулина с арабиногалактаном в виде порошка и пленок с распределением ДАБ в матрице полимера. Показано, что после выпаривания водного раствора физической или механоактивированной смеси компонентов получены легко растворимые в воде композиции диацетата бетулина с арабиногалактаном в виде аморфных прозрачных пленок, содержащих 2-2,5 мас.% ДАБ. Поскольку полученная композиция ДАБ-АГ имеет повышенную растворимость и, следовательно, биодоступность, по сравнению с чистым ДАБ, она будет иметь улучшенные известные свойства: гепатопротекторные, гиполипидемические, желчегонные и антиоксидантные.
1. Композиция производного бетулина с биосовместимым носителем, отличающаяся тем, что в качестве производного бетулина используют диацетат бетулина, а в качестве биосовместимого носителя - арабиногалактан, при следующем соотношении компонентов, мас.%: диацетат бетулина - 10%, арабиногалактан - остальное, при этом ее получают механохимической активацией диацетата бетулина с арабиногалактаном либо растворением смеси исходных или механоактивированных компонентов в воде с последующим выпариванием раствора.
2. Композиция по п.1, отличающаяся тем, что представляет собой порошок белого цвета с желтоватым оттенком.
3. Композиция по п.1, отличающаяся тем, что представляет собой аморфные прозрачные пленки, легко растворимые в воде.
4. Композиция по п.1, отличающаяся тем, что проявляет противоопухолевые свойства.