Способ идентификации и оценки количества микробных клеток возбудителя чумы в исследуемых пробах посредством пцр в режиме реального времени
Иллюстрации
Показать всеИзобретение относится к области биохимии, в частности к способу идентификации возбудителя чумы и оценки количества микробных клеток, идентифицируемых в качестве возбудителя чумы в исследуемых пробах посредством ПЦР с учетом результатов в режиме реального времени, включающий следующие стадии: выделение ДНК микроорганизма из исследуемых проб, подготовка калибровочной панели, исследование выделенной ДНК в ПЦР с использованием специфических праймеров и зондов с флуоресцентной меткой, идентификация исследуемой ДНК как ДНК микробного или немикробного штамма по наличию нарастания флуоресцентного свечения или его отсутствию соответственно, определение по калибровочной панели концентрации ДНК в пробе. Использование изобретения позволяет повысить эффективность идентификации исследуемой пробы и сократить сроки ее тестирования в режиме реального времени. 2 з.п. ф-лы, 2 ил., 2 табл., 2 пр.
Реферат
Изобретение относится к молекулярной биологии, а именно к медицинской биотехнологии, и может быть использовано для детекции, идентификации возбудителя чумы, а также для определения концентрации микробных клеток Yersinia peutis в исследуемой пробе.
Известна тест система «ГенПест - Тест-система для выявления ДНК Y.pestis методом ПЦР», ТУ 8895-005-01898109-2007, заключающаяся в том, что учет реакции проводят с помощью электрофоретического разделения фрагментов амплифицированной ДНК.
Однако, при этом возникает необходимость переноса амплифицированного материала на гель, что удлиняет процедуру детекции и создает условия для загрязнения реактивов и лабораторного оборудования продуктами ПЦР, что может привести к получению ложных результатов анализа.
Кроме того, недостатком является и то, что праймерами в этом методическом подходе являются олигонуклеотиды, комплементарные участкам ДНК на плазмидах, но не хромосомах, что не позволяет детектировать бесплазмидные штаммы возбудителя чумы.
Наиболее близким аналогом (прототипом) является способ мультиплексной ПЦР с оценкой результатов в реальном времени для детекции возбудителей чумы и псевдотуберкулеза (см. Matero P, Pasanen Т, Laukkanen R, Tissari P, Tarkka E, Vaara M, Skurnik M. Real-time multiplex PCR assay for detection of Yersinia pestis and Yersinia pseudotuberculosis. APMIS 2009; 117:34-44), заключающийся в том, что предложенный тест включает 4 пары праймеров, два из которых специфичны для возбудителя чумы, один для возбудителя псевдотуберкулеза и один для бактериофага лямбда, при этом описанные праймеры используют как в простой, так и в мультиплексной реакции, применяя специфические зонды, меченные различными флуорохромами.
Однако в данной работе представлены данные испытания разработанных авторами праймеров и зондов для детекции возбудителя чумы на ограниченном числе штаммов (всего двух), что не может являться доказательством эффективного использования тест-системы авторов на других штаммах возбудителя чумы.
Техническая задача предлагаемого изобретения состояла в разработке новой тест-системы, в которой используют сконструированные хромосомные праймеры и флуоресцентно-меченый зонд, позволяющие повысить эффективность идентификации исследуемой пробы и сократить сроки ее тестирования в режиме реального времени.
Поставленная задача достигается тем, что в известном способе идентификации и оценки количества микробных клеток возбудителя чумы в исследуемых пробах посредством ПЦР с учетом результатов в режиме реального времени, включающем выделение из микробной клетки ДНК возбудителя чумы, с последующим исследованием ее в ПЦР с использованием специфических праймеров и зонда с флуоресцентной меткой, и отличающимся тем, что флуоресцентную детекцию проводят сконструированными праймерами:
AL12for - 5'-TCCTGAATCAGGAGAGCAGATTACC-3'
AL12rev - 5'-TGAAGCCGCTCACACGATGT-3'
и флуоресцентно-меченым зондом:
Fam-AL12 - Fam-TTTGAAGGCGATAATGACGGCGGGA-HBQ1,
при этом регистрацию результатов проводят по присутствию и нарастанию флуоресцентного свечения, чем оно выше, тем больше молекул ДНК возбудителя Y.pestis в пробе, позволяя по интенсивности свечения идентифицировать возбудитель чумы от других близкородственных чуме микроорганизмов, а использование калибровочной панели дает возможность одновременно по графикам кривых флуоресценции отражать концентрацию ДНК во время амплификации в пробах, по которым оценивают количество микробных клеток в исследуемой пробе.
При этом смесь для амплификации состоит из следующих реагентов: специфические праймеры (каждый)-15 пм, зонд с флуоресцентной меткой - 15 пм, dNTP - 3 мМ, TRIS-HCl (при рН 8,6) - 84 мМ, (NH4)2SO4 - 21 мМ, MgCl2 - 3 мМ, Taq -полимераза - 5 ед.
Кроме того, ПЦР реакция проходит с соблюдением следующих температурных режимов:
нагрев: 95°С - 15 мин;
5 циклов: денатурация - 95°С - 5 с, отжиг - 60°С - 20 с, элонгация - 72°С - 15 с;
40 циклов: денатурация - 95°С - 5 с, отжиг - 60°С - 10 с, детекция флуоресценции - 60°С - 15 с, элонгация - 72°С - 15 с;
хранение - 4°С.
Способ осуществляется следующим образом.
Для проведения способа были сконструированы новые специфические для ДНК возбудителя чумы олигонуклеотидные последовательности (праймеры) и зонд с флуоресцентной меткой (см. Таблица 1).
Из материала, содержащего микробные клетки возбудителя чумы, выделяют ДНК, которую добавляют в смесь для амплификации. ДНК из клеток возбудителя чумы выделяют стандартным методом, описанным в МУ 1.3.1794-03 «Организация работы при исследованиях методом ПЦР материала, инфицированного микроорганизмами I-II группы патогенности», - М., 2003.
В состав смеси входят следующие комплекты реагентов: помимо специфических праймеров (по 15 пМ каждого) и флуоресцентно-меченого зонда (15 пМ), 3 мМ каждого dNTP; 84 мМ TRIS-HCl (рН 8,6); 21 мМ (NH4)2SO4; 3 мМ MgCl2, а также 5 единиц Taq-полимеразы.
Затем проводят амплификацию ДНК с помощью детектирующего амплификатора в закрытых амплификационных пробирках. Режим амплификации представлен в таблице 2.
Детекция результатов проходит во время проведения ПЦР с помощью флуоресцентного ПЦР-детектора. Анализ результатов проводится в табличной и графической формах с помощью программного обеспечения, поставляемого совместно с амплификатором. Так как зонд мечен флуорохромом Fam, то его флуоресцентное свечение фиксируется при длине волны 520 нм.
Для определения количества микробных клеток в пробе перед проведением ПЦР готовят калибровочную панель путем выделения ДНК из взвеси вакцинного штамма возбудителя чумы концентрацией 1×109 микробных клеток в 1 миллилитре (мк.кл./мл), и последовательного десятикратного разведения ДНК. Эта калибровочная панель используется при анализе проб.
Количественный анализ проводят с применением в анализе, совместно с опытной пробой, референтных проб, с различной концентрацией ДНК возбудителя чумы, эквивалентной определенным концентрациям микробных клеток.
Таким образом, сущность предлагаемого изобретения заключается в использовании новых специфических праймеров и флуоресцентно-меченого зонда для обнаружения хромосомных последовательностей ДНК в ПЦР с учетом результата в реальном времени. В ходе ПЦР флуоресцентно-меченый зонд, меченный молекулами флуорофора и гасителя флуоресценции, гибридизуется на специфических ампликонах и разрушается Taq-полимеразой, в результате чего флуорофор оказывается свободным от гасителя. Уровень флуоресценции в амплификационных пробирках возрастает пропорционально количеству образовавшихся специфических продуктов ПЦР.
Предлагаемые праймеры и зонд позволяют эффективно проводить идентификацию штаммов возбудителя чумы ввиду того, что они испытаны на значительном числе как типичных, так и атипичных штаммов, выделенных в различных очагах и полученных в лабораторных условиях. В Ростовском-на-Дону противочумном институте с помощью этого способа успешно протестировано более 250 исследований штаммов возбудителя чумы и других микроорганизмов в качестве отрицательного контроля. Этот факт позволяет оценивать вероятность уклонения от детекции штаммов возбудителя чумы, у которых отсутствуют маркеры, обычно используемые для выявления клеток Y.pestis, стандартными лабораторными методами, как низкую при применении предложенных праймеров и зонда.
Примеры конкретного выполнения.
Пример 1. Идентификация штаммов возбудителя чумы.
Были проанализированы три пробы, содержащие 1 млн. м.кл. в мл: 1) взвеси микробных клеток возбудителя псевдотуберкулеза (Y.pseudotuberculosis), возбудителя, по своему генотипу, являющемуся очень близким к возбудителю чумы; 2) взвеси микробных клеток типичного штамма возбудителя чумы (Y.pestis EV1290НИИЭГ); 3) взвеси микробных клеток атипичного штамма возбудителя чумы, у которого отсутствовала плазмидная ДНК (Y.pestis 2357).
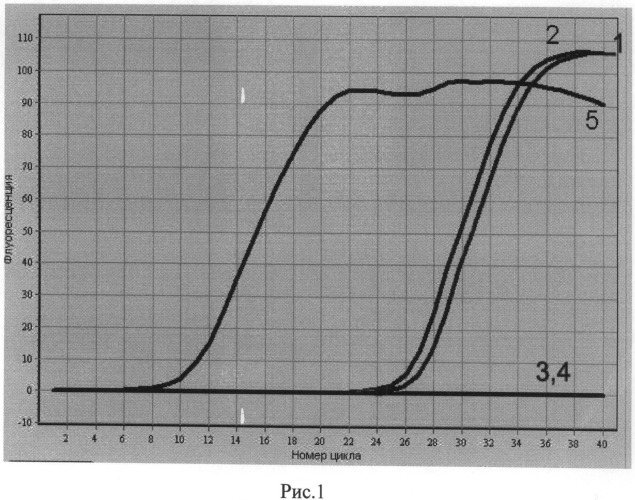
ДНК выделяют в соответствии с МУ 1.3.1794-03. Для проведения ПНР тестирования предложенных проб составляют взвеси, содержащие следующие комплекты реагентов: помимо специфических праймеров (по 15 пМ каждого) и флуоресцентно-меченого зонда (15 пМ), 3 мМ каждого dNTP; 84 мМ TRIS-HCl (рН 8,6); 21 мМ (NH4)2SO4; 3 мМ MgCl2 а также 5 единиц Taq-полимеразы. Смесь распределяют по отдельным пробиркам, предназначенным для проведения ПЦР. Выделенная ДНК из трех исследуемых образцов в отдельную пробирку добавлялась в количестве 5 мкл. Общий объем реакционной смеси составил 35 мкл. В качестве отрицательного контроля в реакционную смесь добавляют 5 мкл дистиллированной воды. Положительным контролем служит взвесь реагентов, к которую добавляли ДНК из 1 млрд м.кл. в мл штамма Y.pestis EV1290НИИЭГ. Амплификацию и детекцию проводят в детектирующем амплификаторе ДТ-322 (ДНК-технология, Россия). Режим амплификации соответствует режиму, представленному в таблице 1. Детекцию осуществляют датчиком прибора с учетом того, что флуоресценция флуорофора зонда (Fam) фиксируется при длине волны, близкой 520 нм. Анализ результатов проводят с помощью программного обеспечения ДТ-322 v5.3, поставляемого совместно с амплификатором. Результаты тестирования проб представлены на графике (см. рис.1).
На рис.1 изображен график кривых флуоресценции, отражающих динамику накопления фрагментов специфической ДНК во время амплификации в пробах: 1) ДНК взвеси микробных клеток вакцинного штамма Y.pestis EV 1290НИИЭГ; 2) ДНК взвеси микробных клеток атипичного штамма Y.pestis 2357, у которого отсутствуют плазмиды; 3) ДНК взвеси микробных клеток возбудителя псевдотуберкулеза Y.pseudotuberculosis; 4) Отрицательный контроль: дистиллированная вода; 5) Положительный контроль: ДНК взвеси микробных клеток возбудителя чумы в количестве, эквивалентном концентрации 109 мк.кл./мл.
Полученные результаты свидетельствуют о том, что в пробах 1, 2 и 5, в которых присутствует ДНК возбудителя чумы, отмечено нарастание флуоресцентного свечения по мере накопления продукта амплификации, в то время, как в пробах 3 и 4, в которых были внесены ДНК псевдотуберкулеза и дистиллированная вода (отрицательный контроль), подобного сигнала не наблюдалось. Таким образом, можно констатировать, что праймеры и зонд, используемый в примере, показали возможность идентифицировать штаммы возбудителя чумы и не участвовали в амплификации и детекции ДНК штамма возбудителя псевдотуберкулеза, близкородственного чуме микроорганизма. Кроме того, в ПЦР с учетом результатов в реальном времени были идентифицированы как типичный штамм Y.pestis, с наличием плазмид, так и атипичный, в котором отсутствовали три плазмиды возбудителя чумы.
Пример 2. Определение концентрации микробных клеток возбудителя чумы в исследуемой пробе.
Исследовали взвесь культуры возбудителя чумы неопределенной концентрации. Для этого выделяют ДНК из пробы и из взвеси культуры вакцинного штамма, концентрацией 1×109 мк.кл./мл, для использования при калибровке. Готовят десятикратные разведения ДНК и получают калибровочную панель с концентрациями ДНК, эквивалентными концентрациям мк.кл./мл Y.pestis 109, 108, 107, 106, 105, 104, 103. Все пробы (по 5 мкл) внесят в отдельные пробирки с реакционной смесью. В состав смеси входят следующие комплекты реагентов: помимо специфических праймеров (по 15 пМ каждого) и флуоресцентно-меченого зонда (15 пМ), 3 мМ каждого dNTP; 84 мМ TRIS-HCl (рН 8,6); 21 мМ (NH4)2SO4; 3 мМ MgCl2, а также 5 единиц Taq-полимеразы.
Режим амплификации соответствует режиму, представленному в таблице 1. Детекцию осуществляют датчиком прибора с учетом того, что флуоресценция флуорофора зонда (Fam) фиксируется при длине волны, близкой 520 нм.
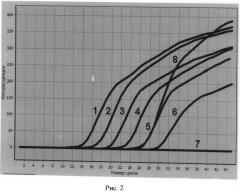
Анализ результатов проводят с помощью программного обеспечения ДТ-322 v5.3, поставляемого совместно с амплификатором. Результаты тестирования проб представлены на графике (см. рис.2).
На рисунке 2 изображен график динамики накопления фрагментов специфической ДНК во время амплификации в пробах: 1) ДНК возбудителя чумы в концентрации, эквивалентной 109 мк.кл./мл; 2) ДНК возбудителя чумы в концентрации, эквивалентной 108 мк.кл./мл; 3) ДНК возбудителя чумы в концентрации, эквивалентной 107 мк.кл./мл; 4) ДНК ДНК возбудителя чумы в концентрации, эквивалентной 106 мк.кл./мл; 5) ДНК возбудителя чумы в концентрации, эквивалентной 105 мк.кл./мл; 6) ДНК возбудителя чумы в концентрации, эквивалентной 103 мк.кл./мл; 7) Отрицательный контроль: дистиллитрованная вода; 8) Проба с неизвестной концентрацией ДНК Yersinia pestis.
Результаты исследования показали, что концентрация ДНК возбудителя чумы в исследуемой пробе (8 на графике рис.2) эквивалентна концентрации 105 мк.кл./мл, так как кривая графика флуоресценции исследуемой пробы совпадает с графиком флуоресценции калибровочной пробы (5 на графике рис.2) данной концентрации.
Следовательно, в предложенном способе ПЦР-амплификацию проводят с использованием нового набора олигонуклеотидов, включающего специфические праймеры и флуоресцентно-меченый зонд, позволяющие эффективно идентифицировать как типичные, так и атипичные штаммы возбудителя чумы.
Эффективность идентификации доказана на большом числе штаммов. Детекция результатов ПЦР проводится в закрытых амплификационных пробирках с помощью флуоресцентного ПЦР-детектора, что полностью исключает возможность загрязнения реактивов и оборудования продуктами ПЦР и предотвращает получение ложных результатов анализа. Детекция проводится во время самого анализа и результат анализа получают значительно раньше, что позволяет сократить сроки тестирования в режиме реального времени и принимать более оперативные решения по определению эпидемической значимости микроорганизмов и их количества, обнаруженных в исследуемой пробе.
| Таблица 1 | |||
| N | Праймеры (1, 2) и зонд (3) | Нуклеотидная последовательность праймеров и зонда | Длина фрагмента амплификации (п.н.) |
| 1 | AL12for | 5'-TCCTGAATCAGGAGAGCAGATTACC-3' | 224 |
| 2 | AL12rev | 5'-TGAAGCCGCTCACACGATGT-3' | |
| 3 | Fam-AL12 | Fam-TTTGAAGGCGATAATGACGGCGGGA-HBQ1 |
| Таблица 2 | ||||
| Название операции | Температура | Время | Количество циклов | Примечание |
| первоначальный нагрев | 95°С | 15 мин | 1 | |
| денатурация | 95°С | 5 с | 5 | |
| отжиг | 60°С | 20 с | ||
| элонгация | 72°С | 15 с | ||
| денатурация | 95°С | 5 с | 40 | |
| отжиг | 60°С | 10 с | ||
| отжиг | 60°С | 15 с | Детекция | |
| элонгация | 72°С | 15 с | ||
| хранение | 4°С |
1. Способ идентификации возбудителя чумы и оценки количества микробных клеток, идентифицированных в качестве возбудителя чумы в исследуемых пробах посредством ПЦР с учетом результатов в режиме реального времени, включающий следующие стадии:a) выделяют ДНК микроорганизма из исследуемых проб;b) подготавливают калибровочную панель с концентрациями ДНК, эквивалентными концентрациям мк.кл./мл вакцинного штамма (Y.Pestis) 109, 108, 107, 106, 105, 104, 103;c) исследуют выделенную ДНК в ПЦР с использованием специфических праймеров и зонда с флуоресцентной меткой:AL12for-5′-TCCTGAATCAGGAGAGCAGATTACC-3′AL12rev-5′-TGAAGCCGCTCACACGATGT-3′и флуоресцентно-меченого зонда:Fam-AL12-Fam-TTTGAAGGCGATAATGACGGCGGGA-HBQ1;d) идентифицируют исследуемую ДНК как ДНК микробного или немикробного штамма по наличию нарастания флуоресцентного свечения или его отсутствию соответственно при длине волны 520 нм;e) определяют по полученной на стадии (2) калибровочной панели концентрации ДНК в пробе, по которой оценивают количество клеток в исследуемой пробе.
2. Способ по п.1, отличающийся тем, что смесь для амплификации состоит из следующих реагентов: специфические праймеры (каждый) - 15 пм, зонд с флуоресцентной меткой - 15 пм, dNTP - 3 мМ, TRIS-HCl (при pH 8,6) - 84 мМ, (NH4)2SO4 - 21 мМ, MgCl2 - 3 мМ, Taq-полимераза - 5 ед.
3. Способ по п.1, отличающийся тем, что ПЦР реакция проходит с соблюдением следующих температурных режимов:нагрев: 95°C - 15 мин;5 циклов: денатурация - 95°C - 5 с, отжиг - 60°C - 20 с, элонгация - 72°C - 15 с;40 циклов: денатурация - 95°C - 5 с, отжиг - 60°C - 10 с, детекция флуоресценции - 60°C - 15 с, элонгация - 72°C - 15 с;хранение - 4°C.