Терапевтическая система для выделения энергии
Иллюстрации
Показать всеИзобретение относится к терапевтическим средствам для выделения энергии в целевую точку. Терапевтическая система содержит терапевтический модуль, выполненный с возможностью последовательных выделений энергии в целевую зону, причем последовательные выделения разделены периодом охлаждения, термометрический модуль, выполненный с возможностью измерения максимальной температуры в поле измерений, расположенном вне фокуса выделяемой энергии, и модуль управления, выполненный с возможностью регулировки периода охлаждения в зависимости от измеренной максимальной температуры вне фокуса во время периода выделения энергии перед периодом охлаждения. Машиночитаемый носитель системы имеет сохраненную на нем компьютерную программу, содержащую инструкции, которые при выполнении предписывают терапевтической системе выполнять последовательные выделения энергии, измерения максимальной температуры и регулировку периода охлаждения на основе измеренной максимальной температуры вне фокуса во время периода выделения энергии перед периодом охлаждения. Использование изобретения позволяет повысить точность выделения энергии в целевую зону для более точной установки периода охлаждения. 2 н. и 1 з.п. ф-лы, 2 ил.
Реферат
Уровень техники
Настоящее изобретение относится к терапевтической системе для выделения энергии в целевую зону.
Такая терапевтическая система известна из публикации "Determination of the optimal delay between sonications during focused ultrasound surgery in rabbits by using MR imaging to monitor thermal build-up in vivo" (Определение оптимальной задержки между воздействиями ультразвуком во время сфокусированной ультразвуковой хирургической операции на кроликах путем использования МР-визуализации для мониторинга аккумулирования теплоты в живом организме), N.J.McDannold и др., Radiology 211(1999)419-426.
В этом документе описан эксперимент по воздействию ультразвуком на живой организм, в котором исследуется система контроля абляции ткани. Эта известная система контролирует процесс абляции, при котором контролируется тепловое повреждение ткани. Эта известная система контроля абляции выполняет мониторинг, например, на основе магниторезонансных изображений. Кроме того, в упомянутом документе указано, что энергия может подаваться посредством воздействия ультразвуком в виде сфокусированных ультразвуковых волн. Далее упомянуто, что осуществляется воздействие ультразвуком с малым промежутком, который представляет собой задержку между воздействиями ультразвуком для минимизации аккумулирования тепла. То есть последовательные выделения энергии разделены по времени периодами охлаждения. Чтобы минимизировать эту задержку между воздействиями ультразвуком во время лечения, следует измерять повышение температуры. Эта информация о температуре затем используется для управления задержкой между воздействиями ультразвуком.
Период охлаждения между последовательными выделениями энергии позволяет снизить температуру в области вокруг фокальной области, в которую непосредственно выделяется энергия. Таким образом, повышение температуры в области вокруг фокальной области, т.е. так называемое повышение температуры вне фокуса, снижается. Таким образом, снижен риск теплового повреждения здоровой ткани вне фокальной области.
Предлагается терапевтическая система с термометрическим модулем для измерения температуры в поле измерений. В основном, поле измерений содержит фокальную область, в которую напрямую выделяется энергия. Продолжительность периода охлаждения между последовательными выделениями энергии управляется на основе измеренной температуры. Таким образом, удается избежать того, что время, требуемое для последовательных выделений энергии, будет превышать необходимое время, в то же время избегая повышение температуры вне фокуса.
Сущность изобретения
В соответствии с целью настоящего изобретения предлагается терапевтическая система, позволяющая более точно применять энергию в целевой зоне, в частности, для более точной установки периода охлаждения.
Эта цель достигается посредством терапевтической системы согласно настоящему изобретению, содержащей терапевтический модуль для выполнения последовательного выделения энергии в целевой зоне, причем последовательное выделение разделено периодом охлаждения, терапевтическая система снабжена
- термометрическим модулем для измерения температуры в поле измерений и
- модулем управления для регулировки периода охлаждения в зависимости от измеренной максимальной температуры вне фокуса во время выделения энергии перед периодом охлаждения.
Согласно настоящему изобретению период охлаждения устанавливают на основе максимальной температуры вне фокальной области при предшествующем выделении энергии. Это подразумевает относительно простое измерение максимальной температуры. Поскольку продолжительность периода охлаждения более точно устанавливается для инициации следующего выделения энергии, как только температура достаточно снижается, чтобы риск повышения температуры вне фокуса был низким.
В частности, когда используется МР-термометрия, достигается относительное измерение температуры именно целевой зоны, а также области вне фокуса. То есть температуру получают точно относительно значения базовой линии в начале конкретного выделения энергии. Поскольку период охлаждения между последовательными выделениями энергии точно установлен уже по первому выделению энергии, надежные равные температуры базовой линии применяют для последующих выделений энергии.
Один из результатов интерпретации настоящего изобретения состоит в том, что повышение температуры ткани вне фокальной области зависит от плотности выделенной энергии. Именно это случай выделения энергии в виде сфокусированного ультразвукового пучка. Плотность выделенной энергии можно точно рассчитать заранее и использовать для оценки максимальной температуры в области вне фокуса. Максимальная температура в области вне фокуса приблизительно линейно зависит от плотности выделенной энергии, т.е. плотности ультразвуковой энергии, выделенной в области вне фокуса. Фокальный внефокус образован сечением, поперечным по отношению к траектории пучка. Линейная зависимость, по-видимому, справедлива, когда снижением температуры из-за диффузии тепла можно пренебречь в середине ультразвукового конуса вне фокуса во время нагрева.
Согласно другому аспекту настоящего изобретения относительно простая аппроксимация продолжительности периода охлаждения пропорциональна квадрату максимальной температуры области вне фокуса, достигаемой при предшествующем выделении энергии. Эта зависимость периода охлаждения от максимальной температуры сохраняется для случая, когда сечение траектории пучка при выделении энергии является круглым (например, как если бы траектория пучка имела форму конуса). В других случаях квадратичная зависимость будет несколько нарушена, но точное соотношение можно пересчитать для любого сечения траектории пучка.
Эти и другие аспекты настоящего изобретения пояснены дополнительно со ссылкой на варианты осуществления, определенные в зависимых пунктах формулы изобретения.
В одном конкретном варианте осуществления настоящего изобретения терапевтический модуль представляет собой сфокусированный ультразвуковой излучатель с высокой интенсивностью. В этом варианте осуществления выделение энергии осуществляется путем воздействия на целевую зону сфокусированного ультразвукового пучка с высокой интенсивностью (HIFU), часто называемого "ультразвуковым воздействием". HIFU-пучок вызывает локальный нагрев ткани главным образом в фокальной области, что вызывает тепловую абляцию фокальной области. Также происходит незначительный нагрев других областей в пределах HIFU пучка.
В другом варианте осуществления настоящего изобретения терапевтический модуль представляет собой микроволновой излучатель. В этом варианте осуществления выделение энергии осуществляется путем воздействия на целевую зону микроволнового излучения. Микроволновое излучение вызывает локальный нагрев ткани, который вызывает термическую абляцию в фокальной области, хотя также происходит незначительный нагрев тканей в областях вне фокуса.
В другом варианте осуществления настоящего изобретения терапевтический модуль представляет собой РЧ-антенну. В этом варианте осуществления энергия выделяется посредством теплопроводности от антенны, расположенной в контакте с целевой зоной. РЧ-нагрев вызывает локальное повышение температуры, которое вызывает термическую абляцию вокруг антенны, и, путем изменения зависимости выделения энергии от подъема максимальной температуры, могут быть применены все описанные выше аспекты.
В другом варианте осуществления настоящего изобретения модуль контроля может быть основан на МР-визуализации, ультразвуковых или КТ-изображениях для контроля терапии. Также могут быть использованы любые другие чувствительные к температуре модальности визуализации.
Настоящее изобретение дополнительно относится к компьютерной программе, как указано в п.3 формулы изобретения. Компьютерная программа согласно настоящему изобретению может быть предусмотрена на носителе данных, таком как CD-диск или карта памяти USB, или компьютерная программа согласно настоящему изобретению может быть загружена из сети данных, такой как всемирная сеть. Когда она установлена на компьютере, входящем в терапевтическую систему, терапевтическая система способна функционировать в соответствии с настоящим изобретением и достигать высокой безопасности использования и более точной установки периода охлаждения.
Эти и другие аспекты настоящего изобретения пояснены со ссылкой на варианты осуществления, описанные далее со ссылкой на сопроводительные чертежи.
Краткое описание чертежей
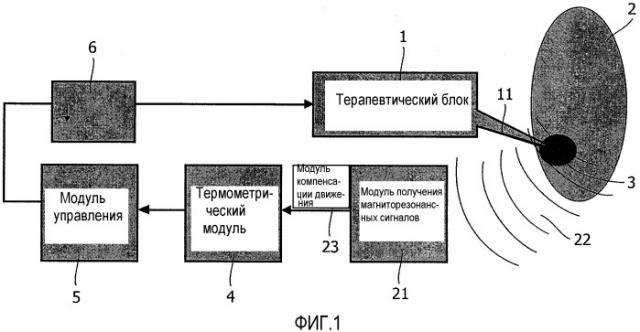
На фиг.1 схематично показана терапевтическая система, в которой осуществлено настоящее изобретение.
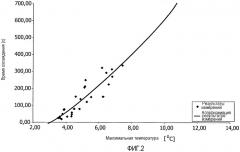
На фиг.2 показан пример времени охлаждения.
Подробное описание вариантов осуществления
На фиг.1 схематично показана терапевтическая система, в которой осуществлено настоящее изобретение. Терапевтический блок 1, например, в виде сфокусированного ультразвукового блока высокой интенсивности (HIFU), генерирует терапевтическое действие в виде сфокусированного ультразвукового пучка 11. Сфокусированный ультразвуковой пучок 11 точно направлен на целевую зону 2, которая содержит фактическую цель 3. Например, целью является опухоль в (части) органе 2 пациента, подлежащего воздействию терапии. Блок 1 HIFU функционирует таким образом, чтобы сфокусированный ультразвуковой пучок 11 перемещался по объему целевой зоны 2. Ультразвуковой пучок 11 выделяет энергию в целевую зону, вызывая повышение температуры, особенно в опухоли. Таким образом, температура нужных частей ткани поднимается до уровня, когда происходит некроз ткани. В конечном итоге происходит некроз ткани опухоли и вокруг нее в целевой зоне, когда достигнута нужная доза теплоты или температура. В частности, доза теплоты может быть рассчитана простой аппроксимацией, как
T D = ∫ 0 t r 43 − T ( τ ) d τ ,
где r=0,25, когда T<43°C, и r=0,5, когда T>=43°C. Обычно считается, что предел дозы 240 эквивалентных минут при 43°C приводит к некрозу. Существует модифицированная версия этого уравнения, которая позволяет учесть неопределенность. В этом смысле один или несколько пределов (или потенциально нижний предел) могут быть проверены, чтобы гарантировать, что когда он будет достигнут, выделение энергии прекратится. Наблюдение только температуры говорит нам, что некроз, наиболее вероятно, имеет место, поскольку доза теплоты обеспечивает это.
Например, некроз достигается, когда интенсивность в фокусе сфокусированного ультразвукового пучка составляет примерно 1600 Вт·см-2 для продолжительности порядка нескольких десятков секунд. На этом максимальном уровне энергии эффективный некроз достигается без риска кавитации. Ультразвуковой пучок также может быть использован для повышения температуры ткани до уровней температур, не соответствующих образованию некроза. Эти более низкие температуры применяются для гипертермии.
Температурное распределение в поле измерений получают по магниторезонансным сигналам. Для этого пациента помещают в систему для исследования, использующую магнитный резонанс (не показана), и генерируют магниторезонансные сигналы 22. Магниторезонансные сигналы получает система 21 получения МР-сигналов, то есть часть системы исследования с помощью магнитного резонанса. Система получения магниторезонансных сигналов содержит радиочастотные приемные антенны (катушки) и систему обработки сигналов, такую как спектрометр. Полученные магниторезонансные сигналы подаются на термометрический модуль 4, который получает распределение температур в целевой зоне. Фаза магниторезонансных сигналов, а также другие параметры зависят от температуры. Магниторезонансные сигналы пространственно закодированы посредством кодирующих магнитных градиентных полей, таких как градиенты фазового кодирования и считывания. Пространственное разрешение магниторезонансных сигналов и последующее распределение температур представлено в масштабе одного миллиметра; можно достичь даже субмиллиметровое разрешение, когда самая мелкая деталь, которую можно различить, имеет размер несколько десятых долей миллиметра.
Например, если имеется несколько срезов при пакетном контроле температуры, то используемое поле измерений предпочтительно может быть спроектировано на все параллельные срезы в фокальной области, даже хотя траектория точки фокуса находится только в среднем срезе пакета. Поскольку самая широкая и самая горячая плоскость обычно эллипсоидальной нагретой области может перемещаться по направлению к преобразователю во время нагревания, это снижает риск того, что радиус подвергаемой воздействию терапии области будет больше, чем требуемый, измеренный от оси пучка. Поле измерений вдоль оси пучка может быть применено только для контроля того, чтобы продолжительность дозы 240 эквивалентных минут не превысила максимальную продолжительность, если имеется сагиттальная плоскость (что и есть на самом деле). Это значительно повышает безопасность.
Срезы вне фокуса (например, два из них) также могут быть добавлены в областях интереса, например, границы контакта с тканью, где акустическое сопротивление меняется значительно, поскольку такие области предрасположены к нагреву вне фокуса. Они могут быть использованы для автоматической регистрации чрезмерного нагрева и/или тепловой дозы в этих областях интереса вне фокуса для любого одиночного выделения энергии и чрезмерного кумулятивного нагрева и/или тепловой дозы в течение всей терапевтической процедуры.
Точные результаты в движущейся ткани получают, когда применяется корректировка движения, и вклад фазы из-за движения отделен от вкладов фаз из-за изменения температуры. Корректировка движения может быть получена по магниторезонансным сигналам, в значительно мере по избыточным магниторезонансным сигналам, от центрального участка k-пространства. Модуль 23 компенсации движения предусмотрен для получения корректировки движения и применения коррекции движения к магниторезонансным сигналам. Магниторезонансные сигналы с корректировкой движения применяют на термометрическом модуле 4, позволяющем получить локальное распределение температур в целевой зоне 3. В альтернативном варианте модуль 23 компенсации движения может быть конфигурирован или запрограммирован в программном обеспечении для получения отдельного вклада в фазу магниторезонансных сигналов за счет движения и расчета вклада в фазу за счет изменений температуры. Локальное распределение температуры передается на модуль 5 управления, который управляет терапевтическим модулем, т.е. блоком 1 HIFU для фокусировки сфокусированного ультразвукового пучка вдоль следующей траектории. Центр концентричности, например, может оцениваться непрерывно (например, посредством гауссовской аппроксимации или взвешенного среднего), чтобы учитывать возможность некоторого сдвига подвергаемой воздействию терапии области (заметно нагретой) (обычно l-2 вокселя или 0,5-5 мм) во время терапевтической процедуры, например, из-за спазмов или несколько неравномерной тепловой диффузии.
Терапевтическая система согласно настоящему изобретению снабжена модулем 6 задержки, который задерживает приведение в действие терапевтического модуля 1. Задержка приводит к периоду охлаждения. Задержку устанавливает блок управления на основе измеренной температуры. Блок задержки может быть выполнен с возможностью запуска терапевтического модуля. В другом варианте осуществления терапевтический модуль выполнен с возможностью применения регулярных выделений энергии, например применения регулярных ультразвуковых импульсов (т.е. воздействий ультразвуком). В этом варианте осуществления модуль задержки выполнен с возможностью прерывания работы терапевтического модуля. На практике большое число воздействий ультразвуком прерывают или отменяют, чтобы вызвать период охлаждения.
На фиг.2 показан пример времени охлаждения для достижения допуска в пределах 3°C от начальной температуры в зависимости от максимальной температуры около поля. Аппроксимацией является квадратная, т.е. квадратичная функция максимальной температуры, аппроксимированная до 3°C, и значение R составляет 0,90. В этих случаях температура фильтруется медианным фильтром 5×5 вокселов (размер воксела 2,5×2,5 мм2). В значительной мере пространственная фильтрация измеренной температуры, например, посредством медианного фильтра улучшает отношение сигнал-шум результатов измерения температуры. Потеря пространственного разрешения не приводит к проблемам, поскольку нагрев вне фокуса обычно не дает резких пространственных градиентов. Эти данные получены для HIFU-терапевтического модуля с круглым сечением траектории пучка. Аппроксимация до 3°C может быть изменена заранее на любой нужный определенный уровень температур базовой линии.
1. Терапевтическая система, содержащаятерапевтический модуль, выполненный с возможностью последовательных выделений энергии в целевую зону, причем последовательные выделения разделены периодом охлаждения,термометрический модуль, выполненный с возможностью измерения максимальной температуры в поле измерений, расположенном вне фокуса выделяемой энергии, имодуль управления, выполненный с возможностью регулировки периода охлаждения в зависимости от измеренной максимальной температуры вне фокуса во время периода выделения энергии перед периодом охлаждения.
2. Терапевтическая система по п.1, в которой терапевтическим модулем является ультразвуковой излучатель высокой интенсивности или микроволновой излучатель.
3. Машиночитаемый носитель, имеющий сохраненную на нем компьютерную программу, содержащую инструкции, которые при выполнении предписывают терапевтической системе выполнятьпоследовательные выделения энергии в целевой зоне, причем последовательные выделения разделены периодом охлаждения, разделяющим последовательные выделения,измерения максимальной температуры в поле измерений, расположенном вне фокуса выделяемой энергии, ирегулировки периода охлаждения на основе измеренной максимальной температуры вне фокуса во время периода выделения энергии перед периодом охлаждения.