Способ диагностики нарушения сократимости муфт легочных вен после процедуры радиочастотной аблации
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к сердечнососудистой хирургии. Выполняют измерение диаметра муфт легочных вен при помощи внутрисердечной эхокардиографии и одновременную регистрацию электрокардиограммы. При этом измерение диаметра выполняют во временные интервалы, соответствующие началу и пику ретроградного кровотока, зафиксированные на ЭКГ-кривой. Нарушение сократимости муфт легочных вен диагностируют при увеличении их диаметра на пике ретроградного кровотока относительно диаметра, измеренного в его начале. Способ позволяет повысить точность диагностики нарушения сократительной функции муфт легочных вен после процедуры радиочастотной изоляции коллекторов легочных вен, за счет сопоставления результатов эхокардиографии и электрокардиограммы. 1пр., 3 ил.
Реферат
Изобретение относится к области медицины, а именно к сердечно-сосудистой хирургии, и может быть использовано в интервенционной аритмологии при лечении фибрилляции предсердий.
Мышечные муфты легочных вен играют важную роль в процессах внутрисердечной гемодинамики. Обладая сократительной способностью, они выполняют запирательную функцию при систоле предсердий, предотвращая регургитацию крови в легочные вены. Кроме того, муфты легочных вен являются основным аритмогенным субстратом, участвующим в механизмах инициации и поддержания фибрилляции предсердий. При этом в клинической электрофизиологии наиболее актуальным решением в лечении фиблилляций предсердий являются операции антральной радиочастотной изоляции легочных вен или операции «Лабиринт». Поэтому диагностика сократимости муфт легочных вен представляет собой важный этап в оценке эффективности проведенной процедуры и сохранения адекватной внутрисердечной гемодинамики.
Известен способ диагностики нарушения сократимости муфт легочных вен по результатам чреспищеводной эхокардиографии (Pinheiro L, Nanda N.C., Jain H., Sanyal R. Transesophageal echocardiographic imaging of the pulmonary veins // Echocardiography. - 1991. - Vol.8(6). - P.741-748). Способ основан на регистрации спектра кровотока в левой верхней легочной вене и его изменениях, на основании которых делают заключение о сократительной функции муфт легочных вен. Однако при помощи чреспищеводной эхокардиографии можно изучить кровоток лишь в одной из четырех легочных вен, что является недостатком аналога.
Известен способ оценки сократительной функции муфт легочных вен с использованием внутрисердечной эхокардиографии (Szili-Torok Т., McFadden E.P., Jordaens L.J., Roelandt J.R.T.C. Visualization of elusive structures using intracardiac echocardiography: Insights from electrophysiology // Cardiovascular Ultrasound. - 2004. - Vol.2. - P.6.), при помощи которого можно измерить диаметр всех легочных вен на уровне их муфт и оценить его изменения в процессе сердечного цикла. Нарушение сократимости муфт легочных вен диагностируют только в том случае, если регистрируют существенное снижение амплитуды колебаний диаметра их просвета. В случае, если диаметр просвета легочных вен в процессе сердечного цикла существенно изменяется, считают, что муфты легочных вен сокращаются нормально. Данный способ принят в качестве прототипа. Недостатком способа является невозможность дифференцировать изменения диаметров легочных вен вследствие их пассивного растяжения кровью от их активного сокращения. Поэтому данный способ является не прямым, а косвенным, а заключения о наличии нарушения сократительной функции муфт легочных вен, сделанные на основании его результатов, могут быть ложноположительными.
Техническим результатом изобретения является повышение точности диагностики нарушения сократительной функции муфт легочных вен после радиочастотной изоляции коллекторов легочных вен, за счет измерения диаметра легочных вен при помощи внутрисердечной эхокардиографии, регистрации ретроградного кровотока в них и сопоставления полученных данных с результатами электрокардиограммы.
Предложенный способ основан на результатах исследования, проведенного в отделении рентгенхирургических методов диагностики и лечения ФГБУ «НИИ КПССЗ» СО РАМН, показавшего, что в норме муфты легочных вен сокращаются в момент активной систолы левого предсердия, препятствуя обратному току крови в легочные сосуды. Однако если сократимость муфт легочных вен нарушена, то в момент активной систолы происходит их пассивное растяжение за счет переполнения ретроградным потоком крови. Данные изменения регистрировали при помощи внутрисердечной эхокардиографии и оценивали не только диаметр легочных вен, но и кривую допплеровского спектра кровотока на уровне устья легочной вены. Одновременно с выполнением внутрисердечной эхокардиографии (ЭХО-КГ) регистрировали электрокардиограмму (ЭКГ) и проводили анализ предсердного комплекса возбуждения миокарда в фазу активной систолы левого предсердия.
Полученные данные ЭХО-КГ и ЭКГ сопоставляли по времени. При этом на ЭКГ-кривой отмечали события, соответствующие началу ретроградного кровотока и его пику. Для этого измеряли временные интервалы от момента начала комплекса QRS и соответствующими событиями на кривой допплеровского спектра кровотока.
После того как временные интервалы измерены и зафиксированы на ЭКГ-кривой их сопоставляли с данными изображения устья легочной вены в двухмерном режиме, полученными при помощи внутрисердечной эхокардиографии. Измерение диаметра легочных вен сначала выполняли в момент начала ретроградного кровотока, а затем повторно на его пике. В том случае, если диаметр легочных вен на уровне их устья на пике ретроградного кровотока увеличивался в сравнении с их диаметром в начале ретроградного кровотока, то диагностировали нарушение сократительной способности муфт легочных вен. Предложенный способ использован более чем у 40 пациентов клиники, в результате чего получены данные о его высокой эффективности и безопасности.
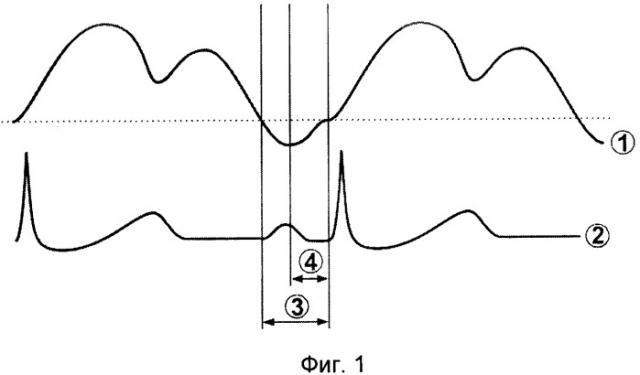
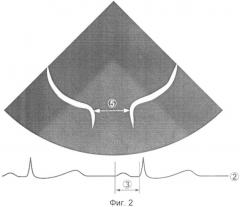
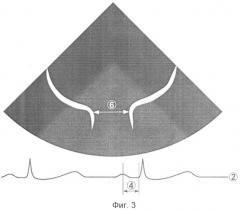
Изобретение поясняется чертежами, где на фиг.1 показан момент одновременной регистрации электрокардиограммы и кровотока на уровне устья легочной вены; на фиг.2 - двухмерное изображение легочной вены, зарегистрированное в начале ретроградного кровотока в легочной вене; на фиг.3 - двухмерное изображение легочной вены на пике ретроградного кровотока.
На фиг.1 показаны: 1 - допплеровский спектр кровотока на уровне устья легочной вены; 2 - электрокардиограмма; 3 - временной интервал между началом комплекса QRS и началом ретроградного кровотока в легочной вене; 4 - временной интервал между пиком ретроградного кровотока в легочной вене и началом комплекса QRS электрокардиограммы.
На фиг.2 показаны: 2 - электрокардиограмма; 3 - временной интервал между началом комплекса QRS и началом ретроградного кровотока в легочной вене; 5 - диаметр легочной вены, измеренный в начале ретроградного кровотока в легочной вене.
На фиг.3 показаны: 2 - электрокардиограмма; 4 - временной интервал между началом комплекса QRS и пиком ретроградного кровотока в легочной вене; 6 - диаметр легочной вены, измеренный на пике ретроградного кровотока в легочной вене.
Способ осуществляется следующим образом. Через правую бедренную вену в правое предсердие вводят внутрисердечный ультразвуковой катетер, например AcuNav (Siemens, Германия), и позиционируют таким образом, чтобы визуализировать устье любой из легочных вен. Затем контрольный объем импульсноволнового допплера устанавливают на уровне устья легочной вены и одновременно регистрируют электрокардиограмму 2 и спектр кровотока 1. При этом измеряют интервал 3 между началом комплекса QRS и началом ретроградного кровотока в легочной вене и интервал 4 между началом комплекса QRS и пиком ретроградного кровотока в легочной вене. После этого регистрируют кинопетлю изображения устья легочной вены в двухмерном режиме и измеряют диаметр легочной вены перед началом ретроградного кровотока 5 в легочной вене и на его пике 6, останавливая кинопетлю в моменты, соответствующие измеренным ранее временным интервалам на электрокардиограмме. При совпадении пика ретроградного кровотока в легочных венах с уменьшением диаметра легочных вен на уровне их устья диагностируют нормальную сократимость их муфт, а при совпадении ретроградного кровотока в легочных венах с увеличением их диаметра - нарушенную сократимость их муфт.
Пример. Пациент З., 58 лет, находился в отделении рентгенохирургических методов диагностики и лечения с диагнозом: пароксизмальная фибрилляция предсердий.
Предъявлял жалобы на приступы ускоренного неритмичного сердцебиения, сопровождающиеся головокружением. Приступы беспокоят в течение четырех лет. Принимает антиаритмические препараты без эффекта.
По объективным данным патологических отклонений не выявлено. На нескольких поверхностных электрокардиограммах, зарегистрированных в покое, имеется как ритм фибрилляций предсердий со средней частотой сердечных сокращений 128 ударов в минуту, так и синусовый ритм. По данным эхокардиографии имелась начальная дилатация левого предсердия, в остальном - без патологических изменений.
Пациенту 04.12.2012 на фоне синусового ритма проведена процедура антральной радиочастотной изоляции легочных вен. Исходно во время процедуры по данным ЭКГ-синхронизированной регистрации кровотока в легочных венах и кинопетли изображения каждого из устьев легочных вен в двухмерном режиме у пациента регистрировалось совпадение пика ретроградного кровотока в легочных венах с уменьшением диаметра легочных вен на уровне их устья.
Далее была выполнена процедура антральной радиочастотной изоляции легочных вен с мощностью 30-40 Вт и температурой 45°C в орошаемом режиме под контролем нефлюороскопической навигационной системы с последующим электрофизиологическим подтверждением наличия изоляции легочных вен. Непосредственно после окончания процедуры проведена повторная ЭКГ-синхронизированная регистрация кровотока в легочных венах и кинопетли изображения каждого из устьев легочных вен в двухмерном режиме. При этом отмечено совпадение ретроградного кровотока во всех легочных венах с увеличением их диаметра, что позволило диагностировать нарушенную сократимость муфт всех легочных вен.
В данном клиническом случае предложенный способ продемонстрировал возможность диагностики нарушения сократимости муфт всех четырех легочных вен, в то время как при помощи прототипа было бы сделано ошибочное заключение о нормальной сократимости муфт легочных вен.
После операции пациенту была назначена терапия антагонистами AT1-рецепторов ангиотензина-II, направленная на снижение нагрузки на левые отделы сердца и улучшение гемодинамики в левом предсердии и легочных венах. Спустя три месяца наблюдения пациент чувствовал себя удовлетворительно, пароксизмов фибрилляции предсердий или нарушений внутрисердечной гемодинамики зарегистрировано не было.
Таким образом, предложенный способ радиочастотной аблации фибрилляции предсердий позволяет повысить точность диагностики нарушения сократительной функции муфт легочных вен.
Способ диагностики нарушения сократимости муфт легочных вен после процедуры радиочастотной аблации, включающий измерение диаметра муфт легочных вен при помощи внутрисердечной эхокардиографии и одновременную регистрацию электрокардиограммы, с последующим анализом полученных результатов, отличающийся тем, что измерение диаметра выполняют во временные интервалы, соответствующие началу и пику ретроградного кровотока, зафиксированные на ЭКГ-кривой, а нарушение сократимости муфт легочных вен диагностируют при увеличении их диаметра, зафиксированного на пике ретроградного кровотока относительно диаметра, измеренного в его начале.