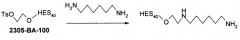Опосредующие транспорт коллоидные лекарственные соединения
Иллюстрации
Показать всеИзобретение относится к связанным с транспортными посредниками коллоидам, содержащим фармацевтические вещества или флуоресцентные маркеры, к способу их получения, а также к фармацевтическому препарату, содержащему указанные соединения. 3 н. и 19 з.п. ф-лы, 9 пр., 2 ил.
Реферат
Изобретение относится к связанным с транспортными посредниками коллоидам, которые могут содержать лекарственные соединения или флуоресцентные маркеры, к способу их получения и к фармацевтической композиции, содержащей такие соединения.
Ковалентное связывание с коллоидами позволяет входить посредством фагоцитоза в клетки иммунной системы веществам, которые без такой модификации не могли бы поглощаться, а если бы и могли, то лишь в очень незначительных количествах. В ЕР 1230935 А1 описано химическое присоединение активных с медицинской точки зрения веществ к полисахариду с образованием линкера. Поглощение веществ соответствующим образом специализированными клетками ретикулогистиоцитарной системы показано для широкого круга коллоидов и частиц. Однако введение больших молекул в клетки организма, которые не специализированы для фагоцитоза, является проблемой. Кроме того, частицы и коллоиды, фагоцитированные макрофагами, после поглощения клеткой очень быстро попадают в лизосомы, где они расщепляются различными литическими ферментами. Ферментативный потенциал лизосом высок; соответственно, широкий спектр лекарственных соединений быстро расщепляется лизосомальными ферментами. Про Chlamydia trachomatis известно, что эта бактерия поглощается эукариотическими эпителиальными клетками без ферментативного расщепления в лизосомах. Это поглощение может быть значительно уменьшено в присутствии гепаринов или гепаринсульфата. Stephens et al. (Infection and Immunity, March 2000, p.1080-1085, Vol. 68, No. 3) показали, что этот эффект основан на блокировании гепарин-связывающего домена.
С другой стороны, авторы показывают, что полистирольные микросферы поглощаются эукариотическими клетками путем эндоцитоза после покрытия их гепарином. Гепарин сам связывается с широким спектром ферментов. Пациенты, имеющие повышенную активность супероксиддисмутазы в сыворотке крови, часто обладают мутантным вариантом фермента (CHU et al. Arteriosclerosis, Thrombosis, and Vascular Biology. 2006; 26: 1985).
В мутантном варианте (R213G) присутствует глицин вместо аминокислоты аргинина на позиции 213. Из-за этого связывание фермента с гепарином невозможно. Вследствие этого, страдающие пациенты имеют повышенную активность фермента, поскольку фермент в основном присутствует в сыворотке, а не в клетках. Для носителей такого генетического дефекта это означает в 2,3 раза более высокий риск возникновения ишемической болезни сердца. В EP 083768 A1 описаны прямые гепарин-белковые конъюгаты, в которых концевая альдоза гепарина связана с N-концевой аминогруппой серпина для усиления эффекта серпинов на коагуляцию крови и синдромы расстройства дыхания. После связывания с гепаринами белки и ферменты очень быстро выводятся из сыворотки. Небольшие белки размером менее 70 кДа исчезают практически полностью уже в процессе первого прохождения через почки. Кроме того, как известно, многие белки имеют проблемы со стабильностью и растворимостью, на которые может положительно повлиять ковалентное связывание с водорастворимым полисахаридом.
Гепарин принадлежит к группе глюкозаминогликанов, которые состоят из линейных цепей из сульфатированных дисахаридных единиц. Каждая дисахаридная единица состоит из одной гексуроновой кислоты, которая является или глюкуроновой или идуроновой кислотой, и 2-амино-2-дезокси-D-глюкозы или N-сульфо-D-глюкозамина. Подобно полисахаридам, гепарин и глюкозаминогликаны имеют свободную альдегидную группу в концевой части. Гепарин находится внутри клеток, почти исключительно в тучных клетках. Однако более высокосульфатированные гепарины, или гепаринсульфаты, встречаются почти повсеместно на клеточных мембранах высших млекопитающих, независимо от вида органов.
Антикоагулянтный эффект гепарина основан прежде всего на его сродстве к ингибитору сериновой протеазы антитромбину III. Наименьший из гепаринов, который обладает таким эффектом на AT III, содержит 5 сахаридных единиц с 3-O-сульфатной группой на глюкозаминовой группе. Этот пентасахарид может образовывать комплекс гепарин/AT III, который ингибирует фактор свертывания Xa. Тромбин также может ингибироваться путем связывания со специфическими гепариновыми структурами, которые, однако, не присутствуют на пентасахариде, имеющем только 5 сахаридных единиц. Для ингибирования тромбина необходимы гепариновые соединения, имеющие по меньшей мере 18 сахаридных единиц.
Молекулярный размер и степень сульфатации имеют решающее значение не только для избирательного действия гепарина на факторы свертывания крови, но и для взаимодействия с широким кругом эндогенных цитокинов и факторов роста. Для взаимодействия гепарина с фактором роста фибробластов (FGF) необходимо как минимум 18 глюкозаминогликановых единиц со специфической сульфатацией атома кислорода, находящегося на C2. Сульфатированные гепарины от 8 сахаридных единиц оказывают ингибиторный эффект на ангиогенез. Для этих сульфатированных октасахаридов обсуждается ингибирование ангиогенеза в опухолевых клетках. В то же время, эти гепарины, очевидно, не влияют на свертываемость крови. Молекулярный размер и химические свойства, такие как количество и локализация сульфатных, карбоксильных и аминогрупп, оказывают решающее влияние на эффект гепаринов. Сульфатные группы и, что менее важно, карбоксильные группы идуроновой и глюкуроновой групп являются причиной того, что гепарин является одной из наиболее сильно электроотрицательно заряженных молекул в организме млекопитающих. Молекулярный размер, а также количество и положение сульфатных и карбоксильных групп создают определенную зарядную матрицу или определенное распределение зарядов на молекулах гепарина. Определенное распределение зарядов играет важную роль для сродства соединений в отношении прокоагулянтных белков и протеаз, а также в отношении гепарин-связывающих доменов эндотелиальных клеток. Транспортно-посредническая функция гепаринов, которая проявляется на клеточных мембранах, еще более сильно зависит от структуры зарядов глюкозаминогликана. Вследствие этого, ковалентное включение гепаринов в водорастворимые полисахариды, как транспортных посредников, существенно отличается от включения активных с медицинской точки зрения соединений. По возможности, гепарин должен быть связан с коллоидом таким образом, чтобы сайт связывания с определенным числом дисахаридных единиц и зарядов стереоизбирательно соответствовал гепарин-связывающему домену клеток. Это означает, что этот сегмент гепарина остается химически несвязанным и, кроме того, имеет нестерические препятствия со стороны остальной молекулы. В данном случае, как и в случае со специфическим эффектом гепарина на AT III и тромбин, длина цепи и число сульфатированных единиц гексуроновой кислоты и аминодезоксиглюкозы, свободно выступающих из полисахарида, имеют большое значение. Кроме того, существуют указания на то, что сегменты молекулы гепарина, имеющие отношение к гепарин-связывающим доменам, обнаружены преимущественно в середине молекулы гепарина. Часть молекулы, используемая для описанного соединения со связывающими доменами, сильно электроотрицательно заряжена из-за карбоксильных и сульфатных групп. Блокировка или нарушение этой стереоспецифически соответствующей зарядной матрицы ковалентным связыванием с полисахаридом с помощью линкера должно быть, по возможности, предотвращено на этих участках.
Будучи строго линейным глюкозаминогликаном, гепарин имеет функциональные группы, которые могут быть использованы для связывания с другими молекулами. В области идуроновой и глюкуроновой кислоты карбоксильные группы присутствуют на C6. Существуют гидроксильные группы на C2 и C3, и C1 первой сахаридной единицы. Каждая вторая сахаридная группа несет аминогруппу на атоме С2. Эта аминогруппа и карбоксильная группа могут быть сульфатированы. И наконец, гепарин имеет альдегидную группу на концевом фрагменте.
Известно, что точечные мутации в некоторых генах, кодирующих белки, приводят к замене диаминомонокарбоновых кислот другими аминокислотами. В некоторых из этих случаев (супероксиддисмутаза) это изменение аминокислотной последовательности сопровождается потерей способности связываться с гепаринсульфатами, в результате чего белок больше не транспортируется в клетку. Эти результаты также показывают, что включение гепаринов в макромолекулы, как транспортных посредников, то есть с целью регулирования прохода через клеточные мембраны, зависит от региоселективных условий на части макромолекулы. В данном случае, утрата аминогрупп, не связанных пептидными связями, означает потерю способности встраиваться в транспортный посредник гепарин. В медицинской практике часто пытаются предотвратить образование сгустков крови на имплантатах путем неспецифического ковалентного связывания с гепарином.
Для введения активных с медицинской точки зрения веществ в определенные органы и клеточные системы организма должны быть выполнены следующие условия:
1. Поглощение связанного лекарственного средства также осуществляется в клетках, не специализированных для фагоцитоза.
2. После прохождения через внешнюю мембрану клетки связанное лекарственное средство не должно поглощаться лизосомами и не должно разрушаться ферментами.
3. Лекарственный комплекс, состоящий из лекарственного средства, химически связанного с транспортным посредником и/или коллоидом, должен быть растворим в воде и циркулировать в крови в течение достаточного периода времени.
4. Лекарственный комплекс не должен оказывать никакого влияния на свертываемость крови.
Удивительно, но было обнаружено, что связывание транспортного посредника с коллоидом (коллоидно-активным соединением) решает вышеуказанные проблемы и служит, в частности, подходящей транспортной системой для лекарственных средств и/или флуоресцентных маркеров, ковалентно присоединенных к нему. Это относится, в частности, к случаю, когда коллоид и транспортный посредник стереоизбирательно связаны друг с другом. Кроме того, к удивлению было обнаружено, что продукт связывания может связываться с мембраносвязанными и внутриклеточными связывающими доменами, если стереоспецифические структуры соединения транспортный посредник/коллоид остаются свободными для ассоциации и связывания с клеточными связывающими доменами.
Настоящее изобретение относится к соединению общей формулы (I)
,
где
Т представляет собой транспортный посредник;
Р представляет собой коллоидно-активное соединение;
Z представляет собой первый линкер, с помощью которого Т и Р ковалентно связаны друг с другом; и
n представляет собой целое число, по меньшей мере равное 1;
и где транспортный посредник Т и/или коллоид Р несет m групп -(L-A), где
А представляет собой активное с медицинской точки зрения вещество или флуоресцентный маркер;
L представляет собой второй линкер, посредством которого Р ковалентно связан с A, или посредством которого T ковалентно связан с A; и
m представляет собой целое число, равное 0 или по меньшей мере 1.
Предпочтительно, транспортный посредник T имеет по меньшей мере один сайт связывания для соединения с клеточными связывающими доменами.
В соответствии с изобретением, транспортные посредники T отличаются от коллоидов P.
Транспортные посредники T по настоящему изобретению способствуют проникновению в клетки.
Транспортный посредник T представляет собой гликан, более предпочтительно, выбранный из группы, состоящей из сиаловой кислоты, полисиаловой кислоты, нейраминовой кислоты, N-ацетилнейраминовой кислоты, маннозы, N-ацетилманнозы, N-пропанолманнозамина, фукозы, N-ацетилфукозы, галактозы, N-ацетилгалактозы, глюкозы, N-ацетилглюкозы, гексоз, N-ацетилгексоз, керамидов, глюкозо-6-фосфата, маннозо-6-фосфата, глюкозилфосфатидилинозитола, ретиноевой кислоты, иммуноглобулинов, моноглицератов, диацилглицератов, сфингомиелина, бисфосфонатов, гликопротеинов и глюкозаминогликанов.
Глюкозаминогликаны или производные глюкозаминогликанов оказались особенно подходящими транспортными посредниками T.
Вследствие этого, в предпочтительном варианте осуществления транспортный посредник T выбирают из группы, состоящей из гепарина и гепаринсульфата, в частности гепарина или гепаринсульфата, имеющих менее 6 сахаридных единиц. Гепарины, имеющие менее 6 сахаридных единиц, в качестве транспортных посредников имеют то особое преимущество, что при использовании таких гепаринов можно в значительной степени избежать возможной индукции аутоантител.
Коллоидно-активное соединение P (также для простоты в дальнейшем называемое «коллоид P») предпочтительно выбирают из группы, состоящей из амилоз, амилопектинов, ацеманнанов, арабиногалактанов, галактоманнанов, галактоглюкоманнанов, ксантанов, каррагенанов, крахмала и модифицированного крахмала.
Модифицированные крахмалы оказались особенно подходящими. Крахмалы можно модифицировать, например, путем гидроксиалкилирования или эстерификации. Кроме того, крахмалы можно также аминировать, например, путем восстановительного аминирования.
Удивительно, но оказалось, что аминирование коллоида P путем восстановительного аминирования может приводить к образованию аминированных коллоидов, в частности модифицированных крахмалов, таких как аминированный гидроксиэтилкрахмал или аминированный карбоксиметилкрахмал, которые могут включаться в транспортные посредники с высокой стереоизбирательностью таким образом, что полученное соединение очень похоже на соединения, поглощаемые клетками организма из комплексов с транспортными посредниками.
В предпочтительном варианте осуществления настоящего изобретения связывание транспортного посредника и коллоида происходит стереоизбирательно. Кроме того, предпочтительно, если соединение активного с медицинской точки зрения вещества или флуоресцентного маркера с коллоидом и/или транспортным посредником также происходит стереоизбирательно.
В предпочтительном варианте осуществления коллоид P выбирают из группы, состоящей из гидроксиалкилкрахмалов, этерифицированных крахмалов, карбоксиалкилкрахмалов, гидроксиалкилкарбоксиалкилкрахмала, аминированного гидроксиалкилкрахмала, аминированного гидроксиалкилкарбоксиалкилкрахмала и аминированного карбоксиалкилкрахмала.
Карбоксиалкилкрахмалы предпочтительно выбирают из карбоксиметилкрахмала и карбоксиэтилкрахмала.
Преимущественно, другие специальные фрагменты, делающие возможным химическое связывание активного с медицинской точки зрения вещества или флуоресцентного маркера или транспортного посредника, например биотин, аминокислоты или фрагменты, несущие сульфидные группы, такие как цистеин, также можно включать в коллоиды.
Более предпочтительно, в соответствии с настоящим изобретением, коллоид P представляет собой модифицированный крахмал, выбранный из группы, состоящей из гидроксиэтилкрахмала или аминированного гидроксиэтилкрахмала, в частности гидроксиэтилкрахмала, аминированного путем восстановительного аминирования.
Гидроксиалкильные группы в гидроксиэтилкрахмале (HES) введены в молекулу для препятствования ферментативному расщеплению крахмала в сыворотке и для улучшения растворимости в воде. Степень замещения, DS, определяется как отношение общего количества замещенных мономерных единиц к общему количеству мономерных единиц. В дальнейшем степень замещения, DS, указывают при введении заместителей.
В другом варианте осуществления настоящего изобретения коллоидно-активное соединение имеет средний молекулярный вес от 20000 до 800000 дальтон, предпочтительно от 25000 до 500000 дальтон, в частности от 30000 до 200000 дальтон.
Степень замещения, DS, модифицированных крахмалов, в частности гидроксиэтилкрахмала, предпочтительно составляет от 0,2 до 0,8, в частности от 0,3 до 0,6.
Что касается лекарственных средств A, можно использовать все вещества, которые можно включать в вышеупомянутые коллоиды и/или транспортные посредники T через линкер L.
Соединения по изобретению могут быть необязательно связаны с активными с медицинской точки зрения соединениями или флуоресцентными маркерами. Предпочтительно, активное с медицинской точки зрения соединение выбирают из группы, состоящей из антибиотиков, химиотерапевтических средств, цитостатиков, антигенов, олигонуклеотидов, медиаторов, ложных метаболических субстратов, анальгетиков и цитотоксических веществ.
Флуоресцентные маркеры предпочтительно выбирают из группы, состоящей из флуоресцеинизотиоцианата (FITC), фикоэритрина, родамина и 2-аминопиридина.
Помимо чистых активных с медицинской точки зрения веществ, флуоресцентные маркеры, например флуоресцеинизотиоцианат, можно также терапевтически использовать в связи с комплексом транспортный посредник/коллоид. Некоторые опухоли, как известно, экспрессируют мембраносвязанные связывающие домены в больших количествах, например, для того, чтобы получить доступ к сосудистой системе (рецепторы FGF). Маркировка комплексов транспортный посредник/коллоид по изобретению, специфичных для таких связывающих доменов, флуоресцентными маркерами, такими как флуоресцеинизотиоцианат (A.N. De Belder, K. Granath: Preparation and Properties of fluorescein-labelled dextrans, Carbohydrate Research, 30 (1973) 375-378) позволяет хирургу оптически определять участки органов, имеющие большее число клеток с такими связывающими доменами, после инъекции данного соединения (флуоресцентное изображение в ближней инфракрасной области спектра, NIRF).
В соединении формулы (I), (T-Z)n-P, транспортный посредник T ковалентно связан с коллоидом P через первую линкерную группу Z. В предпочтительном варианте осуществления настоящего изобретения линкер Z представляет собой функциональную группу, выбранную из сложного эфира карбоновой кислоты, амидов карбоновых кислот, уретана, эфира и аминогрупп, либо содержит по меньшей мере одну такую функциональную группу. Более предпочтительно, ковалентная химическая связь T с P через линкер Z является обратимой, то есть может быть вновь расщеплена без труда, например, ферментативно.
Второй линкер L, через который коллоид P ковалентно связан с активным с медицинской точки зрения веществом или флуоресцентным маркером, или через который транспортный посредник ковалентно связан с активным с медицинской точки зрения веществом или флуоресцентным маркером, также соответствует первому линкеру Z по своей функциональности и конструкции. Что качается линкера L, особым преимуществом являлась бы возможность расщеплять его вновь без труда, например, ферментативно, что способствовало бы высвобождению активного с медицинской точки зрения вещества или флуоресцентного маркера.
Образование линкера Z или L можно осуществлять способами, описанными в известном уровне техники для образования сложных эфиров карбоновых кислот, амидов карбоновых кислот, уретанов, эфиров и аминов.
В предпочтительном варианте осуществления соединение по изобретению можно получать реакцией по меньшей мере одной свободной
изоцианатной группы (-NCO);
карбоксильной группы (-COOH);
галоидной группы карбоновой кислоты (-CO-A, где A=Cl, Br или I);
алкиленкарбоксильной группы (-(CH2)q-COOH, где q=1-10);
сложноэфирной группы (-COOR, где R = органический радикал);
эпоксигруппы;
или нуклеофильной уходящей группы;
исходного коллоида P со свободной
гидроксильной группой (-OH)
исходного транспортного посредника T с образованием линкера Z, где указанный коллоид P и/или транспортный посредник связан с m единицами -(L-A).
В другом варианте осуществления настоящего изобретения соединение по изобретению можно получать реакцией по меньшей мере одной свободной
гидроксильной группы (-OH)
исходного коллоида P со свободной
изоцианатной группой (-NCO);
карбоксильной группой (-COOH);
галоидной группой карбоновой кислоты (-CO-A, где A = Cl, Br или I);
алкиленкарбоксильной группой (-(CH2)q-COOH, где q = 1-10);
сложноэфирной группой (-COOR, где R = органический радикал);
эпоксигруппой;
или нуклеофильной уходящей группой;
исходного транспортного посредника T с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
В другом варианте осуществления настоящего изобретения соединение по изобретению можно получать реакцией по меньшей мере одной свободной
аминогруппы (-NH2)
исходного коллоида P со свободной
изоцианатной группой (-NCO);
карбоксильной группой (-COOH);
галоидной группой карбоновой кислоты (-CO-A, где A=Cl, Br или I);
алкиленкарбоксильной группой (-(CH2)q-COOH, где q=1-10);
сложноэфирной группой (-COOR, где R = органический радикал);
эпоксигруппой;
или нуклеофильной уходящей группой;
исходного транспортного посредника T с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
Кроме того, в предпочтительном варианте осуществления соединение по изобретению можно получать реакцией по меньшей мере одной свободной
изоцианатной группы (-NCO);
карбоксильной группы (-COOH);
галоидной группы карбоновой кислоты (-CO-A, где A=Cl, Br или I);
алкиленкарбоксильной группы (-(CH2)q-COOH, где q=1-10);
сложноэфирной группы (-COOR, где R = органический радикал);
эпоксигруппы;
или нуклеофильной уходящей группы;
исходного коллоида P со свободной
аминогруппой (-NH2)
исходного транспортного посредника T с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
Более предпочтительно, соединение по изобретению можно получать реакцией по меньшей мере одной свободной
гидроксильной группы (-OH); или
аминогруппы (-NH2)
исходного коллоида P со свободной
изоцианатной группой (-NCO);
карбоксильной группой (-COOH);
галоидной группой карбоновой кислоты (-CO-A, где A=Cl, Br или I);
алкиленкарбоксильной группой (-(CH2)q-COOH, где q=1-10);
сложноэфирной группой (-COOR, где R = органический радикал);
эпоксигруппой;
или нуклеофильной уходящей группой;
исходного транспортного посредника T с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
В соответствии с настоящим изобретением, нуклеофильные уходящие группы предпочтительно выбирают из группы галоидов и тозилатов.
Кроме того, соединения по изобретению можно получать реакцией диамина общей формулы II
R1(-NH2)2 (II)
где R1 выбирают из
одинарной связи;
линейных или разветвленных, насыщенных или ненасыщенных, алифатических или алициклических углеводородных групп с 1-22 атомами углерода;
арильных, арил-C1-C4-алкильных и арил-C2-C6-алкенильных групп с 5-12 атомами углерода в арильной группе, которые необязательно могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами; или
гетероарильных, гетероарил-C1-C4-алкильных и гетероарил-C2-C6-алкенильных групп с 3-8 атомами углерода в гетероарильной группе и одним или двумя гетероатомами, выбранными из N, O и S, которые могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами;
со свободной функциональной группой исходного транспортного посредника T и по меньшей мере одной свободной функциональной группой исходного коллоида P, которые независимо выбирают из
изоцианатной группы (-NCO);
карбоксильной группы (-COOH);
галоидной группы карбоновой кислоты (-CO-A, где A=Cl, Br или I);
алкиленкарбоксильной группы (-(CH2)q-COOH, где q=1-10);
сложноэфирной группы (-COOR, где R = органический радикал);
эпоксигруппы;
или нуклеофильной уходящей группы;
с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
Подходящие диамины включают, например, 1,2-диаминоэтан, 1,2- или 1,3-диаминопропан, 1,2-, 1,3- или 1,4-диаминобутан, 1,5-диаминопентан, 2,2-диметил-1,3-диаминопропан, гексаметилендиамин, 1,7-диаминогептан, 1,8-диаминооктан, триметил-1,6-диаминогексан, 1,9-диаминононан, 1,10-диаминодекан, 1,12-диаминододекан, 1,2-диаминоциклогексан, 1,4-диаминоциклогексан, 1,3-циклогексанбис(метиламин), 1,2-фенилендиамин, 1,3-фенилендиамин, 1,4-фенилендиамин, 4,4'-этилендианилин, 4,4'-метилендианилин, 4,4'-диаминостилбен, 4,4'-тиодианилин, 4-аминофенилдисульфид, 2,6-диаминопиридин, 2,3-диаминопиридин, 3,4-диаминопиридин, 2,4-диаминопиридин, 4,5-диаминопиридин, 4,6-диаминопиридин.
Кроме того, в следующем варианте осуществления настоящего изобретения соединения по изобретению можно получать реакцией диола общей формулы III
R2(-OH)2 (III),
где R2 выбирают из
линейных или разветвленных, насыщенных или ненасыщенных, алифатических или алициклических углеводородных групп с 2-22 атомами углерода;
арильных, арил-C1-C4-алкильных и арил-C2-C6-алкенильных групп с 5-12 атомами углерода в арильной группе, которые необязательно могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами; или
гетероарильных, гетероарил-C1-C4-алкильных и гетероарил-C2-C6-алкенильных групп с 3-8 атомами углерода в гетероарильной группе и одним или двумя гетероатомами, выбранными из N, O и S, которые могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами;
со свободной функциональной группой исходного транспортного посредника T и по меньшей мере одной свободной функциональной группой исходного коллоида P, которые независимо выбирают из
изоцианатной группы (-NCO);
карбоксильной группы (-COOH);
галоидной группы карбоновой кислоты (-CO-A, где A=Cl, Br или I);
алкиленкарбоксильной группы (-(CH2)q-COOH, где q=1-10);
сложноэфирной группы (-COOR, где R = органический радикал);
эпоксигруппы;
или нуклеофильной уходящей группы;
с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
Подходящие диолы включают, например, этиленгликоль, пропиленгликоль, бутиленгликоль и неопентилгликоль, пентандиол-1,5,3-метилпентандиол-1,5, бисфенол A, 1,2- или 1,4-циклогександиол, капролактондиол (продукт реакции капролактона и этиленгликоля), гидроксиалкилированные бисфенолы, триметилолпропан, триметилолэтан, пентаэритритол, гександиол-1,6, гептандиол-1,7, октандиол-1,8, бутандиол-1,4, 2-метилоктандиол-1,8, нонандиол-1,9, декандиол-1,10, циклогександиметилол, ди-, три- и тетраэтиленгликоль, ди-, три- и тетрапропиленгликоль, полиэтилен- и полипропиленгликоли со средним молекулярным весом от 150 до 15000.
В другом варианте осуществления настоящего изобретения соединения по изобретению можно получать реакцией дикарбоновой кислоты общей формулы IV
R3(-COOH)2 (IV)
где R3 выбирают из
одинарной связи;
линейных или разветвленных, насыщенных или ненасыщенных, алифатических или алициклических углеводородных групп с 1-22 атомами углерода;
арильных, арил-C1-C4-алкильных и арил-C2-C6-алкенильных групп с 5-12 атомами углерода в арильной группе, которые необязательно могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами; или
гетероарильных, гетероарил-C1-C4-алкильных и гетероарил-C2-C6-алкенильных групп с 3-8 атомами углерода в гетероарильной группе и одним или двумя гетероатомами, выбранными из N, O и S, которые могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами;
со свободной функциональной группой исходного транспортного посредника T и по меньшей мере одной свободной функциональной группой исходного коллоида P, которые независимо выбирают из
аминогруппы (-NH2); или
гидроксильной группы (-OH)
с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
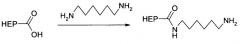
Подходящие дикарбоновые кислоты включают, например, щавелевую кислоту, малоновую кислоту, янтарную кислоту, глутаровую кислоту, адипиновую кислоту, пимелиновую кислоту, азелаиновую кислоту, себациновую кислоту, малеиновую кислоту, фумаровую кислоту, сорбиновую кислоту, фталевую кислоту, терефталевую кислоту, изофталевую кислоту или агарициновую кислоту.
В частности, соединения по изобретению можно также получать реакцией галоида дикарбоновой кислоты общей формулы V
R4(-CO-A)2 (V)
где A=Cl, Br или I и R4 выбирают из
одинарной связи;
линейных или разветвленных, насыщенных или ненасыщенных, алифатических или алициклических углеводородных групп с 1-22 атомами углерода;
арильных, арил-C1-C4-алкильных и арил-C2-C6-алкенильных групп с 5-12 атомами углерода в арильной группе, которые необязательно могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами; или
гетероарильных, гетероарил-C1-C4-алкильных и гетероарил-C2-C6-алкенильных групп с 3-8 атомами углерода в гетероарильной группе и одним или двумя гетероатомами, выбранными из N, O и S, которые могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами;
со свободной функциональной группой исходного транспортного посредника T и по меньшей мере одной свободной функциональной группой исходного коллоида P, которые независимо выбирают из
аминогруппы (-NH2); или
гидроксильной группы (-OH)
с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
Кроме того, в следующем предпочтительном варианте осуществления соединения по изобретению можно получать реакцией сложного диэфира общей формулы VI
R5(-COOR')2 (VI)
где R1 представляет собой C1-10 алкильную группу и R5 выбирают из
одинарной связи;
линейных или разветвленных, насыщенных или ненасыщенных, алифатических или алициклических углеводородных групп с 1-22 атомами углерода;
арильных, арил-C1-C4-алкильных и арил-C2-C6-алкенильных групп с 5-12 атомами углерода в арильной группе, которые необязательно могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами; или
гетероарильных, гетероарил-C1-C4-алкильных и гетероарил-C2-C6-алкенильных групп с 3-8 атомами углерода в гетероарильной группе и одним или двумя гетероатомами, выбранными из N, O и S, которые могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами;
соответственно с одной свободной функциональной группой исходного транспортного посредника T и по меньшей мере одной свободной функциональной группой исходного коллоида P, которые независимо выбирают из
аминогруппы (-NH2); или
гидроксильной группы (-OH)
с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
Более предпочтительно, соединения по изобретению можно получать реакцией диизоцианата общей формулы VII
R6(-NCO)2 (VII)
где R6 выбирают из
линейных или разветвленных, насыщенных или ненасыщенных, алифатических или алициклических углеводородных групп с 1-22 атомами углерода;
арильных, арил-C1-C4-алкильных и арил-C2-C6-алкенильных групп с 5-12 атомами углерода в арильной группе, которые необязательно могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами; или
гетероарильных, гетероарил-C1-C4-алкильных и гетероарил-C2-C6-алкенильных групп с 3-8 атомами углерода в гетероарильной группе и одним или двумя гетероатомами, выбранными из N, O и S, которые могут быть замещены C1-C6 алкильными и/или C2-C6 алкокси группами;
соответственно с одной свободной функциональной группой исходного транспортного посредника T и по меньшей мере одной свободной функциональной группой исходного коллоида P, которые независимо выбирают из
аминогруппы (-NH2); или
гидроксильной группы (-OH)
с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
Подходящие диизоцианаты включают, например, толуилендиизоцианат, битолуилендиизоцианат, дианизидиндиизоцианат, тетраметилендиизоцианат, гексаметилендиизоцианат, м-фенилендиизоцианат, м-ксилилендиизоцианат, C1-C6 алкилбензолдиизоцианат, 1-хлорбензол-2,4-диизоцианат, циклогексилметандиизоцианат, 3,3'-диметоксидифенилметан-4,4'-диизоцианат, 1-нитробензол-2,4-диизоцианат, 1-алкоксибензол-2,4-диизоцианат, этилендиизоцианат, пропилендиизоцианат, циклогексилен-1,2-диизоцианат, 3,3'-дихлор-4,4'-бифенилендиизоцианат, дифенилендиизоцианат, 2-хлортриметилендиизоцианат, бутилен-1,2-диизоцианат, этилидендиизоцианат, дифенилметан-4,4'-диизоцианат, дифенилэтандиизоцианат, 1,5-нафталиндиизоцианат, циклогександиизоцианат и изофорондиизоцианат.
Более предпочтительно, соединения по изобретению можно получать реакцией диэпоксида соответственно с одной свободной функциональной группой исходного транспортного посредника T и по меньшей мере одной свободной функциональной группой исходного коллоида P, которые независимо выбирают из
аминогруппы (-NH2); или
гидроксильной группы (-OH)
с образованием линкера Z, где указанный коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
В частности, 1,2,3,4-диэпоксибутан или 1,2,7,8-диэпоксиоктан оказались подходящими диэпоксидами.
Соединения, в которых связывание транспортного посредника T и коллоида P осуществляется путем восстановительного аминирования, оказались особенно подходящими. Таким образом, более предпочтительно, соединения по изобретению можно получать путем восстановительного аминирования коллоида P, имеющего свободные аминогруппы (-NH2), с транспортным посредником T, имеющим по меньшей мере одну альдегидную или кетогруппу, и где коллоид P и/или транспортный посредник T связан с m единицами -(L-A).
В данном документе коллоид P, имеющий аминогруппы, предпочтительно выбирают из группы, состоящей из аминированного крахмала, аминированного гидроксиалкилкрахмала, аминированного гидроксиалкилкарбоксиалкилкрахмала и аминированного карбоксиалкилкрахмала. Особенно предпочтительным является аминированный гидроксиалкилкрахмал, который сам может быть получен, например, путем восстановительного аминирования.
Более предпочтительно, коллоиды P, связанные путем восстановительного аминирования с транспортными посредниками T, включают транспортные посредники, выбранные из группы гепарина или производных гепарина.
В особенно предпочтительном варианте осуществления настоящего изобретения транспортный посредник T представляет собой гепарин и коллоид P представляет собой гидроксиэтилкрахмал, а первый линкер Z представляет собой -NH группу.
Как уже изложено выше, второй линкер L предпочтительно представляет собой функциональную группу, выбранную из сложного эфира карбоновой кислоты, амида карбоновой кислоты, уретана, эфира и аминогрупп, либо содержит по меньшей мере одну такую функциональную группу.
Кроме того, несколько коллоидов P также могут быть связаны через линкерные молекулы L и/или Z в более крупные кластеры. Эта реакция может конкурировать с присоединением A и/или T к коллоиду P. В соответствии с изобретением, на соотношение этих конкурирующих реакций можно влиять соответствующим изменением используемого метода. Проще всего это можно сделать, изменяя соотношение используемых реагентов и субстратов и изменяя молекулярный вес коллоида. Кроме того, условия реакции, такие как температура, давление и катализаторы, также влияют на соотношение двух реакций.
Коллоид P может иметь один или более транспортных посредников T, связанных через первый линкер Z. Число транспортных посредников T, связанных с коллоидом P, определяется параметром n. В предпочтительном варианте осуществления настоящего изобретения n представляет собой целое чи