Применение ангиогенина или агонистов ангиогенина для лечения заболеваний и нарушений
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к терапии, и касается применения ангиогенина или его агонистов для лечения заболеваний, обусловленных нарушением активности миостатина. Для этого вводят эффективное количество ангиогенина или его агониста. Это обеспечивает рост и нормализацию функции мышечной ткани за счет стимуляции дифференцировки мышечных клеток в мышечные трубочки. 9 з.п. ф-лы, 15 ил., 5 прим.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к способам лечения мышечных нарушений, в том числе вызывающих мышечное истощение нарушений, и способам улучшения мышечной формы посредством улучшения функции, силы, массы мышц или толерантности к физической нагрузке. Это изобретение относится также к способам уменьшения жира, улучшения отношения мышцы - жир и лечения заболеваний, вызываемых субоптимальным отношением мышцы - жир или включающим в себя субоптимальное отношение мышцы - жир. Это изобретение относится также к лечению заболеваний, которые могут лечиться улучшением опосредованной фоллистатином стимуляции клеток.
Уровень техники
Хотя мышца имеет ее собственную клетку-предшественник для регенерации, утраченная вследствие заболевания или повреждения масса и сила мышц зачастую никогда не восстанавливаются полностью. Таким образом, терапии, которые могут стимулировать рост мышц и предотвращать потерю мышц, будут полезными значительной доле населения.
Увеличение роста, массы или функции мышцы являются важными для лечения вредных состояний этой мышцы, включающих в себя, например, повреждение мышцы, мышечное истощение, мышечную дегенерацию, мышечную атрофию или уменьшенные скорости мышечной репарации. Такие вредные состояния мышцы могут происходить из нормальных состояний употребления мышцы или травмы, или очень часто в результате состояний хронических заболеваний.
Кроме различных мышечных нарушений, которые могут требовать лечения, улучшение отношения мышц к жиру, так чтобы иметь большую нежирную массу, предлагалось для улучшения плотности костей. Была показана корреляция между нежирной массой и более высокой общей плотности костей тела в мышах и людях. Напротив, было показано, что люди с более высокой массой жира имеют уменьшенную плотность костей. Таким образом, улучшение отношения мышц к жиру может улучшать плотность костей и быть особенно полезным в лечении нарушений костей, таких как остеопороз.
Кроме того, совершенно здоровые люди могут желать улучшенную форму или функцию мышц. Может быть желательным улучшение способности ношения тяжестей, выносливости, скорости или общей конституции (телосложения), все из которых могут быть достигнуты улучшением массы или функции мышц. Кроме того, может быть желательным улучшение восстановления мышцы из повреждения или уменьшения времени, требующегося мышце для восстановления из продолжительного употребления, например, для уменьшения времени между тренировками для спортсменов, с улучшением посредством этого толерантности к физической нагрузке.
В животноводческом хозяйстве, таком как хозяйство для разведения животных в качестве источника пищи, способы, которые увеличивают долю и массу мышц, будут очень полезными в этой отрасли промышленности.
При условии важности этой области большое количество исследований развертывается для развития способов контроля развития или роста мышц. Многие исследования сосредоточены на обнаружении ингибиторов миостатина, так как миостатин, во взрослых, является негативным регулятором мышечного роста (т.е. он подавляет мышечный рост).
Фоллистатин является гликопротеином 35 кД, который синтезируется во многих тканях и действует в качестве связывающего белка для активина и других членов суперсемейства TGFβ, таких как миостатин и некоторые морфогенетические белки костей. Сообщается, что фоллистатин является одним из нескольких природных ингибиторов миостатина, хотя его физиологическая роль в регуляции мышц в настоящее время является неизвестной. Тем не менее, наблюдали, что введение фоллистатина в мышцу приводило к увеличению мышечной массы, что обусловлено, как считается, его связыванием с миостатином и нейтрализацией миостатина. Одной из трудностей использования фоллистатина в качестве терапевтического вещества является то, что фоллистатин связывает другие лиганды TGFβ, наряду с миостатином, например, активин. Потеря активности активина в мышах приводит к многочисленным дефектам развития и неонатальной смерти. Активин также ограничивает рост многих типов эпителиальной ткани, так что ингибирование действия активина через введение фоллистатина могло бы приводить к отклоняющемуся от нормы росту этих тканей и, в конечном счете, к раку.
В настоящее время не существует одобренный коммерческий фармацевтический способ для ингибирования активности миостатина, который не изменяет одновременно активность активина. Были разработаны антитела против миостатина, которые связывают и нейтрализуют миостатин без связывания других лигандов семейства TGFβ. Однако антитела могут иметь определенные недостатки, которые могут ограничивать их применимость в качестве терапевтических веществ для нарушений с мышечным истощением, и определенно применение антител для мышечного роста вне терапевтического места действия было бы слишком дорогим, чтобы быть применимым коммерчески.
Одной целью предпочтительного варианта осуществления данного изобретения является решение одной или нескольких из вышеуказанных проблем и в идеале обеспечение лечения мышечных нарушений для улучшения мышечной функции, силы, массы и/или толерантности к физической нагрузке.
Все ссылки, включающие в себя любые патенты или заявки на патент, цитируемые в этом описании, включены здесь в качестве ссылки. Будет ясно понятно, что, хотя здесь делаются ссылки на ряд публикаций предшествующего уровня техники, эта ссылка не является признанием того, что какие-либо из этих документов образует часть обычного общего знания в данной области.
Раскрытие изобретения
Это изобретение, в общем, обеспечивает способы увеличения мышц и уменьшения жира введением ангиогенина.
Первый аспект обеспечивает способ лечения нарушения, характеризуемого повышенным или имеющим нарушенную регуляцию миостатином в индивидууме, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Второй аспект обеспечивает способ лечения нарушений, где взаимодействие между фоллистатином и ангиогенином может быть использовано для улучшения функции в тканях введением эффективного количества ангиогенина или агониста ангиогенина.
Третий аспект обеспечивает способ стимуляции мышечного роста в индивидууме, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Четвертый аспект обеспечивает способ улучшения восстановления мышцы из повреждения или применения в индивидууме, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Пятый аспект обеспечивает способ улучшения мышечной силы в индивидууме, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Шестой аспект обеспечивает способ улучшения толерантности к физической нагрузке индивидуума, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Седьмой аспект обеспечивает способ увеличения доли мышц в индивидууме, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Восьмой аспект обеспечивает способ уменьшения жира в индивидууме, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Девятый аспект обеспечивает способ уменьшения отношения жира к мышцам индивидуума, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Вследствие связи между массой мышц или отношением мышц к жиру и чувствительностью к инсулину/метаболическим синдромом (Guo Т, Jou W, Chanturiya T, Portas J, Gavrilova O, McPherron AC. PLoS ONE. 2009; 4 (3):e4937. Epub 2009 Mar 19), предполагается, что способы седьмого - девятого аспектов могут лечить метаболический синдром или усиливать чувствительность к инсулину.
Десятый аспект обеспечивает способ улучшения плотности костей индивидуума улучшением их отношения мышц к жиру в соответствии со способом девятого аспекта.
Предполагается, что ангиогенин способен подавлять или обращать действие миостатина в качестве негативного регулятора роста мышц.
Предполагается также, что миостатин и/или фоллистатин и/или ангиогенин действуют на клетки, другие чем мышечные клетки; они могут действовать на нервные клетки, клетки костей (остеокласты) и эндотелиальные клетки.
Таким образом, одиннадцатый аспект обеспечивает способ лечения неврологических заболеваний или нарушений, повреждений или заболеваний спинного мозга, заболеваний или нарушений костей, заболеваний, включающих в себя гомеостаз глюкозы, заживления ран или обеспечения нейропротекции, функциональной поддержки нервной системы и лечения метаболических заболеваний, предусматривающий введение эффективного количества ангиогенина или агониста ангиогенина.
Хотя предполагается, что введение ангиогенина перорально может действовать вместе с эндогенным фоллистатином, авторами этого изобретения было показано, что ангиогенин или агонист ангиогенина, вводимый с фоллистатином (одновременно или последовательно), имеет более чем аддитивное действие в сравнении с введением одного фоллистатина или одного ангиогенина.
Будет понятно, что будет верным обратное положение открытий авторов этой заявки, заключающееся в том, что ингибиторы или антагонисты ангиогенина могут быть полезными для лечения заболеваний или состояний, в которых является желательным уменьшение роста или массы мышц или увеличение жира или отношения жира к мышцам или увеличенный миостатин.
Авторы этого изобретения изучали действие коровьего ангиогенина, экстрагированного из молока и клеток человека. Они определили, что коровий ангиогенин способен индуцировать васкулярное развитие эндотелиальных клеток пупочной вены человека (HUVEC) на матригеле таким же образом, что и эндотелиальный фактор роста сосудов (VEGF).
Затем авторы этого изобретения тестировали действие коровьего ангиогенина, экстрагированного из молока, в здоровых мышах. Тест-группа обнаруживала увеличенную мышечную массу четырехглавых мышц и уменьшенную массу абдоминальных жировых скоплений при кормлении пищевым рационом, включающим в себя коровий ангиогенин. Продемонстрированная роль ангиогенина в увеличении массы нежирных мышц и уменьшении массы жира показывает, что способы, предусматривающие введение ангиогенина или агониста ангиогенина, имеют большое разнообразие применений, в которых увеличение мышечной ткани было бы терапевтически полезным, например, в животноводстве, мышечных нарушениях, и для общего фитнеса и физического развития (телосложения). Это изобретение может быть также полезным для лечения заболеваний и нарушений, связанных с метаболизмом и жировой тканью.
Это открытие авторов данного изобретения является особенно удивительным при условии, что в известном уровне техники предлагалось введение фоллистатина для увеличения мышечной массы и уменьшения массы жира. Не желая быть связанными теорией, авторы этого изобретения предполагают, что ангиогенин и фоллистатин стимулируют образование мышечных трубочек и что миостатин существенно ингибирует образование мышечных трубочек. Предполагается, что ангиогенин существенно обращает это действие миостатина. Авторы этого изобретения предполагают, что взаимодействие между ангиогенином и фоллистатином является механизмом, который важен для стимуляции, пролиферации и развития и типов клеток, других чем только мышечные клетки. Таким образом, введение ангиогенина может быть использовано для лечения состояний, в которых улучшение опосредованных фоллистатином действий на клетки является полезным для лечения заболевания или состояния.
Это предположение, что механизм действия ангиогенина на рост мышц и потерю жира осуществляется через его взаимодействие с фоллистатином, подтверждается исследованиями in vitro авторов этого изобретения, в которых обработка миобластов мышц либо ангиогенином, либо фоллистатином не стимулирует рост мышц выше контроля, в то время как введение как ангиогенина, так и фоллистатина стимулирует рост мышц.
В одном варианте любого из первого - одиннадцатого аспектов ангиогенин или агонист ангиогенина вводят вместе с фоллистатином.
В одном варианте любого из первого - одиннадцатого аспектов ангиогенин или агонист ангиогенина вводят перорально.
В одном варианте любого из первого - одиннадцатого аспектов ангиогенин или агонист ангиогенина вводят перорально, а фоллистатин вводят парентерально.
Двенадцатый аспект обеспечивает композицию, содержащую ангиогенин или агонист ангиогенина и фоллистатин.
В одном варианте любого из первого - двенадцатого аспектов ангиогенин обеспечивают в виде обогащенного экстракта из молока или плазмы, в частности, из коровьего молока или из плазмы коровы или человека. Такой обогащенный экстракт является агонистом ангиогенина в том смысле, что он не является чистым ангиогенином, но обеспечивает активность ангиогенина.
Фоллистатин, используемый в этих способах или в этой композиции, может быть рекомбинантным или обеспеченным в виде обогащенного экстракта из молока или плазмы, в частности, из коровьего молока или плазмы коровы или человека.
Тринадцатый аспект обеспечивает композицию, пищевую добавку или нутрицевтик, содержащие ангиогенин или агонист ангиогенина, для лечения нарушения, характеризуемого повышенным миостатином, для лечения нарушений, в которых взаимодействие между фоллистатином и ангиогенином может быть использовано для улучшения функции в тканях, для стимуляции мышечного роста, для улучшения мышечной силы, для улучшения толерантности к физической нагрузке, для увеличения доли мышц, для уменьшения жира, для уменьшения отношения жира к мышцам индивидуума, для лечения неврологических заболеваний или нарушений, для лечения повреждений или заболеваний позвоночника, для лечения заболеваний или нарушений костей, для лечения заболеваний, включающих в себя гомеостаз глюкозы, для заживления ран или для обеспечения нейропротекции, функционального поддержания нервной системы, лечения метаболических заболеваний и/или увеличения плотности костей индивидуума.
Четырнадцатый аспект обеспечивает применение ангиогенина или агонистов ангиогенина в приготовлении лекарственного средства для лечения нарушения, характеризуемого повышенным миостатином, для лечения нарушений, в которых взаимодействие между фоллистатином и ангиогенином может быть использовано для улучшения функции в тканях, для стимуляции роста мышц, для улучшения восстановления мышц от повреждения или применения, для улучшения мышечной силы, для улучшения толерантности к физической нагрузке, для увеличения доли мышц, для уменьшения жира, для уменьшения отношения жира к мышцам индивидуума и/или для увеличения плотности костей индивидуума.
В одном варианте четырнадцатого аспекта это лекарственное средство содержит также фоллистатин.
В другом варианте четырнадцатого аспекта это лекарственное средство предназначено для введения индивидууму, который лечится фоллистатином.
Краткое описание фигур
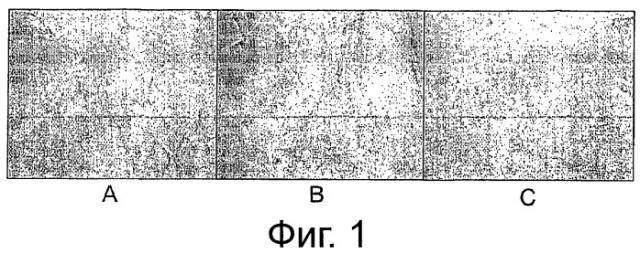
Фигура 1 показывает эндотелиальные клетки (HUVEC), сфотографированные при увеличении 10X. А показывает развитие сосудов, вызываемое обработкой ангиогенином (100 нг/мл), В показывает положительный контроль VEGF (10 нг/мл) и С является отрицательным контролем.
Фигура 2 показывает диаграмму в виде столбцов, иллюстрирующую рост мышиных миобластов C2C12 in vitro при введении казеина, БСА, фоллистатина, ангиогенина или фоллистатина + ангиогенина или положительного контроля (DMEM и 10% ФТС).
Фигура 3 показывает, что ангиогенин коровы (bAngiogenin) и ангиогенин человека (hAngiogenin) могут индуцировать дифференцировку миобластов в мышечные трубочки в отсутствие сыворотки зависимым от дозы образом. Миобластные клетки C2C12 культивировали в 6-луночных чашках в DMEM (контроль), дополненной ангиогенином коровы (bAngiogenin) (bANG) или ангиогенином человека (hAngiogenin) (hANG). Изображения, полученные спустя 96 часов, показывают, что как bANG, так и hANG индуцируют образование мышечных трубочек в сравнении с контрольной культурой DMEM.
Фигура 4 показывает, что ангиогенин коровы индуцирует образование мышечных трубочек в присутствии 2% HS зависимым от дозы образом. Миобластные клетки C2C12 культивировали в среде для дифференцировки (DMEM + 2% HS; контроль), дополненной ангиогенином коровы (bAngiogenin) (bANG) или ангиогенином человека (hAngiogenin) (hANG). Изображения, полученные спустя 96 часов, показывают, что bANG индуцирует образование мышечных трубочек в сравнении с контрольной культурой. rhANG подтверждает, что ангиогенин является индуцирующим фактором.
Фигура 5 показывает, что ангиогенин коровы взаимодействует с FS с усилением образования мышечных трубочек. Миобластные клетки C2C12 культивировали в среде для дифференцировки (DMEM + 2% HS; контроль), дополненной ангиогенином коровы (bANG), фоллистатином (FS) или их комбинацией. Изображения (а) и CK-анализ (b) при 96 часах показывают, что bANG взаимодействует с FS с синергической индукцией образования мышечных трубочек в сравнении с любым реагентом по отдельности.
Фигура 6 показывает иерархическую кластеризацию дифференциально экспрессируемых генов (на основе кратного изменения ±1,6 и Р<0,05) в клетках С2С12 после 2 часов дифференцировки с образованием мышечных трубочек. Миобластные клетки С2С12 культивировали в среде для дифференцировки (DMEM + 2% HS; контроль), дополненной ангиогенином коровы, фоллистатином или их комбинацией. Гены, обнаруживающие увеличенную экспрессию, представлены красным цветом, гены с уменьшенной экспрессией синим цветом, гены без изменения экспрессии представлены желтым цветом.
Фигура 7 показывает, что блокирующий ангиогенин пептид ингибирует образование мышечных трубочек. Этот пептид (VFSVRVSILVF) специфически блокирует взаимодействие ангиогенин/актин и ингибирует индукцию ангиогенином образования мышечных трубочек.
Фигура 8 показывает, что ангиогенин коровы может регулировать действия миостатина на образование мышечных трубочек. Ангиогенин способен устранять отрицательное действие миостатина (Myo) на образование мышечных трубочек. Синергический механизм ангиогенина-фоллистатина восстанавливает образование мышечных трубочек до контрольных уровней в присутствии миостатина.
Фигура 9 показывает, что ангиогенин может регулировать действия миостатина на образование мышечных трубочек. Ангиогенин способен устранять отрицательное действие миостатина (Myo) на образование мышечных трубочек мышц. Синергический механизм ангиогенина-фоллистатина восстанавливает образование мышечных трубочек до контрольных уровней в присутствии миостатина.
Фигуры 10 и 11 показывают защиту клеток PC12 против смерти клеток после сывороточного голодания в присутствии rhAngiogenin + rhFollistatin (рекомбинантного ангиогенина человека + рекомбинантного фоллистатина человека) относительно одного rhAngiogenin (рекомбинантного ангиогенина человека) или одного rhFollistatin (рекомбинантного фоллистатина человека). Результаты представлены в виде Среднего ±SEM повторяемых культур (12 повторностей для среды, содержащей только контроль; 6 повторностей для rhAngiogenin (рекомбинантного ангиогенина человека) (1,0 мкг/мл), bAngiogenin (рекомбинантного ангиогенина коровы) (10 мкг/мл) и rhFollistatin (рекомбинантного фоллистатина человека) (0,1 мкг/мл); 3 повторности для rhNGF-контролей).
Фигура 12 показывает, что ангиогенин, предоставляемый в рационе при 2,5 мкг/г корма в условиях кормления ad libitum, увеличивает массу четырехглавых мышц в мышах, получавших такой рацион в течение 1 месяца, и позволял свободно бегать на стандартных колесах для бега грызунов.
Фигура 13 показывает, что ангиогенин, предоставляемый в рационе при 2,5 мкг/г корма в условиях кормления ad libitum, увеличивает результаты изменений площади поперечного среза мышечного волокна (SA) в мышах, получавших этот рацион в течение 1 месяца, и позволял свободно бегать на стандартных колесах для бега грызунов. Средние величины для контрольных животных представлены белыми столбцами, а средние величины для обработанныых ангиогенином животных представлены черными столбцами. Приведены стандартные отклонения.
Фигура 14 показывает, что ангиогенин, предоставляемый в рационе при 2,5 мкг/г корма в условиях кормления ad libitum, увеличивает расстояние, пробегаемое в день, в мышах, получавших этот рацион в течение 1 месяца, и позволял свободно бегать на стандартных колесах для бега грызунов.
Фигура 15 показывает, что ангиогенин, предоставляемый в рационе при 2,5 мкг/г корма в условиях кормления ad libitum, уменьшает площадь мышечного некроза в четырехглавых мышцах мышей и позволял свободно бегать на стандартных колесах для бега грызунов.
Осуществление изобретения
Ангиогенин является негликозилированным полипептидом 14 кДа, который продуцируется несколькими растущими типами клеток, включающими в себя эндотелиальные клетки, клетки гладких мышц аорты, фибробласты и некоторые опухоли, такие как карциномы ободочной кишки, карциномы яичника и раковые опухоли молочной железы. Ангиогенин был выделен из ряда источников, включающих в себя нормальную плазму человека, плазму коровы, коровье молоко и сыворотки мыши, кролика и свиньи.
Ангиогенин является гомологом панкреатической рибонуклеазы и имеет специфическую рибонуклеолитическую активность. Этот белок способен индуцировать рост новых кровеносных сосудов; однако установлено, что рибонуклеолитическая активность ангиогенина играет роль в ангиогенезе, индуцируемом этим белком.
Было показано также, что, наряду с тем, что ангиогенин является сильным стимулятором ангиогенеза, он имеет ряд других активностей. Однако не существует предшествующего описания действия ангиогенина на мышцы, другого чем увеличение ангиогенеза.
Авторы этого изобретения показали, что богатые ангиогенином очищенные препараты, получаемые катионообменной хроматографией фракций молока, содержат также фоллистатин, белок со значимо отличающимися свойствами заряда относительно ангиогенина (данные не показаны). В известном уровне техники было показано, что ангиогенин и фоллистатин связываются один с другим в двухгибридной модели дрожжей. Авторы изобретения впервые показывают биологически значимое взаимодействие между ангиогенином и фоллистатином в клетках млекопитающих. Фоллистатин известен как антагонист миостатина, белка, который, как указано, регулирует рост и развитие мышц.
Это изобретение в одном аспекте относится к лечению нарушений. Термины "лечение" и "обработка", используемые здесь, относятся к уменьшению тяжести и/или частоты симптомов, элиминации симптомов и/или лежащей в основе нарушения причины, предупреждению возникновения симптомов (профилактике) и/или лежащей в их основе причины и улучшению или излечению повреждения. Так, например, данный способ "лечения" нарушения включает в себя как предупреждение этого нарушения в предрасположенном индивидууме, так и лечение этого нарушения в клинически симптоматическом индивидууме.
"Лечение" включает в себя, в данном контексте, любую обработку или предупреждение состояния в позвоночном, млекопитающем, в частности, человеке, и включает в себя: ингибирование этого состояния, т.е. остановку его развития; или облегчение или ослабление эффектов этого состояния, т.е. вызывание регресса эффектов этого состояния.
"Профилактика" или "профилактическая" или "превентивная" терапия включает в себя, в данном контексте, предотвращение возникновения состояния или ослабление последующего прогрессирования этого состояния в субъекте, который может быть предрасположен к этому состоянию, но еще не диагностирован как имеющий его.
В известном уровне техники сообщается, что миостатин играет роль в развитии мышц и ряде связанных с этим нарушений или заболеваний. У взрослых, мРНК миостатина детектируется первично в скелетных мышцах, хотя более низкие концентрации обнаруживаются также в жировой ткани и ткани сердца. Мыши с нокаутом миостатина имеют в два-три раза большую массы мышц, чем их однопометные животные дикого типа. Увеличенная масса мышц является результатом гипертрофии и гиперплазии волокон. Кроме того, мыши с нокаутом миостатина накапливали меньше жира, чем однопометные животные дикого типа, но в остальном казались нормальными и здоровыми. Недавно было показано, что миостатин является важным регулятором липогенеза. Кроме того, недавно была изучена структура и содержание костной массы в миостатин-недостаточных мышах.
Поскольку авторы этого изобретения предполагают, что миостатин действительно противодействует действию ангиогенина на мышцы, они предполагают, что ангиогенин может быть использован для лечения любого заболевания, в котором ранее предполагалось ингибирование миостатина.
Таким образом, ангиогенин может быть использован в соответствии с данным изобретением для увеличения массы мышц, плотности костей, уменьшения гипотрофии (истощения) мышц или может быть использован для лечения или предупреждения состояний, в которых присутствие миостатина вызывает нежелательные патологические действия или способствует нежелательным патологическим действиям или уменьшение уровней миостатина имеет полезное терапевтическое действие, в млекопитающих, предпочтительно в людях. Кроме того, ангиогенин может быть использован для лечения состояний, в которых регуляция миостатина не нарушена, но улучшенная опосредованная фоллистатином стимуляция клеток может достигаться добавлением экзогенного ангиогенина.
Ангиогенин может быть использован для уменьшения тяжести патологического состояния, которое характеризуется, по меньшей мере частично, аномальным количеством, развитием или аномальной метаболической активностью мышечной или жировой ткани в субъекте. Он может быть введен для предупреждения, облегчения или уменьшения тяжести вызывающего истощение нарушения, такого как кахексия, анорексия, синдром истощения СПИДа, мышечные дистрофии, нервно-мышечные заболевания, заболевания двигательных нейронов (мотонейронов), заболевания нервно-мышечных синапсов (соединений) и воспалительные миопатии.
Термин "нарушение, ассоциированное с миостатином" относится к нарушениям мышцы, кости или гомеостаза глюкозы и включает в себя нарушения, ассоциированные с отклоняющимся от нормы миостатином.
Это изобретение включает в себя также лечение мышечных нарушений и заболеваний, ассоциированных с признаками мышечной дегенерации. Не ограничивающими изобретение примерами таких нарушений являются различные нервно-мышечные заболевания, сердечная недостаточность, слабость одиночных мышц, таких как, например, сфинктер мышцы мочевого пузыря, гипо- или гипертензия, вызываемая проблемами констрикторной функции клеток гладких мышц сосудов, импотенция/эректильная дисфункция, недержание, связанная со СПИДом слабость мышц и общая или связанная со старением амиотрофия.
Приведенные здесь нарушения мышц включают в себя, в частности, состояния или нарушения гипотрофии мышц (истощения мышц), в которых истощение мышц является одним из первичных симптомов.
Мышца является тканью тела, которая первично функционирует в качестве источника силы. В теле имеются три типа мышц: a) скелетная мышца - поперечно-полосатая мышца, ответственная за генерирование силы, которая переносится к скелету для возможности движения, поддержания осанки и дыхания; b) сердечная мышца (миокард) - мышца сердца и c) гладкая мышца - мышца, которая находится в стенках артерий и пищеварительного тракта. Способ этого изобретения особенно применим к скелетной мышце, но может иметь некоторое действие на сердечную и/или гладкую мышцу.
Волокна скелетных мышц обычно классифицируются как волокна типа I (оксилительные/медленные) или типа II (гликолитические/быстрые). Они проявляют заметные различия в отношении концентраци, метаболизма и предрасположенности к усталости. Волокна типа I является богатыми митохондриями и используют в основном окислительный механизм для производства энергии, который обеспечивает стабильную и продолжительную подачу АТФ, и, следовательно, являются резистентными в отношении усталости. Волокна типа II содержат три подтипа: IIa, IIx и IIb. Волокна типа IIb имеют самые низкие уровни содержания митохондрий и окислительных ферментов и являются предрасположенными к усталости, в то время как окислительные и сократительные функции типа На и Их лежат между типом I и типом IIb. Скелетная мышца взрослых обнаруживает пластичность и может подвергаться превращению между различными типами волокон в ответ на физическую тренировку или модуляцию активности двигательных нейронов (мотонейронов).
Определение состава мышечных волокон у спортсменов выявило, что участвующие в соревнованиях выносливые спортсмены имеют относительно больше волокон типа I, чем волокон типа II в тренированной маскулатуре. Бегуны в марафоне также обнаруживают тенденцию большего наличия волокон типа I. Было сделано предположение, что волокно типа I может быть фактором, управляющим способностью к физической выносливости.
Напротив, старение и физическая неактивность являются условиями, ассоциированными с уменьшением волокон типа I, окислительной способности и чувствительности к инсулину. По-видимому, окислительная способность мышц является критическим фактором для определения выносливости и резистентности к усталости. По-видимому, существует адаптивная метаболическая реакция скелетных мышц на тренировку выносливости посредством регуляции количества окислительных мышечных волокон (волокон типа I).
Превращение волокна типа IIb скелетной мышцы в тип IIa и тип I регулируется различными путями передачи сигналов, таких как, например, Ras/митоген-активируемая протеинкиназа (MAPK), кальцинейрин, кальций/кальмодулин-зависимая протеинкиназа FV и коактиватор 1 пролифератора γ пероксисом (PGC-I). Ангиогенин может модулировать эти пути и таким образом влиять на волокна скелетных мышц.
"Истощение мышц" относится к прогрессирующей потере массы мышц и/или прогрессирующему ослаблению и дегенерации мышц, в том числе скелетных мышц или произвольно сокращающихся мышц, которые контролируют движение, сердечных мышц, которые контролируют сердце, и гладких мышц. В одном варианте, состоянием или нарушением с истощением мышц является состояние или нарушение хронического мышечного истощения "Хроническое мышечное истощение" определяется здесь как хроническая (т.е. персистирующая на протяжении продолжительного периода времени) прогрессирующая потеря мышечной массы и/или хроническое прогрессирующее ослабление и дегенерация мышцы.
Потеря мышечной массы, которая происходит во время мышечного истощения (мышечной гипотрофии) может быть охарактеризована распадом или деградацией мышечного белка, катаболизмом мышечного белка. Катаболизм белков происходит вследствие атипично высокой скорости деградации белка, атипично низкой скорости синтеза белка или их комбинацией. Катаболизм или уменьшение белка, независимо от того, вызывается ли он высокой степенью деградации белка или низкой степенью синтеза белка, приводит к уменьшению мышечной массы и истощению (гипотрофии) мышц. Термин "катаболизм" имеет значение, обычно известное в данной области, конкретно, обозначает сжигающую энергию форму метаболизма.
Мышечное истощение может иметь место как результат патологии, заболевания, состояния или нарушения. В одном варианте, эти патология, болезнь, заболевание или состояние являются хроническими. В другом варианте, эти патология, болезнь, заболевание или состояние являются генетическими. В другом варианте, эти патология, болезнь, заболевание или состояние являются неврологическими. В другом варианте, эти патология, болезнь, заболевание или состояние являются инфекционными. Как описано здесь, эти патологии, заболевания, состояния или нарушения, для которых вводят соединения и композиции данного изобретения, являются патологиями, заболеваниями, состояниями или нарушениями, которые прямо или опосредованно производят истощение (т.е. потерю) мышечной массы, т.е. являются нарушением с гипотрофией мышц.
Особенно предпочтительным является лечение нервно-мышечных заболеваний, которые находятся в одном ряду с дефектами суставов или скелета. В одном варианте, истощение мышц в субъекте является результатом того, что этот субъект имеет мышечную дистрофию; мышечную атрофию или X-связанную спинально-бульбарную мышечную атрофию (SBMA).
Мышечные дистрофии являются генетическими заболеваниями, характеризуемыми прогрессирующей слабостью и дегенерацией скелетных или произвольно сокращающихся мышц, которые контролируют движение. Мышцы сердца и некоторые другие произвольно сокращающиеся мышцы также подвергаются воздействию в некоторых формах мышечной дистрофии. Основными формами мышечной дистрофии (MD) являются: мышечная дистрофия Дюшенна, миотоническая дистрофия, мышечная дистрофия Беккера, тазово-плечевая мышечная дистрофия, плече-лопаточно-лицевая дистрофия, врожденная мышечная дистрофия, глазофарингеальная дистрофия, дистальная мышечная дистрофия и мышечная дистрофия Эмери-Дрейфуса.
Мышечная дистрофия может поражать людей во всех возрастах. Хотя некоторые формы сначала становятся очевидными в младенчестве или в детстве, другие могут не появляться, пока не наступит пожилой возраст или позже. MD Дюшенна является наиболее обычной формой, обычно поражающей детей. Миотоническая дистрофия является наиболее обычным из этих заболеваний у взрослых.
Мышечная дистрофия (MA) характеризуется истощением и уменьшением мышцы и уменьшением массы мышц. Например, постполиомиелитное мышечное истощение является мышечным истощением, которое встречается в качестве части синдрома постполиомиелитного синдрома (PPS). Эта атрофия включает в себя слабость, мышечную усталость и боль.
Другим типом МА является X-связанная спинально-бульбарная мышечная атрофия (SBMA - также известная как болезнь Кеннеди). Это заболевание возникает из дефекта в гене рецептора андрогена на X-хромосоме, поражает только мужчин, и его появление имеет место только в состоянии зрелости.
Саркопения является истощающим заболеванием, которое поражает пожилых и хронически больных пациентов и характеризуется потерей мышечной массы и функции. Далее, увеличенная нежирная масса тела ассоциирована с пониженной болезненностью и смертностью для некоторых нарушений с мышечным истощением. Кроме того, другие обстоятельства и состояния связаны с истощающими нарушениями и могут вызывать истощающие нарушения. Например, исследования показали, что в тяжелых случаях хронической боли нижней части спины имеется паравертебральное (вдоль позвоночника) истощение мышц.
Мышечное истощение и истощение других тканей ассоциировано также с престарелым возрастом. Считается, что общая слабость в старом возрасте обусловлена мышечным истощением. По мере старения организма, увеличивающаяся доля скелетных мышц заменяется волокнистой соединительной (фиброзной) тканью. Результатом является значительное уменьшение мышечной силы, трудоспособности и выносливости.
Продолжительная госпитализация вследствие болезни или повреждения или детренированность, которая имеет место, например, при иммобилизации конечности, может также приводить к истощению мышц или истощению другой ткани. Исследования показали, что в пациентах, страдающих от повреждений, хронических болезней, ожогов, травмы или рака, которые госпитализированы в течение продолжительных периодов времени, имеется долго длящееся истощение односторонней мышцы и уменьшение массы тела.
Повреждения или поражение центральной нервной системы (ЦНС) также ассоциированы с мышечным истощением и другими истощающими нарушениями. Повреждения или поражения ЦНС могут быть, например, обусловлены заболеваниями, поранениями или химикалиями. Примерами являются повреждение или поражение центральных нервов, повреждение или поражение периферических нервов и повреждение или поражение спинного мозга. В одном варианте, поражение или повреждение ЦНС включает в себя болезни Альцгеймера (AD); инсульт, гнев (настроение); анорексию, нервную а