Замещенные тетрагидропиранспиропирролидинон и тетрагидропиранспиропиперидинон, фармацевтическая композиция на их основе и применение в лечебных целях
Иллюстрации
Показать всеИзобретение описывает группу замещенных N-фенилбипирролидинкарбоксамидов формулы (I).
где m равно 1 или 2; n равно 1 или 2; p равно 1 или 2; R1 - водород, (С1-С4)-алкил, CF3, (С1-С4)-алкокси-(С1-С4)-алкил; и R2 - водород, галоген, (С1-С4)-алкил или CF3; или их соль, или энантиомер, или диастереомер. Более конкретно, соединения данного изобретения являются модуляторами рецепторов Н3 и, следовательно, пригодны для использования в качестве фармацевтических средств, в особенности, при лечении и (или) предотвращении различных заболеваний, модулируемых рецепторами Н3, включая заболевания, связанные с центральной нервной системой. Технический результат - получены новые соединения, обладающие полезными биологическими свойствами. 3 н. и 12 з.п. ф-лы, 1 табл., 44 пр.
Реферат
УРОВЕНЬ ТЕХНИКИ
Область изобретения
Настоящее изобретение относится к группе замещенных производных тетрагидропиранспиропирролидинона и тетрагидропиранспиропиперидинона. Соединения данного изобретения являются модуляторами рецепторов Н3 и, следовательно, пригодны для использования в качестве фармацевтических средств, в особенности, при лечении и (или) предотвращении различных заболеваний, модулируемых рецепторами Н3, включая заболевания, связанные с центральной нервной системой. Кроме того, настоящее изобретение также относится к способам получения замещенных тетрагидропиранспиропирролидинона и тетрагидропиранспиропиперидинона и их промежуточных соединений.
Описание области техники
Гистамин является универсальной молекулой-мессенджером, выделяемой мастоцитами, энтерохромаффин-подобными клетками и нейронами. Физиологическое действие гистамина опосредовано четырьмя фармакологически определяемыми рецепторами (Н1, Н2, Н3 и Н4). Все гистаминовые рецепторы имеют семь трансмембранных доменов и относятся к суперсемейству рецепторов, связанных с G-белком (GPCR).
Рецептор Н1 был первым членом семейства гистаминовых рецепторов, которые удалось определить фармакологически, в процессе разработки классических антигистаминовых препаратов (антагонистов), например дифенгидрамина и фексофенадина. Несмотря на то, что антагонизм рецептора Н1 в иммунной системе обычно используется для лечения аллергических реакций, рецептор Н1 также экспрессируется в различных периферических тканях и центральной нервной системе (ЦНС). В головном мозге Н1 участвует в контроле бодрствования, настроения, аппетита и секреции гормонов.
Рецептор Н2 также экспрессируется в ЦНС, где он может модулировать несколько процессов, в том числе когнитивную функцию. Вместе с тем антагонисты рецепторов Н2 в основном разрабатывались для улучшения состояния при язвах желудка за счет ингибирования опосредованной гистаминами секреции желудочной кислоты париетальными гландулоцитами. К классическим Н2 антагонистам относятся циметидин, ранитидин и фамотидин.
Следует также отметить, что функция рецепторов Н4 по-прежнему точно не установлена, но она может затрагивать иммунное регулирование и воспалительные процессы.
С другой стороны, рецепторы Н3 также были фармакологически идентифицированы в ЦНС, сердце, легких и желудке. Рецептор Н3 существенно отличается от других гистаминовых рецепторов, демонстрируя низкую гомологию последовательности (Н1: 30%, Н2: 28%, Н4: 51%). Н3 является пресинаптическим ауторецептором на гистаминовых нейронах в головном мозге, а также пресинаптическим гетерорецептором в не содержащих гистамина нейронах в центральной и периферической нервной системах. Кроме гистамина, Н3 также модулирует высвобождение и/или синтез других нейтротрансмиттеров, в том числе ацетилхолина, дофамина, норэпинефрина и серотонина. Особенно важно отметить, что опосредованная Н3 пресинаптическая модуляция высвобождения гистамина обеспечивает активное регулирование рецепторов Н1 и Н2 в головном мозге. Модулируя множество каналов передачи сигналов нейротрансмиттера, Н3 может участвовать в самых различных физиологических процессах. В самом деле, результаты обширных доклинических исследований показывают, что Н3 играет определенную роль в когнитивности, цикле сон-бодрствование и энергетическом гомеостазе.
Модуляторы функции Н3 могут использоваться для лечения расстройств центральной нервной системы, таких как когнитивные нарушения при шизофрении (КНШ), деменция типа Альцгеймера (ДТА), шизофрения, болезнь Альцгеймера, синдром дефицита внимания с гиперактивностью, болезнь Паркинсона, депрессия, эпилепсия, расстройства сна (нарколепсия и бессонница), сердечно-сосудистые заболевания (острый инфаркт миокарда), заболевания органов дыхания (астма), ожирение и желудочно-кишечные расстройства. См., в общем случае, Hancock, Biochem. Pharmacol. 2006 Apr 14; 71(8):1103-13 и Esbenshade et al. Mol Interv. 2006 Apr; 6(2):77-88, 59.
В патенте США №7223788 раскрывается группа соединений, в том числе замещенных бис-пирролидинов, имеющих антагонисты рецептора меланинконцентрирующего гормона (МКГ). Однако не приводятся сведения об активности соединений, представленных в настоящем документе, в отношении сайта рецептора Н3.
Все приведенные здесь источники включаются в настоящий документ полностью в силу ссылки на них.
Таким образом, целью настоящего изобретения является предоставить группу замещенных тетрагидропиранспиропирролидинона и тетрагидропиранспиропиперидинона как селективных рецепторов Н3 для лечения регулируемых рецептором Н3 нарушений ЦНС.
Также целью настоящего изобретения является предоставить процессы получения замещенных тетрагидропиранспиропирролидинона и тетрагидропиранспиропиперидинона, как указано в настоящем документе.
Иные цели и другие области применения настоящего изобретения станут очевидны из детального описания, следующего ниже.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К настоящему времени было установлено, что соединения с формулой (I) можно использовать в качестве антагонистов и/или обратных агонистов рецепторов Н3. Итак, в соответствии с практикой настоящего изобретения, предлагается соединение с формулой (I):
где
m равно 1 или 2,
n равно 1 или 2,
p равно 1 или 2,
R1 - водород, (С1-С4)-алкил, CF3, (С1-С4)-алкокси-(С1-С4)-алкил,
R2 - водород, галоген, (С1-С4)-алкил или CF3.
Настоящее изобретение также включает различные соли соединений с формулой (I), в том числе различные энантиомеры или диастереомеры соединений с формулой (I).
В других аспектах настоящего изобретения также предлагаются различные фармацевтические композиции, содержащие одно или более соединений формулы (I), а также их применение в лечебных целях для купирования различных заболеваний, отчасти или полностью опосредованных рецепторами H3.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Используемые в настоящем документе термины имеют следующие значения.
Используемое в настоящем документе выражение «(С1-С4)-алкил» включает метильную и этильную группы, а также линейные или разветвленные пропильную и бутильную группы. Конкретными алкильными группами являются метильная, этильная, н-пропильная, изопропильная и трет-бутильная. Производные выражения, такие как «(С1-С4)-алкокси», «(С1-С4)-алкокси-(С1-С4)-алкил» или «гидрокси-(С1-С4)-алкил» следует толковать соответствующим образом.
Используемое здесь выражение «(С1-С6)-перфторалкил» означает, что все атомы водорода в указанной алкильной группе замещены атомами фтора. Наглядными примерами являются трифторметильная и пентафторэтильная и линейные или разветвленные гептафторпропильная, нонафторбутильная, ундекафторпентильная и тридекафторгексильная группы. Производное выражение «(С1-С6)-перфторалкил» следует толковать соответствующим образом.
«Галоген» означает хлор, фтор, бром или иод.
Используемый здесь термин «пациент» означает теплокровных животных, например крыс, мышей, собак, кошек, морских свинок и приматов, таких как люди.
Используемое в настоящем документе выражение «фармацевтически приемлемый носитель» обозначает нетоксичный растворитель, диспергатор, наполнитель, вспомогательное или другое вещество, которое смешивают с соединением, составляющим предмет настоящего изобретения, чтобы образовать фармацевтическую композицию, то есть лекарственную форму, которую можно вводить пациенту. Одним из примеров такого носителя является фармацевтически приемлемое масло, обычно используемое для парентерального введения.
Используемый в настоящем документе термин «фармацевтически приемлемые соли» означает, что соли соединений настоящего изобретения могут использоваться в лекарственных препаратах. Вместе с тем и другие соли могут быть полезны в приготовлении соединений в соответствии с настоящим изобретением или их фармацевтически приемлемых солей. К подходящим фармацевтически приемлемым солям соединений настоящего изобретения относятся соли, образованные при добавлении кислот, которые могут получаться, например, при смешении раствора соединения в соответствии с настоящим изобретением с раствором фармацевтически приемлемой кислоты, например соляной кислоты, бромистоводородной кислоты, азотной кислоты, сульфаминовой кислоты, серной кислоты, метансульфоновой кислоты, 2-гидроксиэтансульфоновой кислоты, п-толуолсульфоновой кислоты, фумаровой кислоты, малеиновой кислоты, гидроксималеиновой кислоты, яблочной кислоты, аскорбиновой кислоты, янтарной кислоты, глутаровой кислоты, уксусной кислоты, пропионовой кислоты, салициловой кислоты, коричной кислоты, 2-феноксибензойной кислоты, гидроксибензойной кислоты, фенилуксусной кислоты, бензойной кислоты, щавелевой кислоты, лимонной кислоты, винной кислоты, гликолевой кислоты, молочной кислоты, пировиноградной кислоты, малоновой кислоты, угольной кислоты или фосфорной кислоты. Могут также получаться кислые соли металлов, например, моногидроортофосфат натрия и гидросульфат калия. Кроме того, получаемые таким образом соли могут представлять собой моно- или дизамещенные кислые соли и могут быть в значительной степени обезвоженными или существовать в форме гидратов. Более того, если соединения настоящего изобретения включают кислотную функциональную группу, то к подходящим фармацевтически приемлемым их солям могут быть отнесены соли щелочных металлов, например соли натрия или калия, соли щелочноземельных металлов, например соли кальция или магния, и соли, образованные подходящими органическими лигандами, например четвертичные аммониевые соли.
Выражение «стереоизомеры» является общим термином, используемым для всех изомеров индивидуальных молекул, которые отличаются только пространственной ориентацией своих атомов. К ним, как правило, относятся зеркальные изомеры, которые обычно существуют при наличии, по крайней мере, одного центра асимметрии (энантиомеры). Если соединения, составляющие предмет настоящего изобретения, обладают двумя или более центрами асимметрии, они могут также существовать в форме диастереоизомеров, кроме того, некоторые индивидуальные молекулы могут существовать в форме геометрических изомеров (цис/транс). Аналогичным образом, соединения настоящего изобретения могут существовать в смеси двух или более структурно различающихся форм, которые находятся в состоянии быстрого равновесия, обычно известных как таутомеры. К характерным примерам таутомеров относятся кетоэнольные таутомеры, фенолкетонные таутомеры, нитрозооксимные таутомеры, иминоэнаминовые таутомеры и пр. Следует понимать, что все подобные изомеры и их смеси в любой пропорции попадают в сферу охвата настоящего изобретения.
Используемые в настоящем документе обозначения «R» и «S» применяются как повсеместно употребляемые в органической химии для указания специфической конфигурации хирального центра. Обозначение «R» (rectus, правый) относится к конфигурации хирального центра с расположением высших по приоритету групп по часовой стрелке (от группы с наибольшим приоритетом к группе со вторым наименьшим), если смотреть вдоль связи в направлении группы, с наименьшим приоритетом. Обозначение «S» (sinister, левый) относится к конфигурации хирального центра с расположением высших по приоритету групп против часовой стрелки (от группы с наибольшим приоритетом к группе со вторым наименьшим), если смотреть вдоль связи в направлении группы, с наименьшим приоритетом. Приоритет групп определяется правилами последовательности, причем приоритет, в первую очередь, основан на атомном номере (в порядке убывания атомных номеров). Перечень и обсуждение приоритета групп приводится в работе Stereochemistry of Organic Compounds, Ernest L. Eliel, Samuel H. Wilen and Lewis N. Mander, editors, Wiley-Interscience, John Wiley & Sons, Inc., New York, 1994.
Кроме системы (R)-(S), в настоящем документе может также применяться более старая система D-L для обозначения абсолютной конфигурации, особенно в отношении аминокислот. В данной системе формула проекции Фишера ориентируется таким образом, чтобы первый атом углерода основной цепи находился в верхней части. Префикс «D» используется для описания абсолютной конфигурации изомера, в котором функциональная (определяющая) группа находится справа от углерода хирального центра, а «L» - для изомера, в котором она расположена слева.
В широком смысле предполагается, что термин «замещенный» включает все допустимые заместители органических соединений. В приведенном в настоящем документе ряде конкретных осуществлений термин «замещенный» означает замещенный одним или несколькими заместителями, которые независимым образом выбираются из группы, включающей (С1-С6)-алкил, (С2-С6)-алкенил, (C1-C6)-перфторалкил, фенил, гидрокси, СO2Н, эфир, амид, (С1-С6)-алкокси, (С1-С6)-тиоалкил, (С1-С6)-перфторалкокси, -NH2, Cl, Br, I, F, NH низший алкил и -N(низший алкил)2. Вместе с тем в указанных осуществлениях может также использоваться любой другой из подходящих заместителей, известных специалистам.
«Терапевтически эффективное количество» означает количество соединения, эффективное для лечения названного заболевания, расстройства или состояния.
Термин «лечение» означает:
(i) профилактику заболевания, расстройства или состояния у пациента, который может быть предрасположен к заболеванию, расстройству и/или состоянию, однако, его наличие еще не было диагностировано;
(ii) подавление заболевания, расстройства или состояния, то есть замедление его развития; или
(iii) устранение заболевания, расстройства или состояния, то есть регрессия заболевания, расстройства и/или состояния.
Итак, в соответствии с настоящим изобретением, предлагается соединение с формулой I
где m равно 1 или 2,
n равно 1 или 2,
p равно 1 или 2,
R1 - водород, (С1-С4)-алкил, CF3, (С1-С4)-алкокси-(С1-С4)-алкил,
R2 - водород, галоген, (С1-С4)-алкил или CF3.
Настоящее изобретение также включает различные соли соединений с формулой (I), в том числе различные энантиомеры или диастереомеры соединений с формулой (I). Как отмечено выше и в конкретных примерах, приводимых ниже, все соли, которые могут быть образованы, включая фармацевтически приемлемые соли, являются частью настоящего изобретения. Как также было отмечено выше и в продолжении настоящего документа, все возможные энантиомерные и диастереомерные формы соединений с формулой (I) являются частью настоящего изобретения.
В одном из осуществлений предлагаются соединения с формулой (I), где m, n и p равны 1. R1 - метил, этил, изопропил, н-пропил или метоксиметил. R2 - водород, фтор, хлор, метил, этил или CF3.
В другом осуществлении настоящего изобретения предлагается соединение с формулой (I), где n равно 2 и m равно 1 или n равно 1 и m равно 2, p равно 1 или 2. R1 - метил, этил, изопропил, н-пропил или метоксиметил. R2 - водород, фтор, хлор, метил, этил или CF3.
В следующем аспекте настоящего изобретения можно перечислить следующие соединения, входящие без ограничения в сферу применения настоящего изобретения:
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[3-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{2-метил-4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[4-(2-этил-[1,3′]бипирролидинил-1′-ил)-2-фторфенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-(2-изопропил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-(2-пропил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{2-фтор-4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((S)-2-метил-[1,4′]бипиперидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{4-[4-(2-изопропилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-{4-[4-(2-пропилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[4-(2-метоксиметил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[3-фтор-4-(2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-{4-[4-(2-этилпирролидин-1-ил)-пиперидин-1-ил]-2-трифторметилфенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-{4-[4-(2-изопропилпирролидин-1-ил)-пиперидин-1-ил]-2-трифторметилфенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[4-(2-пропил-[1,3′]бипирролидинил-1′-ил)-2-трифторметилфенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-2-трифторметилфенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-2-трифторметилфенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[4-((S)-2-метил-[1,4′]бипиперидинил-1′-ил)-2-трифторметилфенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{2-этил-4-[4-(2-пропилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-{2-этил-4-[4-(2-метоксиметилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-этил-4-((2S,3S′)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-(2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-фтор-4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-фтор-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он; и
2-[2-фтор-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он.
Все вышеперечисленные соединения могут также включать, где это возможно, соответствующие соли, в том числе их фармацевтически приемлемые соли.
В следующем аспекте настоящего изобретения можно перечислить следующие соединения, входящие без ограничения в сферу применения соединения с формулой (I) настоящего изобретения:
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[3-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{2-метил-4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{2-фтор-4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((S)-2-метил-[1,4′]бипиперидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-{4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-фенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[3-фтор-4-(2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-{4-[4-((S)-2-метилпирролидин-1-ил)-пиперидин-1-ил]-2-трифторметилфенил}-8-окса-2-азаспиро[4.5]декан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-2-трифторметилфенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[4-((S)-2-метил-[1,4′]бипиперидинил-1′-ил)-2-трифторметилфенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-этил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-мeтил-4-((2R,3′S)-2-мeтил-[1,3′]бипиppoлидинил-1′-ил)-фeнил]-9-oкca-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-фтор-4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-фтор-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он; и
2-[2-фтор-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5,5]ундекан-1-он.
Все возможные соли вышеперечисленных соединений, в том числе фармацевтически приемлемые соли, также являются частью настоящего изобретения.
В следующем аспекте настоящего изобретения можно перечислить следующие соединения, входящие в сферу применения настоящего изобретения:
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[3-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-мeтил-4-((2R,3′S)-2-мeтил-[1,3′]бипиppoлидинил-1′-ил)-фeнил]-8-oкca-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[3-фтор-4-(2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-2-трифторметилфенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-этил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-метил-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-фтор-4-((2R,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-фтор-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он; и
2-[2-фтор-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он.
Все возможные соли вышеперечисленных соединений, в том числе фармацевтически приемлемые соли, также являются частью настоящего изобретения.
В следующем аспекте настоящего изобретения можно перечислить следующие соединения, входящие в сферу применения настоящего изобретения:
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-этил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[2-фтор-4-((2R,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он; и
2-[2-фтор-4-((2S,3′R)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он.
Все возможные соли вышеперечисленных соединений, в том числе фармацевтически приемлемые соли, также являются частью настоящего изобретения.
В следующем аспекте настоящего изобретения можно перечислить следующие соединения, входящие в сферу применения настоящего изобретения:
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-метил-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он;
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-8-окса-2-азаспиро[4.5]декан-1-он;
2-[2-фтор-4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он; и
2-[4-((2S,3′S)-2-метил-[1,3′]бипирролидинил-1′-ил)-фенил]-9-окса-2-азаспиро[5.5]ундекан-1-он.
Все возможные соли вышеперечисленных соединений, в том числе фармацевтически приемлемые соли, также являются частью настоящего изобретения.
Еще в одном аспекте настоящего изобретения соединение настоящего изобретения может быть представлено определенной стереоизомерической формой формулы (II)
где R1, R2, m, n и р представлены в соответствии с определениями выше.
Соединения настоящего изобретения могут быть синтезированы любым из известных специалистам методов. В частности, некоторые исходные материалы, используемые при получении соединений настоящего изобретения, являются известными или коммерчески доступными. Соединения настоящего изобретения и некоторые исходные соединения также могут быть получены методами, используемыми для получения аналогичных соединений, как сообщается в литературе, а также как описано далее в настоящем документе. См., например, R.С.Larock, "Comprehensive Organic Transformations," VCH publishers, 1989.
Также хорошо известно, что в различных органических реакциях может возникать необходимость защитить реакционные функциональные группы, например аминогруппы, чтобы избежать их нежелательного участия в реакциях. Обычные защитные группы могут использоваться в соответствии со стандартными процедурами, известными специалистам в области, например, см. T.W.Greene and P.G.M.Wuts в "Protective Groups in Organic Chemistry" John Wiley and Sons, Inc., 1991. Например, подходящие аминозащитные группы включают, без ограничения, сульфонил (напр., тозил), ацил (напр., бензилоксикарбонил или т-бутоксикарбонил) и арилалкил (напр., бензил), которые могут быть впоследствии удалены гидролизом или гидрированием, в зависимости от конкретного случая. Другие подходящие аминозащитные группы включают трифторацетил [-С(=O)CF3], который может быть удален катализируемым основаниями гидролизом, или твердофазная полимерно-связанная бензильная группа, такая как связанная с полимером Меррифилда 2,6-диметоксибензильная группа (линкер Элмана) или 2,6-диметокси-4-[2-(полистирилметокси)этокси]бензил, который может быть удален кислотно-катализируемым гидролизом, например ТФК.
Более конкретно, описанные в настоящем документе соединения и различные предшественники, использованные для них, могут быть синтезированы при помощи следующих методов, указанных в схемах 1-7, где R1, R2, m, n и p соответствуют определениям, приведенным для формулы I, если не указано иное.
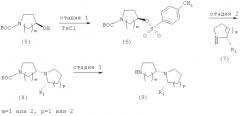
Например, на схеме 1 приведен пример получения промежуточного соединения с формулой (4), в котором R1, m и p соответствуют определению в настоящем документе. Сначала в стадии 1, схема 1, подходящим образом защищенный (например, трет-бутоксикарбонилом (Boc)) пирролидинон с формулой (1) конденсируется с искомым замещенным пирролидином с формулой (2) любыми известными методами восстановительного аминирования для образования промежуточного соединения с формулой (3). Так, подобные реакции конденсации обычно протекают в присутствии восстанавливающих агентов, таких как триацетоксиборгидрид, в инертной атмосфере, например в атмосфере азота. Реакция может протекать при значениях температуры и давления ниже комнатных, при комнатных значениях или при значениях выше комнатных. Обычно такие реакции протекают при комнатной температуре и атмосферном давлении азота. Реакционную смесь затем обрабатывают при помощи процессов, известных специалистам в данной области, для выделения промежуточного соединения с формулой (3).
На стадии 2 схемы 1 у промежуточного соединения (3) затем удаляются защитные группы для образования искомого [1,3′]-пирролидинилпирролидина с формулой (4). Такие реакции удаления защитных групп обычно протекают в кислой среде, например, в присутствии соляной кислоты, при температуре ниже комнатной до комнатной температуры, например, в диапазоне температур от примерно -10°С до комнатной температуры. Однако также могут использоваться другие подходящие температуры реакции, в зависимости от характера промежуточного соединения с формулой (3).
Схема 1
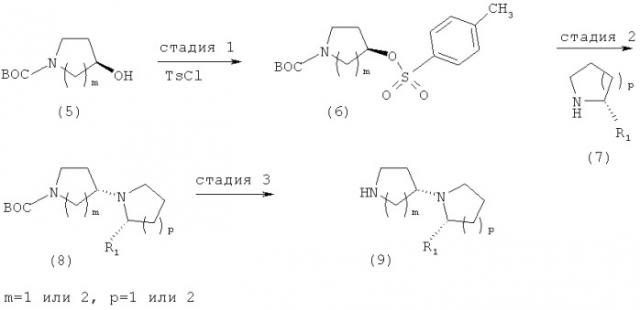
На схеме 2 приведен пример получения энантиомерически чистых изомеров [1,3′]-пирролидинилпирролидина с формулой (9), в котором R1, m и p соответствует определению в настоящем документе. На стадии 1 схемы 2 подходящим образом защищенный (например, Boc) пирролидиновый или пиперидиновый спирт с формулой (5) обрабатывается п-толуолсульфонилхлоридом для образования промежуточного соединения с формулой (6). Данная реакция может проводиться с использованием любого метода, известного специалистам в области, например проведение реакции в присутствии подходящего основания, например триэтиламина и DMAP в подходящем органическом растворителе, предпочтительно апротонном растворителе, например дихлорметане, при температурах ниже температуры окружающей среды или равных ей.
На стадии 2 схемы 2 промежуточное соединение с формулой (6) конденсируется с искомым пирролидином или пиперидином с формулой (7). Такие реакции конденсации также могут быть проведены с использованием любого известного специалистам метода для получения промежуточного соединения с формулой (8). Как правило, такие реакции конденсации проводятся в присутствии основания, например карбоната калия, в присутствии растворителей, таких как ацетонитрил, при температуре окружающей среды или повышенной температуре.
На стадии 3 схемы 2 промежуточное соединение с формулой (8) затем реагирует с кислотой, например соляной кислотой, в подходящем растворителе, например диоксане, с образованием искомого стереоспецифического изомера промежуточного соединения с формулой (9). К настоящему времени установлено, что промежуточные соединения с формулой (9) могут легко получаться в соответствии с процессом настоящего изобретения с высокой энантиомерной чистотой, причем конкретные детали настоящего процесса приводятся ниже в настоящем документе в различных примерах. В общем случае, энантиомерную чистоту можно определить посредством хиральной ВЭЖХ.
Схема 2
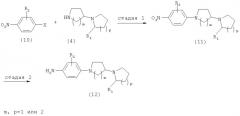
На схеме 3 приведен пример получения промежуточного аминофенилпирролидинилпирролидина с формулой (12), в котором R1, R2, m и p соответствуют определению в настоящем документе. На стадии 1 схемы 3 надлежащим образом замещенный нитробензол с формулой (10), в котором X, обозначающий приемлемую уходящую группу, например Cl, F, Br или трифлат (OTf), конденсируется с [1,3′]-пирролидинилпирролидином с формулой (4) для получения промежуточного соединения с формулой (11). Такие реакции восстановления также могут проводиться с использованием любого из известных в данной области методов. Например, такая реакция замещения может проводиться в полярном растворителе, таком как ДМСО, в присутствии такого основания, как карбонат калия, при комнатной температуре или при температуре, превышающей комнатную.
На стадии 2 схемы 3 промежуточное соединение с формулой (11) восстанавливается путем гидрирования или другими известными химическими методами, например путем использования двухлористого олова в соляной кислоте, для образования основного промежуточного соединения (12).
Схема 3
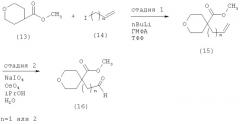
На схеме 4 приведен пример получения соединений с формулой (16). На стадии 1 схемы 4 коммерчески доступные эфиры тетрагидропиран-4-карбоновой кислоты, например метиловый или этиловый эфир формулы (13), обрабатывают соответствующим основанием, таким как nBuLi, в присутствии ГМФА в ТГФ, с последующим добавлением алкенилгалогенидов, для получения промежуточного соединения с формулой (15). Данная реакция может проводиться с использованием любого метода, известного специалистам в области, например, описанного в литературе (Nagumo S., Matoba A. et al., Tetrahedron, 2002, 58(49), 9871-9877; Stafford J.A.; Heathcock С.H. J. Org. Chem., 1990, 55(20), 5433-5434). На стадии 2 схемы 4 алкен (15) расщепляют при помощи OsO4 и NaIO4 на пропанол и воду с образованием альдегида (16).
Схема 4
Соединения настоящего изобретения могут быть получены при помощи промежуточных соединений, приготовляемых в соответствии со схемами 1-4, и затем с использованием способа (А) или способа (В), как более подробно показано ниже.
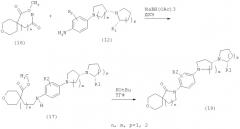
На схеме 5 показан способ получения соединений настоящего изобретения с использованием способа (А). На стадии 1 схемы 5 альдегид с формулой (16) конденсируют с искомым промежуточным соединением с формулой (12) любыми известными методами восстановительного аминирования для образования промежуточного соединения с формулой (17). Так, подобные реакции конденсации обычно протекают в присутствии восстанавливающих агентов, таких как триацетоксиборгидрид, в инертной атмосфере, например в атмосфере азота. Реакция может протекать при температуре и давлении ниже комнатных, при комнатных или при температуре и давлении выше комнатных. Обычно такие реакции протекают при комнатной температуре и атмосферном давлении азота. Реакционную смесь затем обрабатывают при помощи процессов, известных специалистам в данной области, для выделения промежуточного соединения с формулой (17). Затем вызывают циклизацию каталитическим количеством основания, например трет-бутоксида калия, в апротонных растворителях, таких как ТГФ, для образования соединений с формулой (18).
Способ (А)
Схема 5
На схемах 6 и 7 показан способ получения соединений настоящего изобретения с использованием способа (В). Альдегид с формулой (16) конденсируют с искомым коммерчески доступным бромидом с формулой (19) любыми известными методами восстановительного аминирования для образования промежуточного соединения с формулой (20). Так, подобные реакции конденсации обычно протекают в присутствии восстанавливающих агентов, таких как триацетоксиборгидрид, в инертной атмосфере, например в атмосфере азота. Реакция может протекать при температуре и давлении ниже комнатных, при