Соединения и фармацевтические композиции для лечения вирусных инфекций
Иллюстрации
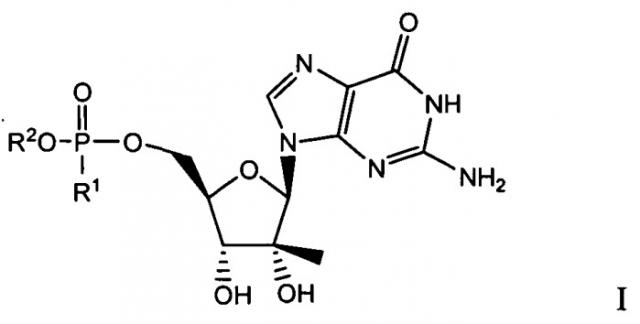
Показать всеИзобретение относится к производным нуклеозидов, композициям на их основе и способам лечения расстройств печени, опосредованных инфекцией Flaviviridae, включая гепатит С. Указанные производные нуклеозидов включают
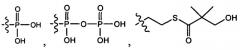
где R1 представляет собой гидроксил, амино или бензиламино; и R2 представляет собой водород,
, , или , и когда R1 представляет собой гидроксил, R2 отличен от водорода, и, , когда R1 представляет собой бензиламино, R2 отличен от .
Предложены новые эффективные противовирусные соединения. 11 н. и 32 з.п. ф-лы, 64 табл., 18 пр., 6 ил.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА СВЯЗАННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет на основании заявок США № 61/133844, поданной 2 июля 2008 года, и 61/147722, поданной 27 января 2009 года, содержание каждой из которых включено в настоящий документ в качестве ссылки в полном объеме.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
В настоящем документе представлены соединения, способы и фармацевтические композиции для применения в лечении вирусных инфекций, включая инфекцию вирусом гепатита C и инфекцию вирусом гепатита B, у хозяина, нуждающегося в этом.
УРОВЕНЬ ТЕХНИКИ
Вирусы Flaviviridae
Семейство вирусов Flaviviridae включает по меньшей мере три различных рода: пестивирусы, которые вызывают заболевания у крупного рогатого скота и свиней; флавивирусы, которые являются основной причиной таких заболеваний, как лихорадка денге и желтая лихорадка; и гепацивирусы, единственным представителем которого является HCV. Род флавивирусов включает более 68 представителей, разделенных на группы на основе серологической родственности (Calisher et al., J. Gen. Virol, 1993, 70, 37-43). Клинические симптомы варьируют и включают лихорадку, энцефалит и геморрагическую лихорадку (Fields Virology, Editors: Fields, B. N., Knipe, D. M., and Howley, P. M., Lippincott-Raven Publishers, Philadelphia, PA, 1996, Chapter 31, 931-959). Представляющие мировой интерес флавивирусы, которые ассоциированы с заболеванием у человека, включают вирусы геморрагической лихорадки денге (DHF), вирус желтой лихорадки, вирус синдрома шока и японского энцефалита (Halstead, S. B., Rev. Infect. Dis., 1984, 6, 251-264; Halstead, S. B., Science, 239:476-481, 1988; Monath, T. P., New Eng. J. Med, 1988, 319, 641-643).
Род пестивирусов включает вирус вирусной диареи крупного рогатого скота (BVDV), вирус классической свиной лихорадки (CSFV, также называемый вирусом холеры свиней) и вирус пограничной болезни (BDV) овец (Moennig, V. et al. Adv. Vir. Res. 1992, 41, 53-98). Инфекции пестивирусом домашнего скота (крупного рогатого скота, свиней и овец) вызывают существенные экономические потери по всему миру. BVDV вызывает заболевание слизистой оболочки крупного рогатого скота и имеет большое экономическое значение в промышленном животноводстве (Meyers, G. and Thiel, H.-J., Advances in Virus Research, 1996, 47, 53-118; Moennig V., et al., Adv. Vir. Res. 1992, 41, 53-98). Пестивирусы человека не настолько широко охарактеризованы, как пестивирусы животных. Однако серологические исследования указывают на значительное воздействие пестивирусов на человека.
Пестивирусы и гепацивирусы являются близкородственными группами вирусов в семействе Flaviviridae. Другие близкородственные вирусы в этом семействе включают вирус-A GB, подобные вирусу-A GB агенты, вирус-B GB и вирус-C GB (также называемый вирусом гепатита G, HGV). Группа гепацивирусов (вирус гепатита C; HCV) состоит из ряда близкородственных, но генотипически отличающихся вирусов, которые инфицируют людей. Существует приблизительно 6 генотипов HCV и более 50 субтипов. Вследствие сходства между пестивирусами и гепацивирусами в сочетании с низкой способностью гепацивирусов расти эффективно в клеточной культуре, часто в качестве заместительного вируса для исследования вируса HCV используют вирус вирусной диареи крупного рогатого скота (BVDV).
Генетическая организация пестивирусов и гепацивирусов является высоко сходной. Эти РНК-вирусы с положительными цепями имеют одну большую открытую рамку считывания (ORF), кодирующую все вирусные белки, необходимые для репликации вируса. Эти белки экспрессируются в качестве полибелка, который котрансляционно и посттрансляционно процессируется как клеточными, так и кодируемыми вирусом протеазами с образованием зрелых вирусных белков. Вирусные белки, ответственные за репликацию вирусной геномной РНК, расположены около C-конца. Две трети ORF называют неструктурными (NS) белками. Генетическая организация и процессинг полибелка в неструктурной части белка ORF для пестивирусов и гепацивирусов являются высоко сходными. Как для пестивирусов, так и для гепацивирусов зрелые неструктурные (NS) белки, в последовательном порядке от N-конца кодирующей неструктурные белки области к С-концу ORF, состоят из p7, NS2, NS3, NS4A, NS4B, NS5A и NS5B.
NS-белки пестивирусов и гепацивирусов обладают доменами с общими последовательностями, которые являются характерными для определенных белковых функций. Например, белки NS3 вирусов в обеих группах обладают мотивами аминокислотной последовательности, характерными для сериновых протеаз и хеликаз (Gorbalenya et al. (1988) Nature 333:22; Bazan and Fletterick (1989) Virology 171:637-639; Gorbalenya et al. (1989) Nucleic Acid Res. 17, 3889-3897). Аналогично, белки NS5B пестивирусов и гепацивирусов имеют мотивы, характерные для РНК-направленных РНК-полимераз (Koonin, E.V. and Dolja, V.V. (1993) Crit. Rev. Biochem. Molec. Biol. 28:375-430).
Истинные роли и функции NS-белков пестивирусов и гепацивирусов в жизненном цикле вирусов являются полностью аналогичными. В обоих случаях сериновая протеаза NS3 отвечает за протеолитический процессинг предшественников полибелков ниже ее положения в ORF (Wiskerchen and Collett (1991) Virology 184:341-350; Bartenschlager et al. (1993) J. Virol. 67:3835-3844; Eckart et al. (1993) Biochem. Biophys. Res. Comm. 192:399-406; Grakoui et al. (1993); J. Virol. 67:2832-2843; Grakoui et al. (1993) Proc. Natl. Acad. Sci. USA 90:10583-10587; Hijikata et al. (1993) J. Virol. 67:4665-4675; Tome et al. (1993) J. Virol. 67:4017-4026). Белок NS4A в обоих случаях действует в качестве кофактора для сериновой протеазы NS3 (Bartenschlager et al. (1994) J. Virol. 68:5045-5055; Failla et al. (1994) J. Virol. 68: 3753-3760; Lin et al. (1994) 68:8147-8157; Xu et al. (1997) J. Virol. 71:5312-5322). Белок NS3 обоих вирусов также выполняет функцию хеликазы (Kim et al. (1995) Biochem. Biophys. Res. Comm. 215: 160-166; Jin and Peterson (1995) Arch. Biochem. Biophys., 323:47-53; Warrener and Collett (1995) J. Virol. 69:1720-1726). Наконец, белки NS5B пестивирусов и гепацивирусов имеют предсказанную активность РНК-направленной РНК полимеразы (Behrens et al. (1996) EMBO J. 15:12-22; Lchmann et al. (1997) J. Virol. 71:8416-8428; Yuan et al. (l997) Biochem. Biophys. Res. Comm. 232:231-235; Hagedorn, PCT WO 97/12033; патенты США № 5981247; 6248589 и 6461845 Zhong et al. (1998) J. Virol. 72, 9365-9369).
Вирус гепатита C
Вирус гепатита C (HCV) является основной причиной хронического заболевания печени во всем мире. (Boyer, N. et al. J. Hepatol. 32:98-112, 2000). HCV обусловливает медленнорастущую вирусную инфекцию, и он является основной причиной цирроза и печеночно-клеточной карциномы (Di Besceglie, A. M. and Bacon, B. R., Scientific American, Oct.: 80-85, (1999); Boyer, N. et al. J. Hepatol. 32:98-112, 2000). Согласно оценкам 170 миллионов по всему миру инфицировано HCV. (Boyer, N. et al. J. Hepatol. 32:98-112, 2000). В США цирроз, вызываемый хронической инфекцией гепатитом C, является причиной 8000-12000 смертей в год, и инфекция HCV является основным показанием для трансплантации печени.
Известно, что HCV является причиной по меньшей мере 80% просттрансфузионного гепатита и значительной части спорадического острого гепатита. Предварительные данные также указывают на участие HCV во многих случаях "идиопатического" хронического гепатита, "криптогенного" цирроза и, вероятно, печеночно-клеточной карциномы, не связанной с другими вирусами гепатита, такими как вирус гепатита B (HBV). Небольшая доля здоровых людей, по-видимому, являются хроническими носителями HCV, варьируя по географии и другим эпидемиологическим факторам. Их количества могут существенно превышать эти количества для HBV, хотя информация все еще является предварительной; неясно, сколько из этих людей имеют бессимптомное хроническое заболевание печени. (The Merck Manual, 18th ed., (2006)).
HCV является оболочечным вирусом, содержащим геном из положительной одноцепочечной РНК размером приблизительно 9,4 т.п.н. Геном вируса состоит из 5'-нетранслируемой области (UTR), длинной открытой рамки считывания, кодирующей полибелок-предшественник приблизительно из 3011 аминокислот, и короткой 3'-UTR. 5'-UTR является наиболее высоко консервативной частью генома HCV, и она важна для инициации и контроля трансляции полибелка. Трансляция генома HCV инициируется независимым от кэппирования механизмом, известным как внутренняя посадка рибосомы. Этот механизм вовлекает связывание рибосом с последовательностью РНК, известной как участок внутренней посадки рибосомы (IRES). Недавно было определено, что структура псевдоузла РНК является необходимым структурным элементом IRES HCV. Вирусные структурные белки включают нуклеокапсидный коровый белок (C) и два гликопротеина оболочки, E1 и E2. HCV также кодирует две протеазы, цинкзависимую металлопротеиназу, кодируемую областью NS2-NS3, и сериновую протеазу, кодируемую областью NS3. Эти протеазы требуются для расщепления определенных областей полибелка-предшественника на зрелые пептиды. С-концевая половина неструктурного белка 5, NS5B, содержит РНК-зависимую РНК-полимеразу. Функция остальных неструктурных белков, NS4A и NS4B, и функция NS5A (N-концевая половина неструктурного белка 5) остается неизвестной.
Значительная часть современных противовирусных исследований направлена на разработку усовершенствованных способов лечения хронических инфекций HCV у человека (Di Besceglie, A. M. and Bacon, B. R., Scientific American, Oct.: 80-85, (1999)).
Ввиду того факта, что инфекция HCV достигла эпидемических уровней по всему миру и имеет трагические последствия для инфицированного пациента, остается острая потребность в предоставлении новых эффективных фармацевтических средств для лечения гепатита C, которые обладают низкой токсичностью для хозяина.
Кроме того, с учетом возрастающей угрозы других инфекций flaviviridae, остается острая потребность в предоставлении новых эффективных фармацевтических средств для лечения инфекций flaviviridae.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
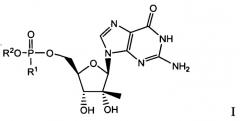
В определенных вариантах осуществления соединения, представленные в настоящем документе, представляют собой соединения формулы I
или их фармацевтически приемлемую соль, сольват, гидрат, стереоизомерную или таутомерную форму, где R1 представляет собой гидроксил, амино или бензиламино; и R2 представляет собой водород, или так что когда R1 представляет собой гидроксил, R2 отличен от водорода, и, и когда R1 представляет собой бензиламино, R2 отличен от
В одном варианте осуществления в настоящем документе предусматривается соединение 1a формулы:
или его фармацевтически приемлемая соль, сольват или гидрат.
В одном варианте осуществления в настоящем документе предусматривается соединение 1b формулы:
или его фармацевтически приемлемая соль, сольват или гидрат.
В определенных вариантах осуществления соединения, представленные в настоящем документе, имеют формулу VI.
или ее фармацевтически приемлемую соль, сольват, гидрат, стереоизомерную или таутомерную формы, где Ra и Rb выбраны следующим образом:
i) Ra представляет собой водород или алкил, и Rb представляет собой алкил, циклоалкил, карбоксиалкил, алкоксикарбонилалкил или диалкиламиноалкил; или
ii) Ra и Rb вместе с атомом азота, на котором они являются заместителями, образуют 3-7-членное гетероциклическое или гетероарильное кольцо, необязательно замещенное одной или двумя алкильными группами.
В определенных вариантах осуществления соединение 1 представляет собой пролекарство исходного лекарственного средства 2'-C-метилгуанозина. Иными словами, исходное лекарственное средство может образовываться путем метаболизма соединения 1 в печени, и, таким образом, исходное лекарственное средство способно накапливаться в печени хозяина.
В определенных вариантах осуществления соединения, представленные в настоящем документе, пригодны для предупреждения и лечения инфекций Flaviviridae и других родственных состояний, таких как положительные по антителам против Flaviviridae и положительные по Flaviviridae состояния, хроническое воспаление печени, вызванное HCV, цирроз, фиброз, острый гепатит, молниеносный гепатит, хронический персистирующий гепатит и утомляемость. Эти соединения или составы также можно использовать профилактически для предупреждения или замедления прогрессирования клинического заболевания у индивидов, которые являются положительными по антителам против Flaviviridae или положительными по антигенам Flaviviridae или которые подвергались воздействию Flaviviridae. В одном варианте осуществления Flaviviridae представляет собой гепатит C. В определенных вариантах осуществления соединение применяют для лечения любого вируса, который реплицируется с помощью РНК-зависимой РНК-полимеразы.
В одном варианте осуществления предусматривается способ лечения инфекции Flaviviridae у хозяина, в том числе человека, который включает введение эффективного количества соединения, представленного в настоящем документе, либо отдельно, либо в комбинации или поочередно с другим средством против Flaviviridae, необязательно в фармацевтически приемлемом носителе.
В одном аспекте соединения, описанные в настоящем документе, предоставляют или вводят в комбинации со вторым лекарственным средством, таким как средство, пригодное для лечения или предупреждения инфекций HCV. Иллюстративные лекарственные средства подробно описаны в представленных ниже разделах.
В одном варианте осуществления предусматривается способ лечения инфекции Flaviviridae у хозяина, в том числе человека, который включает введение S-(2-{[(2R,3R,4R,5R)-5-(2-амино-6-оксо-1,6-дигидропурин-9-ил)-3,4-дигидрокси-4-метилтетрагидрофуран-2-илметокси]бензиламинофосфорилокси}этилового сложного эфира) в количестве от приблизительно 1 мг/сутки до приблизительно 150 мг/сутки, либо отдельно, либо в комбинации или поочередно с другим средством против Flaviviridae, необязательно в фармацевтически приемлемом носителе.
В другом варианте осуществления в настоящем документе предусматривается способ лечения инфекции Flaviviridae у хозяина, в том числе человека, который включает введение S-(2-{[(2R,3R,4R,5R)-5-(2-амино-6-оксо-1,6-дигидропурин-9-ил)-3,4-дигидрокси-4-метилтетрагидрофуран-2-илметокси]бензиламинофосфорилокси}этилового сложного эфира) в количестве от приблизительно 1 мг/сутки до приблизительно 150 мг/сутки, в комбинации или поочередно с терапевтически эффективным количеством рибавирина, необязательно в фармацевтически приемлемом носителе. В одном варианте осуществления вводимое количество рибавирина составляет от приблизительно 800 мг до приблизительно 1400 мг.
В другом аспекте предусматриваются фармацевтические композиции, стандартные лекарственные формы и наборы, пригодные для применения для лечения или предупреждения расстройств, таких как инфекции HCV, которые содержат терапевтически или профилактически эффективное количество соединения, описанного в настоящем документе, и терапевтически или профилактически эффективное количество второго лекарственного средства, такое как лекарственное средство, пригодное для лечения или предупреждения инфекций HCV.
В определенных вариантах осуществления предусматривается способ лечения расстройства печени, включающий введение индивиду, нуждающемуся в таком лечении, эффективного количества соединения, представленного в настоящем документе.
В некоторых вариантах осуществления в настоящем документе предусматриваются
(a) соединения, как описано в настоящем документе, и их фармацевтически приемлемые соли и композиции;
(b) соединения, как описано в настоящем документе, и их фармацевтически приемлемые соли и композиции для применения для лечения и/или профилактики расстройства печени, в том числе инфекции Flaviviridae, особенно у индивидов, у которых диагностировано наличие инфекции Flaviviridae или которые имеют риск инфицирования гепатитом C;
(c) способ получения соединений, как описано в настоящем документе;
(d) фармацевтические препараты, содержащие соединение, как описано в настоящем документе, или его фармацевтически приемлемую соль вместе с фармацевтически приемлемым носителем или разбавителем;
(e) фармацевтические препараты, содержащие соединение, как описано в настоящем документе, или его фармацевтически приемлемую соль вместе с одним или несколькими другими эффективными средствами против HCV, необязательно в фармацевтически приемлемом носителе или разбавителе;
(f) способ лечения и/или профилактики у хозяина инфекции Flaviviridae, который включает введение эффективного количества соединения, как описано в настоящем документе, его фармацевтически приемлемой соли или композиции; и
(g) способ лечения и/или профилактики у хозяина инфекции Flaviviridae, который включает введение эффективного количества соединений, как описано в настоящем документе, их фармацевтически приемлемых солей или композиций в комбинации и/или поочередно с одним или несколькими эффективными средствами против HCV.
Flaviviridae, от которых можно лечить, рассмотрены, например, главным образом, в Fields Virology, Editors: Fields, B. N., Knipe, D. M., and Howley, P. M., Lippincott-Raven Publishers, Philadelphia, PA, Chapter 31, 1996. В конкретном варианте осуществления Flaviviridae представляет собой HCV. В альтернативном варианте осуществления Flaviviridae представляет собой флавивирус или пестивирус. Конкретные флавивирусы включают, но не ограничиваются ими: Абсеттаров, Алфуи, Апои, Ароа, Багаза, Банзи, Боубоуи, Буссуквара, Касипакор, острова Керри, летучих мышей Дакара, денге 1, денге 2, денге 3, денге 4, Эдж-хилл, летучих мышей Энтеббе, Гаджетс Галли, Гансалова, Гипр, Ильеус, менингоэнцефалита индюков Израиля, японского энцефалита, Югры, Джутиапа, Кадама, Карши, Кедоугоу, Кокобера, Коутангу, Кумлинге, Кунжин, киасанурской лесной болезни, Лангат, шотландского энцефалита овец, Мибан, Модока, лейкоэнцефалита Монтана-Миотис, энцефалита долины Муррей, Наранжал, Негиши, Нтайя, омской геморрагической лихорадки, летучих мышей Пномпеня, Повассан, Рио-Браво, Росио, Ройял-Фарм, русского весенне-летнего клещевого энцефалита, Сабойи, энцефалита Сент-Луис, Сал-Виеджа, Сан Перлита, рифов Саумарез, Сепик, Сокулук, Спондвени, Стратфорд, Тембусу, Тюлений, Уганда S, Усуту, Вессельсброна, западного Нила, Яунде, желтой лихорадки и Зика.
Пестивирусы, от которых можно лечить, рассмотрены, главным образом, в Fields Virology, Editors: Fields, B. N., Knipe, D. M., and Howley, P. M., Lippincott-Raven Publishers, Philadelphia, PA, Chapter 33, 1996. Конкретные пестивирусы включают, но не ограничиваются ими, вирус вирусной диарии крупного рогатого скота ("BVDV"), вирус классической свиной лихорадки ("CSFV", также называемый вирусом холеры свиней) и вирус пограничной болезни ("BDV").
КРАТКОЕ ОПИСАНИЕ ФИГУР
На ФИГ. 1 представлена хроматограмма ВЭЖХ, иллюстрирующая разделение двух диастереомеров соединения 1 с помощью обращенно-фазовой ВЭЖХ - два пика на записи: пик 1 (диастереомер 1) и пик 2 (диастереомер 2), соответствуют диастереомерам соединения 1.
На ФИГ. 2 представлена иллюстративная хроматограмма ВЭЖХ для соединения 1 и стандартов метаболитов, полученных способом 1 примера 14.
На ФИГ. 3 представлена иллюстративная хроматограмма ВЭЖХ соединения 1 и стандартов метаболитов, полученных способом 2 примера 15.
На ФИГ. 4 представлена иллюстративная хроматограмма ВЭЖХ соединения 1 и стандартов метаболитов, полученных способом 2 примера 16.
На ФИГ. 5 представлен результат анализа MacSynergyTM II (независимость Bliss) для пяти индивидуальных групп экспериментальных данных при 99,9% доверительном интервале.
На ФИГ. 6 представлены различия между вычисленными аддитивными и наблюдаемыми эффектами против HCV для всех комбинаций лекарственных средств из 5 независимых экспериментов, которые были получены с помощью программного обеспечения CombiTool с использованием модели аддитивности Loewe.
ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
В настоящем документе представлены соединения, композиции и способы, пригодные для лечения расстройств печени, таких как инфекция HCV, у индивидуума. Кроме того, представлены лекарственные формы, пригодные для таких способов.
Определения
При описании соединений, представленных в настоящем документе, представленные ниже термины имеют следующие значения, если нет иных указаний.
"Фармацевтически приемлемая соль" включает любую соль соединения, представленного в настоящем документе, которая сохраняет его биологические свойства и которая не является токсичной или иным образом нежелательной для фармацевтического применения. Такие соли можно получать из множества органических и неорганических противоионов, хорошо известных в данной области. Такие соли включают (1) кислотно-аддитивные соли, образованные с органическими или неорганическими кислотами, такими как хлористоводородная, бромистоводородная, серная, азотная, фосфорная, сульфаминовая, уксусная, трифторуксусная, трихлоруксусная, пропионовая, капроновая, циклопентилпропионовая, гликолевая, глутаровая, пировиноградная, молочная, малоновая, янтарная, сорбиновая, аскорбиновая, яблочная, малеиновая, фумаровая, вино-каменная, лимонная, бензойная, 3-(4-гидроксибензоил)бензойная, пикриновая, коричная, миндальная, фталевая, лауриновая, метансульфоновая, этансульфоновая, 1,2-этандисульфоновая, 2-гидроксиэтансульфоновая, бензолсульфоновая, 4-хлорбензолсульфоновая, 2-нафталинсульфоновая, 4-толуолсульфоновая, камфорная, камфорсульфоновая, 4-метилбицикло[2.2.2]-окт-2-ен-1-карбоновая, глюкогептоновая, 3-фенилпропионовая, триметилуксусная, трет-бутилуксусная, лаурилсерная, глюконовая, бензойная, глутаминовая, гидроксинафтойная, салициловая, стеариновая, циклогексилсульфаминовая, хинная, муконовая кислота и сходные с ними кислоты; или (2) соли, образованные, когда кислотный протон, присутствующий в исходном соединении, либо (a) заменяется ионом металла, например, ионом щелочного металла, ионом щелочноземельного металла или ионом алюминия, или гидроксидами щелочных металлов или щелочноземельных металлов, такими как гидроксид натрия, калия, кальция, магния, алюминия, лития, цинка и бария, аммиаком, либо (b) координируется с органическим основанием, таким как алифатическим, алициклические или ароматические органические амины, такие как аммиак, метиламин, диметиламин, диэтиламин, пиколин, этаноламин, диэтаноламин, триэтаноламин, этилендиамин, лизин, аргинин, орнитин, холин, N,N'-дибензилэтилендиамин, хлорпрокаин, диэтаноламин, прокаин, N-бензилфенэтиламин, N-метилглюкаминпиперазин, трис(гидроксиметил)аминометан, гидроксид тетраметиламмония и т.п.
Кроме того, соли включают, только в качестве примера, соли натрия, калия, кальция, магния, аммония, тетраалкиламмония и т.п., и когда соединение содержит основную функциональную группу, соли нетоксических органических или неорганических кислот, такие как гидрогалогениды, например гидрохлорид и гидробромид, сульфат, фосфат, сульфамат, нитрат, ацетат, трифторацетат, трихлорацетат, пропионат, гексаноат, циклопентилпропионат, гликолят, глутарат, пируват, лактат, малонат, сукцинат, сорбат, аскорбат, малат, малеат, фумарат, тартрат, цитрат, бензоат, 3-(4-гидроксибензоил)бензоат, пикрат, циннамат, манделат, фталат, лаурат, метансульфонат (мезилат), этансульфонат, 1,2-этандисульфонат, 2-гидроксиэтансульфонат, бензолсульфонат (безилат), 4-хлорбензолсульфонат, 2-нафталинсульфонат, 4-толуолсульфонат, камфорат, камфорсульфонат, 4-метилбицикло[2.2.2]-окт-2-ен-1-карбоксилат, глюкогептонат, 3-фенилпропионат, триметилацетат, трет-бутилацетат, лаурилсульфат, глюконат, бензоат, глутамат, гидроксинафтоат, салицилат, стеарат, циклогексилсульфамат, хинат, муконат и т.п.
Термин "чистый" или "очищенный" в отношении соединения, предоставленного в настоящем документе, включает композицию, которая включает по меньшей мере от 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, 99,5%, 99,8%, 99,9% до 100% по массе, соединения, а остальная часть содержит другие химические вещества или диастереомеры. Как используют в настоящем документе термин "чистый", когда его применяют к хиральному соединению, относится к энантиомеру или диастереомеру хирального соединения, по существу, не содержащему его противоположного энантиомера или диастереомера (т.е. в энантиомерном или диастереомерном избытке). Например, чистая "R"-форма соединения по существу не содержит "S"-формы соединения и, таким образом, находится в энантиомерном или диастереомерном избытке относительно "S"-формы. Термин "энантиомерно или диастереомерно чистый" или "чистый энантиомер или диастереомер" означает, что соединение содержит избыток энантиомера или диастереомера, например, более 75% по массе, более 80% по массе, более 85% по массе, более 90% по массе, более 91% по массе, более 92% по массе, более 93% по массе, более 94% по массе, более 95% по массе, более 96% по массе, более 97% по массе, более 98% по массе, более 98,5% по массе, более 99% по массе, более 99,2% по массе, более 99,5% по массе, более 99,6% по массе, более 99,7% по массе, более 99,8% по массе или более 99,9% по массе энантиомера или диастереомера. В определенных вариантах осуществления масса представлена в расчете на общую массу соединения, т.е. всех энантиомеров или диастереомеров соединения. В определенных вариантах осуществления один энантиомер или диастереомер может быть в избытке на 30-80% или на 30-70%, 30-60%, 30%, 35%, 40%, 45%, 50%, 55% или 60%, или на любой процент между этими значениями.
Аналогично термин "выделенный" в отношении соединения включает композицию, которая включает по меньшей мере от 75%, 80%, 85%, 90%, 95%, 98%, 99% до 100% по массе, соединения, а остальная часть содержит другие химические вещества или энантиомеры или диастереомеры.
"Сольват" включает соединение, представленное в настоящем документе, или его соль, которая, кроме того, включает стехиометрическое или нестехиометрическое количество растворителя, связанного нековалентными межмолекулярными силами. Когда растворитель представляет собой воду, сольват представляет собой гидрат.
Термин "хозяин", как используют в настоящем документе, включает любой одноклеточный или многоклеточный организм, в котором может реплицироваться вирус, включая клеточные линии и животных, и предпочтительно человека. Альтернативно хозяин может содержать часть генома вируса Flaviviridae, репликация или функция которого могут быть изменены с помощью соединений, представленных в настоящем документе. Термин "хозяин" конкретно включает инфицированные клетки, клетки, трансфицированные всем геномом Flaviviridae или его частью, и животных, в частности, приматов (в том числе шимпанзе) и людей. В большинстве применений у животных хозяином является пациент-человек. Однако также в настоящем документе предусматриваются ветеринарные применения при определенных показаниях (например, у шимпанзе).
Как используют в настоящем документе, термины "индивидуум" и "пациент" используют в настоящем документе взаимозаменяемо. Термины "индивидуум" и "индивидуумы" относятся к животному, такому как млекопитающее, включающее не примата (например, корову, свинью, лошадь, кошку, собаку, крысу и мышь) и примата (например, обезьяну, такую как яванский макак, шимпанзе и человек), и например, человека. В одном варианте осуществления индивидуум являются рефрактерным или не отвечающим на современные способы лечения инфекции гепатитом C. В другом варианте осуществления индивидуумом является сельскохозяйственное животное (например, лошадь, корова, свинья и т.д.) или домашнее животное (например, собака или кошка). В одном варианте осуществления индивидуумом является человек.
Как используют в настоящем документе, термины "лекарственное средство" и "лекарственные средства" относятся к любому средству(ам), которое можно использовать для лечения или предупреждения расстройства или одного или нескольких его симптомов. В определенных вариантах осуществления термин "лекарственное средство" включает соединение, представленное в настоящем документе. В одном варианте осуществления лекарственное средство представляет собой средство, которое, как известно, является пригодным для лечения или предупреждения расстройства или одного или нескольких его симптомов, или средство, которое использовали или в настоящее время используют для лечения или предупреждения расстройства или одного или нескольких его симптомов.
"Терапевтически эффективное количество" включает количество соединения или композиции, которое при введении индивидууму для лечения заболевания является достаточным для осуществления такого лечения заболевания. "Терапевтически эффективное количество" может варьировать, в зависимости, помимо прочего, от соединения, заболевания и его тяжести и возраста, массы тела и т.д. индивидуума, подвергаемого лечению.
"Проведение лечения" или "лечение" любого заболевания или расстройства относится, в одном варианте осуществления, к смягчению заболевания или расстройства, которое имеется у индивидуума. В другом варианте осуществления "проведение лечения" или "лечение" включает смягчение по меньшей мере одного физического параметра, который может быть неощутимым для индивидуума. В другом варианте осуществления "проведение лечения" или "лечение" включает модулирование заболевания или расстройства, либо физически (например, стабилизация ощущаемого симптома), либо или физиологически (например, стабилизация физического параметра) или обоими путями. В другом варианте осуществления "проведение лечения" или "лечение" включает замедление начала заболевания или расстройства.
Как используют в настоящем документе, термины "профилактическое средство" и "профилактические средства" относятся к любому средству(ам), которое можно использовать для предупреждения расстройства или одного или нескольких его симптомов. В определенных вариантах осуществления термин "профилактическое средство" включает соединение, представленное в настоящем документе. В некоторых других вариантах осуществления термин "профилактическое средство" не относится к соединению, представленному в настоящем документе. Например, профилактическое средство представляет собой средство, которое известно в качестве пригодного для предупреждения или препятствования возникновению, развитию, прогрессированию и/или тяжести расстройства, или средство, которое использовали или в настоящее время используют для этого.
Как используют в настоящем документе, выражение "профилактически эффективное количество" включает количество лекарственного средства (например, профилактического средства), которое является достаточным, чтобы обеспечить предупреждение или снижение развития, рецидива или возникновения одного или нескольких симптомов, ассоциированных с расстройством (или чтобы усилить или улучшить профилактический эффект(ы) другого лекарственного средства (например, другого профилактического средства).
Как используют в настоящем документе, "изотопный состав" относится к количеству каждого изотопа, присутствующего для данного атома, и "природный изотопный состав" относится к встречающемуся в природе изотопному составу или преобладанию для данного атома. Атомы, имеющие их природный изотопный состав, могут также называться "необогащенными" атомами. Если нет иных обозначений, подразумевается, что атомы соединений, приведенных в настоящем документе, соответствуют любому стабильному изотопу этого атома. Например, если нет иных указаний, когда положение обозначено, в частности, как "H" или "водород", подразумевают, что в данном положении находится водород в соответствии с его природным изотопным составом.
Как используют в настоящем документе, "изотопно обогащенный" относится к атому, имеющему изотопный состав, отличный от природного изотопного состава для этого атома. "Изотопно обогащенный" также может относиться к соединению, содержащему по меньшей мере один атом, имеющий изотопный состав, отличный от природного изотопного состава для этого атома.
Как используют в настоящем документе "изотопное обогащение" относится к проценту включения количества конкретного изотопа данного атома в молекуле вместо изотопа этого атома, преобладающего в природе. Например, обогащение дейтерием, составляющее 1%, в данном положении, означает, что 1% молекул в данном образце содержит дейтерий в указанном положении. Поскольку встречающееся в природе распределение дейтерия составляет приблизительно 0,0156%, обогащение дейтерием в данном положении соединения, синтезированного с использованием необогащенных исходных материалов, составляет приблизительно 0,0156%. Изотопное обогащение соединений, представленных в настоящем документе, можно определять с использованием общепринятых аналитических способов, известных специалисту в данной области, включая масс-спектрометрию и ядерную магнитно-резонансную спектроскопию.
Соединения
Соединения, представленные в настоящем документе, являются производными 2'-C-метилгуанозина. Соединения пригодны для лечения и/или профилактики инфекций Flaviviridae и вирусом гепатита C.
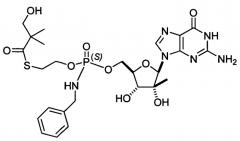
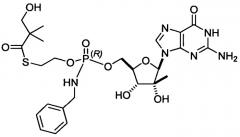
В одном варианте осуществления соединения, представленные в настоящем документе, представляют собой диастереомеры или метаболиты S-2-{[(2R,3R,4R,5R)-5-(2-амино-6-оксо-1,6-дигидропурин-9-ил)-3,4-дигидрокси-4-метилтетрагидрофуран-2-илметокси]бензиламинофосфорилокси}этилового сложного эфира 3-гидрокси-2,2-диметилтиопропионовой кислоты, обозначенного в настоящем документе как соединение 1. Соединение 1 имеет следующую структуру:
Соединение 1
В одном варианте осуществления в настоящем документе предусматривается соединение 1a, имеющее формулу:
или его фармацевтически приемлемая соль, стереоизомер, сольват или гидрат. В одном варианте осуществления в настоящем документе предусматривается чистое соединение 1a. В другом варианте осуществления в настоящем документе предусматривается диастереомерно чистое соединение 1a.
В одном варианте осуществления в настоящем документе предусматривается соединение 1b, имеющее формулу:
или его фармацевтически приемлемая соль, стереоизомер, сольват или гидрат. В одном варианте осуществления в настоящем документе предусматривается соединение 1b. В другом варианте осуществления в настоящем документе предусматривается диастереомерно чистое соединение 1b.
В одном варианте осуществления в настоящем документе предусматривается соединение формулы I:
или его фармацевтически приемлемая соль, сольват, гидрат, стереоизомерная или таутомерная форма, где R1 представляет собой гидроксил, амино или бензиламино; и R2 представляет собой водород, или так что когда R1 представляет собой гидроксил, R2 отличен от водорода, и, и когда R1 представляет собой бензиламино, R2 отличен от
В одном варианте осуществления в настоящем документе предусматривается чистое соединение формулы I.
В одном варианте осуществления в настоящем документе предусматривается соединение формулы Ia:
или его фармацевтически приемлемая соль, сольват, гидрат, стереоизомерная или таутомерная форма.
В одном варианте осуществления в настоящем документе предусматривается соединение формулы Ib:
или его фармацевтически приемлемая соль, сольват, гидрат, стереоизомерная или таутомерная форма. В одном варианте осуществления в настоящем документе предусматривается чистое соединение формулы Ia или Ib. В одном варианте осуществления в настоящем документе предусматривается диастереомерно чистое соединение формулы Ia или Ib.
В одном варианте осуществления R1 представляет собой гидроксил, амино или бензиламино. В другом варианте осуществления R1 представляет собой амино или бензиламино. В другом варианте осуществления R1 представляет собой гидрокси.
В одном варианте осуществления R2 представляет собой водород, или
В другом варианте осуществления R2 представляет собой водород, или