Производные жирных кислот для перорального введения, обеспечивающие высокие вкусовые качества
Иллюстрации
Показать всеИзобретение относится к новым производным жирных кислот с короткой цепью, в частности масляной кислоты, которые обладают физико-химическими характеристиками, подходящими для удобного перорального введения, поскольку они лишены неприятных органолептических свойств, характерных для бутирата. Новые соединения имеют удобную для взвешивания форму, устойчивы к действию кислот и щелочей и способны высвобождать кислоту в тонком и толстом кишечнике непрерывно в течение длительного времени. 4 н. и 3 з.п. ф-лы, 5 ил., 15 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к вводимым перорально производным жирных кислот, в частности, производным масляной кислоты. Изобретение также относится к составам, содержащим их, и их клиническому применению. Более конкретно, изобретение относится к новым соединениям, получаемым из масляной кислоты, полезным в случае всех известных клинических применений последней и обеспечивающим физико-химические характеристики, подходящие для удобного перорального введения, поскольку они лишены неприятных органолептических свойств, характерных для бутирата. Новые соединения, кроме того, легко синтезируются и имеют хорошую растворимость и устойчивость при хранении.
Уровень техники
Известно, что жирные кислоты с короткой цепью (ЖККЦ) являются слабыми кислотами, содержащими от 2 до 5 атомов углерода (pK 4,8), и что их эндогенная продукция происходит в результате бактериальной ферментации олиго- и полисахаридов и в меньшей степени белков, пептидов и гликопротеинов нормальной кишечной сапрофитной флорой. С количественной точки зрения, основными ЖККЦ, получаемыми в результате ферментации углеводов, являются, в следующем порядке и с указанием соответствующих анионов, бутират, ацетат, пропионат, формиат, валерат и капронат, в то время как изобутират, 2-метилизобутират и изовалерат образуются в меньших количествах посредством катаболизма аминокислот с разветвленной цепью (валина, лейцина, изолейцина). С количественной точки зрения, ЖККЦ являются наиболее важными анионами, присутствующими в просвете толстого кишечника, где достигается их концентрация выше 100 мМ. Каждая ЖККЦ обладает специфическими характеристиками и характерными физиологическими эффектами. Ежедневно в кишечнике продуцируется приблизительно 5 г бутирата, который присутствует в просвете толстого кишечника в концентрации 10-30 мМ и является основным альтернативным глюкозе источником энергии для эпителиальных клеток толстого кишечника. Действительно, 60-70% энергии, потребляемой данными клетками, производится из бутирата. Также известно, что зависимость эпителиальных клеток толстого кишечника от бутирата как источника энергии увеличивается при продвижении от дистального отдела к проксимальному отделу толстого кишечника. ЖККЦ потенциально абсорбируются каждым пищеварительным отделом кишечника, что было показано на животных моделях и у людей-добровольцев. Энтероциты способны абсорбировать бутират, пропионат и ацетат главным образом посредством диффузии неионных соединений и параклеточным всасыванием. Всасывание данных жирных кислот обладает значительным влиянием на абсорбцию NaCl и в целом на водно-электролитный баланс. В частности, бутират способен вызывать сильный стимул в отношении абсорбции на уровне кишечника в случае электронейтрального транспорта NaCl и сильный ингибирующий эффект в отношении секреции Cl-. Данное стимулирующее абсорбцию/противосекреторное регуляторное действие в отношении трансэпителиального транспорта жидкостей осуществляется посредством ряда различных механизмов, таких как
- стимулирование абсорбции NaCl посредством совместного действия двух транспортных систем, представленных в щеточной кайме энтероцита, Cl-/HCO3 - и Na+/H+ и Cl-/бутират и Na+/H+;
- ингибирование секреции Cl- посредством ингибирования активности котранспортера Na-K-2Cl (NKCC1), представленного на базолатеральной части энтероцита.
Исследования in vitro показали, что бутират обладает ингибирующим действием на секрецию Cl-, индуцируемую простагландином E2, фосфохолином и холерным токсином. Этот эффект является результатом снижения внутриклеточной продукции циклического АМФ на фоне регулирования аденилатциклазной экспрессии и активности. Сравнительные исследования демонстрируют, что стимулирующее абсорбцию действие бутирата в базальных состояниях и его ингибирующее действие на активные секреторные агенты является много больше в отношении как силы, так и продолжительности действия относительно других ЖККЦ.
Исследование in vivo на животных показали, что бутират обладает профилактическим действием в отношении возможного воспаления в кишечнике в результате диеты, богатой отрубями и волокнами, которые могут раздражающе действовать на слизистую оболочку кишечника. Подтверждение его эффективности обеспечивается тем фактом, что благодаря поддерживаемой абсорбции он дает возможность свиньям достичь оптимального веса за более короткий период времени (Mazzoni M. et al., J. Nutr., август 2008, 138(8):1426-31; Biagi G. et al., J. Anim. Sci., май 2007, 85(5):1184-91. Epub 12 февраля 2007). У человека бутират применяется в качестве диетической добавки при язвенном ректоколите благодаря его способности снижать частоту поноса и поддерживать функционирование толстого кишечника на хорошем уровне.
Помимо действия на кишечный трансэпителиальный транспорт жидкостей, бутират является сильным стимулятором трофики слизистой оболочки кишечника посредством сосудистых, гормональных и нейрональных механизмов. Понижение концентрации бутирата в кишечнике связано с увеличением воспаления слизистой оболочки и с изменениями моторики и различных функций, вовлеченных в механизм роста, дифференцировки и регенерации слизистой оболочки, в степени, приводящей к повышенному риску злокачественного новообразования. В то же время, бутират обладает способностью отрицательно регулировать рост кишечных опухолевых клеток.
В отношении конкретного примера из области гастроэнтерологии, клинические исследования, проводимые у детей с острой диареей, вызванной V. cholerae, демонстрировали уменьшение массы фекалий и более быстрое восстановление у пациентов, которым дополнительно к получению регидратирующей терапии вводили в диету резистентные амидные предшественники ЖККЦ (Ramakrishna B.S. et al., New. Engl. J. Med., 2000, 324:308-31316; Rabbani G.H., et al., Dig. Dis. Sci., 1999, 44:1547-1553). Данные результаты также были подтверждены в случае других форм инфекционной диареи у детей и в исследованиях на животных моделях (Rabbani B.S. et al., Gastroenterology, 2001, 121:554-56; Alam N.H. et al., Gastroenterology, 1997, 112:A; Alam N.H. et al., Pediatr. Лекарственные средства, 2003, 5:151-165). Механизмы данных терапевтических эффектов связаны со стимулирующим абсорбцию действием ЖККЦ, и в частности бутирата, на трансэпителиальный транспорт жидкостей в кишечнике, способный компенсировать потерю фекалий во время диареи, таким образом уменьшая продолжительность и тяжесть состояния (Sellin J.H. et al, Gastroenterology, 1998, 114:737-747; Mush M.W. et al., Am. J. Physiol. Gastrointest. Liver Physiol., 2001, 280:687-693). Благодаря его важному регуляторному действию на всасывание жидкостей в кишечнике, бутират успешно используется у пациентов с врожденной хлоридореей, тяжелым аутосомно-рецессивным генетическим заболеванием, характеризующимся тяжелой хронической диареей с неонатального возраста (Berni Canani R. et al., Gastroenterology, 2004, 127:630-63423). Данное исследование показывает, что пероральное введение бутирата, в дозе 100 мг/кг/день, способствует значительному снижению числа опорожнений/день и улучшению консистенции стула, до полной нормализации стула. Данный терапевтический эффект происходит как из-за стимуляции Cl-/бутират-котранспортера, так и регуляции механизмов синтеза и экспрессии в плазматической мембране энтероцитов молекул, ответственных за трансэпителиальный транспорт жидкостей в кишечнике. Данные свойства также делают вероятным терапевтическое применение бутирата при других заболеваниях желудочно-кишечного тракта, характеризующихся нарушениями в механизмах транспорта жидкостей и питательных веществ.
Бутират также играет центральную роль в поддержании целостности слизистой оболочки кишечника. Эксперименты in vivo на животных моделях показали, что бутират обладает трофическим действием на кишечник, обусловленным повышением уровня гастрина и зависящим от сохранности симпатической и парасимпатической нервных систем (Reilly K.J. et al., Gut., 1995, 37:81-86). Его действие на трансэпителиальный транспорт жидкостей и на трофику слизистой оболочки кишечника делает бутират потенциально идеальным терапевтическим инструментом для профилактики и лечения желудочно-кишечных расстройств в курсе лечения антибиотиками, и главным образом в случае антибиотик-ассоциированной диареи (ААД), которая поражает 15-40% субъектов, принимающих данный тип лекарственных средств (Mortensen P.B. et al., Scand. J. Gastroenterol. Suppl., 1996, 216:132-148; Krishnan S. et al., Scand. J. Gastroenterol., 1998, 33:242-246). Кроме того, действие на трансэпителиальный транспорт жидкостей и на моторику кишечника говорит в пользу терапевтического применения бутирата при лечении желудочно-кишечных функциональных расстройств, характеризующихся изменением моторики, таких как синдром раздраженного кишечника (Scarpellini E. et al., Dig. Liver Dis., 2007, Suppl. 1:19-22).
В литературе выдвигается предположение о возможном применении бутирата при лечении хронических воспалительных заболеваний кишечника. Бутират индуцирует клиническое и гистологическое заживление экспериментального колита, индуцированного посредством тринитробензолсульфоновой кислоты (Butzner J.D. et al., Gut., 1996, 38:568-573). При язвенном ректоколите (ЯРК) происходит изменение метаболизма ЖККЦ в эпителиальных клетках толстого кишечника (Roediger W.E.W., Lancet, 1980, 2:712-715), что вызывает понижение внутрипросветной концентрации данных жирных кислот. Было сделано предположение, что низкие концентрации ЖККЦ, обнаруженные у пациентов с тяжелым ЯРК, могут приводить к повреждению слизистой оболочки (Chapman M.A.S. et al., Gut., 1994, 35:73-76). В различных клинических исследованиях, бутират, вводимый местно (посредством клизмы) пациентам с ЯРК, давал положительные результаты, ускоряя клинический, эндоскопический и гистологический процесс заживления, когда вводился в комбинации с другими противовоспалительными лекарственными средствами, такими как месалазин (Scheppach et al., Dig. Dis. Sci., 1991, 36:185-187; Bruer R.I. et al., Gut., 1997, 40:485-491; Vernia P. et al., Dig. Dis. Sci., 1995, 40:305-307). Эффективность комбинации бутират/месалазин также была подтверждена в исследованиях с применением перорально вводимых составов (Vernia P. et al., Dig. Dis. Sci., 2000, 45:976-981).
В литературе существуют указания, что группы населения с низким числом случаев заболеваний толстого кишечника (также включая злокачественное новообразование толстого кишечника) имеют диету, богатую углеводами - основными предшественниками ЖККЦ. Защитное действие бутирата в отношении развития злокачественного новообразования толстого кишечника и полипоза достоверно подтверждено как in vitro, так и in vivo исследованиями: бутират в действительности способен in vitro ингибировать рост основной линии клеток опухоли толстого кишечника как путем снижения пролиферации, так и путем стимуляции дифференцировки и апоптоза. Доказано непосредственное противоопухолевое действие бутирата посредством регуляции транскрипции различных генов, вовлеченных в процесс онкогенеза (Boffa L. et al., J. Biol. Chem., 1981, 256:9612-9621; Avivi-Green C. et al., Oncol. Res., 2000, 12:83-95). Однако данное защитное действие бутирата определяется длительностью воздействия в отношении процесса онкогенеза (Basson M.D. et al., Proc. Soc. Exp. Biol. Med., 1998, 217:476-483; Hague A. et al., Int. J. Cancer, 1993, 55:498-505; Heerdt B.G. et al., Cancer Res., 1994, 54:3288-3294; Lupton J.R., Am. Soc. Nutr. Sci., 2004, 134:479-482).
Натрия 4-фенилбутират (4PBA) - аналог бутирата, вводимый перорально, рассматривается как потенциальное лекарственное средство для лечения муковисцидоза (у пациентов с мутацией ΔF 508). Действительно, 4PBA и позднее 2,2-диметилбутират (ST20) и альфа-метилгидрокоричная кислота (ST7) способны индуцировать повышенную экспрессию МВТР (трансмембранный регулятор муковисцидоза) в эпителии дыхательных путей как in vitro, так и in vivo (Rubenstein R.C. et al., J. Clin. Invest., 1997, 100:2457-2465; Nguyen T.D. et al., Biochem. Bioph. Res. Com., 2006, 342:245-252).
В гематологии бутират известен как индуктор продукции фетального гемоглобина (HbF) путем селективного стимулирования активности генов, кодирующих гамма-глобиновые цепи (Ikuta T. et al., Blood, 1998, 92:2924-2933). Данная активность привела к его применению у пациентов с промежуточной β-талассемией, у которых небольшое увеличение количества HbF индуцирует нормализацию внекостномозгового кроветворения со значительным снижением осложнений и улучшением качества жизни (Olivieri N.F. et al., Lancet, 1997, 350:491-492; Faller D.V. et al., Curr. Opin. Hematol., 1995, 2:109-117).
В первых исследованиях, проведенных у пациентов с талассемией, соответствие лечению было слабым, поскольку были необходимы внутривенные вливания в течение 4 дней с интервалами 3-4 недели. Позднее было показано, что перорально активные соединения масляной кислоты (фенилацетат натрия и 4-фенилбутират натрия) способны увеличивать продукцию HbF у субъектов с серповидно-клеточной анемией. Пероральное введение изобутирамида в дозе 350 мг/кг/день пациентам, страдающим β-талассемией, удлиняет интервал между переливаниями и уменьшает избыток железа. В настоящее время, однако, применение бутирата и его аналогов, по сравнению с контролируемыми клиническими испытаниями, не так широко распространено, вследствие плохого соблюдения режима терапии, демонстрируемого также для пероральных составов.
Что касается генетических метаболических заболеваний, 4-фенилбутират натрия одобрен Управлением по контролю качества продуктов и лекарств США (FDA) для применения у пациентов с дефицитом ферментов цикла мочевины, у которых он действует как акцептор аммиака. В действительности 4-фенилбутират натрия окисляется до фенилацетата, который связывается с глутамином и вызывает его выделение с мочой. У пациентов с дефицитом орнитин-транскарбамилазой применение 4-фенилбутирата натрия позволяет лучше контролировать метаболизм и лучше усваивать природные белки с пищей (Burlina A.B. et al., Molecular Genetics and Metabolism, 2001, 72:351-355). Также в стадии исследования является возможность применения 4-фенилбутирата натрия при лечении X-сцепленной адренолейкодистрофии (X-АЛД), пероксисомное заболевание, характеризующееся изменением метаболизма и накоплением жирных кислот с очень длинной цепью. Натрия 4-фенилбутират, применяемый либо in vitro на фибробластах пациентов с X-АЛД, либо in vivo у X-АЛД-нокаутированных морских свинок, приводит к увеличению бета-окисления жирных кислот с очень длинной цепью и индуцирует пролиферацию пероксисом (Kemp S. et al., Nat. Med., 1998, 4:1261-1268).
И, наконец, совсем недавно было показано, что пероральное введение бутирата может предотвращать и лечить инсулинорезистентность и увеличение веса в животной модели ожирения у крыс. Данные эффекты являются по меньшей мере частично связанными со стимуляцией расхода энергии и ряда митохондриальных функций и открывают новые интересные перспективы для применения в профилактике и лечении метаболических нарушений, связанных с ожирением.
Исходя из данных научных исследований в литературе и клинических исследований ряда исследовательских групп, появляется широкий спектр возможностей для терапевтического применения бутирата при пероральном введении и отсутствие серьезных нежелательных явлений.
Некоторое количество основанных на бутирате продуктов находится в продаже, но их применение все еще очень сильно ограничено и очень низко относительно широкого спектра возможных показаний, особенно при хронических заболеваниях, где предусмотрено длительное применение соединения. Основная проблема возникает вследствие трудностей, связанных с доступностью составов для бутирата, которые легко вводятся перорально, особенно пациентам детского возраста, главным образом в связи с чрезвычайно плохими вкусовыми качествами препаратов, существующих на рынке. Очень неприятный вкус и запах делают пероральное введение доступных в настоящее время препаратов на основе бутирата чрезвычайно трудным и данные затруднения еще более значительны в случае пациентов детского возраста, для которых введение таких препаратов оказывается действительно очень трудным. Проблемы, связанные с возможными фармацевтическими составами бутирата, возникают из-за того, что препарат имеет конкретные физико-химические характеристики. Масляная или н-бутановая кислота (C4H8O2) при комнатной температуре представляет собой густую жидкость, характеризующуюся очень неприятным, интенсивным запахом несвежего сыра и с течением времени подвергается деградации, что изменяет ее стабильность. В этом виде окислительные явления являются более явными, и обычные фармацевтические формы (сиропы, капсулы и таблетки) являются непригодными, за исключением, с определенными ограничениями, мягких желатиновых капсул, применение которых, однако, является невозможным у грудных детей и в раннем детстве. Большинство легко получаемых производных масляной кислоты представляют собой соли щелочных и щелочноземельных металлов, которые, в свою очередь, обладают далеко не незначительными недостатками. Соли натрия представляют собой твердые вещества с высокой степенью гигроскопичности и сильным запахом масляной кислоты. Соли кальция, несмотря на твердую форму, обладают очень плохой растворимостью в воде и соли магния, также твердые, являются растворяющимися. Соли кальция и магния, в любом случае, также сохраняют сильный характерный запах. В цитируемой выше литературе представлены многочисленные данные о недостатках, связанных с крайне неприятным вкусом и запахом и сопутствующими эпигастральными расстройствами вследствие перорального введения бутирата или его производных и его аналогов с нормальной или разветвленной цепью с вплоть до 6 атомами углерода. Это происходит, например, в случае введения фенилбутирата натрия или изобутирамида при клинических исследованиях с участием пациентов с талассемией (Collins A.F. et al., Blood, 1998, 85:43-49; Reich S. et al., Blood, 2000, 96:3357-3362). Основываясь на упомянутых выше факторах, существует очевидная необходимость в доступном соединении бутирата (или соединении жирных кислот с нормальной или разветвленной цепью с вплоть до 6 атомов углерода), которое сохраняет терапевтическую эффективность, но в то же время позволяет легко вводить препарат перорально, также благодаря улучшенным вкусовым качествам, кроме того, имеющее небольшую стоимость. Также препарат может быть пригоден для длительного лечения и также может быть полезен для медицины. Рассматривая возможные химические модификации масляной кислоты для получения производного, которое обладает хорошей стабильностью и растворимостью, отсутствием запаха и вкуса и приемлемыми вкусовыми качествами и которое не является гигроскопичным в твердом состоянии и легко синтезируется и очищается, может быть замечено, что хлорангидриды жирных кислот легко взаимодействуют в безводной среде как со спиртовыми, так и с аминогруппами, давая в качестве продуктов реакции сложные эфиры и ряд фармакологически активных молекул. Преимуществом сложных эфиров является приятный запах, до такой степени, что метиловые и этиловые эфиры масляной кислоты используются в качестве вкусовых и ароматизирующих агентов в пищевой промышленности, но они в основном являются маслами или поглощающими влагу твердыми веществами с низкой температурой плавления, и это не может решить проблемы из-за жидкого состояния, также не все из них являются стабильными на воздухе. Кроме того, сложноэфирная форма имеет низкую стабильность в кислой среде, и при pH желудка гидролиз приводит к формированию кислоты и спирта, из которых эти сложные эфиры получены, с последующим высвобождением масляной кислоты, снова приводя, хотя и в меньшей степени, к упомянутым выше проблемам со вкусовыми качествами. Сложноэфирные производные бутирата описаны, например, в патенте США 5763488, в котором предлагается пероральное введение пролекарств, состоящих из сложных эфиров масляной кислоты с треитолом, для клинического применения при заболеваниях, связанных с β-гемоглобином. Такие заболевания предлагаются с целью улучшения биодоступности бутирата, но в документе не принимаются во внимание аспекты, связанные со вкусовыми качествами пероральных лекарственных средств на основе данного активного компонента.
На конкретном примере желудочно-кишечных заболеваний, в международной патентной заявке WO 98/40064 предлагается применение, путем перорального введения, пролекарств бутирата с молочной кислотой. Целью является преодоление недостатков вследствие плохих фармакокинетических свойств бутирата и получение пероральных лекарственных средств, которые обеспечивают хорошую биодоступность и приемлемый период полувыведения, делая возможным эффективное высвобождение бутирата в плазму крови. Также, при этом, в документе не принимается во внимание особенность вкусовых качеств перорального лекарственного средства на основе бутирата. В настоящее время обнаружено, что некоторые амидные производные ЖККЦ, и в частности масляной кислоты, решают упомянутые выше проблемы.
Краткое описание рисунков
На фиг.1-5 демонстрируются изменения тока короткого замыкания (Iкз) в зависимости от времени (мин). Эффект был дозозависимым. В частности:
на фиг.1 показано действие добавления бутирата Na на Iкз в клетках Caco-2, помещенных в камеру Уссинга. Уменьшение Iкз, вызванное добавлением бутирата Na со стороны слизистой, указывает на абсорбцию ионов. Данные представлены в виде средних значений из трех экспериментов. Вещество добавляли в нулевой момент времени;
на фиг.2 показано действие добавления соединения 1 (пример 1) на Iкз в клетках Caco-2, помещенных в камеру Уссинга. Уменьшение Iкз, вызванное добавлением соединения 1 со стороны слизистой, указывает на абсорбцию ионов. Данные представлены в виде средних значений ± из трех экспериментов. Вещество добавляли в нулевой момент времени;
на фиг.3 показано действие добавления соединения 2 (пример 1) на Iкз в клетках Caco-2, помещенных в камеру Уссинга. Уменьшение Iкз, вызванное добавлением соединения 2 со стороны слизистой, указывает на абсорбцию ионов. Данные представлены в виде средних значений ± из трех экспериментов. Вещество добавляли в нулевой момент времени;
на фиг.4 показано действие добавления соединения 3 (пример 1) на Iкз в клетках Caco-2, помещенных в камеру Уссинга. Уменьшение Iкз, вызванное добавлением соединения 3 со стороны слизистой, указывает на абсорбцию ионов. Данные представлены в виде средних значений ± из трех экспериментов. Вещество добавляли в нулевой момент времени;
на фиг.5 показано действие добавления смеси соединений 1, 2 и 3 (пример 1) на Iкз в клетках Caco-2, помещенных в камеру Уссинга. Уменьшение Iкз, вызванное добавлением смеси соединений 1, 2 и 3 со стороны слизистой, указывает на абсорбцию ионов. Данные представлены в виде средних значений ± из трех экспериментов. Вещество добавляли в нулевой момент времени.
Подробное описание изобретения
В рамках исследований, которые привели к настоящему изобретению, рассматривалось, что амидные производные ЖККЦ, в частности масляной кислоты, обычно существующие в твердой, не имеющей запаха и вкуса форме, являются более стабильными, чем сложные эфиры, в условиях рН желудка и способны высвобождать соответствующую кислоту при щелочном гидролизе в тонком и толстом кишечнике. Данные фармакокинетические характеристики делают эти производные потенциальными пролекарствами с конкретными свойствами в отношении пролонгированного высвобождения в кишечнике, который составляет очень важную терапевтическую мишень, отвечающего в особенно эффективном способе необходимости в точном нацеливании лекарств.
Согласно изобретению было обнаружено, что синтез амидов ЖККЦ с нормальной или разветвленной цепью с применением нетоксичных, в высокой степени биосовместимых молекул, таких как аминокислоты, и в числе последних, в частности, фенилаланина, обеспечивает производные, наделенные всеми органолептическими и физико-химическими характеристиками, требуемыми для оптимального применения конечного продукта в виде перорального лекарственного средства, требуемого в медицине, также для длительной терапии или для лечения хронических заболеваний. Среди различных наиболее широко доступных природных аминокислот, фенилаланин обеспечивает самые лучшие амидные производные в отношении органолептических и физико-химических характеристик, давая не имеющие запаха и цвета твердые кристаллические продукты, и делает возможным чрезвычайно экономически выгодную очистку касательно отношения цена:выход. Наиболее предпочтительным, согласно изобретению, является кислотоустойчивый амид масляной кислоты с аминокислотой фенилаланин, фенилаланин-бутирамид (ФБА), который представляет собой твердое вещество, малогигроскопичное, удобное для взвешивания, устойчивое к действию кислот и щелочей и способное высвобождать масляную кислоту в тонком и толстом кишечнике непрерывно в течение длительного времени. Данный продукт, исследования токсичности для которого, описанные далее в данном документе, показали профиль токсичности, сравнимый с бутиратом, обладает физико-химическими свойствами, значительно более подходящими для широкого клинического применения по сравнению с последним. Отличительной чертой ФБА является то, что он не имеет неприятного запаха бутирата и практически безвкусный, таким образом, позволяя преодолеть основное ограничение для применения бутирата в терапии, а именно его очень плохие вкусовые качества. Более того, растворимость ФБА в воде является удовлетворительной, так как получаются прозрачные растворы вплоть до концентрации 0,1 M и суспензии при более высоких концентрациях.
Амидное производное масляной кислоты с фенилаланином или подходящими производными последнего получают путем взаимодействия соответствующего производного фенилаланина с бутирилхлоридом или эквивалентным производным масляной кислоты (простым или смешанным сложным эфиром или ангидридом) - см. Y в п.1, в полярном апротонном инертном органическом растворителе при комнатной температуре. В результате данной реакции образуется монобутирильное производное, которое является основным компонентом, в количественном выражении, сопровождаемым, в зависимости от структуры исходных реагентов, также дибутирильным производным исходного соединения фенилаланина и других производных, получаемым, например, в результате циклизации основного продукта в процессе реакции.
Хотя возможно выделение и очистка соединений, полученных известными способами, также было замечено, согласно изобретению, что реакционная смесь может успешно применяться без предварительного разделения на индивидуальные компоненты и что в данном состоянии также демонстрировались желаемые физико-химические, органолептические и фармакокинетические свойства.
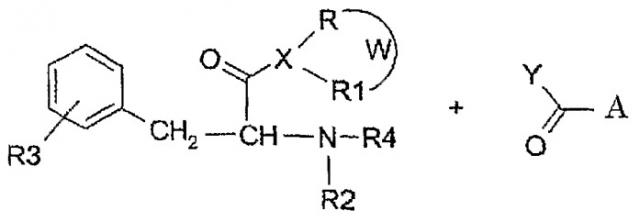
Вследствие этого, конкретной целью настоящего изобретения является обеспечение амидного производного ЖККЦ, получаемого по реакции производного указанной жирной кислоты с производным фенилаланина в соответствии со следующей общей схемой:
где
Y представляет собой атом галогена, алкоксил (2-6 атомов углерода), ацил (2-6 атомов углерода);
A представляет собой нормальную или разветвленную C(1-5) алкильную цепь, возможно замещенную фенилом;
X представляет собой кислород, азот или серу, при условии, что:
- когда X представляет собой кислород или серу, R представляет собой водород или (C1-6) алкильную группу и R1 и W отсутствуют;
- когда X представляет собой азот, R и R1 представлены независимо водородом или (C1-6) алкильной группой или (C1-6) ацильной группой и W отсутствует; или
W представляет собой 1,2-алкиленовую цепь с 2-6 атомами углерода, и R и R1 являются метиленовыми группами;
R2 и R4 представлены независимо водородом или (C1-6) алкильной группой или (C1-6) ацильной группой;
R3 выбирают из группы, состоящей из H, (C1-6)алкила, (C1-6)алкоксила, галогена, гидроксила, циано, нитро, амино, моно- или ди(C1-6)алкиламино, (C2-6)ациламино, формила, гидроксииминометила, (C1-6)алкоксииминометила и карбамоила;
при следующих условиях: полагая, что все описанное ранее понятно, производные по настоящему изобретению включают соли с фармацевтически приемлемыми основаниями и кислотами и возможные диастереомерные и энантиомерные формы.
C1-C6 алкильные группы, определенные для целей настоящего изобретения, могут быть нормальными или разветвленными и по существу представляют собой метил, этил, пропил, изопропил, бутил, изопентил, н-гексил и их аналоги, тогда как C1-C6 алкоксильные группы предпочтительно выбирают из группы, состоящей из метоксила, этоксила, пропоксила, изопропоксила, бутоксила, 2-метилпропоксила и трет-бутоксила.
Кроме того, для целей настоящего изобретения, алкиленовая цепь может быть нормальной или разветвленной, такой как, например, этилен, 1,3-пропилен, 2-метилэтилен, 1,4-бутилен, 2-метил-1,3-пропилен, 2-этилэтилен, 1,5-пентилен, 2-этил-1,3-пропилен, 2-метил-1,4-бутилен и тому подобное, тогда как под галогеном по существу подразумевается фтор, хлор, бром и йод. В соответствии с принятой в настоящее время химической номенклатурой C2-C6 ацильная группа по существу определяет ацетил, пропионил, бутирил, пентаноил, пивалоил, гексаноил и тому подобное. Термины алкоксил, алкиламино, ациламино, алкоксииминометил и карбамоил также имеют значения в соответствии с номенклатурой в данной области техники.
Соединения по настоящему изобретению получают путем взаимодействия двух соединений, указанных выше, предпочтительно в по существу эквимолярных количествах в полярном апротонном инертном растворителе, таком как, например, бензол, толуол или хлороформ, при комнатной температуре реакционной смеси, предпочтительно в течение периода времени от четырех до двадцати четырех часов, с последующими одной или несколькими стадиями разделения и очистки полученного продукта, предпочтительно путем перекристаллизации. В случае взаимодействия производного фенилаланина и бутирильного производного будет получена смесь бутирильных производных, где основной продукт будет состоять из монопроизводного с другими продуктами реакции, такими как дибутирильное производное и циклическое производное, указанное здесь далее.
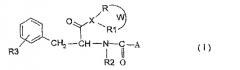
В соответствии с некоторыми конкретными примерами осуществления, объектом изобретения является амидное производное жирной кислоты с короткой цепью, имеющее следующую общую формулу:
где A, X, W, R, R1, R2 и R3 определены ранее, и соответствующие соли с фармацевтически приемлемыми основаниями, а также возможные диастереомерные и энантиомерные формы.
Несколько предпочтительных форм соединения формулы (I), представленные также в следующих примерах синтеза, представляют собой соединение формулы (I), где A представляет собой -(CH2)2CH3, X представляет собой азот и R, R1, R2 и R3 представляет собой водород (N-(1-карбамоил-2-фенилэтил)бутирамид, и соединение, где A представляет собой -(CH2)2CH3, X представляет собой кислород, R представляет собой метоксильную группу и R2 и R3 представляют собой водород (метиловый эфир 2-бутириламино-3-фенилпропионовой кислоты).
В соответствие с другим конкретным примером осуществления изобретения, объектом настоящего изобретения является смесь амидных производных масляной кислоты, получаемая путем взаимодействия бутирилгалогенида с производным фенилаланина по схеме, представленной выше, и их соли с фармацевтически приемлемыми основаниями или кислотами, а также возможные диастереомеры и энантиомеры. Особенно выгодной для целей настоящего изобретения является смесь, полученная при проведении процесса, описанного в примере 1, и по существу содержащая следующие три соединения:
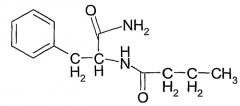
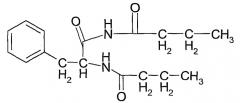
N-(1-карбамоил-2-фенилэтил)бутирамид (соединение 1) формулы:
N-(1-бутирилкарбамоил-2-фенилэтил)бутирамид (соединение 2) формулы:
5-бензил-2-пропил-1H-имидазол-4(5H)-он (соединение 3) формулы:
Полученные таким образом соединения могут применяться в виде их смеси или могут быть выделены и очищены известными способами. Они могут быть выделены как в виде свободных форм, так и в виде соответствующих солей фармацевтически приемлемых оснований или кислот, при добавлении подходящего количества выбранного основания или кислоты к свободным формам или к реакционной смеси. Примерами таких солей являются фармацевтически приемлемые соли натрия или калия, соли аммония, с этилендиамином и алифатическими или ароматическими азотсодержащими основаниями, гидрохлориды, сульфаты, с алифатическими или ароматическими кислотами. Соединения по изобретению, принимая во внимание природу заместителей A, X, R, R1, R2 и R3, а также фенильную группу, имеют по меньшей мере один хиральный центр, поэтому они могут существовать в виде рацемических форм или в виде диастереоизомерных форм, которые могут быть получены способами, хорошо знакомыми квалифицированному химику. Например, один из них предполагает препаративную хроматографию на пластинах с хиральной подложкой с применением соответствующей системы элюента. Как указано выше, возможные диастереоизомеры соединений формулы (I) составляют дополнительный объект настоящего изобретения. Важно отметить, что указанные соединения, а также их соли с фармацевтически приемлемыми основаниями или кислотами, сохраняют действие в кишечнике, которое ранее было описано в отношении бутирата. Для проверки этого были получены экспериментальные данные на моделях in vitro эпителия кишечника человека. В другом аспекте, объектом изобретения является применение одного или более амидных производных жирных кислот с короткой цепью, в частности, производных масляной кислоты, получаемых путем взаимодействия, описанного выше, или их смесей для производства фармацевтического препарата, и более конкретно, препарата, полезного для лечения и профилактики заболеваний у человека или животного.
Возможные терапевтические применения соединений по изобретению суммированы в таблице далее.
| Таблица Терапевтические показания для жирных кислот с короткой цепью | |
| Гастроэнтерологи-ческие заболевания | Опухоли желудочно-кишечного тракта, острый гастроэнтерит, хроническая неспецифическая диарея, диарея путешественников, антибиотик-ассоциированная диарея, синдром раздраженного кишечника, холера, врожденная хлоридорея, врожденная натриевая диарея, хроническая секреторная диарея, муковисцидоз, хроническое воспалительное заболевание кишечника (ХВЗК), индуцированная неправильным питанием энтеропатия, атрофия слизистой, индуцированная полным парентеральным питанием, энтеропатия, индуцированная лучевой терапией и химиотерапией, синдром короткого кишечника и кишечная недостаточность, профилактика и лечение аденокарциномы толстого кишечника, кишечный полипоз, паучит, аллергический энтероколит |
| Гематологические заболевания | промежуточная β-талассемия, серповидно-клеточная анемия |
| Генетические метаболические заболевания | дефицит орнитин-транскарбамилазы, X-сцепленная адренолейкодистрофия (X-АЛД) |
| Ожирение | резистентность к инсулину, метаболический синдром |
В заключение, фармацевтические композиции по изобретению содержат в качестве активного компонента по меньшей мере одно соединение общей формулы (I) и его соответствующие производные, предпочтительно, по меньшей мере одно из амидных производных масляной кислоты, описанных выше, или более предпочтительно, смесь трех соединений 1, 2 и 3, вместе с одним или более фармацевтически приемлемыми адъювантами и/или носителями. Как указано во введении, тип композиции по изобретению, которая обеспечивает наибольшее преимущество для указанных терапевтических целей, является композицией, составленной для перорального введения, которая позволяет улучшить соблюдение режима терапии пациентом, особенно при продолжительной терапии и применении в педиатрии и ветеринарии. Фармацевтические препараты, подходящие для перорального введения, могут, например, быть в форме таблеток, капсул, сиропов, растворов и год