Способ получения сложных метиловых эфиров жирных кислот с использованием смеси липаз (варианты)
Иллюстрации
Показать всеИзобретение относится к области биотехнологии. Предложены варианты способа получения сложных метиловых эфиров жирных кислот (биодизеля) в микроводной системе, не содержащей растворителей. Осуществляют поэтапное добавление метанола к триглицеридам в присутствии препарата липаз и обеспечивают протекание реакции в подходящих условиях до тех пор, пока триглицериды не превратятся в сложные метиловые эфиры жирных кислот. Препарат липаз содержит по меньшей мере две липазы, по отдельности или вместе иммобилизованные на пористом гидрофобном носителе, где одна из липаз обладает повышенной аффинностью к неполным глицеридам, другая является позиционно специфичной к положению sn-1,3, a необязательная третья липаза обладает высокой селективностью в отношении положения sn-2 глицерина. Носитель выбирают из группы, включающей пористые гидрофобные носители на основе алифатических или ароматических полимеров. Также предложен способ получения смеси липаз, иммобилизованных на указанном носителе. Смесь содержит липазу из Candida antarctica В и по меньшей мере одну липазу, полученную из Pseudomonas sp., Alcaligenes sp., Burkholderia sp. и Thermomyces lanuginosa. Препараты липаз обладают высокой устойчивостью в отношении гидрофильных субстратов, демонстрируют синергизм между иммобилизованными липазами и позволяют достичь высокой степени превращения за короткий промежуток времени. 7 н. и 11 з.п. ф-лы, 4 ил., 5 табл., 12 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к получению иммобилизованных мультиферментных систем, предназначенных для трансэстерификации или эстерификации триглицеридов масел и жиров или жирных кислот с помощью короткоцепочечных спиртов для получения сложных короткоцепочечных алкиловых эфиров жирных кислот, предпочтительно для применения в качестве биодизеля. Изобретение также относится к способу получения таких иммобилизованных мультиферментных систем и различным применениям их в промышленности в одностадийных или многостадийных процессах, в частности для получения сложных метиловых эфиров, обычно используемых в качестве биодизеля, при приблизительно полном превращении.
Уровень техники
Липазы (триацилглицеролгидролаза Е.С. 3.1.1.3) определяют как гидролитические ферменты, которые действуют на сложноэфирную связь в триацилглицероле в водных системах с получением свободных жирных кислот, неполных глицеридов и глицерина. Эта группа ферментов при низкой активности воды способна катализировать реакцию, обратную гидролизу. Обратную каталитическую активность липаз широко применяли для синтеза ценных соединений, которые содержат сложноэфирные и амидные связи, или других родственных химических веществ, содержащих такие функциональные группы, как гидроксильные, карбоксильные группы и аминогруппы. В частности, липазы применяли для риформинга жирных кислот, масел, восков, фосфолипидов и сфинголипидов для получения новых требуемых функциональных свойств и для разделения оптически активных соединений из их рацемических смесей. Особенно интересно отметить, что будет раскрыто применение мультиферментной системы, включавшей различные липазы, иммобилизованные на полимерном носителе, для синтеза сложных эфиров короткоцепочечных алкилов и жирных кислот (биодизеля).
В настоящее время существует более чем 40 различных коммерчески доступных липаз и фосфолипаз, однако, только некоторые из них получают в промышленном количестве. Некоторые из наиболее многообещающих с точки зрения промышленного производства ферменты, функционирующие на разделе фаз, получают из Candida antarctica, Candida rugosa, Rhizomucor miehei, Pseudomonas sp., Rhizopus niveus, Mucor javanicus, Rhizopus oryzae, Aspergillus niger, Penicillium camembertii, Alcaligenes sp., Burkholderia sp., Thermomyces lanuginosa, Chromobacterium viscosum, семян папайи и панкреатина.
Наиболее известные способы иммобилизации в основном делятся на следующие.
1. Физическая адсорбция ферментов на твердом носителе, таком как кремнезем и нерастворимые полимеры.
2. Адсорбция на ионообменных смолах.
3. Ковалентное связывание ферментов с веществом твердого носителя, такого как эпоксидные неорганические или полимерные носители.
4. Включение ферментов в растущий полимер.
5. Помещение ферментов в мембранный реактор или полупроницаемые гели.
6. Перекрестно-сшитые кристаллы ферментов (CLECs) или агрегаты (CLEA's).
Физическая адсорбция липаз, основанная на применении полимерных носителей с высокой пористостью или на применении ионообменных смол, представляет собой наиболее используемые на практике методы иммобилизации липаз. Этот способ характеризуется простотой и приводит к получению надежной синтетической активности.
Применение свободных или иммобилизованных липаз для трансэстерификации триглицеридов и короткоцепочечных спиртов для образования сложных алкиловых эфиров жирных кислот приводило к неудовлетворительным результатам в отношении активности и стабильности фермента. Также, экономическая эффективность иммобилизованных ферментов все еще препятствует энзиматическому получению сложных алкиловых эфиров жирных кислот в промышленных количествах. Кроме того, было показано, что все имеющиеся в продаже в настоящее время липазы, существующие или в своей свободной, или в иммобилизованной формах, не способны приводить к практически полному превращению триглицеридов масел в сложные алкиловые эфиры жирных кислот, предпочтительно достигающему более 99% в разумное время реакции, составляющее, в частности, менее 8 часов.
Другой основной недостаток липаз происходит из-за их низкой устойчивости в отношении гидрофильных субстратов, в частности, в отношении короткоцепочечных спиртов, короткоцепочечных жирных кислот (и те, и другие состоят из менее чем 4 атомов С), воды и глицерина, обычно присутствующих в реакционной среде для трансэстерификации. Во многих исследованиях было показано, что короткоцепочечные спирты и короткоцепочечные жирные кислоты, такие как метанол и уксусная кислота, соответственно, являются причиной отщепления молекул воды от четвертичной структуры таких ферментов, что приводит к их денатурации и последующей потере их каталитической активности. Также, присутствие таких гидрофильных молекул в реакционной среде приводит к отщеплению молекул воды от носителя и последующему снижению срока эксплуатации ферментов. Таким образом, не удивительно, что применение липаз для получения приемлемых для продажи количеств сложных метиловых эфиров жирных кислот «биодизеля» с применением триглицеридов масел и метанола в качестве субстратов является невозможным.
В работе [Lee, D.H. et at., Biotechnology and Bioprocess Engineering 2006, 11:522-525] было предложено применение смесей липаз. В этой публикации описано получение биодизеля с помощью смеси химически связанных, иммобилизованных липаз Rhizopus oryzae и Candida rugosa. Как можно было увидеть, для того чтобы достигнуть более 96%-ного превращения сырья в биодизель, требовалось относительно долгое время реакции, обычно превышавшее 24 часа. Также, результаты, приведенные в этой публикации, показывают, что используемая смесь ферментов теряла более 20% своей исходной активности уже спустя всего 10 циклов применения. Это может быть вызвано накоплением неполных глицеридных промежуточных продуктов в реакционной системе, которое уменьшает реакцию трансэстерификации и поэтому увеличивает время реакции. Деактивация биокатализатора в системе, описанная в этой публикации, является главным недостатком, который препятствует его промышленному применению.
Поэтому целью этого изобретения является обеспечение нового способа получения высокоактивных и стабильных иммобилизованных липаз, предназначенных, в особенности, для синтеза сложных алкиловых эфиров жирных кислот, в частности сложных метиловых эфиров жирных кислот, для использования в качестве «биодизеля».
Другой целью настоящего изобретения является обеспечение высокоактивного и стабильного иммобилизованного мультиферментного препарата, который обладает высокой устойчивостью в отношении короткоцепочечных спиртов и короткоцепочечных жирных кислот, в особенности в отношении метанола, этанола и уксусной кислоты, соответственно, и других полиолов, таких как глицерин, а также других ингибирующих факторов, обычно присутствующих в маслах и жирах, в особенности в их технических сортах.
Другой целью настоящего изобретения является обеспечение компоновки одностадийного или многостадийного ферментативного реактора для получения требуемого продукта, а именно сложных алкиловых эфиров жирных кислот, при практически полном превращении в разумное время реакции, составляющее обычно менее 5 часов.
Эти и другие цели изобретения станут понятными в представленном ниже описании изобретения.
Раскрытие изобретения
В первом аспекте изобретение относится к способу получения сложных алкиловых эфиров жирных кислот, предпочтительно короткоцепочечных сложных алкиловых эфиров жирных кислот, таких как сложные метиловые эфиры жирных кислот (биодизель) в микроводной системе, не содержащей растворителей, включающему предоставление источника жирных кислот, поэтапное добавление свободного спирта, предпочтительно короткоцепочечного свободного спирта, в частности метанола, или донора любого другого спирта, к указанному источнику жирных кислот в присутствии препарата липаз, и обеспечение протекания реакции в подходящих условиях до тех пор, пока триглицериды, являющиеся указанным источником жирных кислот, не превратятся в сложные алкиловые эфиры жирных кислот, предпочтительно в сложные метиловые эфиры жирных кислот (FAME), где указанный препарат липаз включает, по меньшей мере, две липазы, предпочтительно три липазы, указанные липазы по отдельности или вместе иммобилизованы на подходящем носителе, и где, по меньшей мере, одна из указанных липаз обладает повышенной активностью в отношении неполных глицеридов и, по меньшей мере, одна из указанных липаз позиционно специфична к положению sn-1,3, и необязательно третью липазу, обладающую высокой селективностью в отношении положения sn-2 углеродного скелета глицерина.
Липазу, позиционно специфичную к положению sn-1,3, можно выбирать из группы, состоящей из липаз Thermomyces lanuginosa, Rhizomucor miehei, Mucor miehei, Pseudomonas sp., Rhizopus sp., Mucor javanicus, Penicillium roqueforti, Aspergillus niger, Acromobacter sp. и Burkholderia sp., но не ограниченной только ими. Указанную липазу, обладающую повышенной аффинностью в отношении неполных глицеридов, можно выбирать из группы, состоящей из липаз Candida antarctica В, Candida antarctica A, Candida rugosa, Alcaligenes sp. и Penicillium camembertii, но не ограниченной только ими. Третья липаза может, в частности, быть липазой, обладающей высокой селективностью в отношении положения sn-2, полученной из Candida antarctica А или Pseudozyma sp.
Источник жирных кислот, применяемый в способе изобретения, может включать, по меньшей мере, один из перечисленных компонентов, таких как соевое масло, масло канолы, рапсовое масло, оливковое масло, касторовое масло, пальмовое масло, подсолнечное масло, арахисовое масло, хлопковое масло, ятрофное масло, жир животного происхождения, отходы кулинарного жира, триглицериды масел из несъедобных растительных источников или любые их смеси, по меньшей мере, смеси из двух компонентов.
Липазы могут быть вместе иммобилизованы на подходящем носителе, предпочтительно на носителе на основе гидрофобного алифатического полимера или на гидрофобном ароматическом полимерном носителе. Любая из указанных липаз может быть иммобилизована на подходящем носителе, где носители, на которых иммобилизованы указанные липазы, или идентичны, или различаются.
Носитель предпочтительно является пористым носителем, который может быть органическим или неорганическим. Примерами носителей являются пористые неорганические носители, такие как носители на основе оксида кремния или оксида алюминия, но не ограниченные только ими, и органические носители, такие как полимерные носители или носители на основе полимера, но не ограниченные только ими, и носители необязательно могут содержать активные функциональные группы, выбираемые из эпоксигрупп и альдегидных групп, или ионных групп.
В способе этого аспекта изобретения за превращением ацильных групп жирных кислот или свободных жирных кислот, включенных в указанный источник жирных кислот, в сложные метиловые эфиры жирных кислот можно следить в различные моменты времени в ходе реакции, реакционную среду можно удалять с помощью подходящих способов в любой требуемый момент в ходе реакции, останавливая таким образом реакцию, и образованные сложные метиловые эфиры жирных кислот и необязательно образованный глицерин выделяют из реакционной среды. Реакцию можно специфически останавливать, если превращение ацильных групп жирных кислот или свободных жирных кислот, включенных в указанный источник жирных кислот, в сложные метиловые эфиры жирных кислот достигло, по меньшей мере, 70%, предпочтительно, по меньшей мере, 85%, более предпочтительно, по меньшей мере, 95%.
В следующем аспекте изобретение относится к способу получения короткоцепочечных сложных алкиловых эфиров жирных кислот, предпочтительно сложных метиловых эфиров жирных кислот (биодизеля) в микроводной системе, не содержащей растворителей, включающему предоставление источника жирных кислот, поэтапное добавление короткоцепочечного свободного спирта, предпочтительно метанола или донора любого другого спирта, к указанному источнику жирных кислот в присутствии препарата липаз и обеспечение протекания реакции в подходящих условиях до тех пор, пока превращение ацильных групп жирных кислот или свободных жирных кислот, включенных в указанный источник жирных кислот, в сложные метиловые эфиры жирных кислот не достигнет, по меньшей мере, 70%, где указанный препарат липаз включает одну единственную липазу, иммобилизованную на подходящем носителе, или смесь, по меньшей мере, двух липаз, вместе или по отдельности иммобилизованных на подходящем носителе, при постоянном удалении образующегося глицерина и любого избыточного количества воды из реакционной среды.
Также в способе этого аспекта указанный препарат липаз может включать, по меньшей мере, две липазы, предпочтительно три липазы, указанные липазы по отдельности или вместе иммобилизованы на подходящем носителе. По меньшей мере, одна из указанных липаз обладает повышенной аффинностью к неполным глицеридам и, по меньшей мере, одна из указанных липаз позиционно специфична к положению sn-1,3. Необязательная третья липаза предпочтительно обладает более высокой селективностью к положению sn-2, чем позиционно неспецифичные липазы.
Липазы, позиционно специфичные к положению sn-1,3, без ограничений могут быть ферментом из любого источника: Thermomyces lanuginosa, Rhizomucor miehei, Mucor miehei, Pseudomonas sp., Rhizopus sp., Mucor javanicus, Penicillium roqueforti, Aspergillus niger, Acromobacter sp. и Burkholderia sp. Указанная липаза, обладающая повышенной аффинностью к неполным глицеридам, без ограничений может быть ферментом из любого источника: Candida antarctica В, Candida rugosa, Alcaligenes sp. и Penicillium camembertii, и указанная необязательная третья липаза, обладающая более высокой селективностью в отношении положения sn-2, чем позиционно неспецифичные липазы, без ограничений, может быть получена из Candida antarctica А и Pseudozyma sp.
Также в этом способе источник жирных кислот может включать, по меньшей мере, один из компонентов, таких как соевое масло, масло канолы, рапсовое масло, оливковое масло, касторовое масло, пальмовое масло, подсолнечное масло, арахисовое масло, хлопковое масло, ятрофное масло, жир животного происхождения, отходы кулинарного жира, триглицериды масел из несъедобных растительных источников или любую смесь, по меньшей мере, двух из них.
Липазы могут быть вместе иммобилизованы на подходящем носителе, предпочтительно на носителе на основе гидрофобного алифатического полимера или на гидрофобном ароматическом полимерном носителе. Любая из указанных липаз может быть иммобилизована на подходящем носителе, где носители, на которые иммобилизованы указанные липазы, идентичны или различаются.
Носитель предпочтительно является пористым носителем, который может быть органическим или неорганическим. Примерами носителей являются пористые неорганические носители, такие как носители на основе кремнезема или глинозема, но не ограниченные только ими, и органические носители, такие как полимерные носители или носители на основе полимера, но не ограниченные только ими, и носители необязательно могут содержать активные функциональные группы, выбираемые из эпоксигрупп и альдегидных групп, или ионных групп.
Также в способе этого аспекта изобретения за превращении ацильных групп жирных кислот или свободных жирных кислот, включенных в указанный источник жирных кислот, в сложные метиловые эфиры жирных кислот можно следить в различные моменты времени в ходе реакции, реакционную среду можно удалять с помощью подходящих способов в любой требуемый момент в ходе реакции, останавливая таким образом реакцию, и образованные сложные метиловые эфиры жирных кислот и необязательно образованный глицерин выделяют из реакционной среды. Реакцию можно специфически останавливать, если превращение ацильных групп жирных кислот или свободных жирных кислот, включенных в указанный источник жирных кислот, в сложные метиловые эфиры жирных кислот достигло, по меньшей мере, 70%, предпочтительно, по меньшей мере, 85%, более предпочтительно, по меньшей мере, 95%.
В еще одном аспекте изобретение относится к микроводному способу в отсутствие растворителей для получения сложных алкиловых эфиров жирных кислот, предпочтительно сложных короткоцепочечных алкиловых эфиров жирных кислот, таких как сложные метиловые эфиры (биодизель), включающему:
(а) предоставление источника жирных кислот, поэтапное добавление короткоцепочечного спирта, предпочтительно метанола или донора любого другого спирта, к указанному источнику жирных кислот в присутствии препарата липаз и обеспечение протекания реакции в подходящих условиях до тех пор, пока превращение ацильных групп жирных кислот или свободных жирных кислот, включенных в указанный источник жирных кислот, в сложные метиловые эфиры жирных кислот не достигнет, по меньшей мере, 70%, где указанный препарат липаз включает, по меньшей мере, одну липазу, иммобилизованную на подходящем носителе, или смесь, по меньшей мере, двух липаз и предпочтительно трех липаз, которые вместе или по отдельности иммобилизованы на подходящем носителе, при постоянном удалении образующегося глицерина из реакционной среды, для получения органической фазы, содержащей в основном отстатки непрореагировавших глицеридов и образованных сложных алкиловых эфиров жирных кислот; и (b) реакцию указанной органической фазы с короткоцепочечным свободным спиртом, предпочтительно метанолом или донором любого другого спирта, в присутствии препарата липаз, как указано на стадии (а) в подходящих условиях, пока превращение ацильных групп жирных кислот или свободных жирных кислот, включенных в указанный источник жирных кислот, в сложные метиловые эфиры жирных кислот не достигнет, по меньшей мере, 95%.
Липазы, препараты липаз, носитель ферментов, источник жирных кислот в способе этого аспекта сходны с теми, которые применяют в других аспектах.
Еще изобретение относится к способу получения смеси липаз, иммобилизованных на нерастворимом носителе, указанная смесь включает липазу, полученную из Candida antarctica В и, по меньшей мере, одну липазу, полученную из Pseudomonas sp., Alcaligenes sp., Burkholderia sp. и Thermomyces lanuginosa, способ включает стадии (а) контакта буферного раствора, содержащего одну из указанных выше липаз и другого буферного раствора, содержащего вторую липазу, или одного единственного буферного раствора, содержащего смесь указанных выше липаз, с полимерным носителем, предпочтительно с ионообменной смолой или адсорбентом; в частности, с гидрофобным алифатическим носителем или носителем на основе ароматического полимера, предпочтительно в присутствии гидрофобного органического растворителя, такого как н-гексан, добавленного в среду для иммобилизации в соотношениях буфер : органический растворитель от 1:10 до 10:1, соответственно; (b) смешивания системы, полученной на стадии (а), в течение, по меньшей мере, 4 часов при комнатной температуре; (с) фильтрования смеси иммобилизованных липаз и высушивания ее до тех пор, пока содержание воды не станет меньше 5%.
Нерастворимый носитель, применяемый в этом аспекте изобретения, предпочтительно является пористым и сетчатым гидрофобным алифатическим носителем или носителем на основе ароматического полимера, в частности, Amberlite XAD 7НР или Amberlite XAD 1600, соответственно.
Изобретение также относится к биодизелю, полученному с помощью способа, в котором применяют смесь иммобилизованных липаз, полученную с помощью способа изобретения.
Указанные сложные эфиры короткоцепочечных алкилов и жирных кислот во всех аспектах изобретения предпочтительно являются сложными метиловыми, этиловыми, изо-пропиловыми или бутиловыми эфирами жирных кислот (биодизелем).
В еще одном аспекте изобретение относится к способу получения сложных алкиловых эфиров жирных кислот, предпочтительно сложных эфиров короткоцепочечных алкилов и жирных кислот, в частности сложных метиловых эфиров жирных кислот, в системе, не содержащей растворителя, включающему предоставление источника жирных кислот, поэтапное добавление свободного спирта, предпочтительно короткоцепочечного свободного спирта, в частности метанола или более высокомолекулярного спирта, или донора любого другого спирта, к указанному источнику жирных кислот в присутствии препарата липаз и обеспечение протекания реакции в подходящих условиях до тех пор, пока триглицериды, являющиеся указанным источником жирных кислот, не превратятся в сложные алкиловые эфиры жирных кислот, предпочтительно в сложные эфиры короткоцепочечных алкилов и жирных кислот, в частности сложные метиловые эфиры жирных кислот (FAME), где указанный препарат липаз включает первую липазу и вторую липазу, указанные липазы по отдельности или вместе иммобилизованы на подходящем носителе и где указанная первая липаза демонстрирует более высокую трансэстерификационную активность в отношении триглицеридов по сравнению с ее активностью в отношении неполных глицеридов, а указанная вторая липаза демонстрирует более высокую трансэстерификационную активность в отношении неполных глицеридов по сравнению с ее активностью в отношении триглицеридов, и где две указанные липазы демонстрируют синергический эффект в своей трансэстерификационной активности при получении конечного продукта.
В еще одном аспекте изобретение относится к способу получения сложных алкиловых эфиров жирных кислот, предпочтительно сложных эфиров короткоцепочечных алкилов и жирных кислот, в частности сложных метиловых эфиров жирных кислот, в системе, не содержащей растворителей, включающему предоставление источника жирных кислот, поэтапное добавление свободного спирта, в частности, короткоцепочечного свободного спирта, предпочтительно метанола или более высокомолекулярного спирта, или донора любого другого спирта, к указанному источнику жирных кислот в присутствии препарата липаз и обеспечение протекания реакции в подходящих условиях до тех пор, пока триглицериды, являющиеся указанным источником жирных кислот, не превратятся в сложные алкиловые эфиры жирных кислот, предпочтительно сложные эфиры короткоцепочечных алкилов и жирных кислот, в частности, в сложные метиловые эфиры (FAME), где указанный препарат липаз включает первую липазу и вторую липазу, указанные липазы по отдельности или вместе иммобилизованы на подходящем носителе, и где указанная первая липаза высвобождает промежуточные продукты в первой реакции трансэстерификации, которые являются предпочтительными для указанной второй липазы в трансэстерификации со спиртом с образованием сложных алкиловых эфиров жирных кислот.
Изобретение, кроме того, относится к способу получения сложных алкиловых эфиров жирных кислот, предпочтительно сложных эфиров короткоцепочечных алкилов и жирных кислот, в частности сложных метиловых эфиров жирных кислот, в микроводной системе, не содержащей растворителей, включающему предоставление источника жирных кислот, поэтапное добавление свободного спирта, предпочтительно короткоцепочечного свободного спирта, в частности метанола или более высокомолекулярного спирта, или любого другого свободного спирта или донора спирта, к указанному источнику жирных кислот в присутствии препарата липаз и обеспечение протекания реакции в подходящих условиях до тех пор, пока триглицериды, являющиеся указанным источником жирных кислот, не превратятся в сложные алкиловые эфиры жирных кислот, предпочтительно в сложные эфиры короткоцепочечных алкилов и жирных кислот, в частности в сложные метиловые эфиры (FAME), где указанный препарат липаз включает первую липазу и вторую липазу, указанные липазы по отдельности или вместе иммобилизованы на подходящем носителе, и где указанные липазы демонстрируют различные субстратные специфичности, которые обеспечивают их трансэстерификационную активность в отношении триглицеридов, при условии, что их используют вместе, тогда как, по меньшей мере, одна из двух указанных липаз теряет активность в среде для реакции трансэстерификации, если ее используют отдельно саму по себе с триглицеридами в качестве субстрата, но демонстрирует высокую трансэстерификационную/эстерификационную активность с неполными глицеридами и жирными кислотами в качестве субстратов, соответственно.
Источник жирных кислот, по меньшей мере, является одним из триглицеридов, неполных глицеридов, одной из свободных жирных кислот, одним из фосфолипидов, сложных эфиров и амидов жирных кислот или смесью, включающей, по меньшей мере, два указанных источника.
Носитель может быть сетчатым гидрофобным полимером, состоящим из дивинилбензола или смеси дивинилбензола и стирола, и сетчатым гидрофобным алифатическим полимером, состоящим из алифатических акриловых полимеров. Носитель предпочтительно является пористым матриксом с размером пор в диапазоне 25-1000 Å и предпочтительно в диапазоне 40-100 Å.
Изобретение будет описано более подробно с помощью прилагаемых чертежей.
Краткое описание чертежей
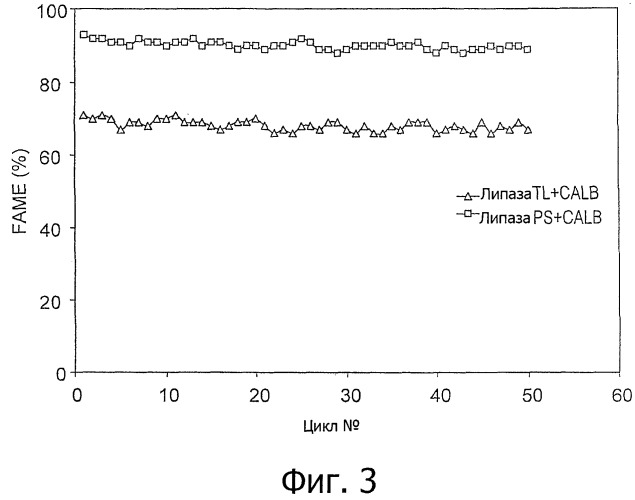
Фигура 1: Эстерификационная активность CALB, липазы PS, липазы TL, каждая из которых по отдельности иммобилизована на Amberlite XAD 7HP. Условия реакции: олеиновую кислоту (2,5 г) и метанол (3 порции, каждая по 95 мг) смешивали с 250 мг иммобилизованной липазы при 30°С в течение 6 часов. Одну и ту же порцию биокатализатора использовали в 50 реакционных циклах в одних и тех же условиях.
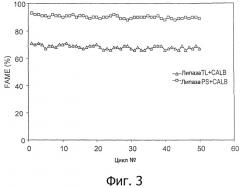
Фигура 2: Трансэстерификационная активность CALB, липазы PS, липазы TL, все ферменты были иммобилизованы по отдельности на Amberlite XAD 7HP. Условия реакции: соевое масло (2,5 г) и метанол (3 порции, каждая по 91 мг) смешивали с 250 мг иммобилизованной липазы при 30°С в течение 6 часов. Одну и ту же порцию биокатализатора использовали в 50 реакционных циклах в одних и тех же условиях.
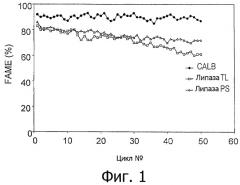
Фигура 3: Трансэстерификационная активность мультилипазы, иммобилизованной на Amberlite XAD 7HP, или для CALB и липазы TL, или для CALB и липазы PS. Условия реакции: соевое масло (2,5 г) и метанол (3 порции, каждая по 91 мг) смешивали с 250 мг иммобилизованной липазы при 30°С в течение 6 часов. Одну и ту же порцию биокатализатора использовали в 50 реакционных циклах в одних и тех же условиях.
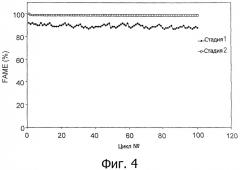
Фигура 4: FAME в % в двухстадийном способе трансэстерификации с помощью липазы PS и CALB, оба фермента иммобилизованы на Amberlite XAD 7HP. Условия реакции: реакцию начинали добавлением биокатализатора (30 г) к соевому маслу (220 г) и метиловому спирту (23,9 г) в стеклянном реакторе с двойной рубашкой, имеющем дно с фильтром из спеченного стекла с пористостью 70-100 мкм. Метанол добавляли порциями, каждая порция составляла 1/3 от стехиометрического количества, или титровали по каплям. Реакционную систему механически перемешивали при 30°С в течение 2 часов. Реакционную среду после первой стадии удаляли, центрифугировали, чтобы убрать глицерин и затем вводили в реактор для второй стадии и перемешивали в течение двух часов.
Осуществление изобретения
Чтобы усовершенствовать и облегчить энзиматическое получение биодизеля, настоящее изобретение в первую очередь нацелено на предупреждение деактивации ферментов или потери ферментативной активности вследствие отсоединения иммобилизованного фермента от носителя, на котором он иммобилизован, которое обычно происходит из-за воздействия метанола, который является одним из исходных веществ, или из-за воздействия глицерина и воды, образуемых в этом процессе. Липаза Novozyme 435 {липаза Candida antarctica Б), иммобилизованная на адсорбенте, которую использовали в прошлом, характеризуется потерей активности менее чем через 10 реакционных циклов из-за указанного выше снижения ферментативной активности. Целью настоящего изобретения является решение этой проблемы.
Кроме того, чтобы достичь превращений до уровня более чем 96%, время реакции трансэстерификации масел и метанола становится относительно долгим и обычно составляет диапазон 24-48 часов с указанным ферментом Novozyme 435, а также с другими липазами. Также целью изобретения является обеспечение способа и препаратов ферментов, которые должны значительно уменьшить время реакции.
Кроме того, побочный продукт глицерин, образующийся при этом способе, приводит к снижению ферментативной активности, так как он остается на частицах биокатализатора. Прилипание глицерина к биокатализаторам приводит к снижению или иногда к полной потере ферментативной активности. Способ и препараты изобретения также нацелены на решение этой проблемы.
Кроме того, в работах предшествующего уровня техники использовали липазы, которые приводили к образованию и аккумуляции в реакционной системе неполных глицеридов, включающих моно- и диглицериды. Низкие скорости реакции трансэстерификации у таких липаз для этих субстратов вызывали увеличение времени реакции, необходимого для того, чтобы достигнуть превращения более чем на 96%. Настоящее изобретение обеспечивает препараты ферментов, систему и способ, которые облегчают высокую скорость выведения образующихся интермедиатов в ходе ферментативной трансэстерификации и таким образом достигают высокой степени превращения в короткие времена реакции.
В частности, изобретение обеспечивает применение мультиферментной системы в одно- или двухстадийных способах, которое преодолевает указанные выше затруднения, приводит к неожиданным результатам, и демонстрирует синергизм между иммобилизованными ферментами и устраняет деактивацию ферментов или потерю ферментативной активности, в том числе и из-за эффективных комбинаций липаза-липаза, а также комбинаций липаза-матрикс.
Авторы настоящего изобретения, таким образом, усовершенствовали высокоактивные и стабильные препараты иммобилизованных ферментов, обладающих высокой устойчивостью в отношении гидрофильных субстратов, таких как короткоцепочечные спирты, полиолы и короткоцепочечные жирные кислоты, для улучшения ферментативных способов получения сложных алкиловых эфиров жирных кислот, в особенности сложных метиловых эфиров жирных кислот «биодизеля». Кроме того, как было указано выше в разделе «Раскрытие изобретения», смесь липаз также может состоять из более чем двух липаз, предпочтительно быть смесью из трех липаз, где первая липаза обладает позиционной специфичностью к положению sn-1,3, вторая липаза обладает большей селективностью в отношении положения sn-2, чем позиционно неспецифичные липазы, в частности чем позиционно неспецифичные липазы, полученные из Candida rugosa, и третья липаза обладает повышенной аффинностью в отношении моно- и диглицеридов.
Следует отметить, что по всему тексту заявки, если ссылаются на положения sn-1, sn-2- или sn-3, то речь идет о положениях в углеродном скелете глицерина в различных глицеридах.
То, что липаза обладает более высокой селективностью в отношении положения sn-2, чем позиционно неспецифичная липаза, означает, что такой фермент предпочтительно катализирует реакцию между спиртом или донором спирта с жирнокислотной группой в положении sn-2, тогда как позиционно неспецифичные липазы демонстрируют одну и ту же трансэстерификационную активность в отношении жирнокислотных групп во всех трех положениях углеродного скелета глицерина.
Как будет показано ниже в разделе «Примеры» (например, при отсылке к Candida Antarctica A (CALA)), некоторые ферменты уникальным образом демонстрируют позиционную активность в отношении положения sn-2, в особенности в специфических условиях, определяемых субстратами, продуктами и т.д. Ферменты, применяемые в этом документе в этом качестве, демонстрируют дифференцированную позиционную селективность относительно положения sn-2 и способность к трансэстерификации sn-2 неполных глицеридов.
Усовершенствованный биокатализатор состоит из смеси липаз различных типов, иммобилизованных на полимерном матриксе, предпочтительно пористом, сетчатом матриксе на основе гидрофобных алифатических или ароматических полимеров. В соответствии с изобретением различные липазы могут быть иммобилизованы в одном и том же реакционном сосуде или по отдельности, на одном и том же или различных носителях. Необязательно различные липазы могут быть иммобилизованы по отдельности на различных носителях, в зависимости от наилучшей комбинации фермент-носитель, в соответствии с их устойчивостью к короткоцепочечным спиртам, эстерификационной/трансэстерификационной активностью и временем эксплуатации для биокатализатора. Смесь липаз в соответствии с изобретением включает липазу, которая является позиционно специфичной к положению sn-1, 3, вместе с позиционно неспецифичной липазой, в частности, липазу, которая обладает аффинностью в отношении неполных глицеридов, и необязательно третью липазу с высокой аффинностью в отношении положения sn-2.
Липаза, позиционно специфичная к положению sn-1,3, может быть липазой из Thermomyces lanuginosa, Rhizomucor miehei, Mucor miehei, Pseudomonas sp., Rhizopus sp., Mucor javanicus, Penicillium roqueforti, Aspergillus niger, Acromobacter sp. или Burkholderia sp., но не ограничивается только ими. Липаза с более высокой специфичностью в отношении положения sn-2 по сравнению с позиционно неспецифичными липазами может быть липазой из Candida antarctica А и липазой из Pseudozyma sp., но не ограничивается только ими. Липаза, обладающая повышенной аффинностью к неполным глицеридам, может быть липазой из Candida antarctica В, Candida rugosa, Alcaligenes sp. или Penicillium camembertii, но не ограничивается только ими. Другие липазы, рассматриваемые в объеме настоящей заявки, могут быть липазами из Rhizopus niveus, Rhizopus oryzae, Burkholderia sp., Chromobacterium viscosum, липазой семян папайи или панкреатина.
Иммобилизацию различных липаз можно проводить или в одном сосуде, или по отдельности.
Нерастворимый носитель способен к связыванию липаз путем физической адсорбции или путем ковалентного связывания с его функциональными группами. Термины «физически адсорбированный» или «физическая адсорбция», используемые в этом документе, могут быть синонимами терминов «иммобилизованный» и «иммобилизация», соответственно. Термины «носитель» и «матрикс» могут быть использованы в этом документе как синонимы. Носитель предпочтительно является гидрофобным пористым носителем, который может быть органическим или неорганическим, и который предпочтительно выбирают из группы, состоящей из пористого неорганического носителя, такого как носители на основе оксида кремния или оксида алюминия, органических носителей, например, включающих без ограничения гидрофобные алифатические и акриловые сетчатые полимеры, или носителя на основе гидрофобных ароматических сетчатых полимеров, такого как AmberliteR XAD 7HP и AmberliteR XAD 1600, соответственно, где указанный носитель необязательно может содержать активные функциональные группы, такие как эпоксигруппы или альдегидные группы, или ионные группы. Специфическими примерами подходящих носителей, не ограничивающих настоящее изобретение, являются Amberlite XAD, такой как XAD 4, XAD 16, XAD-1600, XAD 7HP, XAD 16HP, XAD 1180, Amberlite FPA53, Amberlite FPC22H, Amberlite FPA40C1, Amberlite IRC50, Duolite, такой как A7, A561, A568 и Duolite C467, Amberlyst A-21, Dowex Monosphere 77, Dowex Optipore L493, Dow Styrene DVB, MTO Dowex Optipore SD-2, Dowex MAC-3, Purolire A109, и Sepabeads, такой как EC-EA, EC-EP, EC-BU и EC-OD. Предпочтительными являются носители, которые состоят из гидрофобных сетчатых ароматических полимеров, состоящих из дивинилбензола или дивинилбензола и стирола, и гидрофобных алифатических полимеров, состоящих из сетчатых алифатических акриловых полимеров.
В следующем аспекте изобретение обеспечивает способ получения биодизеля, как было детально описано в разделе «Раскрытие изобретения».
Кроме того, в способе получения биодизеля в соответствии с изобретением может происходить постоянное удаление всех или некоторых продуктов реакции и/или побочных продуктов, которые самопроизвольно десорбируются с носителя фермента. Самопроизвольная или спонтанная десорбция продукта/побочных продуктов с носителя, несущего фермент, является уникальным свойством иммобилизованных ферментных систем изобретения. Не ограничиваясь рамками определенного механизма, следует отметить, что это свойство может быть обусловлено гидрофобной природой матрикса, который отвечает за отталкивание образованного гидрофильного глицерина или других гидрофильных веществ, находящихся рядом с иммобилизованным биокатализатором. Раскрытый энзиматический способ можно осуществлять или в одну стадию, или в две стадии, чтобы достичь превращения исходных материалов в соответствующие сложные алкиловые эфиры жирных кислот более чем на 98%. В новом способе, относящемся к настоящему изобретен