Предупреждение и лечение субклинической формы болезней, вызываемых цирковирусом свиней (pcvd)
Иллюстрации
Показать всеЗаявленная группа изобретений относится к области ветеринарии и предназначена для лечения субклинической формы вызываемой PCV2 инфекции у животных. Заявлены способ лечения субклинической формы вызываемой PCV 2 инфекции; способ уменьшения нарушения роста из-за субклинической формы вызываемой PCV2 инфекции; способ снижения количества животных с вирусной нагрузкой, превышающей 106 геномных копий на мл сыворотки; способ снижения выделения вируса из носа и/или продолжительности виремии у животных, инфицированных субклинической формой PCV2. Заявленные способы включают этап введения терапевтически эффективного количества протеина OFR-2 PCV2 или иммуногенной композиции, содержащей протеин OFR-2 PCV2, животному, которое нуждается в таком введении. При этом субклиническая форма вызываемой PCV2 инфекции отличается уровнем вирусной нагрузки в организме индивидуального животного менее 106 геномных копий PCV2 на мл сыворотки. Заявлено также применение протеина OFR-2 PCV2 для приготовления лекарственного средства, предназначенного для осуществления заявленных способов. Заявленная группа изобретений высокоэффективна для лечения субклинической формы вызываемой PCV2 инфекции животных. 8 н. и 16 з.п. ф-лы, 5 ил., 3 табл., 3 пр.
Реферат
В настоящую заявку входит перечень последовательностей в бумажной и электронной версии, сущность и содержание которых включены в настоящее описание в качестве ссылки. Перечень последовательностей идентичен перечню, включенному в WO 06/072065.
Предпосылки создания изобретения
Область техники, к которой относится изобретение
Настоящее изобретение относится к применению иммуногенной композиции, которая содержит антиген цирковируса свиней типа 2 (PCV2), для предупреждения и лечения субклинических (хронических) форм вызываемых PCV2 инфекций у животных, предпочтительно у молодых (не достигших половой зрелости) свиней.
Описание известного уровня техники
Цирковирус свиней типа 2 (PCV2) представляет собой небольшой (диаметром 17-22 нм) ДНКовый не имеющий оболочки вирус с икосаэдральной структурой, который несет одноцепочечный кольцевой геном. Последовательность PCV2 примерно на 80% идентична последовательности цирковируса свиней типа 1 (PCV1). Однако в настоящее время установлено, что в отличие от PCV1, который, как правило, является невирулентным, заражение свиней PCV2 ассоциировано с рядом болезненных синдромов, которые в целом обозначают как болезни, вызываемые цирковирусом свиней (PCVD) (известные также как цирковирус-ассоциированные заболевания свиней (PCVAD)) (Allan и др., IPVS Congress, 2006). Как правило, основным клиническим проявлением PCVD считается синдром послеотъемного мультисистемного истощения (PMWS) (Harding и др., Swine Health Prod; 5, 1997, cc.201-203; Kennedy и др., J Comp Pathol; 122, 2000, cc.9-24). Из литературы известно несколько других потенциально родственных состояний, включая комплекс респираторных болезней свиней (PRDC), синдром свиного дерматита и нефропатии (PDNS), снижение репродуктивной функции, гранулематозные энтериты и, возможно, врожденный тремор (CT-AII) и перинатальный миокардит (Chae, Veterinary J., 169, 2005, cc.326-336).
PCVD поражает молодых свиней возрастом 5-22 недели. С клинической точки зрения PCVD характеризуется истощением, бледностью кожи, худосочностью, респираторным дистресс-синдромом, диареей, желтухой и разлитием желчи. У некоторых пораженных заболеванием свиней проявляется комбинация всех симптомов, в то время как у других свиней проявляются только один или два из указанных симптомов (Muirhead, Vet. Rec., 150, 2002, с.456). Коэффициенты смертности у свиней, инфицированных PCV2, могут достигать 50%. При вскрытии трупа выявляют также микроскопические и макроскопические повреждения многих тканей и органов, причем наиболее часто повреждения встречаются в лимфоидных органах (Allan и Ellis, J Vet. Diagn. Invest., 12, 2001, cc.3-14). Обнаружена выраженная корреляция между уровнем нуклеиновой кислоты или антигена PCV2 и серьезностью микроскопических лимфоидных повреждений (Brunborg, 2004). Кроме того, обнаружена корреляция между уровнем нуклеиновой кислоты или антигена в крови и серьезностью клинических симптомов (Brunborg, 2004; Liu, 2000; Olvera, 2004). Установлено, что у молодых свиней, страдающих PCVD, уровень вирусной нагрузки превышал 106 геномных эквивалентов на мл.
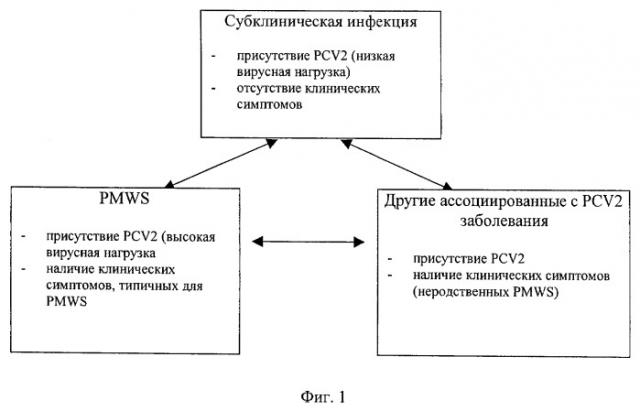
В отличие от клинически выраженных проявлений болезней, вызываемых PCV2, считается, что субклинические формы вызываемых PCV2 инфекций присутствуют у тех животных, которые инфицированы PCV2, но имеют клинически бессимптомное течение. В целом, существует взаимосвязь между этими формами вызываемых PCV2 инфекций, поскольку субклинические формы инфекций могут легко переходить в PCVD, и поэтому выздоравливающие животные могут оставаться постоянно зараженными в течение длительного периода времени (хронически) (см. фиг.1).
В современных исследованиях продемонстрировано, что субклинические формы вызываемых PCV2 инфекций часто встречаются. Наличие субклинической формы инфекций продемонстрировано как экспериментально, так и в полевых условиях. В лабораторных опытах можно продемонстрировать, что вызываемая PCV2 инфекция индивидуальных молодых свиней не всегда связана с клиническими симптомами или повреждениями (Harms и др. Vet. Pathol., 38, 2001, cc.528-539). Кроме того, в нескольких полевых опытах установлено, что заболеваемость инфицированных PCV2 серопозитивных стад выше, чем заболеваемость стад, пораженных PCVD (Olvera и др., J. Virol. Methods, 117, 2004, cc.75-80). Часто стада, в которых обнаружена острая вспышка PCVD, остаются инфицированными PCV2 без проявления заметных клинических симптомов. В литературе принято обозначать также эту субклиническую (постоянную) форму заражения стада как «хроническую» инфекцию (Burch D., Pig International, 2006).
Экономическая роль PCV2 в инфицированных субклинической формой стадах, если это имеет место, является неизвестной, и ранее никогда не была описана. В частности, пока не известно и не установлено, могут ли субклинические формы вызываемых PCV2 инфекций оказывать влияние на показатели роста животных или на общее состояние здоровья в целом пораженных животных.
Подходы к лечению вызываемых PCV2 инфекций, основанные на применении ДНК-вакцины, описаны в US 6703023. В WO 03/049703 описано получение живой химерной вакцины, содержащей каркас PC VI, в котором ген каркаса PCV1 заменен на иммуногенный ген патогенных штаммов PCV2. В WO 99/18214 описано несколько штаммов PCV2 и процедуры получения убитой вакцины против PVC2. Однако отсутствуют данные об их эффективности. Эффективная субъединичная вакцина на основе ОРС-2 (открытая рамка считывания 2) описана в WO 06/072065. Любая из указанных вакцин предназначена для применения с целью вакцинации/лечения свиней или молодых свиней старше 3 недель. Ни для одной из указанных вакцин не описано применение для профилактики или лечения животных с субклинической формой вызываемой PCV2 инфекции. Кроме того, не описано, что такие вакцины могут вызывать иммунитет против вызываемой PCV2 инфекции у групп животных с субклинической формой заболевания и улучшать показатели их роста. Краткое описание чертежей
На чертежах показано:
на фиг.1 - различные формы вызываемых PCV2 инфекций,
на фиг.2 - коэффициент смертности и среднесуточный прирост массы в период откорма, определенный на опытной ферме до и после начала эксперимента,
на фиг.3 - динамика различия между массой тела (IVP-CP (обработка исследуемым ветеринарным продуктом/контрольным продуктом)) и средним уровнем вирусной нагрузки (log 10) в процессе эксперимента,
на фиг.4 - сравнение процента животных с уровнем вирусной нагрузки >10 геномных эквивалентов/мл сыворотки в обеих обрабатываемых группах,
на фиг.5 - сравнение процента животных с уровнем вирусной нагрузки в сыворотке 104-10Е6 геномных эквивалентов/мл сыворотки в обеих обрабатываемых группах.
Подробное описание изобретения
Клиническое проявление вызываемых PCV2 инфекций ассоциировано с различными синдромами заболевания. В зависимости от формы проявления выражения родственного PCV2 заболевания клинические симптомы острой вызываемой PCV2 инфекции могут представлять собой один или несколько из следующих показателей: а) существенное повышение коэффициента смертности (повышение на 4-20%), б) существенное повышение частоты встречаемости «малорослых» животных (повышение на 5-50%) или в) другие симптомы клинического проявления, такие как респираторные симптомы, диарея, бледность кожи, желтуха, худосочность (коэффициент заболеваемости 4-60%). Кроме того, высокие вирусные титры, превышающие 106 или 107 на мл сыворотки или ткани, являются характерным признаком у большинства животных с острыми симптомами PCVD. Помимо острой вызываемой PCV2 инфекции, субклиническая форма вызываемых PCV2 инфекций, отличающаяся отсутствием заболеваемости или низким коэффициентом заболеваемости, становится все более и более распространенной. В некоторых случаях острая вызываемая PCV2 инфекция может переходить в субклиническую форму вызываемой PCV2 инфекции. Однако субклинические формы инфекций могут также иметь место без наличия каких-либо предшествующих симптомов острой вызываемой PCV2 инфекции.
При создании изобретения неожиданно было установлено, что субклиническая форма вызываемой PCV2 инфекции оказывает существенное воздействие на характеристики внешне здоровых молодых свиней, в частности на показатель роста молодых свиней. Даже если при субклинической форме у инфицированных животных не развиваются типичные клинические симптомы, которые позволяют идентифицировать PCVD, или у них обнаружен лишь невысокий уровень заболеваемости, эти животные в значительной степени поражены субклинической формой вызываемой PCV2 инфекции. Субклиническая форма вызываемых PCV2 инфекций у молодых свиней приводит к заметной потере прироста массы (см. пример 3). Как отмечалось ранее, в существующих к настоящему времени прототипах отсутствуют данные о том, что субклиническая форма вызываемых PCV2 инфекций оказывает какое-либо воздействие на здоровье, в частности показатель роста молодых свиней.
Кроме того, при создании изобретения неожиданно было установлено, что снижение прироста массы, обусловленное субклинической формой вызываемой PCV2 инфекции, можно уменьшать путем лечения/вакцинации животных, которые приобрели субклиническую форму заболевания, антигеном PCV2 (например, см. пример 3). Таким образом, при создании изобретения не только было установлено, что субклиническая форма вызываемых PCV2 инфекций влияет по показатель роста молодых свиней, но получены также данные о том, что такое отрицательное воздействие можно существенно снижать путем лечения/вакцинации животных антигеном PCV2. Другими словами, даже если из существующего уровня техники известен феномен субклинической формы инфекций, при создании изобретения впервые были получены данные о том, что
- субклиническая форма вызываемой PCV2 инфекции, иногда обнаруживаемая в полевых условиях, может оказывать существенное влияние на показатель роста молодых свиней;
- вакцинация пораженных субклинической формой молодых свиней или стад с помощью антигена PCV2 может существенно снижать отрицательное воздействие этой субклинической формы вызываемой PCV2 инфекции.
Таким образом, одним из объектов настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции у животного или группы животных, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении.
«Субклиническая форма вызываемой PCV2 инфекции» в контексте настоящего описания характеризуется I) вирусной нагрузкой в организме индивидуального животного, которая сохраняется в течение всей жизни на уровне ниже 106 геномных копий PCV2 на мл сыворотки, II) низким относительным количеством РСV2-позитивных животных в группе или стаде с вирусными титрами, превышающими 106 геномных копий на мл сыворотки, III) сохранением вируса в группе или стаде в течение по меньшей мере 6 недель, предпочтительно по меньшей мере 8 недель, более предпочтительно по меньшей мере 10 недель, наиболее предпочтительно по меньшей мере 12 недель, IV) отсутствием типичных клинических симптомов у РСV2-позитивного животного, V) отсутствием или лишь невысоким коэффициентом заболеваемости в группе животных или стаде РСV2-позитивных животных и/или VI) невысоким коэффициентом смертности в группе животных или стаде РСV2-позитивных животных.
Понятие «низкое относительное количество РСV2-позитивных животных», которое используется выше в качестве критерия II), означает, что менее 20%, предпочтительно менее 15%, еще более предпочтительно менее 10%, еще более предпочтительно менее 8%, еще более предпочтительно менее 6%, еще более предпочтительно менее 4%, наиболее предпочтительно менее 3% PCV-2-позитивных животных в группе животных или в стаде имеют вирусные титры, превышающие 106 геномных копий на мл сыворотки. Другими словами, понятие «низкое относительное количество РСV2-позитивных животных в группе животных или в стаде, которые имеют вирусные титры, превышающие 10 геномных копий на мл сыворотки» означает также, что более 80%, предпочтительно более 85%, еще более предпочтительно более 90%, еще более предпочтительно более 92%, еще более предпочтительно более 94%, еще более предпочтительно более 96%, наиболее предпочтительно более 97% PCV2-позитивных животных в группе или стаде имеют вирусные титры ниже 10 геномных копий PCV2 на мл сыворотки.
Понятие «РСV2-позитивный» в контексте настоящего описания означает, но, не ограничиваясь только указанным, что животное содержит выявляемое количество геномных эквивалентов PCV2 (т.е. вирусных копий) в образце (1 мл сыворотки или 1 мг ткани). Выявляемое количество геномных эквивалентов PCV2 означает, что геномные эквиваленты PCV2 можно выявлять с помощью анализа на основе полимеразной цепной реакции (ПЦР). Образец считается ПЦР-позитивным, если два независимых образца дают положительный результат по данным ПЦР при таком анализе.
Методы количественной оценки PCV2 с помощью ПЦР-анализа хорошо известны в данной области. Фактически количественную оценку геномных эквивалентов PCV2 осуществляли/осуществляют с помощью метода, описанного у Brunborg и др., J.Virol Methods 122, 2004, cc.171-178. Для амплификации PCV2 применяли/применяют праймеры PCV2-84-1265U21 и PCV2-84-1319L21. Такой метод можно применять в качестве референс-анализа в случае любых сомнений.
Понятие «сохранение вируса» в контексте настоящего описания означает, что зараженное животное имеет вирусную нагрузку по меньшей мере 104 вирусных копий PCV2 на мл сыворотки в течение указанного выше периода времени, т.е. по меньшей мере 6 недель или более.
Понятие «отсутствие типичных клинических симптомов у PCV2-позитивного животного» в контексте настоящего описания означает отсутствие любых видимых клинических симптомов, которые в норме ассоциированы с клиническим проявлением вызываемой PCV2 инфекции, что позволяет точно и недвусмысленно идентифицировать вызываемую PCV2 инфекцию только на основе типичного клинического проявления. Эти клинические симптомы соответствуют известным для PCVD, в частности представляют собой бледность кожи, худосочность, респираторный дистресс-синдром, диарею, желтуху или разлитие желчи.
Понятие «невысокий коэффициент заболеваемости» в контексте настоящего описания является показателем отсутствия клинических симптомов, которые позволяют идентифицировать острую вызываемую PCV2 инфекцию по ее клиническому проявлению. Это является также показателем присутствия субклинической формы вызываемой PCV2 инфекции. Понятие «невысокий коэффициент заболеваемости» в контексте настоящего описания относится к проценту животных с измененным общим состоянием здоровья. Понятие «измененное общее состояние здоровья» в контексте настоящего описания относится к наличию одного или нескольких связанных с PCVD клинических симптомов, таких как наличие «малорослых» животных (к которым в контексте настоящего описания относятся животные, у которых масса тела на 25% ниже, чем средняя массы животных такой же возрастной группы), бледность кожи, худосочность, респираторный дистресс-синдром, диарея, желтуха или разлитие желчи. Таким образом, «невысокий коэффициент заболеваемости» в контексте настоящего описания означает, что у менее 25%, предпочтительно у менее 20%, более предпочтительно у менее 15%, еще более предпочтительно у менее 12%, еще более предпочтительно у менее 10%, еще более предпочтительно у менее 8%, еще более предпочтительно у менее 6%, наиболее предпочтительно у менее 4% животных в группе животных или в стаде обнаружен один или несколько клинических симптомов PCVD, предпочтительно обнаружено наличие «малорослых» животных, как определено выше, бледности кожи, худосочности, респираторного дистресс-синдрома, диареи, желтухи или разлития желчи.
Понятие «отсутствие коэффициента заболеваемости» в контексте настоящего описания означает, что менее чем у 1% РСV2-позитивных животных в группе животных или стаде обнаружен один или несколько клинических симптомов PCVD, предпочтительно обнаружено наличие «малорослых» животных, как определено выше, бледности кожи, худосочности, респираторного дистресс-синдрома, диареи, желтухи или разлития желчи.
Понятие «невысокий коэффициент смертности» в контексте настоящего описания означает, но, не ограничиваясь только указанным, что коэффициент смертности РСV2-позитивных животных в группе животных или стаде составляет менее 20%, предпочтительно менее 15%, более предпочтительно менее 12%, еще более предпочтительно менее 10%, еще более предпочтительно менее 8%, еще более предпочтительно менее 6%, наиболее предпочтительно менее 4%.
Понятие «нуждающийся в таком введении» или «нуждающийся в таком лечении» в контексте настоящего описания означает, что введение/лечение ассоциировано с профилактикой здоровья или с любым другим положительным воздействием на здоровье животных, получающих антиген PCV2.
Согласно предпочтительному варианту осуществления изобретения принимается, что субклиническая форма вызываемой PCV2 инфекции относится к случаю, удовлетворяющему по меньшей мере критерию I) «вирусная нагрузка в организме индивидуального животного, которая сохраняется с течение всей жизни на уровне ниже 106 геномных копий PCV2 на мл сыворотки», критерию
II) «низкое относительное количество РСV2-позитивных животных в группе или стаде с вирусными титрами, превышающими 106 геномных копий на мл сыворотки», или критерию III) «сохранение вируса в группе или стаде в течение по меньшей мере 6 недель, предпочтительно по меньшей мере 8 недель, более предпочтительно по меньшей мере 10 недель, наиболее предпочтительно по меньшей мере 12 недель». Наиболее предпочтительно принимается, что субклиническая форма вызываемой PCV2 инфекции относится к случаю, удовлетворяющему указанным выше критериям I) и II).
В случаях, когда критерий I) и/или критерий II) объединены с критерием
III) «сохранение вируса в группе или стаде в течение по меньшей мере 6 недель, предпочтительно по меньшей мере 8 недель, более предпочтительно по меньшей мере 10 недель, наиболее предпочтительно по меньшей мере 12 недель» или в любых других случаях, удовлетворяющих критерию III), как указано выше, то субклиническая форма инфекции рассматривается как «хроническая субклиническая форма вызываемой PCV2 инфекции».
Другим объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, в котором субклиническая форма вызываемой PCV2 инфекции отличается вирусной нагрузкой в организме индивидуального животного на уровне ниже 10 геномных копий PCV2 на мл сыворотки, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно субклиническая форма вызываемой PCV2 инфекции отличается также присутствием менее 20% животных, несущих более 106, предпочтительно более 107 вирусных копий PCV2 на мл сыворотки, в группе животных или стаде и/или отличается сохранением вируса в такой группе или стаде в течение по меньшей мере 6 недель, предпочтительно по меньшей мере 8 недель, более предпочтительно по меньшей мере 10 недель, наиболее предпочтительно по меньшей мере 12 недель. Более предпочтительно такая субклиническая форма инфекции отличается также отсутствием каких-либо клинических симптомов у индивидуального РСV2-позитивного животного, как определено выше, отсутствием или невысоким коэффициентом заболеваемости, как определено выше, и/или невысоким коэффициентом смертности, как определено выше.
Следующим объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, в котором субклиническая форма вызываемой PCV2 инфекции отличается вирусной нагрузкой в организме индивидуального животного, которая может сохраняться в течение всей его жизни на уровне ниже 106 геномных копий PCV2 на мл сыворотки, в отсутствии какого-либо введения антигена PCV2, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно субклиническая форма вызываемой PCV2 инфекции отличается также присутствием менее 20% животных в группе животных или в стаде, которые имеют вирусные титры, превышающие 106, предпочтительно 107 вирусных копий PCV2 на мл сыворотки, и/или отличается сохранением вируса в такой группе или стаде в течение по меньшей мере 6 недель, предпочтительно по меньшей мере 8 недель, более предпочтительно по меньшей мере 10 недель, наиболее предпочтительно по меньшей мере 12 недель. Более предпочтительно такая субклиническая форма инфекции отличается также отсутствием каких-либо клинических симптомов у индивидуального РСV2-позитивного животного, как определено выше, отсутствием или невысоким коэффициентом заболеваемости, как определено выше, и/или невысоким коэффициентом смертности, как определено выше.
Таким образом, следующим объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, в котором субклиническая форма вызываемой PCV2 инфекции отличается присутствием менее 20% животных в группе животных или в стаде, которые имеют вирусные титры, превышающие 106, предпочтительно 107 вирусных копий PCV2 на мл сыворотки, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно субклиническая форма вызываемой PCV2 инфекции отличается также сохранением вируса в такой группе или стаде в течение по меньшей мере 6 недель, предпочтительно по меньшей мере 8 недель, более предпочтительно по меньшей мере 10 недель, наиболее предпочтительно по меньшей мере 12 недель. Более предпочтительно такая субклиническая форма инфекции отличается также отсутствием каких-либо клинических симптомов у индивидуального РСV2-позитивного животного, как определено выше, отсутствием или невысоким коэффициентом заболеваемости, как определено выше, и/или невысоким коэффициентом смертности, как определено выше.
Следующим объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, в котором субклиническая форма вызываемой PCV2 инфекции отличается сохранением вируса в такой группе или стаде в течение по меньшей мере 6 недель, предпочтительно по меньшей мере 8 недель, более предпочтительно по меньшей мере 10 недель, наиболее предпочтительно по меньшей мере 12 недель. Предпочтительно такая субклиническая форма вызываемой PCV2 инфекции отличается также отсутствием каких-либо клинических симптомов у индивидуального РСV2-позитивного животного, как определено выше, отсутствием или невысоким коэффициентом заболеваемости, как определено выше, и/или невысоким коэффициентом смертности, как определено выше.
Еще одним объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, в котором субклиническая форма вызываемой PCV2 инфекции отличается отсутствием каких-либо клинических симптомов у индивидуального PCV2-позитивного животного, как определено выше, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно субклиническая форма вызываемой PCV2 инфекции отличается также отсутствием или невысоким коэффициентом заболеваемости, как определено выше, и/или невысоким коэффициентом смертности, как определено выше. Более предпочтительно субклиническая форма вызываемой PCV2 инфекции отличается также тем, что вирусная нагрузка в организме индивидуального животного сохраняется в течение всей его жизни на уровне ниже 10 геномных копий PCV2 на мл сыворотки и/или низким относительным количеством PCV-2-позитивных животных в группе или стаде, которые имеют вирусные титры, превышающие 106 геномных копий на мл сыворотки.
Еще одним объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, в котором субклиническая форма вызываемой PCV2 инфекции отличается отсутствием или невысоким коэффициентом заболеваемости в группе животных или стаде, предпочтительно на уровне, не превышающем 25% или ниже, как определено выше, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно субклиническая форма вызываемой PCV2 инфекции отличается также тем, что вирусная нагрузка в организме индивидуального животного сохраняется в течение всей его жизни на уровне ниже 106 геномных копий PCV2 на мл сыворотки и/или низким относительным количеством PCV-2-позитивных животных в группе или стаде, которые имеют вирусные титры, превышающие 106 геномных копий на мл сыворотки.
Следующим объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, в котором субклиническая форма вызываемой PCV2 инфекции отличается невысоким коэффициентом смертности, как определено выше, предпочтительно на уровне, не превышающем 20% или ниже, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно субклиническая форма вызываемой PCV2 инфекции отличается также тем, что вирусная нагрузка в организме индивидуального животного сохраняется в течение всей его жизни на уровне ниже 106 геномных копий PCV2 на мл сыворотки и/или низким относительным количеством PCV-2-позитивных животных в группе или стаде, которые имеют вирусные титры, превышающие 106 геномных копий на мл сыворотки.
Введение в эффективном количестве антигена PCV2 животным или группе животных, которые имеют субклиническую форму вызываемой PCV2 инфекции, приводит к повышению прироста массы у этих животных в процессе периода откорма, к снижению количества животных с уровнем вирусной нагрузки, составляющим 10-10 геномных копий на мл сыворотки, к снижению выделения вируса через нос и/или снижению продолжительности виремии.
Таким образом, следующим объектом настоящего изобретения является также способ снижения потери прироста массы у животных с субклинической формой вызываемой PCV2 инфекции, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно средний прирост массы возрастает в период с 10 по 22 неделю жизни более чем на 1,5 кг по сравнению с невакцинированными животными. Понятие «в процессе периода откорма» в контексте настоящего описания означает, но, не ограничиваясь только указанными, животных возрастом от 1 до 36 недель, предпочтительно от 10 до 28 недель.
Понятие «животные с субклинической формой вызываемой PCV2 инфекции» в контексте настоящего описания относится к индивидуальному животному, которое становится субклинически инфицированным PCV2, но относится также к группе животных, где большинство животных в этой группе становятся субклинически инфицированными PCV2. Таким образом, понятие «животные с субклинической формой вызываемой PCV2 инфекции» относится как к I) «животным с субклинической формой вызываемой PCV2 инфекции», так и к II) « животным стада, где стадо субклинически инфицировано PCV2».
Таким образом, еще одним объектом настоящего изобретения является способ снижения количества животных с уровнем вирусной нагрузки, составляющим 104-106 геномных копий на мл сыворотки, в группе животных (стаде), субклинически инфицированном PCV2, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно количество животных с уровнем вирусной нагрузки, составляющим 104-106 геномных копий на мл сыворотки, может снижаться в результате вакцинации антигеном PCV2 до менее чем 30%, предпочтительно до менее чем 20%, еще более предпочтительно до менее чем 10%, наиболее предпочтительно до менее чем 5%, в то время как в невакцинированной контрольной группе субклинически инфицированных животных (с уровнем вирусной нагрузки, составляющим 10-10 геномных копий на мл сыворотки) более чем у 40% возникают титры PCV2, составляющие от 104 до 10 геномных копий на мл сыворотки.
Таким образом, еще одним объектом настоящего изобретения является также способ снижения количества животных с клинически значимым уровнем вирусной нагрузки (превышающим 106 геномных копий на мл сыворотки) в группе животных (стаде), субклинически инфицированной PCV2, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Предпочтительно количество животных с уровнем вирусной нагрузки, превышающим 106 геномных копий на мл сыворотки, можно снижать в результате вакцинации антигеном PCV2 до менее чем 10%, предпочтительно до менее чем 5%, еще более предпочтительно до менее чем 4%, еще более предпочтительно до менее чем 3%, еще более предпочтительно до менее чем 2%, наиболее предпочтительно до менее чем 0,5%.
Таким образом, еще одним объектом настоящего изобретения является также способ снижения выделения вируса через нос, снижения продолжительности виремии у животных с субклинической формой вызываемой PCV2 инфекции, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении. Как описано выше, вакцинация/лечение животных с субклинической формой вызываемой PCV2 инфекции приводит к укорочению фазы виремии по сравнению с невакцинированными контрольными животными. Среднее укорочение продолжительности виремии составляло 17 дней по сравнению с невакцинированными контрольными животными этого же вида. Таким образом, еще одним объектом настоящего изобретения является также способ снижения продолжительности виремии у животных с субклинической формой вызываемой PCV2 инфекции, заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении, где лечение или профилактика приводят к укорочению фазы виремии на 5 или более дней, предпочтительно 6 или более дней, еще более предпочтительно 7 или более дней, еще более предпочтительно 8 или более дней, еще более предпочтительно 9 или более дней, еще более предпочтительно 10 или более дней, еще более предпочтительно 12 или более дней, еще более предпочтительно 14 или более дней, наиболее предпочтительно более 16 дней, по сравнению с невакцинированными контрольными животными этого же вида.
Понятие «антиген» в контексте настоящего описания относится к аминокислотной последовательности, которая вызывает иммунный ответ у хозяина. Антиген в контексте настоящего описания включает полноразмерную последовательность любых белков PCV2, их аналогов или их иммуногенных фрагментов. Понятие «иммуногенный фрагмент» обозначает фрагмент белка, который содержит один или несколько эпитопов и в результате этого вызывает иммунный ответ у хозяина. Такие фрагменты можно идентифицировать с помощью любого из многочисленных методов картирования эпитопов, хорошо известных в данной области (см., например, Epitope Mapping Protocols in Methods in Molecular Biology, том 66, под ред. Glenn E.Morris, изд-во Humana Press, Totowa, New Jersey, 1996). Например, линейные эпитопы можно выявлять, например, осуществляя конкурентный синтез большого количества пептидов на твердых подложках, где пептиды соответствуют фрагментам молекулы белка, и, подвергая пептиды взаимодействию с антителами, при этом пептиды остаются прикрепленными к подложкам. Такие методы известны в данной области и описаны, например в US 4708871; у Geysen и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc. 3998-4002; Geysen и др., Molec. Immunol. 23, 1986, cc.709-715. Аналогично этому, конформационные эпитопы легко можно идентифицировать путем определения пространственной конформации аминокислот, например, с помощью рентгеновской кристаллографии и 2-мерного ядерного магнитного резонанса (см., например, Epitope Mapping Protocols, выше).
Понятие включает также синтетические антигены, например, полиэпитопы, фланкирующие эпитопы и другие полученные методами рекомбинации или синтеза антигены (см., например, Bergmann и др., Eur. J. Immunol. 23, 1993, cc.2777-2781; Bergmann и др., J. Immunol. 157, 1996, cc.3242-3249; Suhrbier A., Immunol, и Cell Biol. 75, 1997, cc.402-408; Gardner и др., 12th World AIDS Conference, Geneva, Switzerland (12-ая Всемирная конференция по СПИДу Женева, Швейцария) 28 июня-3 июля 1998 г.).
Понятие «иммунный ответ» относится, но не ограничиваясь только указанным, к формированию в хозяине клеточно- и/или антитело-опосредованного иммунного ответа на представляющий интерес антиген, композицию или вакцину. Как правило, «иммунный ответ» включает, но, не ограничиваясь только ими, одну или несколько из следующих реакций:
производство или активацию антител, В-клеток, Т-клеток-хелперов, Т-клеток-супрессоров и/или цитотоксических Т-клеток, специфически направленных на антиген или антигены, включенный(е) в представляющую интерес композицию или вакцину. Предпочтительно организм-хозяин должен вырабатывать либо терапевтический, либо защитный иммунологический (вторичный иммунный) ответ так, чтобы повышалась устойчивость к новой инфекции и/или снижалась клиническая серьезность заболевания. Такое защитное действие можно выявлять либо по снижению уровня или серьезности, либо по отсутствию одного или нескольких симптомов, ассоциированных с вызываемыми PCV2 инфекциями у хозяина, замедлению появления вируса в крови (виремия), снижению персистентности вируса, снижению общей вирусной нагрузки и/или снижению вирусной экскреции.
Понятия «иммуногенная композиция» или «вакцина» (оба понятия являются синонимами) в контексте настоящего описания относятся к любой фармацевтической композиции, которая содержит антиген PCV2, при этом, композицию можно применять для предупреждения или лечения заболевания или состояния, ассоциированного с вызываемой PCV2 инфекцией, у животного. Предпочтительная иммуногенная композиция может индуцировать, стимулировать или повышать иммунный ответ на PCV2. Под это понятие подпадают как субъединичные иммуногенные композиции, описанные ниже, так и композиции, которые содержат убитые (полностью обезвреженные) или ослабленные и/или инактивированные PCV2.
Таким образом, другим объектом настоящего изобретения является способ профилактики и лечения субклинической формы вызываемой PCV2 инфекции, способ повышения среднего прироста массы у животного или группы животных (стадо) с субклинической формой вызываемой PCV2 инфекции, способ снижения количества животных с уровнем вирусной нагрузки, составляющим от 10 до 10 геномных копий на мл сыворотки, способ снижения количества животных с уровнем вирусной нагрузки, превышающим 106 геномных копий на мл сыворотки, в субклинически инфицированном стаде, способ снижения выделения вируса из носа, способ снижения продолжительности виремии у животных с субклинической формой вызываемой PCV2 инфекции, способ снижения коэффициента заболеваемости в субклинически инфицированном стаде, способ снижения коэффициента смертности в субклинически инфицированном стаде, в каждом случае заключающийся в том, что вводят в терапевтически эффективном количестве антиген PCV2 или иммуногенную композицию, содержащую антиген PCV2, животному, которое нуждается в таком введении, где иммуногенная композиция представляет собой субъединичную иммуногенную композицию, композицию, содержащую полностью обезвреженные или ослабленные и/или инактивированные PCV2.
В контексте настоящего описания понятие «субъединичная иммуногенная композиция» относится к композиции, которая содержит по меньшей мере один иммуногенный полипептид или антиген, но не все антигены, выведенные или являющиеся гомологами антигена PCV2. Такая композиция практически свободна от интактного PCV2. Таким образом, «субъединичную иммуногенную композицию» получают по