Способ изготовления металл-оксидного каталитического электрода для низкотемпературных топливных элементов
Иллюстрации
Показать всеИзобретение относится к области химических источников тока, а именно к способу изготовления и материалу каталитического электрода - элемента мембранно-электродного блока для водородных и спиртовых топливных элементов. Металл-оксидный каталитический электрод представляет собой пористый наноструктурированный слой композита толщиной 2 -15 мкм, состоящий из: катализатора - монокристаллических частиц допированного рутением и сурьмой диоксида олова, со средним диаметром около 30 нм, на которые химически нанесены частицы каталитического металла платиновой группы со средним размером 3 нм, а также 10-30% гидрофибизатора, предпочтительно политетрафторэтилена, и 10-20% ионпроводящей добавки, предпочтительно сульфированный фторполимер. Суспензию активной композитной массы готовят путем диспергирования металл-оксидного катализатора, гидрофобизирующих и ионопроводящих добавок в смеси воды, изопропилового спирта и глицерола в соотношении 0.4:0.2:0.4, соответственно, затем ее наносят любым способом на газодиффузонный слой и термообрабатывают при 120°С. Повышение мощности топливного элемента с таким электродом является техническим результатом заявленного изобретения. 2 н.п. ф-лы, 3 ил., 4 пр.
Реферат
Изобретение относится к области химических источников тока, а именно к способу изготовления и материалу каталитического электрода - элемента мембранно-электродного блока для водородных и спиртовых топливных элементов.
Сущность изобретения: способ изготовления анодного каталитического электрода топливного элемента, включающий изготовление металл-оксидного катализатора и активного каталитического слоя на его основе с добавлением гидрофобизирующих и ионпроводящих добавок. Способ позволяет повысить активность анодного электрода водородных и спиртовых топливных элементов.
Предлагаемый каталитический электрод представляет собой пористый наноструктурированный слой композита толщиной 2-15 мкм, состоящий из: катализатора - монокристаллических частиц допированного рутением и сурьмой диоксида олова, со средним диаметром около 30 нм, на которые химически нанесены частицы каталитического металла платиновой группы со средним размером 3 нм, а также 10-30% гидрофибизатора, предпочтительно политетрафторэтилена, и 10-20% ионпроводящей добавки, предпочтительно сульфированный фторполимер. Приготовление суспензии активной композитной массы проводится путем диспергирования металл-оксидного катализатора, гидрофобизирующих и ионопроводящих добавок в смеси воды, изопропилового спирта и глицерола в соотношении 0.4:0.2:0.4, соответственно, и нанесением суспензии любым способом: кистью, воздушно-капельным или ультразвуковым распылением, трафаретной печатью на газодиффузонный слой с последующей термообработкой при 120°С.
Предложенный способ приготовления позволяет создавать оптимальную пористую структуру каталитического электрода водородных и спиртовых топливных элементов с повышенной электрохимической активностью.
Как правило, низкотемпературные водородные и спиртовые топливные элементы создаются с применением перфторированных протонпроводящих мембран [J.Foumier, G.Faubert, J.Y.Tilquin, R.Cote, D.Guay, J.P.Dodelet. High-Performance Low Pt Content Catalysts for the Electroreduction of Oxygen in Polymer-Electrolyte Fuel Cells/J. Electrochem. Soc., 1997, V.144, P.145]. Мембранно-электродный блок таких топливных элементов состоит из трех основных элементов:) протонпроводящей мембраны, основная функция которой заключается в обеспечении ионной проводимости и разделении электродных пространств; активного слоя (АС) электрода, где протекают электрохимические реакции окисления или восстановления; газодиффузионного слоя (ГДС), обеспечивающего подвод реагентов в область протекания электрохимической реакции, а также водный баланс и токосъем.
Структура активного слоя в большой степени определяет основные параметры топливного элемента. В АС должна быть реализована такая структура, которая в области протекания электрохимической реакции сочетала бы в себе три компонента:
электролит, поры для подвода реагента и электронпроводящую основу, т.е. такая структура должна обеспечивать оптимальную проводимость ионов, электронов и подвод реагентов.
Известно, что наиболее эффективными электрокатализаторами для катода и анода низкотемпературных топливных элементов являются каталитические системы на основе металлов платиновой группы и особенно платины. В первые годы развития технологии низкотемпературных ТЭ в составе активного слоя электродов применялись большие количества платины в виде черни с загрузкой от 4 до 30 мг Pt/см2 [Wilson MS, Valerio JA, Gottesfeld S. Low platinum loading electrodes for polymer electrolyte fuel cells fabricated using thermoplastic ionomers. Electrochim Acta 1995;40:355-63]. Существенным шагом вперед оказался переход от платиновой черни к каталитическим структурам с использованием наноразмерной платины. Для стабилизации нанокластеров активного металла используют электропроводящие носители с высокой площадью поверхности. Известно техническое решение [Raistrick ID. Electrode assembly for use in a solid polymer electrolyte fuel cell. United States patent US 4876115. 1989 Oct 24], в котором электрод представляет собой наноразмерные частицы платины, нанесенные на углеродную сажу, при этом каталитической слой электрода представляет собой композит, состоящий из катализатора и ионпроводящей добавки - иономера. Такая структура электрода позволяет значительно снизить загрузку платины до 0,3-0,4 мг Pt/см2 с сохранением мощностных характеристик топливного элемента.
Дополнительно снизить загрузку платины на электроде топливного элемента позволили технические решения [Raistrick ID. Electrode assembly for use in a solid polymer electrolyte fuel cell. United States patent US 4876115. 1989 Oct 24], [Wilson MS. Membrane catalyst layer for fuel cells. United States patent US 5234777. 1993 Aug 10], в которых было предложено формирование активного слоя электрода методом декалькированной литографии. Данный метод включает два основных шага - это нанесение суспензии катализатора и иономера на подложку, например тонкую гидрофобную пленку из политетрафторэтилена, с последующим переносом полученного таким способом активного слоя на мембрану методом горячего прессования при давлении 70~90 атм в течение 90 секунд, t=140°С.
Более совершенная структура активного каталитического слоя, позволяющая поддерживать водный баланс мембранно-электродного блока, предложена авторами патентов [Zhang H, Dong M, Qiu Y, Yi В, Wang X, Wang X. A multilayer catalyst layer for PEMFCs and its preparation. Republic of China patent CN 1744360. 2006 Mar 8], [Zhang H, Dong M, Qiu Y, Tang Q, Yi B, Liu B, et al. A gas diffusion electrode for PEMFC and its preparation method. Republic of China patent CN 1553534 2006 Sep 6]. Предлагаемые электроды состоят из двух слоев - гидрофобного и гидрофильного. Первый слой на основе политетрафторэтилена наносится непосредственно на газодиффузионный слой и затем выдерживается при температуре 200-350°С в течение 30-60 минут. Второй (гидрофильный) слой получают нанесением суспензии катализатора и раствора иономера непосредственно на первый слой электрода.
Для улучшения ионной проводимости между протонообменной мембраной и каталитическим слоем авторами патентов [Mussel RD, Rehg TJ. Active layer for membrane assembly. United States patent US 5882810. 1999 Mar 16], [Hulett JS. Method of making MEA for PEM/SPE fuel cell. United States patent US 6074692. 2000 Jun 13], [Hunt AT. Materials and processes for providing fuel cells and active membranes. United States patent US 6403245. 2002 Jun 12] предложены технические решения, в основе которых лежит метод формирования мембранно-электродного блока ТЭ, в котором каталитический слой наносится непосредственно на протонообменную мембрану, например, мембрану типа Nation. Приготовленный таким образом МЭБ при напряжении 0.65 В позволяет получать ток около 1.0 А/см2 при температуре 80°С и относительной влажности подаваемых газов 50% HR.
Автором патента [Dhar HP. Method for catalyzing a gas diffusion electrode. United States patent US 5521020. 1996 May 28] предложен метод изготовления электродов для ТЭ методом напыления гидрофильньной смеси каталитических чернил на газодиффузионный слой (например, пористую углеродную бумагу). Для получения высокоэффективного электрода с пониженным содержанием платины, катализатор (20%Pt/C) смешивают с раствором иономера, например раствором Nafion, и напыляют непосредственно на газо-диффузионный слой (например, углеродную бумагу), затем электроды припрессовываются к протонообменной мембране методом горячего прессования. При этом содержание Nafion в активном каталитическом слое составляет 30 мас.%, загрузка платины - 0.12 мг/см. Предложенный способ приготовления электродов позволяет повысить мощность мембранно-электродного блока водородного топливного элемента до 0.72 Вт/см2 при атмосферном давлении подаваемых к электродам газов.
Перечисленные способы формирования каталитических электродов на основе платиновых катализаторов на углеродных носителях позволяют изготавливать высокоактивные мембранно-электродные блоки с пониженным содержанием платины для топливных элементов, работающих на чистом водороде. Однако их серьезным недостатком является низкая эффективность в топливных элементах, работающих на техническом водороде (даже со следовым количеством примеси СО) или в растворах спиртов. Связано это прежде всего с отравлением платиновых катализаторов примесями монооксида углерода в водороде, а также продуктами электроокисления спиртов (СО, формальдегид и др.) [Ota К, Nakagawa Y, Takahashi М. Reaction products of anodic oxidation of methanol in sulfuric acid solution. //J Electroanal Chem. 1984. Vol.179. P.179-86], [Lamy C, Lima A, LeRhun V, Delime F, Coutanceau C, Luger JM. Recent advances in the development of direct alcohol fuel cells (DAFC). //J Power Sources. 2002. Vol.105. P. 283], [Wu J., Yuan X.Z., Wang H, Blanco М.., et al. Durability of PEM fuel cells. Presented at: Hydrogen and Fuel Cells 2007 International Conference and Trade Show; 2007 Apr 29-May 3; Vancouver, Canada].
Для преодоления этой проблемы известны научно-технические решения, основанные на применении композитных платиновых катализаторов, нанесенных на носители, содержащие оксидные материалы. В отличие от углеродных материалов некоторые оксиды могут оказывать промотирующее действие в реакциях окисления СО и органических топлив, в результате чего применение платиновых катализаторов на оксидных носителях приводит к повышению толерантности к каталитическим ядам [J.W.Long, R.M.Stroud, K.E.Swider-Lyons, D.R.Rolison, J.Phys. Chem. В 104 (2000) 9772], [Q.Lu, В.Yang, L.Zhuang, J.Lu, J.Phys. Chem. В 109 (2005) 1715], [L.Jang, G.Sun, S.Sun, J.Liu, S.Tang, H.Li, B. Zhou, Q. Xin, Electrochim. Acta 50 (2005) 5384], [L. Jang, L. Colmenares, Z. Jusys, G.Q. Sun, R.J. Behm, Electrochim.Acta 53 (2007) 377], [K.-W. Park, K.-S. Ahn, Y.-C. Nah, J.-H. Choi, Y.-E. Sung, J. Phys. Chem. В 107(2003)4352].
Известно техническое решение по использованию оксидов SbO2, SnO2, IrO2, ZrO2, CeO2, TiO2 и их комбинации в качестве компонентов носителя для электрокатализаторов топливных элементов [lordache С, Lycke D, Blair S. Catalysts including metal oxides for organic fuel cells. Tekion Inc. Burnaby ВС, Canada. United States patent WO/2008/00620. 2008 Jan 17]. Авторами было проведено сравнение активности окисления муравьиной кислоты и этанола платиновыми электрокатализаторами, нанесенными на композитные смеси углеродной сажи и оксидов. Было показано, что наибольшей активностью в электроокислении муравьиной кислоты и этанола обладают каталитические электроды, в состав которых включены оксиды Sb2O5-SnO2 и CeO2. Недостатком данного технического решения является все еще недостаточная активность каталитических электродов на основе углерод-оксидных носителей. Для увеличения эффективности каталитических электродов (за счет увеличения трехфазной границы катализатор / активный носитель / реагент) предпочтительным представляется использование носителей на основе высокодисперсных оксидных материалов, обладающих достаточной электронной проводимостью, что позволит исключить инертный (углеродный) компонент носителя.
Наиболее близким к заявляемому изобретению является техническое решение [Патент JP. Akihiro Masao, Zhiyun Noda, Fumiaki Takasaki, Kohei Ito, Kazunari Sasaki. Method for producing electrode material for fuel cell. Japan's patent. JP 20100233574. 2010 Sep 16], согласно которому электрод топливного элемента представляет собой каталитический слой, приготовленный на основе катализатора - наноразмерных частиц платины, нанесенных на носитель - диоксид олова, допированный ниобием. Синтез катализатора осуществляется методом соосаждения прекурсоров раствором аммиака. Нанесение платиновых частиц на оксидный носитель проводится в коллоидном растворе платины, с последующим промыванием, высушиванием катализатора и восстановлением металла на оксидном носителе в токе водорода при температуре 80-250°С. Содержание платины на носителе составляет 10-30% масс. Для формирования мембранно-электродного блока каталитический слой наносится на протонообменную мембрану. Полученный электрод предлагается применять в качестве катодного электрода в мембранно-электродном блоке водородного топливного элемента. Преимуществами метода является более высокая стабильность каталитических свойств платино-оксидных электродов, по сравнению с платиновым катализатором на углеродном носителе.
Недостатком этого технического решения является относительно невысокая активность получаемого электрода в катализе катодного процесса ТЭ, а также крайне низкая эффективность при его использовании в качестве анода топливного элемента. Прежде всего, это может быть объяснено как недостаточной электронной проводимостью оксидного носителя, так и неэффективно организованной структурой активного слоя. Описанное техническое решение выбрано за прототип. Технической задачей заявляемого способа является получение высокоактивных каталитических электродов для анода водородных и спиртовых топливных элементов.
Поставленная задача включает разработку способа изготовления каталитического электрода для водородных и спиртовых топливных элементов, который объединяет в себе: метод получения эффективного металл-оксидного катализатора, а также активного каталитического слоя на его основе с добавлением гидрофобизирующих и ионпроводящих добавок с целью наиболее эффективного использования благородного металла в каталитическом электроде.
Для более эффективного использования активной площади электрода необходима организация в его объеме трехфазных границ, однако все известные технические решения по конструкции объемных электродов для топливных элементов, использующих оксидные носители катализаторов, используют те же конструкции, что и для каталитических электродов на основе углеродных наноструктур. Однако в силу меньшей электронной проводимости легированных полупроводниковых оксидов, а также их меньшей плотности эффективно работающим оказывается более тонкий слой наноструктурированного электрокаталитического материала. Как показано в [Фролова Л.А., Укше А.Е., Добровольский Ю.А. Влияние транспортных свойств композиционных каталитических материалов для анодов топливных элементов на их эффективность. // Альтернативная энергетика и экология. 2009. №8 (76). С.151-156.], в силу более высоких электронных сопротивлений оксидного носителя эффективно работает только слой толщиной 2-15 мкм, прилегающий к токосъемной (биполярной) пластине. Кроме того, состав активного слоя также должен быть индивидуально адаптирован для конкретной каталитической системы, например, поскольку оксидные носители более гидрофильны по сравнению с углеродными материалами, то для поддержания водного баланса в МЭБе ТЭ необходимо дополнительное введение оптимального количества гидрофобных и ионпроводящих добавок для создания эффективной структуры электрода.
Поэтому поставленная задача решается за счет того, что с целью более эффективного использования благородного каталитического металла, в предлагаемой конструкции электрода используется более тонкий слой электрокаталитического материала, со средней толщиной 5-10 мкм и не менее 2 мкм и не более 15 мкм, с заполнением промежутков между частицами иономером и образованием пористой структуры электрода за счет гидрофобных добавок. При этом с целью повышения активности электрода в реакциях электроокисления технического водорода и низкомолекулярных органических соединений используется высокоактивный катализатор, обладающий повышенной устойчивостью к отравлению каталитическими ядами и стабильностью каталитических свойств за счет уменьшения деградации электрода, происходящей вследствие агломерации частиц благородного металла. В качестве каталитической основы используется электропроводящий диоксид олова, легированный оксидом рутения и сурьмы с содержанием допантов: Ru=2-7 мол.%, Sb=5 мол.%, с нанесенными на поверхность частиц оксида наночастицами платины с размером около 3 нм. Формирование активной композитной массы проводится путем диспергирования металл-оксидного катализатора, 10-30% гидрофибизатора (предпочтительно политетрафторэтилена) и 10-20% ионпроводящей добавки (предпочтительно сульфированный фторполимер) в смеси воды, изопропилового спирта и глицерола в соотношении 0.4:0.2:0.4, соответственно, и нанесением суспензии на газодиффузонный слой с последующей термообработкой при 120°С, что позволяет создавать оптимальную пористую структуру каталитического электрода с повышенной электрохимической активностью.
Реализация способа иллюстрируется следующими примерами.
Пример 1.
Каталитический электрод для водородного топливного элемента на основе катализатора - платинированного диоксида олова, легированного рутением и сурьмой
10%Pt/Sn0.95-xSb0.05 RuxO2 (х=0.03).
Метод получения катализатора.
Синтез сложных оксидов Sn0.95-xSb0.05RuxO2 (x=0.02-0.07) проводится методом обратных мицелл. Соли металлов SnCl4·5H2O, SbCl3, RuCl3·H2O растворяются в циклогексане, содержащем сурфактант (цетилтриметиламмоний бромид (СТАВ) (5 мкмоль/л), затем добавляется NaOH до рН 13 и после тщательного перемешивания смесь оставляется на сутки для формирования частиц оксида. Полученные материалы отжигаются на воздухе в течение 1 часа при температуре 500°С.
К оксидному носителю (2 г) приливается 50 мл этиленгликоля. Полученная суспензия диспергируется в ультразвуковой ванне в течение 30 мин. Затем в полученную взвесь добавляли NaOH°кр (до рН~13) и перемешивали до полного растворения гидроксида натрия. Затем добавляли прекурсор платины с расчетом 10% мас. платины по отношению к массе носителя. Полученная смесь при постоянном перемешивании выдерживается при температуре 130°С в инертной атмосфере, промывается бидистиллированной водой и высушивается в вакуумном шкафу при температуре 100°С в течение 12 часов.
Метод приготовления каталитического электрода.
Формирование активной композитной массы проводится путем диспергирования металл-оксидного катализатора, 10% масс. гидрофибизатора, политетрафторэтилена и 12% масс. ионпроводящей добавки - раствор сульфированного фторполимера "Naflon" - в смеси воды, изопропилового спирта и глицерола в соотношении 0.4:0.2:0.4, соответственно, в ультразвуковой ванне в течение 1 часа при температуре 45°С. Затем полученная суспензия наносится намазыванием на газодиффузонный слой с последующей термообработкой при 120°С.
Свойства полученных материалов.
Полученный оксидный носитель обладает рутилоподобной структурой (Р4/mnm), имеет сферическую форму частиц со средним диаметром около 30 нм и узким распределением частиц по размеру. Электронная проводимость носителя составляет 4(Ом·см)-1. Удельная поверхность оксида около 100 м2/г. Содержание платины на носителе составляет около 10% масс., средний диаметр частиц платины - 3 нм. Удельная активная поверхность катализатора 62 м2/г (Pt). Толщина электрода составляет 10 мкм.
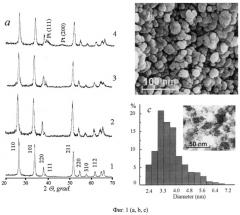
На фигуре 1а представлены дифрактограммы оксидов SnO2-1, Sn0.95-xSb0.05 RuxO2(x=0.03)-2, Sn0.95-xSb0.05RuxO2(x-0.05) - 3 и катализатора of Pt/Sn0.92Sb0.05Ru0.03O2 - 4. На фигуре 1b приведены СЭМ изображения оксидного носителя Sn0.92Sb0.05Ru0.03O2. Фигура 1с иллюстрирует гистограмму распределения по размеру частиц платины в катализаторе Pt/Sn0.92Sb0.05Ru0.03O2 и ПЭМ изображение катализатора Pt/Sn0.92Sb0.05 Ru0.03O2.
Активность каталитического электрода в составе МЭБ водородного топливного элемента при использовании в качестве топлива водорода с примесью СО (100 ppm) составила около 250 мВт/см2 (условия эксперимента: поток газов - 100 мл/мин, влажность газов 50% HR, напряжение 0.5 В). На катоде использовался коммерческий катализатор 20% Pt/C (E-TEK). Во всех сериях экспериментов фиксировались значения токов после выхода на стационарный режим (примерно через час работы ТЭ). Содержание платины на электродах - 0,3 мг/см2.
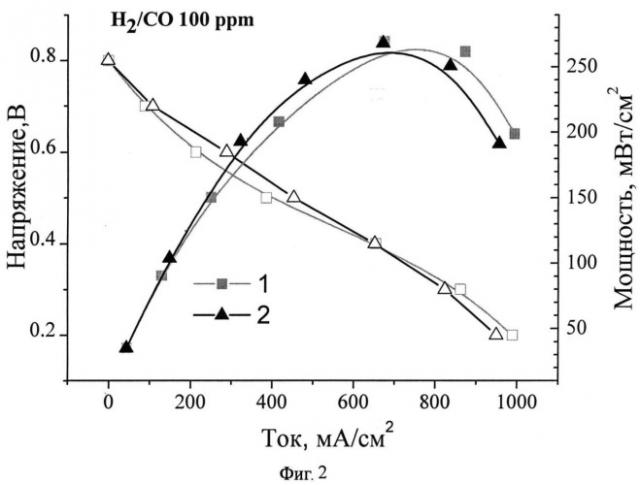
На фигуре 2 приведены вольт-амперные и мощностные характеристики МЭБ с каталитическими электродами на основе 10%Pt/ Sn0.95-xSb0.05RuxO2(x=0.03) - 1 и 10%Pt/Sn0.95-xSb0.05RuxO2(x=0.05) - 2 в составе анода водородно-воздушного ТЭ. Незаштрихованные символы: напряжение ТЭ; заштрихованные символы: удельная мощность.
Пример 2.
Каталитический электрод для спиртового топливного элемента на основе катализатора - платинированного диоксида олова, легированного рутением и сурьмой
10%Pt/Sn0.95-xSb0.05RuxO2(x=0.03).
Процесс приготовления электрода аналогичен приведенному в примере 1 и отличается тем, что содержание гидрофибизатора (политетрафторэтилен) и ионпроводящей добавки (сульфированный фторполимер) составляет 30 и 15% масс., соответственно.
Свойства полученных материалов. Толщина электрода составляет 14 мкм. Активность каталитического электрода в составе МЭБ этанольного топливного элемента при использовании в качестве топлива 0.5 М раствора этанола составила около 45-50 мВт/см2 при напряжении 0.5 В. Условия эксперимента: поток топлива -10 мл/мин, температура 35°С. На аноде загрузка Pt-0.8 мг/см2. Во всех сериях экспериментов фиксировались значения токов после выхода на стационарный режим, примерно, через час работы ТЭ.
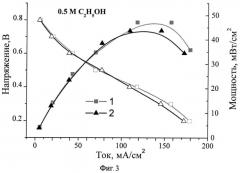
На фигуре 3 приведены поляризационные кривые и удельная мощность МЭБ с каталитическими электродами на основе 10%Pt/Sn0.95-xSb0.05RuxO2(x=0.03) - 1 и (x=0.05) - 2 в составе анода этанольного топливного элемента. Незаштрихованные символы: напряжение ТЭ; заштрихованные символы: удельная мощность. Топливо: 0.5 М раствор этанола.
Пример 3.
Каталитический электрод для водородного топливного элемента на основе катализатора - платинированного диоксида олова, легированного рутением и сурьмой
10%Pt/Sn0.95-xSb0.05RuxO2(х=0.05).
Процесс приготовления электрода аналогичен приведенному в примере 1 и отличается тем, что содержание добавки рутения в оксидном носителе составляет 5 мол.%.
Свойства полученных материалов. Полученный оксидный носитель обладает рутилоподобной структурой (Р4/mnm), имеет сферическую форму частиц со средним диаметром около 30 нм и узким распределением частиц по размеру. Электронная проводимость носителя составляет 2.7 (Ом·см)-1. Удельная поверхность оксида около 100 м/г. Содержание платины на носителе составляет около 10% масс., средний диаметр частиц платины - 3 нм. Удельная активная поверхность катализатора 59 м2/г (Pt). Толщина электрода составляет 12 мкм.
Активность каталитического электрода в составе МЭБ водородного топливного элемента при использовании в качестве топлива водорода с примесью СО 100 ppm составила также около 250 мВт/см2 при напряжении 0.5 В. Условия эксперимента: поток газов - 100 мл/мин, влажность газов 50% HR. На катоде использовался коммерческий катализатор 20% Pt/C (Е-ТЕК). Во всех сериях экспериментов фиксировались значения токов после выхода на стационарный режим, примерно, через час работы ТЭ.
Пример 4.
Каталитический электрод для спиртового топливного элемента, на основе катализатора - платинированного диоксида олова легированного рутением и сурьмой 10%Pt/Sn0.95-xSb0.05 RuxO2(х=0.05).
Процесс приготовления электрода аналогичен приведенному в примере 2 и отличается тем, что используется катализатор с содержанием рутения 5 мол.%, а также тем, что содержание гидрофибизатора - политетрафторэтилен и ионпроводящей добавки - сульфированный фторполимер составляет 28 и 13% масс., соответственно.
Свойства полученных материалов. Толщина электрода составляет 13 мкм. Активность каталитического электрода в составе МЭБ этанольного топливного элемента при использовании в качестве топлива 0.5 М раствора этанола составила около 45 мВт/см2 при напряжении 0.5 В. Условия эксперимента: поток топлива - 10 мл/мин, температура 35°С. Во всех сериях экспериментов фиксировались значения токов после выхода на стационарный режим, примерно, через час работы ТЭ.
Таким образом, заявляемый способ обеспечивает получение высокоактивных каталитических электродов для водородных и спиртовых топливных элементов на основе платинированного электропроводящего диоксида олова, легированных оксидом рутения и сурьмы с оптимальной пористой структурой.
1. Способ изготовления металл-оксидного каталитического электрода для водородных и спиртовых топливных элементов, отличающийся тем, что в составе активного слоя используют композитный катализатор на основе благородного металла, предпочтительно платины, нанесенного на электропроводящий композитный оксид на основе допированного рутением и сурьмой диоксида олова с содержанием допантов 2-7% мол. и 5 мол.% мол., соответственно.
2. Способ изготовления металл-оксидного каталитического электрода по п.1., отличающийся тем, что применяют каталитический электрод, представляющий собой пористый слой композита толщиной 2-15 мкм, состоящий из следующих компонентов: монокристаллических частиц допированного рутением и сурьмой диоксида олова, со средним диаметром около 30 нм, на которые химически нанесены наночастицы каталитического металла платиновой группы со средним размером 3 нм, а также 10-30% гидрофибизатора, предпочтительно политетрафторэтилена, и 10-20% ионпроводящей добавки, предпочтительно сульфированный фторполимер.
3. Способ изготовления металл-оксидного каталитического электрода для водородных и спиртовых топливных элементов по пп.1-2, отличающийся тем, что приготовление суспензии активной композитной массы проводят путем диспергирования металл-оксидного катализатора, гидрофобизирующих и ионопроводящих добавок в смеси воды, изопропилового спирта и глицерола в соотношении 0.4:0.2:0.4, соответственно, и нанесением суспензии на газодиффузонный слой с последующей термообработкой при 120°С.