Способ очистки метилметакрилата
Иллюстрации
Показать всеИзобретение относится к способу очистки метилметакрилата (ММА), включающему осуществление контакта содержащего примеси жидкого ММА с сульфокислотной смолой в присутствии формальдегида или пригодного источника метилена или этилена формулы I, как определено ниже, где R5 и R6 независимо выбирают из углеводородов C1-C12 или Н; Х представляет собой О; n является целым числом от 1 до 100; и m имеет значение 1 или 2, и в котором сульфокислотная смола, необязательно, по меньшей мере, частично деактивирована. Способ позволяет удалять с высокой эффективностью примеси альдегидного типа, диены, триены.
2 н. и 16 з.п. ф-лы, 20 табл., 1 ил., 8 пр.
Реферат
Настоящее изобретение относится к способу очистки, в частности к способу очистки метилметакрилата (ММА).
ММА - хорошо известное химическое соединение, которое имеет широкое применение, но главным образом его используют как мономер в производстве полиметилметакрилата (ПММА). ПММА часто получают в виде тонких листов, из которых можно формовать разнообразные предметы, требуемые для определенного применения.
Для получения ПММА важно использовать ММА высшей степени чистоты, потому что даже низкое содержание примеси может привести к изделию из ПММА, имеющему мутный, непрозрачный или выцветший внешний вид. Кроме того, низкое содержание примести в ММА может привести к изменению структурных свойств изделия из ПММА, что может иметь нежелательные эффекты. Таким образом, важно иметь возможность получения ММА, мономера ПММА, высшей степени чистоты, чтобы попытаться предотвратить возникновение данных проблем.
ММА можно получать многими способами, например реакцией ацетонциангидрина, метанола и концентрированной серной кислоты; окислением третичного бутилового спирта в метакролеин, а затем в метакриловую кислоту с последующей этерификацией метанолом; в качестве альтернативы, катализируемыми реакциями, как описано в патенте EP 1073517. Такие реакции и многие другие, известные в литературе, дают поток ММА, который обычно содержит примеси, способные создавать обсуждаемые выше проблемы, когда ММА полимеризуется с образованием ПММА. Соответственно, обычно пытаются очистить поток ММА перед полимеризацией. Известно отделение примесей, которые значительно отличаются от ММА по температуре кипения, путем дистилляции. Однако такой способ разделения трудно осуществить, если примеси и ММА имеют близкие температуры кипения.
Японский патент 58-183641 описывает использование кислого катализатора для обработки примесей в сыром метилметакрилате.
Японская патентная заявка 63-127952 предлагает использовать соединения, содержащие сульфокислотные группы, для обработки метилметакрилата высокой чистоты.
Патент США 4625059 (патентообладатель Mitsubishi Petrochemical) описывает использование кислой ионообменной смолы в неподвижном слое для отделения примесей от сырого ММА.
Таким образом, сырой ММА, полученный различными способами, содержит весьма разнообразные примеси, которые трудно отделять дистилляцией. ММА, полученный конденсацией формальдегида с метилпропионатом, содержит дополнительно другие еще не определенные примеси, например цветообразующие соединения, которые не описаны в ранее известных способах получения ММА.
Целью аспектов настоящего изобретения является предложение решения проблемы отделения данных или других примесей при очистке ММА.
По первому аспекту настоящего изобретения, предлагается способ очистки метилметакрилата (ММА), состоящий в контакте содержащего примеси жидкого ММА с сульфокислотной смолой в присутствии формальдегида или пригодного источника метилена или этилена формулы I, как определено ниже:
где R5 и R6 независимо выбирают из углеводородов C1-C12, предпочтительно алкила, алкенила или арила C1-C12, как определено в настоящем изобретении, или H, предпочтительнее алкила C1-C10 или H, наиболее предпочтительно алкила C1-C6 или H, особенно метила или H;
X представляет собой O или S, предпочтительно O;
n является целым числом от 1 до 100, предпочтительно от 1 до 10, предпочтительнее от 1 до 5, особенно 1-3;
и m имеет значение 1 или 2, предпочтительно 1.
В наиболее предпочтительном варианте осуществления соединение I получают из формальдегида в присутствии метанола и/или воды. В таком случае соединение I можно определить как пригодный источник формальдегида. Во избежание сомнения пригодный источник формальдегида означает любой равновесный состав, который может служить источником формальдегида. Его примеры включают, без ограничения, метилаль (1,1- диметоксиметан), полиоксиметилены -(CH2-O)i-, где i=1-100, формалин (формальдегид, метанол, вода) и другие равновесные составы, например смесь формальдегида, метанола и метилпропионата.
Как правило, полиоксиметилены - высшие формали формальдегида и метанола CH3-O-(CH2-O)i-CH3 («формаль-i»), где i=1-100, предпочтительно 1-5, особенно 1-3, или другие полиоксиметилены, содержащие, по меньшей мере, одну неметильную концевую группу. Таким образом, источником формальдегида может также служить полиоксиметилен R1-O-(CH2-O-)iR2, где R1 и R2 могут быть одинаковыми или разными группами, и, по меньшей мере, одну из них выбирают из алкильной группы C2-C10, например R1=изобутил и R2=метил.
Предпочтительно, формальдегид или количество формальдегида, которое можно выделить из пригодного источника формальдегида, присутствует в концентрации 0,01-0,1% от массы жидкого ММА.
Предпочтительно, пригодный источник формальдегида выбирают из 1,1-диметоксиметана, высших формалей формальдегида и метанола, например CH3-O-(CH2-O)i-CH3, где i=2 или больше, как указано выше, формалина или смеси, содержащей формальдегид, метанол и метилпропионат.
Предпочтительно, термин «формалин» означает смесь формальдегида, метанола и воды в соотношении 25-65:0,01-25:25-70% мас. Предпочтительнее, термин «формалин» означает смесь формальдегида, метанола и воды в соотношении 30-60:0,03-20:35-60% мас.
Наиболее предпочтительно, термин «формалин» означает смесь формальдегида, метанола и воды в соотношении 35-55:0,05-18:42-53% мас.
Предпочтительно, смесь формальдегида, метанола и метилпропионата содержит менее 5% мас. воды.
Предпочтительнее, смесь формальдегида, метанола и метилпропионата содержит менее 1% мас. воды. Наиболее предпочтительно, смесь формальдегида, метанола и метилпропионата содержит 0,1-0,5% мас. воды.
Предпочтительно, пригодный источник формальдегида имеет температуру кипения в пределах от 69 до 73°C при абсолютном давлении 0,75 бар.
Предпочтительно, формальдегид или его источник смешивают с загрязненным жидким ММА до контакта с сульфокислотной смолой. Как правило, в непрерывном или полунепрерывном процессе поток загрязненного жидкого ММА смешивают с потоком, содержащим формальдегид или его источник, с образованием объединенного жидкого потока перед контактом с сульфокислотной смолой. Формальдегид, таким образом, присутствует в объединенном жидком потоке в концентрации 0,01-0,1% мас.
В качестве альтернативы или дополнения, источник формальдегида может присутствовать как примесь в ММА, предпочтительно как примесь с близкой температурой кипения, до контакта с сульфокислотной смолой. В таких случаях пропускание загрязненного ММА через слой ионообменной смолы приводит к удалению или уменьшению концентрации источника формальдегида и/или изменению в его составе тяжелого или легкого компонента, который можно легко отделить от ММА дистилляцией.
Предпочтительно, примесью с близкой температурой кипения, которая присутствует в ММА, является формаль-2 (CH3-O-(CH2-O)2-CH3).
Предпочтительно легким компонентом по отношению к отделению от ММА является диметоксиметан. Предпочтительно диметоксиметан отделяют от ММА дистилляцией.
Предпочтительно, способ очистки по настоящему изобретению осуществляют при температуре 25-100°C. Предпочтительнее, данный способ осуществляют при температуре 40-90°C. Еще предпочтительнее, данный способ осуществляют при температуре 50-80°C. Наиболее предпочтительно, данный способ осуществляют при температуре 50-70°C.
Предпочтительно сульфокислотная смола составляет уплотненный слой. Предпочтительно, сульфокислотная смола содержит сильнокислую макропористую смолу на основе полимера. Наиболее предпочтительно, сульфокислотная смола представляет собой перекрестносшитую полистироловую смолу в виде сферических шариков размером от 0,4 до 1,64 мм, которая содержит 0,5-3,0 экв/л сульфокислотных групп (предпочтительно 0,7-2,5 экв/л) и имеет крупнопористую структуру со средним диаметром пор от 15 до 90 нм (предпочтительно 20-70 нм), удельную площадь поверхности от 15 до 100 м2/г (предпочтительно 20-80 м2/г) и удельный объем пор, измеряемый по степени удерживания воды влажной смолой, от 30 до 80% (предпочтительно 40-70%). Предпочтительно, кислая ионообменная смола является макросетчатой смолой.
Предпочтительно, в данном способе очистки также присутствует, по меньшей мере, один сложный эфир карбоновой кислоты. Предпочтительно, данный сложный эфир карбоновой кислоты выбирают из метилового, этилового или пропилового эфира любой карбоновой кислоты C2-C6 с линейной или разветвленной цепью. Предпочтительнее, данный сложный эфир, по меньшей мере, одной карбоновой кислоты выбирают из метилового или этилового эфира любой карбоновой кислоты C2-C4 с линейной или разветвленной цепью. К примерам пригодных сложных эфиров карбоновых кислот относятся, без ограничения, метилпропионат, этилпропионат, пропилпропионат, метилбутаноат, метилизобутират, этилбутаноат, пропилбутаноат, бутилбутаноат. В предпочтительном варианте осуществления, в данном способе очистки также присутствуют метилпропионат или метилизобутират.
Как правило, в непрерывном или полунепрерывном процессе, по меньшей мере, один сложный эфир карбоновой кислоты уже присутствует в потоке загрязненного жидкого ММА до контакта с сульфокислотной смолой. Следовательно, в таких вариантах осуществления, как правило, по меньшей мере, один сложный эфир карбоновой кислоты составляет часть объединенного жидкого потока.
Как правило, примеси имеют температуру кипения, которая делает неэффективным разделение дистилляцией. Как правило, разность температур кипения примесей и ММА не превышает 15°C. Чаще разность температур кипения примесей и ММА не превышает 10°C. В большинстве случаев разность температур кипения примесей и ММА не превышает 5°C. Обычно температуры кипения примесей и ММА приблизительно совпадают, т.е. различаются в пределах 1-2°C. Примеси, температура кипения которых в чистом виде отличается от температуры кипения ММА более чем на 15° и которые проявляют неидеальное поведение при дистилляции в смеси с ММА и другими примесями, трудно отделять от ММА дистилляцией вследствие физических эффектов. К примерам таких физических эффектов относится образование азеотропных смесей с высокой или низкой температурой кипения.
Показано, что настоящее изобретение особенно полезно для отделения некоторых примесей от загрязненного жидкого ММА. Показано, что данные примеси могут содержать изобутиральдегид или соединение, которое выделяет изобутиральдегид при воздействии сульфокислотной ионообменной смолы. К примерам таких соединений относятся моно- или диацетали изобутиральдегида и разветвленного или линейного спирта C1-C6, в частности 2,2-диметоксипропана и металлилового спирта.
Отделение изобутиральдегида с помощью сочетания формальдегида и смолы выгодно, несмотря даже на то, что изобутиральдегид отделяют от ММА как примесь с меньшей температурой кипения.
Отделение изобутиральдегида в колонне для низкокипящих примесей вызывает риск инициирования полимеризации смесью изобутиральдегида и кислорода в верхних погонах колонны для низкокипящих примесей, которые содержат, главным образом, ММА и должны насыщаться кислородом для эффективности стабилизаторов полимеризации.
Кроме того, рециркуляция изобутиральдегида вызывает его медленную конверсию в изобутанол над катализатором. Изобутанол попадает в чистый продукт ММА и снижает его качество, а также создает проблемы в тонких листах, потому что он реагирует с инициаторами полимеризации, таким образом, повышая расход данных инициаторов, которые обязятельно окрашиваются в непрореагировавшей и прореагировавшей (с изобутанолом) формах. Эта проблема возникает при получении полимера (оргстекла) аквариумного качества и в некоторых других случаях, в которых требуется очень низкое содержание инициаторов.
К другим успешно отделяемым примесям относятся произвольно замещенные диены C4-C20. Показано, что настоящее изобретение особенно полезно для отделения таких диенов. К полезным замещенным диенам, которые можно отделять, относятся диены C4-C20, содержащие от одного до четырех алкильных заместителей C1-C6, например моно- или диалкилгексадиены. К примерам диенов относятся, без ограничения, любые из следующих: 2,5-диметил-2,4-гексадиен; 2,5-диметил-1,5-гексадиен, 2-метил-1,5-гексадиен; транс-2-метил-2,4-гексадиен; цис-2-метил-2,4-гексадиен; 2-метил-3,5-гексадиен; 2-метил-1,3-гексадиен; 2,5-диметил-1,3-гексадиен и 1,6-гептадиен.
Кроме того, примеси могут также содержать произвольно замещенные триены C6-C20. К примерам триенов относится, без ограничения, любой из следующих: гептатриен и циклогептатриен.
Показано, что настоящее изобретение особенно эффективно для отделения диенов C4-C20 или триенов C6-C20 с внутренними енильными атомами углерода с одним или несколькими заместителями, предпочтительно алкильными, предпочтительнее с алкильными заместителями C1-C6, или с конечными енильными атомами углерода с двумя заместителями, предпочтительно алкильными, предпочтительнее с алкильными заместителями C1-C6, потому что енильные атомы углерода могут образовывать третичные карбокатионы. Наиболее предпочтительно использовать настоящее изобретение для отделения произвольно замещенных диенов C4-C20, как определено выше. В частности, к предпочтительным для отделения диенам по настоящему изобретению относятся: транс-2-метил-2,4-гексадиен; цис-2-метил-2,4-гексадиен; 2-метил-3,5-гексадиен; 2-метил-1,3-гексадиен; 2,5-диметил-1,3-гексадиен и 1,6-гептадиен, в частности, транс-2-метил-2,4-гексадиен и цис-2-метил-2,4-гексадиен.
Другие примеси, которые можно удалять способом по настоящему изобретению, также обычно содержат произвольно замещенные ненасыщенные альдегиды и кетоны. К примерам таких альдегидов или кетонов относятся соединения R'C=OR'', где в качестве R' может быть атом водорода, произвольно замещенный алкил, алкенил или арил, предпочтительнее алкил C1-C6, алкенил C1-C6 или арил, и в качестве R'' может быть произвольно замещенный алкил, алкенил или арил, предпочтительнее алкил C1-C6, алкенил C1-C6 или фенил.
Кроме того, 2-метилен-3-бутеналь может также присутствовать и удаляться способом по настоящему изобретению. Данная примесь в противном случае может быть преимущественно цветообразующей в ММА.
К другим подходящим примесям относятся: дивинилкетон, этилвинилкетон, диэтилкетон, этилизопропенилкетон, 3-метилен-1-гексен-4-он, метакролеин, изобутанол, толуол и пентенали, например 3-пентеналь. К другим предпочтительным примесям, которые можно удалять способом по настоящему изобретению, относятся этилвинилкетон и дивинилкетон.
Соответственно, настоящее изобретение особенно полезно для отделения транс-2-метил-2,4-гексадиена, цис-2-метил-2,4-гексадиена, этилвинилкетона и дивинилкетона.
Пригодный способ подготовки ММА перед очисткой в контакте с формальдегидом или источником метилена или этилена состоит в контакте метилпропионата с пригодным источником метилена формулы I, как определено ниже:
где R5 и R6 независимо выбирают из углеводородов C1-C12, предпочтительно алкила, алкенила или арила C1-C12, как определено в настоящем изобретении, или H, предпочтительнее алкила C1-C10 или H, наиболее предпочтительно алкила C1-C6 или H, особенно метила или H;
X представляет собой O или S, предпочтительно O;
n является целым числом от 1 до 100, предпочтительно от 1 до 10, предпочтительнее от 1 до 5, особенно 1-3;
и m=1;
в присутствии пригодного катализатора и, необязательно, в присутствии спирта.
Данный способ можно осуществлять в присутствии, по меньшей мере, одного пригодного стабилизатора. Предпочтительно, чтобы, по меньшей мере, один стабилизатор можно было выбирать из гидрохинона, п-метоксифенола, топанола-А (2-трет-бутил-4,6-диметилфенола) или фенотиазина.
Термин «алкил» при использовании в настоящем изобретении означает, если не указано иное, алкил C1-C10, например, метильную, этильную, пропильную, бутильную, пентильную, гексильную или гептильную группы. Если не указано иное, алкильные группы могут, при наличии достаточного количества атомов углерода, быть линейными или разветвленными (особенно предпочтительными разветвленными группами являются трет-бутильная и изопропильная), насыщенными, циклическими, ациклическими или частично циклическими/ациклическими, незамещенными, замещенными или заканчивающимися одним или несколькими заместителями, в число которых входят атом галогена, цианогруппа, нитрогруппа или OR19, OC(O)R20, C(O)R21, C(O)OR22, NR23R24, C(O)NR25R26, SR29, C(O)SR30, C(S)NR27R28, незамещенный или замещенный арил, или незамещенный или замещенный гетероцикл, где каждая из групп R19-R30 независимо представляет собой атом водорода, атом галогена, незамещенный или замещенный арил или незамещенный или замещенный алкил, или, в случае R21, атом галогена, нитрогруппу, цианогруппу или аминогруппу, и/или углеродную цепь прерывают один или несколько (предпочтительно менее 4) атомов кислорода, серы, кремния или силановые или диалкилсилановые группы или их сочетания.
Термин «Ar» или «арил» при использовании в настоящем изобретении означает содержащие от пяти до десяти членов, предпочтительно от пяти до восьми членов карбоциклические ароматические или псевдоароматические группы, например, фенил, циклопентадиенильный и инденильный анионы и нафтил, причем данные группы могут быть незамещенными или содержать один или несколько заместителей, в том числе незамещенный или замещенный арил, алкил (сама данная группа может быть незамещенной или замещенной или концевой, как определено в настоящем изобретении), гетероцикл (сама данная группа может быть незамещенной или замещенной или концевой, как определено в настоящем изобретении), атом галогена, цианогруппу, нитрогруппу или OR19, OC(O)R20, C(O)R21, C(O)OR22, NR23R24, C(O)NR25R26, SR29, C(O)SR30, C(S)NR27R28, где каждая из групп R19-R30 независимо представляет собой атом водорода, незамещенный или замещенный арил или алкил (сама данная группа может быть незамещенной или замещенной или концевой, как определено в настоящем изобретении), или, в случае R21, атом галогена, нитрогруппу, цианогруппу или аминогруппу.
Термин «алкенил» при использовании в настоящем изобретении означает алкенил C2-C10 и включает этенильную, пропенильную, бутенильную, пентенильную и гексенильную группы. Если не указано иное, алкенильные группы могут, при наличии достаточного количества атомов углерода, быть линейными или разветвленными, циклическими, ациклическими или частично циклическими/ациклическими, незамещенными, замещенными или заканчивающимися одним или несколькими заместителями, в число которых входят атом галогена, цианогруппа, нитрогруппа или OR19, OC(O)R20, C(O)R21, C(O)OR22, NR23R24, C(O)NR25R26, SR29, C(O)SR30, C(S)NR27R28, незамещенный или замещенный арил, или незамещенный или замещенный гетероцикл, где каждая из групп R19-R30 независимо представляет собой атом водорода, атом галогена, незамещенный или замещенный арил или незамещенный или замещенный алкил, или, в случае R21, атом галогена, нитрогруппу, цианогруппу или аминогруппу, и/или углеродную цепь прерывают один или несколько (предпочтительно менее 4) атомов кислорода, серы, кремния, или силановые или диалкилсилановые группы, или их сочетания.
Атомы галогена, которыми перечисленные выше группы могут быть замещены или закончены, включают фтор, хлор, бром и йод.
Термин «гетероцикл», при использовании в настоящем изобретении, означает содержащие от четырех до двенадцати членов, предпочтительно от четырех до десяти членов циклические системы, циклы которых содержат один или несколько гетероатомов, в том числе атомы азота, кислорода, серы и их сочетания, причем данные циклы могут не содержать или содержать одну или несколько двойных связей или могут быть неароматическими, частично ароматическими или полностью ароматическими по своей природе. Данные циклические системы могут быть моноциклическими, бициклическими или сопряженными. Каждая гетероциклическая группа, определенная в настоящем изобретении, может быть незамещенной или содержать один или несколько заместителей, в том числе атом галогена, цианогруппу, нитрогруппу, оксогруппу, алкил (сама данная группа может быть незамещенной или замещенной или концевой, как определено в настоящем изобретении), -OR19, -OC(O)R20, -C(O)R21, -C(O)OR22, -NR23R24, -C(O)NR25R26, -SR29, -C(O)SR30, -C(S)NR27R28, незамещенный или замещенный арил, или незамещенный или замещенный гетероцикл, где каждая из групп R19-R30 независимо представляет собой атом водорода, атом галогена, незамещенный или замещенный арил или незамещенный или замещенный алкил, или, в случае R21, атом галогена, нитрогруппу, аминогруппу или цианогруппу. Таким образом, термин «гетероцикл» означает такие группы, как произвольно замещенный азетидинил, пирролидинил, имидазолил, индолил, фуранил, оксазолил, изоксазолил, оксадиазолил, тиазолил, тиадиазолил, триазолил, оксатриазолил, тиатриазолил, пиридазинил, морфолинил, пиримидинил, пиразинил, хинолинил, изохинолинил, пиперидинил, пиразолил и пиперазинил. Замещение в гетероцикле может происходить при атоме углерода данного гетероцикла или, насколько это возможно, при одном или нескольких гетероатомах.
«Гетероциклические» группы могут также иметь форму N-оксида.
Термин «гетероатомы» при использовании в настоящем изобретении означает атомы азота, кислорода, серы или их сочетания.
В непрерывном процессе, после периода, составляющего, скажем, несколько месяцев, эффективность сульфокислотной смолы может снижаться приблизительно на 20% по сравнению с эффективностью свежей смолы. Такую смолу часто называют «деактивированной». Однако затем было неожиданно обнаружено, что присутствие пригодного источника формальдегида по настоящему изобретению заставляет «деактивированную» смолу отделять примеси со скоростью, близкой к скорости свежей смолы.
Таким образом, по второму аспекту настоящего изобретения, предлагается способ очистки метилметакрилата (ММА), состоящий в контакте содержащего примеси жидкого ММА с сульфокислотной смолой в присутствии формальдегида или пригодного источника метилена или этилена формулы I, как определено ниже:
где R5 и R6 независимо выбирают из углеводородов C1-C12, предпочтительно из алкила, алкенила или арила C1-C12, как определено в настоящем изобретении, или H, предпочтительнее из алкила C1-C10 или H, наиболее предпочтительно из алкила C1-C6 или H, особенно метила или H;
X представляет собой O или S, предпочтительно O;
n является целым числом от 1 до 100, предпочтительно от 1 до 10, предпочтительнее от 1 до 5, особенно 1-3;
и m имеет значение 1 или 2, предпочтительно 1, причем сульфокислотная смола, по меньшей мере, частично деактивирована.
В особенно предпочтительном варианте осуществления соединение I получают из формальдегида в присутствии метанола и/или воды. В таком случае, соединение I можно определить как пригодный источник формальдегида. Выражение «сульфокислотная смола, по меньшей мере, частично деактивирована» означает, что эффективность сульфокислотной смолы уменьшилась (по сравнению со свежей смолой) вследствие предыдущего воздействия на смолу загрязнителей, в том числе присутствующих в исходном очищаемом потоке, например загрязненном жидком потоке ММА. Предпочтительно, по меньшей мере, частично деактивированная сульфокислотная смола имеет эффективность менее 99,9% по сравнению с эффективностью свежей смолы. Предпочтительно, по меньшей мере, частично деактивированная сульфокислотная смола имеет эффективность менее 99% по сравнению с эффективностью свежей смолы; как правило, эффективность составляет менее 95%, чаще менее 75%, в частности менее 50%.
Предпочтительно, по меньшей мере, частичная деактивация связана со способностью сульфокислотных смол реагировать, по меньшей мере, с одним диеном. Например, предпочтительно, по меньшей мере, частично деактивированная сульфокислотная смола имеет эффективность менее 50% в реакции, по меньшей мере, с одним диеном по сравнению с эффективностью свежей смолы.
По третьему аспекту настоящего изобретения, предлагается метилметакрилат, например жидкий ММА, содержащий одну или несколько примесей, указанных в настоящем изобретении, который находился в контакте с сульфокислотной смолой в присутствии формальдегида или пригодного источника метилена или этилена формулы I, как определено ниже:
где R5 и R6 независимо выбирают из углеводородов C1-C12, предпочтительно из алкила, алкенила или арила C1-C12, как определено в настоящем изобретении, или H, предпочтительнее из алкила C1-C10 или H, наиболее предпочтительно алкила C1-C6 или H, особенно метила или H;
X представляет собой O или S, предпочтительно O;
n является целым числом от 1 до 100, предпочтительно от 1 до 10, предпочтительнее от 1 до 5, особенно 1-3;
и m имеет значение 1 или 2, предпочтительно 1, при нахождении в жидкой фазе.
По четвертому аспекту настоящего изобретения, предлагается полимер, содержащий метилметакрилатные остатки, причем данные метилметакрилатные остатки находились в контакте с сульфокислотной смолой в присутствии формальдегида или пригодного источника метилена или этилена формулы I, как определено ниже:
где R5 и R6 независимо выбирают из углеводородов C1-C12, предпочтительно из алкила, алкенила или арила C1-C12, как определено в настоящем изобретении, или H, предпочтительнее из алкила C1-C10 или H, наиболее предпочтительно алкила C1-C6 или H, особенно метила или H;
X представляет собой O или S, предпочтительно O;
n является целым числом от 1 до 100, предпочтительно от 1 до 10, предпочтительнее от 1 до 5, особенно 1-3;
и m имеет значение 1 или 2, предпочтительно 1, при нахождении в фазе жидкого мономера.
Предпочтительно, загрязненный ММА по настоящему изобретению получают конденсацией формальдегида с метилпропионатом. Показано, что по настоящее изобретение особенно полезно для отделения примесей от жидкого ММА, полученного таким способом. Как правило, загрязненный ММА для очистки способом по настоящему изобретению получают конденсацией формальдегида с метилпропионатом в присутствии пригодного основного катализатора и, необязательно, метанола, чтобы предотвратить образование кислоты. Пригодным основным катализатором для реакции конденсации является диоксид кремния, допированный щелочным металлом, например содержащий ионы цезия диоксид кремния (Cs+/SiO2). В таких случаях, пригодный для использования диоксид кремния представляет собой предпочтительно пористый диоксид кремния с большой удельной поверхностью, например силикагель, осажденный силикагель и спеченный пирогенный силикагель. Предпочтительное содержание щелочного металла в катализаторе на основе диоксида кремния находится в пределах от 1 до 10% мас. (в пересчете на металл).
Все признаки, содержащиеся в настоящем изобретении, можно сочетать с любыми из указанных выше аспектов и в любом сочетании.
Далее настоящее изобретение будет проиллюстрировано следующими примерами со ссылкой на чертеж, в котором:
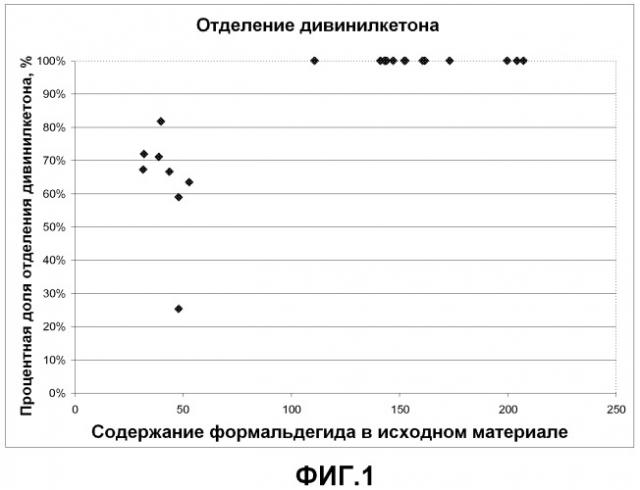
Фиг.1 содержит график отделения дивинилкетона в зависимости от содержания формальдегида в исходном материале.
Примеры
Пример 1
Промывали потоком метанола 100 г смоченной водой сильной сульфокислотной ионообменной смолы Lewatit 2314 (поставщик Lanxess) в стеклянной колонне, наполненной смолой, со скоростью 1 объем слоя в час до тех пор, пока первоначально бурый элюент не становился бесцветным на вид. Затем смолу промывали чистым ММА до снижения концентрации метанола до 100 ч/млн. Помещали 20 г указанной смолы в трехгорлую круглодонную колбу с магнитной мешалкой, термометром и обратным холодильником с водяной рубашкой. В колбу помещали 50 мл образца чистого ММА с добавкой 100 ч/млн 2-метил-1,5-гексадиена. Колбу помещали на подогретую масляную баню и отбирали пробы из колбы пипеткой через определенные промежутки времени. Одну и ту же партию смолы использовали для каждого опыта. Образцы анализировали на газовом хроматографе Varian GC, оборудованном капиллярной колонной CPSil 1701. 2-метил-1,5-гексадиен быстро изомеризовался с образованием 2-метил-2,5-гексадиена. Затем это соединение очень медленно исчезало с образованием 2-метил-2,4-гексадиена. Опыт проводили три раза при 70, 50 и 30°C. Массовые процентные доли всех компонентов приведены в таблицах 1, 3 и 5.
Пример 2
Пример 1 повторяли, но в этом случае 1000 или 7000 ч/млн 1,1-диметоксиметана добавляли к раствору ММА перед нагреванием. Массовые процентные доли всех компонентов приведены в таблицах 2, 4 и 6.
Пример 3
Пример 1 повторяли, за исключением того, что смесь, содержащую по 100 ч/млн 2,5-диметил-1,5-гексадиена и 2,5-диметил-2,4-гексадиена, использовали вместо 100 ч/млн. 2-метил-1,5-гексадиена. Массовые процентные доли всех компонентов при трех различных температурах приведены в таблицах 7, 9 и 11.
Пример 4
Пример 3 повторяли, за исключением того, что 1000 или 7000 ч/млн 1,1-диметоксиметана добавляли к раствору ММА перед нагреванием.
Массовые процентные доли всех компонентов при каждой температуре нагревания приведены в таблицах 8, 10 и 12.
В таблицах 7-12 приведено количество 2,5-диметил-2,4-гексадиена, присутствующего через различные промежутки времени и при различных температурах в присутствии и в отсутствие 1,1-диметоксиметана.
| Таблица 170°C, 0 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2-метил-1,5-гексадиен | 0,0109% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| 2-метил-2,5-гексадиен | 0,0000% | 0,0083% | 0,0072% | 0,0052% | 0,0031% | 0,0014% |
| транс-2-метил-2,4-гексадиен | 0,0000% | 0,0005% | 0,0019% | 0,0022% | 0,0027% | 0,0025% |
| цис-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| Таблица 270°C, 1000 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2-метил-1,5-гексадиен | 0,0117% | 0,0007% | 0,0004% | 0,0005% | 0,0005% | 0,0006% |
| 2-метил-2,5-гексадиен | 0,0000% | 0,0054% | 0,0027% | 0,0011% | 0,0009% | 0,0006% |
| транс-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| цис-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| Таблица 350°C, 0 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2-метил-1,5-гексадиен | 0,0109% | 0,0003% | 0,0004% | 0,0005% | 0,0005% | 0,0000% |
| 2-метил-2,5-гексадиен | 0,0000% | 0,0076% | 0,0072% | 0,0068% | 0,0065% | 0,0049% |
| транс-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0001% | 0,0003% | 0,0007% |
| цис-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| Таблица 450°C, 1000 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2-метил-1,5-гексадиен | 0,0111% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| 2-метил-2,5-гексадиен | 0,0000% | 0,0062% | 0,0047% | 0,0031% | 0,0014% | 0,0008% |
| транс-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| цис-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| Таблица 530°C, 0 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2-метил-1,5-гексадиен | 0,0132% | 0,0002% | 0,0002% | 0,0002% | 0,0002% | 0,0001% |
| 2-метил-2,5-гексадиен | 0,0000% | 0,0067% | 0,0070% | 0,0065% | 0,0065% | 0,0063% |
| транс-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| цис-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| Таблица 630°C, 7000 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2-метил-1,5-гексадиен | 0,0121% | 0,0007% | 0,0002% | 0,0002% | 0,0000% | 0,0000% |
| 2-метил-2,5-гексадиен | 0,0000% | 0,0064% | 0,0052% | 0,0031% | 0,0009% | 0,0000% |
| транс-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
| цис-2-метил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% | 0,0000% |
В отсутствие 1,1-диметоксиметана 2-метил-1,5-диметилгексадиен быстро изомеризуется в 2-метил-2,5-гексадиен и затем медленно превращается частично в 2-метил-2,4-гексадиен. В присутствии 1,1-диметоксиметана за процессом изомеризации следует быстрое удаление 2-метил-2,5-гексадиена, причем в колбе не обнаруживается 2-метил-2,4-гексадиен.
| Таблица 730°C, 0 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2,5-диметил-1,5-гексадиен | 0,0034% | 0,0000% | 0,0049% | 0,0027% | 0,0035% | 0,0034% |
| 2,5-диметил-2,4-гексадиен | 0,0000% | 0,0000% | 0,0000% | 0,0060% | 0,0054% | 0,0044% |
| Таблица 830°C, 7000 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2,5-диметил-1,5-гексадиен | 0,0069% | 0,0023% | 0,0024% | 0,0027% | 0,0023% | 0,0025% |
| 2,5-диметил-2,4-гексадиен | 0,0082% | 0,0068% | 0,0039% | 0,0018% | 0,0000% | 0,0000% |
| Таблица 950°C, 0 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2,5-диметил-1,5-гексадиен | 0,0082% | 0,0006% | 0,0009% | 0,0008% | 0,0008% | 0,0011% |
| 2,5-диметил-2,4-гексадиен | 0,0088% | 0,0111% | 0,0119% | 0,0118% | 0,0120% | 0,0117% |
| Таблица 1050°C, 1000 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2,5-диметил-1,5-гексадиен | 0,0057% | 0,0013% | 0,0016% | 0,0015% | 0,0017% | 0,0016% |
| 2,5-диметил-2,4-гексадиен | 0,0064% | 0,0090% | 0,0071% | 0,0047% | 0,0018% | 0,0013% |
| Таблица 1170°C, 0 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2,5-диметил-1,5-гексадиен | 0,0024% | 0,0005% | 0,0006% | 0,0006% | 0,0010% | 0,0012% |
| 2,5-диметил-2,4-гексадиен | 0,0042% | 0,0133% | 0,0131% | 0,0124% | 0,0104% | 0,0096% |
| Таблица 1250°C, 1000 ч/млн 1,1-диметоксиметана | ||||||
| Компонент | Время, мин | |||||
| 0 | 5 | 10 | 20 | 40 | 60 | |
| 2,5-диметил-1,5-гексадиен | 0,0027% | 0,0013% | 0,0010% | 0,0008% | 0,0007% | 0,0003% |
| 2,5-диметил-2,4-гексадиен | 0,0049% | 0,0050% | 0,0027% | 0,0014% | 0,0009% | 0,0006% |
В отсутствие 1,1-диметоксиметана за быстрой изомеризацией 2,5-диметил-2,5-гексадиена в 2,5-диметил-2,4-гексадиен следует очень медленное разложение последнего. Когда 1,1-диметоксиметан присутствует в растворе, происходит быстрое разложение 2,5-диметил-2,4-гексадиена с образованием другого продукта.
Константы скорости реакции первого порядка для разложения 2-метил-2,5-гексадиена и 2,5-ди