Полимерные системы доставки действующих веществ
Иллюстрации
Показать всеИзобретение относится к композициям, содержащим действующее вещество. Описана композиция для доставки действующего вещества, содержащая: а) по меньшей мере один блоксополимер, содержащий по меньшей мере один поли(2-оксазолиновый) блок А, состоящий из повторяющихся звеньев формулы (I), где RA означает углеводородную группу, которая необязательно может быть замещена -OH, -SH, -COOH, -NR'2, -COOR', -CONR', -CHO, где R' означает Н или С1-3 алкил, и RA выбирают таким образом, что повторяющееся звено формулы (I) является гидрофильным; и по меньшей мере один поли(2-оксазолиновый) блок В, состоящий из повторяющихся звеньев формулы (II), где RB означает углеводородную группу, которая необязательно может быть замещена галогеном, -OH, -SH, -COOH, -NR''2, -COOR'', -CONR'', -CHO, где R'' означает Н, алкил или алкенил, и RB выбирают таким образом, что повторяющееся звено формулы (II) более гидрофобно, чем повторяющееся звено формулы (I); и (b) одно или более действующее вещество. Также описано применение сополимера для солюбилизации действующего вещества в воде или водном растворе. Технический результат - описанные сополимеры служат универсальной системой доставки с высокой загрузкой для лекарственных веществ. 2 н. и 10 з.п. ф-лы, 6 ил.
Реферат
Данное изобретение относится к композициям и препаратам, содержащим действующее вещество, в особенности гидрофобные действующие вещества, совместно с системой доставки, которая способствует растворению данных веществ.
Многие наиболее эффективные лекарственные вещества и потенциальные лекарственные вещества нерастворимы в воде. Препарат малорастворимых лекарственных веществ, таких как паклитаксел (PTX) с водорастворимостью, равной примерно 1 мкг/мл, остается главной проблемой в доставке лекарств (Huh, K. M., et al., J. Controlled Release 126, 122-129 (2008); Dabholkar, R. D., et al. Int. J. Pharm. 315, 148-157 (2006); Yang, T., et al., Int. J. Pharm. 338, 317-326 (2007); Torchilin, V.P., Cell. Mol. Life. Sci 61, 2549-2559 (2004); Haag, R., Angew. Chem. Int. Ed. 43, 278-282 (2004)). В настоящее время клинический препарат паклитаксела, Taxol®, содержит менее 1% мас./мас. действующего лекарственного вещества и 99% мас./мас. носителя, который вызывает значительные побочные эффекты у пациентов. Подобные проблемы имеют действующие вещества, используемые в других технических областях, таких как защита растений от паразитов и т.п. Было разработано несколько способов солюбилизации или диспергирования действующих веществ. Традиционные способы обычно основаны на использовании растворителей, поверхностно-активных веществ или хелатообразующих веществ. Эти способы имеют один или несколько недостатков, связанных с токсичностью носителей, ограниченной стабильностью препаратов в водной среде, в частности, при разбавлении, или со сложностью процесса формулирования.
В последнее время липосомы (Wu, J., et al., Int. J. Pharm. 316, 148-153 (2006)), микро- и наночастицы (Desai, N.P. et al., Anti-Cancer Drugs 19, 899-909 (2008)), а также полимерные мицеллы (Huh, K. M., et al., J. Controlled Release 126, 122-129 (2008); Konno, T., et al., J. Biomed. Mat. Res., Part A, 65A, 210-215 (2002); Kim, S.C., et al., J. Controlled Release 72, 191-202 (2001)) активно изучались как системы солюбилизации/доставки лекарственных веществ. Каждый из этих подходов имеет свои преимущества и недостатки. Одно из главных ограничений полимерных мицелл - это емкость загрузки и общее количество лекарственного вещества, которое может быть растворено. Патентная заявка США 20040185101 раскрывает полимерные композиции со способностью солюбилизировать гидрофобные лекарственные вещества в водной среде. Тем не менее, емкость загрузки этих композиций ограничена к примеру до <10% мас./мас. для паклитаксела или менее чем 1% мас./мас. для циклоспорина А.
Поли(2-оксазолин)ы в последнее время привлекли особое внимание для применения в области биомедицины. В частности, большой интерес вызывают гидрофильные поли(2-метил-оксазолин)ы п(МеОкс) и поли(2-этил-2-оксазолин)ы п(ЭтОкс), так как они обладают маскирующими (Zalipsky, S., et al., J. Pharm. Sci. 85, 133-137 (1996); Woodle, M. C., et al., Bioconjugate Chem. 5, 494-496 (1994)) и белок-отталкивающими свойствами (Konradi, R., et al., Langmuir 24, 613-616 (2008)) и подвергаются быстрому почечному клиренсу (Gaertner, F.C., et al., J. Controlled Release 119, 219-300 (2007)), подобными свойствам поли(этиленгликоля), широко используемого полимера в инъецируемых системах доставки лекарственных веществ.
Задача настоящего изобретения состоит в предоставлении композиций, содержащих систему доставки, которая позволяет эффективно солюбилизировать и/или формулировать действующие вещества, в частности гидрофобные действующие вещества. В частности, композиции должны быть просты в изготовлении и иметь высокую емкость загрузки для конкретного действующего вещества.
Для того чтобы решить эту проблему, настоящее изобретение предоставляет композиции, содержащие
(а) по меньшей мере один сополимер, содержащий повторяющиеся звенья формулы (I),
где RA означает углеводородную группу, необязательно замещенную -OH, -SH, -COOH, -NR'2, -COOR', -CONR', -CHO, где R' означает Н или С1-3 алкил, и RA выбирают таким образом, что повторяющееся звено формулы (I) является гидрофильным,
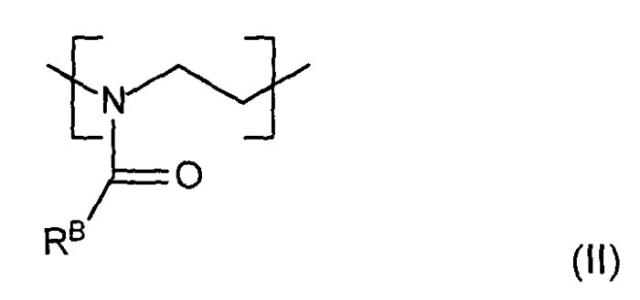
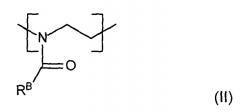
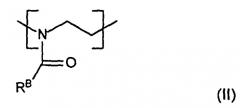
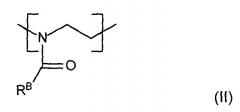
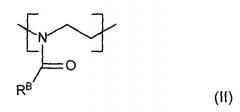
и повторяющиеся звенья формулы (II),
где RB означает углеводородную группу, необязательно замещенную галогеном, -OH, -SH, -COOH, -NR''2, -COOR'', -CONR'', -CHO, где R'' означает Н, алкил, алкенил, а RB выбирается таким образом, что повторяющееся звено формулы (II) более гидрофобно, чем повторяющееся звено формулы (I); и
(b) одно или более действующих веществ.
Более того, данное изобретение предоставляет перечисленные выше сополимеры. Композиции согласно изобретению могут быть использованы в различных технических областях, включая фармацевтику, диагностику (включая ветеринарию) и защиту растений.
На фиг.1 представлены интенсивности флуоресценции и отношения I1/I3 растворов пурина в зависимости от концентрации определенных сополимеров, используемых в контексте изобретения, при 25°C.
На фиг.2 представлены результаты растворения PTX с амфифильными сополимерами методом тонких пленок.
На фиг.3 представлены результаты измерений динамического светорассеяния заполненных лекарством мицелл, сформированных композициями согласно данному изобретению.
На фиг.4 представлены результаты измерений цитотоксичности полимеров, используемых в рамках данного изобретения, в различных клеточных линиях.
На фиг.5 представлена зависимость жизнеспособности клеток с множественной лекарственной устойчивостью линии MCF7/ADR в зависимости от дозы палитакселя, в смесях, приготовленных согласно изобретению.
На фиг.6 представлены относительные массы опухолей (А) и подавление роста опухолей (В) относительно негативных контролей мышей, подвергнутых лечению композициями, приготовленными согласно изобретению и коммерческим продуктом.
Как упомянуто выше, в звеньях формулы (I) RA является углеводородной группой, необязательно замещенной -OH, -SH, -COOH, -NR'2, -COOR', -CONR', -CHO, где R' представляет H или C1-3 алкил, и RA выбран таким образом, что повторяющееся звено формулы (I) является гидрофильным.
Предпочтительно, в качестве RA выбирать C1-8 углеводородную группу, предпочтительно, C1-6 углеводородную группу, более предпочтительно, C1-3 углеводородную группу и в особенности, C1-2 углеводородную группу, все из которых могут быть необязательно замещены. Предпочтительными углеводородными группами являются алкильные группы.
Понятно, что гидрофильное свойство звена формулы (I), как описано выше, будет зависеть от размера углеводородной группы в составе RA. При выборе короткой углеводородной группы, такой как метильная или этильная, полученная группа RA, незамещенная или замещенная перечисленными заместителями, всегда будет гидрофильна. При выборе большей углеводородной группы, наличие заместителей может вносить вклад в дополнительную полярность звеньев формулы (I). Поэтому, предпочтительно, выбирать RA соответственно конкретному случаю из метила или этила, необязательно замещенных галогеном, -OH, -SH, -COOH, -NR'2, -COOR', -CONR', -CHO, где R' представляет H или C1-3 алкил, особенно предпочтительно, RA выбирают из метила или этила.
В звеньях формулы (II), RB является углеводородной группой, необязательно замещенной галогеном, -OH, -SH, -COOH, -NR''2, -COOR'', -CONR'', -CHO, где R'' представляет водород, алкил или алкенил, и RB выбирается таким образом, что повторяющееся звено формулы (II) более гидрофобно, чем повторяющееся звено формулы (I). Если R'' является алкилом или арилом, то предпочтительна C1-8 алкильная или арильная группы. Если присутствуют галогенные заместители, предпочтительно, выбирать Cl или F.
Предпочтительно, в качестве RB выбирать C3-20 углеводородную группу, предпочтительно, C3-12 углеводородную группу, более предпочтительно, C3-6 углеводородную группу, и в особенности, C4-6 углеводородную группу, все из которых могут быть необязательно замещены. Однако, более предпочтительно, чтобы углеводородная группа не имела заместителя.
В качестве углеводородной группы предпочтительны алифатические или ароматические группы, такие как алкильные группы, арильные группы или алкарильные группы. Более предпочтительны алкильные группы, такие как пропил, бутил, пентил, гексил, гептил, октил или нонил, еще более предпочтительны C4-6 алкильные группы, т.е. бутил, пентил, гексил и особенно предпочтительны бутильные группы, особенно н-бутил.
Термины “гидрофильный” и “гидрофобный”, применяемые в контексте данного описания, широко используются в данной области. «Гидрофильный» обозначает предпочтительность водного окружения для субстанции или ее части, т.е. гидрофильная субстанция или ее часть легче растворяются или смачиваются водой, чем неполярными растворителями, такими как углеводороды. «Гидрофобный» обозначает предпочтительность неполярного окружения, т.е. гидрофобная субстанция или ее часть легче растворяются или смачиваются неполярными растворителями, такими как углеводороды, по сравнению с водой. Термин «амфифильный» обозначает одновременное присутствие гидрофильных и менее гидрофильных или более гидрофобных частей в веществе, что часто наблюдается у поверхностно-активных веществ. Таким образом, сополимеры, используемые в контексте данного изобретения, также относятся к амфифильным сополимерам, поскольку включают гидрофильные части структуры и менее гидрофильные/более гидрофобные части, соответственно.
При необходимости, т.е. в случае, если из химической структуры RA и RB не очевидно, что конкретное звено формулы (II) более гидрофобно, чем определенное звено формулы (I), это может быть установлено путем сравнения гомополимеров из соответствующих звеньев и определения для них значений logP в одинаковых условиях. LogP, как известно, является логарифмом коэффициента разделения, наблюдаемого для вещества А между водой и н-октанолом. В частности, коэффициент разделения P для вещества А определяется как отношение коэффициента разделения P=[A]н-октанол/[A]вода, где [A] обозначает концентрацию вещества А в соответствующей фазе. Более гидрофильная субстанция будет иметь большие концентрации в воде. Обычно, для измерений используется одинаковый объем воды и октанола.
В предпочтительном варианте осуществления данного изобретения, надлежащий выбор RB для получения звеньев формулы (II) c большей гидрофобностью по отношению к звеньям формулы (I) может быть проверен путем определения критической концентрации мицелообразования (ККМ) сополимера, содержащего данные структурные звенья, по методике, детально описываемой далее. Если ККМ может быть измерена, требования к гидрофильным свойствам звеньев формулы (I) и более гидрофобным/менее гидрофильным свойствам звеньев формулы (II) надлежаще выполнены.
Требования к звеньям формулы (I) быть гидрофильными, и со звеньями формулы (II) быть более гидрофобными, по сравнению к звеньям формулы (I) также будут надлежаще выполнены для любой возможной комбинации предпочтительных конструкций RA и RB, что будет ясно из соответствующих структур. А именно, в качестве RA предпочтительно, выбирать метил или этил, необязательно замещенные -ОН, -SH, -COOH, -NR'2, -COOR', -CONR', -CHO, где R' может быть Н или C1-3 аклилом, и наиболее предпочтительно, выбирать в качестве RA метил или этил; и RB выбирается из незамещенной C3-20 углеводородной группы, предпочтительно, C3-12 углеводородной группы, более предпочтительно, C3-6 углеводородной группы, и в особенности, C4-6 углеводородной группы, где в качестве углеводородных групп предпочтительны алифатические или ароматические группы, такие как алкильные группы, арильные группы или алкарильные группы. Более предпочтительны алкильные группы, такие как пропил, бутил, пентил, гексил, гептил, октил или нонил, еще более предпочтительны, C4-6 алкильные группы, т.е. бутил, пентил, гексил и особенно предпочтительны, бутильные группы, в частности н-бутил.
Следует понимать, что под водным окружением, водной средой, водными растворами и тому подобным в данной заявке подразумеваются системы растворителей, где 50% (в объемном отношении) или более, предпочтительно, 70% или более, еще более предпочтительно, 90% и более и, в частности, полностью 100% от общего объема растворителя(-лей) является вода.
Сополимер, содержащий повторяющиеся звенья формулы (I) и (II), описанные выше, может быть легко приготовлен путем полимеризации с раскрытием цикла из 2-замещенных-2-оксазолинов (или 2-замещенных-4,5-дигидрооксазолей по номенклатуре IUPAC). Таким образом, полимеры, используемые в контексте данного изобретения, также относятся к поли(2-оксозолин)ам.
Сополимер согласно данному изобретению может включать другие повторяющиеся звенья, помимо повторяющихся звеньев (I) и (II), обозначенных выше. Однако предпочтительно, что большей частью всех повторяющихся звеньев, т.е. больше 50%, более предпочтительно, больше 75%, еще более предпочтительно, больше 90% и особенно предпочтительно, 100%, относительно общего числа повторяющихся звеньев, являются повторяющиеся звенья формулы (I) или (II), как определены выше. При этом все повторяющиеся звенья формулы (II), содержащиеся в сополимере, будут более гидрофобными, чем любые из повторяющихся звеньев формулы (I), содержащихся в сополимере.
Отношение количества повторяющихся звеньев формулы (I) к количеству повторяющихся звеньев формулы (II), как правило, варьирует от 20:1 до 1:2, предпочтительно, от 10:1 до 1:1 и более предпочтительно, от 7:1 до 3:1.
Относительно расположения повторяющихся звеньев (I) и (II), обозначенных выше, сополимеры согласно изобретению могут быть статистическими сополимерами, сополимерами, содержащими сегменты полимеризованных звеньев одного типа (т.е. сегменты, содержащие звенья формулы (I), и/или сегменты, содержащие звенья формулы (II)), градиентными сополимерами или блоксополимерами. Блоксополимеры особенно предпочтительны.
Термин «блоксополимер» используется здесь в соответствии с его установленным значением в данной области и относится к сополимерам, где повторяющиеся звенья определенного типа организованы в блоки, т.е. повторяющиеся звенья одного типа полимеризованы последовательно непосредственно одно за другим, в отличие от, например, последовательностей случайно чередующихся повторяющихся звеньев различных типов. Другими словами, блоки в блоксополимере, такие как блоки А и В, о которых будет говориться ниже, представляют полимерные соединения сами по себе, полученные путем полимеризации идентичных мономеров или имеющих схожие характеристики.
Блоксополимер, который будет использоваться в соответствии с настоящим изобретением, содержит по меньшей мере один блок А поли(2-оксазолин)а, состоящий из повторяющихся звеньев формулы (I), как определено выше (который является гидрофильным благодаря присутствию соответствующих звеньев) и по меньшей мере один блок В поли(2-оксазолин)а, состоящий из повторяющихся звеньев формулы (II), как определено выше (который является более гидрофобным, чем блок А, благодаря присутствию соответствующих звеньев).
Блоксополимер по изобретению может называться амфифильным сополимером благодаря присутствию по меньшей мере одного гидрофильного участка (блок А) и по меньшей мере одного менее гидрофильного или более гидрофобного участка (блок В).
Предпочтительно, чтобы хотя бы один блок А блоксополимера, более предпочтительно, все блоки А в случае, если их много, был(были) представлены формулой (II):
где RA представлен метильной или этильной группой, предпочтительно, метильной группой, и n указывает число повторяющихся звеньев в блоке А. Предпочтительно, n равен 5 или более, более предпочтительно, 10 или более, наиболее предпочтительно, 20 или более. В большинстве случаев n менее 300, более предпочтительно, 200 или менее, еще более предпочтительно, 100 или менее, в особенности 50 или менее.
Предпочтительно, чтобы хотя бы один блок B блоксополимера, более предпочтительно, все блоки В, в случае если их много, - был/были представлены структурой (III):
где RB - это C3-20 углеводородная группа, предпочтительно, C3-12 углеводородная группа, более предпочтительно, C3-6 углеводородная группа и в особенности предпочтительно, C4-6 углеводородная группа. В качестве углеводородных групп предпочтительны алифатические или ароматические группы, такие как алкильные группы, арильные группы или алкарильные группы. Более предпочтительны алкильные группы, такие как пропил, бутил, пентил, гексил, гептил, октил или нонил, еще более предпочтительны C4-6 алкильные группы, т.е. бутил, пентил, гексил и особенно предпочтительны бутильные группы, особенно н-бутил. Вариабельная n предпочтительно, равна 5 или более, более предпочтительно, 10 или более. В большинстве случаев n менее 300, более предпочтительно, 200 или менее или 100 или менее, и особенно предпочтительно, 50 или менее.
Блоксополимер, используемый в контексте данного изобретения в качестве системы доставки лекарственного средства, содержит по крайней мере один блок А и по крайней мере один блок B, как описано выше. Также, он может содержать один или более дополнительных блоков, отличных от A или B. Однако, предпочтительно, чтобы блоксополимер содержал только блоки А и B, которые соответствуют приведенному выше описанию. Более предпочтительно, чтобы все повторяющиеся звенья блоксополимера являлись повторяющимися звеньями формулы (I) или (II), описанными выше.
Касательно расположения блоков A и B в сополимере, используемом в контексте данного изобретения, предпочтительная структура сополимера может быть описана как (AB)m или (BA)m, где m равно 1, 2 или 3, например, ABA или BAB. Более предпочтительно, чтобы блоксополимер являлся AB или BA диблоксополимером или ABA триблоксополимером.
Таким образом, в наиболее предпочтительном варианте исполнения данного изобретения, полимер состоит из А блока(ов), состоящего из полимеризованных 2-метил-2-оксазолина или 2-этил-2-оксазолина (также упоминаемых в тексте как «поли(2-метил-2-оксазолин)овые блоки» или «поли(2-этил-2-оксазолин)овые блоки») и блока(ов) B, состоящего из полимеризованного 2-(C4-6 алкил)-2-оксазолина. Еще более предпочтительно, чтобы сополимер состоял из блока(ов) A, состоящего из полимеризованных 2-метил-2-оксазолина или 2-этил-2-оксазолина и блока(ов) B, состоящих из полимеризованных 2-бутил-2-оксазолина (также называемого «поли(2-бутил-2-оксазолин)овый блок»). Более предпочтительны AB или ABA ди- и триблоксополимеры с вышеуказанной структурой.
Сополимеры, используемые в контексте данного изобретения, обычно имеют среднечисловую молекулярную массу (Mn), измеренную гельпроникающей хроматографией, в пределах от 3 до 30, более предпочтительно, от 4 до 25 и наиболее предпочтительно, от 6 до 20 кг/моль. При этом индекс полидисперсности (ИПД=Mw/Mn, где Mw - средневесовая молекулярная масса) обычно менее 1,3, предпочтительно, менее 1,25 и может даже иметь значение 1,001.
Следует понимать, что композиции также включают комбинации, например смеси или комбинации двух или более разных типов сополимеров, также описанных в данном изобретении, например комбинация сополимеров, содержащих различные группы RA и/или RB, или комбинация сополимеров с различной последовательностью расположения их повторяющихся звеньев, например комбинация статистического полимера и блоксополимера.
Сополимеры, используемые в контексте данного изобретения, могут быть приготовлены общеизвестными методами полимеризации. Например, поли(2-оксазолин)ы могут быть получены путем катионной полимеризации с раскрытием цикла по механизму живых цепей. Получение статистических сополимеров, градиент сополимеров и блоксополимеров детально описано, например, R. Luxenhofer and R. Jordan, Macromolecules 39, 3509-3516 (2006), T. Bonné et al., Colloid. Polym. Sci., 282, 833-843 (2004) или T. Bonné et al. Macromol. Chem. Phys. 2008, 1402-1408, (2007).
Что касается действующего вещества (или действующего соединения), содержащегося в композициях согласно данному изобретению, следует понимать, что композиции обычно являются удобными для формулирования действующих веществ, которые являются малорастворимыми в воде, предпочтительно, гидрофобными действующими веществами или нерастворимыми в воде действующими веществами. Поэтому предпочтительны действующие вещества c растворимостью в воде, например, в деминерализованной воде при 20°C менее 1 мг/мл, предпочтительно, менее 0,1 мг/мл, или даже менее 0,01 мг/мл, и в частности, растворимостью менее чем 0,001 мг/мл. Предпочтительно, чтобы ограниченная растворимость наблюдалась в воде в пределах pH от 4 до 10.
Действующее вещество (или действующее соединение), используемое в контексте данного изобретения, предпочтительно, является биологически активным веществом (или биологически активным соединением), включая, но не ограничиваясь, вещества, используемые в терапии (т.е. лекарствами) или в диагностике, фунгицидах, инсектицидах, пестицидах или гербицидах и любыми другими соединениями, используемыми для защиты растений или урожая, такими как фитогормоны, или действующими веществами, используемыми в ветеринарии. Используемый здесь термин «действующее вещество» также включает соединения, которые подвергаются скринингу в качестве потенциальных лидеров в процессе разработки лекарственных средств или препаратов для защиты растений. Более того, настоящее изобретение включает метод определения действующих соединений, взаимодействующих с интересующей мишенью, обычно биологической мишенью, такой как белок в общем смысле, фермент или рецептор, тестом методом скрининга, включающим этапы введения в состав препарата действующего соединения согласно изобретению и проведения скрининг-теста полученной композиции.
Конкретные примеры биоактивных веществ включают, но не ограничиваются, лекарственными средствами в следующих категориях: лекарственные средства, действующие на синаптические и нейроэффекторные узловые участки, лекарственные средства, действующие на центральную нервную систему, лекарственные средства, влияющие на воспалительные процессы, лекарственные средства, влияющие на состав жидкостей организма, лекарственные средства, влияющие на почечную функцию и метаболизм электролитов, сердечно-сосудистые лекарственные средства, лекарственные средства, воздействующие на желудочно-кишечную функцию, лекарственные средства, влияющие на маточную сократительную способность, химиотерапевтические вещества для гиперпролиферативных заболеваний, в частности рака, химиотерапевтические вещества для паразитических инфекций, химиотерапевтические вещества для микробных заболеваний, противоопухолевые вещества, иммунодепрессивные вещества, лекарственные средства, воздействующие на органы кроветворения и деградации, гормоны и их антагонисты, дерматологические препараты, антагонисты тяжелых металлов, витамины и питательные вещества, вакцины, олигонуклеотиды и генные терапии. Конкретные лекарственные вещества, которые могут быть упомянуты как подходящие для использования в настоящем изобретении, включают амфотерицин В, нифедипин, гризеофульвин, таксаны, включая паклитаксел и доцетаксел, доксорубицин, дауномицин, индометацин, ибупрофен, этопозид, циклоспорин А, витамин Е и тестостерон, в частности, паклитаксел, циклоспорин А и амфотерицин В. Как упоминалось выше, конкретная полезность данного изобретения продемонстрирована для действующих веществ, которые считаются нерастворимыми в воде.
Предполагается, что композиции, содержащие комбинации, например смеси или комбинации двух или более действующих веществ, таких как два лекарственных вещества, также включены в изобретение.
Обычно предпочтительно, что сополимер образует агрегаты в композициях в соответствии с изобретением, и более предпочтительно, что образующиеся агрегаты таковы, что агрегаты сополимеров включают действующее вещество. Особенно предпочтительной формой таких агрегатов является мицелла. Мицелла, как упоминается здесь, в общих чертах является агрегатом амфифильных сополимеров с представленной гидрофильной короной, образованной гидрофильными частями сополимера, и секвестрированными гидрофобными частями упомянутого амфифильного сополимера во внутреннюю часть мицеллы. Особенно подходящими сополимерами для образования мицелл являются блоксополимеры, описанные выше как предпочтительный вариант сополимеров. Мицеллы, упоминаемые в данном изобретении, являются трехмерными структурами. Обычно мицеллы формируются, когда концентрация амфифильных молекул, их составляющих, в водной среде превышает определенное значение. Это значение называется критической концентрацией мицеллообразования (ККМ), которая может быть измерена методом флуоресцентного зонда, такого как пирен, который накапливается в гидрофобной сердцевине мицелл, сформированных при концентрациях выше ККМ. Более конкретно, мицеллы, согласно данному изобретению, формируются, например, путем самоорганизации амфифильных блоксополимеров в гидрофильной, предпочтительно, водной среде. При формировании мицелл гидрофильные области упомянутых амфифильных сополимеров находятся в контакте с окружающим растворителем, тогда как гидрофобные области обращены к центру мицеллы. В контексте данного изобретения, центр мицеллы обычно заключает в себе гидрофобное действующее вещество. Мицеллу также можно назвать «полимерной наночастицей», в связи с ее размером, измеряемым нанометром, и поскольку она образована полимером.
Сополимеры, особенно блоксополимеры, используемые в контексте данного изобретения, обычно имеют низкие значения ККМ, обычно менее 250 мг/мл. В основном, значение ККМ варьирует между 5 и 150 или даже 5 и 100 мг/л.
Согласно данному изобретению, агрегаты, особенно мицеллы различных размеров, могут быть сформированы фармацевтическими композициями согласно изобретению, в зависимости от таких факторов, как молекулярный вес используемого сополимера или объем загрузки лекарственным средством. В основном, предпочтительно, использовать агрегаты или мицеллы с размером в пределах 5-500 нм. Однако агрегаты или мицеллы размером 5-100 или 10-50 нм или даже 10-30 нм, как показано методом динамического светорассеяния, также могут быть успешно сформированы, что особенно удобно для внутривенного введения. Примечательно, что мицеллы обычно имеют узкое распределение частиц по размерам (ИПД ≤0,2 или даже ≤0,1).
Обычно агрегаты и, в частности, мицеллы формируются в воде или водной среде. Поэтому, агрегаты и, в частности, мицеллы композиции согласно изобретению, могут быть сформированы, например, методом растворения тонких пленок. В данном методе сополимер и действующее вещество растворяются в общем растворителе, таком как ацетонитрил или диметилсульфоксид. После удаления растворителя (например, в потоке инертного газа, мягким нагреванием и/или под действием низкого давления), пленки, образованные из полимера и из действующего вещества, могут быть легко растворены в воде или водных растворителях и могут быть доведены до нужного состояния при повышении температуры. После растворения пленок происходит формирование агрегатов, преимущественно мицелл. Стабильность формирующихся агрегатов позволяет высушить полученный раствор для получения порошка. Например, сушку можно проводить путем лиофилизации, обычно без необходимости использовать криозащитные вещества, с возможностью дальнейшего восстановления в воде или водных растворителях без уменьшения емкости загрузки или нарушения целостности частиц.
При использовании описанных выше сополимеров, композиции согласно изобретению обычно формируют агрегаты, растворимые в воде или в водных растворах, где они стабильны по крайней мере 12 часов при комнатной температуре и более высоких температурах, особенно при температурах ниже 40°C, что позволяет парентеральное введение упомянутых композиций животным в общем и человеку в частности.
Соотношение масс действующего(-их) вещества(-в) к сополимеру(-ам) в композициях согласно изобретению составляет обычно 1:20 или выше, в том числе 1:10 и выше. Предпочтительное значение весового соотношения равно по крайней мере 1:9, более предпочтительно, по крайней мере 2:8, еще более предпочтительно, по крайней мере 3:7 и наиболее предпочтительно, - 4:6. В основном, соотношение равно 1:1 или менее, при необходимости, 8:10 или менее.
Композиции согласно изобретению могут быть успешно получены активной загрузкой или лекарственной загрузкой (т.е. отношение массы действующего вещества или лекарственного вещества к суммарной массе действующего вещества и блоксополимера выражается в процентах) на 10% или более, предпочтительно, на 25% или более, еще более предпочтительно, на 30% или более, еще более предпочтительно, на 35% или более и особенно на 40% или более. Примечательно, что достаточная растворимость в воде может быть, в конечном счете, получена даже для композиций согласно изобретению, имеющих настолько высокие уровни лекарственной загрузки даже для действующих веществ с растворимостью 10 мкг/мл или даже менее 5 мкг/мл, таких как паклитаксел. Таким образом, к примеру, композиции согласно изобретению позволяют солюбилизировать более 7 мг/мл паклитаксела, в частности 8 мг/мл или более, в воде и водных растворах.
Высокая емкость даже для гидрофобных действующих веществ совпадает с необычными значениями, полученными при измерении спектров флуоресценции пирена в фармацевтических композициях согласно изобретению. Отношение интенсивностей пиков I1 и I3 в спектре флуоресценции пирена является мерой полярности (K. Kalyanasundaram, J.K. Thomas, J. Am. Chem. Soc. 1977, 99, 2039-2044) окружения пиреновой пробы. В водной или схожей по полярности среде это отношение обычно варьирует между 1,6 и 1,9 (K. W. Street, Jr., W. W. Acree, Jr. Analyst 1986, 111, 1197-1201). В присутствии полимерных мицелл пирену становится доступна менее полярная среда и отношение I1/I3 обычно уменьшается параллельно с увеличением интенсивности флуоресценции. Примечательно, что в случае сополимеров, и в особенности, блоксополимеров, описанных здесь, может наблюдаться противоположный эффект, когда отношение I1/I3 увеличивается до значений выше 2, предпочтительно, 2,1 или даже выше 2,2, например, до 2,35.
Благодаря высокой эффективности солюбилизации описанных выше сополимеров и, в частности, блоксополимеров, для композиций, в частности для фармацевтических композиций, в соответствии с изобретением находящихся в форме водных растворов, в принципе достаточно, если количество сополимера варьирует от настолько низкой концентрации как 1 мг/мл, предпочтительно, 2 мг/мл, до 100 мг/мл, предпочтительно, 50 мг/мл или 20 мг/мл. Поскольку сополимеры являются биосовместимыми, т.е. нетоксичными, и быстро выводятся при почечном очищении крови, высокие концентрации не являются ограничивающим фактором, но обычно не требуются. Это позволяет значительно уменьшить количество солюбилизаторов при парентеральном применении лекарства, по сравнению с препаратами гидрофобных лекарственных средств, имеющихся на рынке, и, таким образом, уменьшить риск побочных эффектов.
Фактически, описанный блоксополимер способен снизить необходимое количество носителя для растворения паклитаксела примерно в 100 и в 9 раз по сравнению с Cremophor EL/этанол (CrEL) и AbraxaneTM, соответственно.
Более того, для композиций, описанных изобретением, емкость загрузки (т.е. количество растворенного действующего вещества/количество исходно используемого действующего вещества)*100%) может быть равна 100% и, как правило, очень высока (>80%). Это является серьезным преимуществом, так как высокая эффективность загрузки очень важна для коммерческого применения для снижения цены производства.
Как описано выше, сополимеры согласно данному изобретению могут быть использованы для повышения растворимости в воде или водных растворах действующих веществ, являющихся малорастворимыми в воде, преимущественно гидрофобными действующими веществами или нерастворимыми в воде действующими веществами, и, таким образом, они действуют как солюбилизатор для данных соединений.
В результате, в предпочтительном варианте исполнения настоящего изобретения, композиции по данному изобретению также содержат воду в виде водного раствора, эмульсии или суспензии, и в частности, предпочтительно, что они являются водными растворами действующего вещества и сополимера. Следует понимать, что термин “раствор” в конкретном контексте включает коллоидные растворы в виде, как их могут образовывать мицеллы в воде. Тем не менее, так как сополимеры, используемые в контексте данного изобретения, позволяют лиофилизацию композиций без снижения активности и стабильности действующего вещества и без необходимости использовать криопротектор, порошки, особенно лиофилизированные порошки, формируют другой предпочтительный вариант исполнения композиций согласно изобретению. Эти порошки могут быть восстановлены в воде или водных растворах.
Таким образом, сополимеры, основанные на поли(2-оксазолин)ах, описанные выше, могут служить, например, универсальной системой доставки с высокой загрузкой для гидрофобных и структурно различных лекарственных веществ, таких как паклитаксел, циклоспорин А и амфотерицин В.
Другие формы данного изобретения подытожены в следующих пунктах:
1. Фармацевтические композиции, состоящие из
(а) по крайней мере одного биосовместимого водорастворимого амфифильного блоксополимера, состоящего по крайней мере из одного блока А и по крайней мере одного блока B, где А является гидрофильным полимером, выбранным из гидрофильных поли(2-оксазолин)ов и B выбран из амфифильных или гидрофобных поли(2-оксазолин)ов и
(b) гидрофобное биоактивное соединение, которое формирует агрегаты, растворимые в воде или водных растворах, которые стабильны по крайней мере 12 часов при комнатной температуре и более высоких температурах, особенно при температурах ниже 40°C, что обеспечивает парентеральное применение упомянутых композиций для животных в общем и человека в частности.
2. Фармацевтические композиции по п.1, где B представлен следующей структурной формулой (III):
где RB - гидрофобная боковая цепь (содержащая насыщенную алифатическую цепь, содержащая ненасыщенную алифатическую цепь, насыщенное алифатическое кольцо или ненасыщенное алифатическое кольцо или их комбинации) и n выбирается равной от 1 до 300.
3. Фармацевтическая композиция по любому из пп.1 или 2, где гидрофобное биоактивное соединение представлено пептидами, пептоидами, полиенами, макроциклами, гликозидами, терпенами, терпеноидами, алифатическими и ароматическими соединениями и их производными и другими соединениями, имеющими растворимость в воде или водной среде при pH в пределах 4-10, равной менее 1 мг/мл, предпочтительно, менее 100 мкг/мл, еще более предпочтительно, менее 50 мкг/мл и наиболее предпочтительно, менее 10 мкг/мл.
4. Фармацевтические композиции по любому из пп.1-3, где гидрофобное биоактивное соединение выбирается из амфотерицина B, нифедипина, гризеофульвина, паклитаксела, докорубицина, дауномицина, индометацина, ибупрофена, этопозида и циклоспорина А.
5. Фармацевтические композиции по любому из пп.1-3, где гидрофобное биоактивное соединение - паклитаксел.
6. Фармацевтические композиции по любому из пп.1-5, где блоксополимеры AB соединены через стабильные или нестабильные сшивки для формирования соединений, которые могут быть описаны как (AB)m, где m варьирует от 2 до 100, формируя, например, линейные или звездчатые блоксополимеры, графт блоксополимеры, дендримеры или гиперразветвленные блоксополимеры.
7. Фармацевтические композиции по любому из пп.2-6, в которых гидрофобная боковая цепь R состоит из 3-6 атомов углерода.
8. Фармацевтические композиции по любому из пп.1-7, где амфифильный блоксополимер содержит блок, который частично или полностью состоит из повторяющихся звеньев производных 2-бутил-2-оксазолина.
9. Фармацевтические композиции по любому из пп.1-8, где гидрофильный полиоксазолин представлен поли(2-метил-2-оксазолин)ом или поли(2-этил-2-оксазолин)ом.
10. Фармацевтические композиции по любому из пп.1-9, где растворимые агрегаты в водной среде имеют размер от 5 до 200 нм, предпочтительно, 10-100 нм.
11. Фармацевтические композиции по любому из пп.1-10, вк