Трициклические индольные производные в качестве лигандов pbr
Иллюстрации
Показать всеИзобретение относится к новым in vivo визуализирующим агентам формулы I
где R1 означает C1-3алкил, C1-3фторалкил; R2 означает Н, ОН, галогено, C1-3алкил, C1-3алкокси, C1-3фторалкил, C1-3фторалкокси; R3 и R4 независимо означают С1-3алкил, C7-C10аралкил или R3 и R4 вместе с атомом азота, к которому они присоединены, образуют азотсодержащее C4-6алифатическое кольцо; Y1 означает CH2; Y2 означает CH2, CH2-CH2, CH(CH3)-CH2 или CH2-CH2-CH2; и где формула I, как она определена, содержит атом, представляющий собой радиоизотоп, подходящий для визуализации in vivo, выбранный из 11C, 18F, 77Br, 123I, 124I и 131I. Указанные соединения с высокой аффинностью связываются с PBR, обладают хорошим поглощением в головном мозге после введения. Описан способ получения in vivo визуализирующего агента и набор для осуществления указанного способа. Описана радиофармацевтическая композиция, содержащая in vivo визуализирующий агент. 8 н. и 13 з.п. ф-лы, 13 ил., 18 пр.
Реферат
Область изобретения
Настоящее изобретение относится к визуализации in vivo и, в частности, визуализации in vivo периферического бензодиазепинового рецептора (PBR). Предложен индольный in vivo визуализирующий агент, который с высокой аффинностью связывается с PBR, обладает хорошим поглощением в головном мозге после введения и который обладает хорошим селективным связыванием с PBR. В изобретении также предложено соединение-предшественник, полезное в синтезе in vivo визуализирующего агента по изобретению, а также способ синтеза указанного соединения-предшественника. Другие аспекты изобретения включают способ синтеза in vivo визуализирующего агента по изобретению, включающий применение соединения-предшественника, набор для осуществления указанного способа и кассету для осуществления автоматического варианта указанного способа. Кроме того, в изобретении предложена радиофармацевтическая композиция, содержащая in vivo визуализирующий агент по изобретению, а также способы применения указанного in vivo визуализирующего агента.
Предшествующий уровень техники
Известно, что периферический бензодиазепиновый рецептор (PBR) в основном локализован в периферических тканях и глиальных клетках, но его физиологическую функцию еще предстоит прояснить. Известно, что внутриклеточно PBR локализован на внешней митохондриальной мембране, что свидетельствует о возможной роли в модулировании митохондриальной функции и в иммунной системе. Кроме того, предполагалось, что PBR вовлечен в клеточную пролиферацию, стероидогенез, поток кальция и клеточное дыхание.
Аномальная экспрессия PBR ассоциируется с воспалительными болезненными состояниями центральной нервной системы (ЦНС), включающими рассеянный склероз (Banati era/2001 Neuroreport; 12(16): 3439-42; Debruyne et al 2002 Acta Neurol Beig; 102(3): 127-35), энцефалит Расмуссена (Banati et al 1999 Neurology; 53(9): 2199-203), церебральный васкулит (Goerres era/2001 Am J Roentgenol; 176(4): 1016-8), герпетический энцефалит (Cagnin et al 2001 Brain; 124(Pt 10): 2014-27) и СПИД-ассоциированную деменцию (Hammoud et al 2005 J Neurovirol; 11(4): 346-55).
Кроме того, в ЦНС документально подтверждена связь с PBR при дегенеративных заболеваниях, таких как болезнь Паркинсона (Gerhard et al 2006 Neurobiol Dis; 21(2): 404-12; Ouchi et al 2005 Ann Neurol; 57(2): 161-2), кортикобазальная дегенерация (Gerhard et al 2004 Mov Disord; 19(10): 1221-6), прогрессирующий надъядерный паралич (Gerhard et al 2006 Neurobiol Dis; 21(2): 404-12), множественная системная атрофия (Gerhard era/2003 Neurology; 61(5): 686-9), болезнь Гентингтона (Pavese era/2006 Neurology; 66(11): 1638-43; Tai et al 2007 Brain Res Bull; 72(2-3): 148-51), боковой амиотрофический склероз (Turner et al 2004 Neurobiol Dis; 15(3): 601-9) и болезнь Альцгеймера (Cagnin et а/2001 Lancet; 358(9283): 766; Yasuno era/2008 Biol Psychiatry; 64(10): 835-41).
Показано, что с аномальной экспрессией PBR связан ряд ишемических состояний ЦНС, включающих: ишемический инсульт (Gerhard et al 2005 Neuroimage; 24(2): 591-5), поражение периферических нервов (Banati et al 2001 Neuroreport; 12(16):3439-42), эпилепсию (Sauvageau 2002 Metab Brain Dis; 17(1): 3-11; Kumar et al 2008 Pediatr Neurol; 38(6)). PBR был указан как биомаркер для определения степени поражения при травматическом повреждении головного мозга (Toyama et al 2008 Ann Nucl Med; 22(5): 417-24), с сообщением об увеличении экспрессии PBR в животной модели травматического повреждения головного мозга (Venneti et al 2007 Exp Neurol; 207(1): 118-27). Интересно то, что острый стресс коррелирует с увеличением экспрессии PBR в головном мозге, в то время как хронический стресс коррелирует с понижающей регуляцией PBR (Lehmann et al 1999 Brain Res; 851(1-2): 141-7). Сообщалось о возможности установления границ глиомы с использованием [11C]PK11195 для визуализации PBR (Junck er а/1989 Ann Neurol; 26(6): 752-8). PBR также может ассоциироваться с невропатической болью, Tsuda et al обнаружил активированную микроглию у субъектов с невропатической болью (2005 TINS 28(2) рр101-7).
На периферии экспрессия PBR связана с воспалением легких (Branley et а/2008 Nucl. Med. Biol; 35(8): 901-9), хроническим обструктивным заболеванием легких и астмой (Jones et al 2003 Eur Respir J; 21(4): 567-73), воспалительным заболеванием кишечника (Ostuni et al Inflamm Bowel Dis; 2010 онлайн публикация), ревматоидным артритом (van der Laken et al 2008 Arthritis Rheum; 58(11): 3350-5), первичной фибромиалгией (Faggioli et al 2004 Rheumatology; 43(10): 1224-1225), поражением нервов (Durrenberger et al 2004 J Peripher Nerv Syst; 9(1): 15-25), атеросклерозом (Fujimura et al 2008 Atherosclerosis; 201(1): 108-111), раком толстой кишки, предстательной железы и молочной железы (Deane et al 2007 Mol Cancer Res; 5(4): 341-9; Miettinen et al 1995 Cancer Res; 55(12): 2691-5; Han et al 2003 J Recept Signal Transduct Res; 23(2-3): 225-38), воспалением почек (Tarn et al 1999 Nephrol Dial Transplant; 14(7): 1658-66; Cook et al 1999 Kidney Int; 55(4): 1319-26) и ишемически-реперфузионным повреждением (Zhang et al 2006 J Am Coil Surg; 203(3): 353-64).
Визуализация при помощи позитронно-эмиссионной томографии (PET) с использованием PBR-селективного лиганда (R)-[11C]PK11195 обеспечивает обобщенный показатель воспаления центральной нервной системы (ЦНС). Однако известно, что (R)-[11C]PK11195 обладает высоким связыванием с белком и низким соотношением специфического связывания к неспецифическому связыванию. Кроме того, роль его меченных радиоизотопами метаболитов не известна, и количественная оценка связывания требует сложного моделирования.
В данной области техники известны трициклические индольные соединения. В Davies et al (J. Med. Chem. 1998; 41(4): 451-67) раскрыт класс трициклических индольных соединений и они охарактеризованы как агонисты и антагонисты мелатонина. В Napper et al (J. Med. Chem. 2005; 48: 8045-54) раскрыта и обсуждается взаимосвязь структура-активность для класса трициклических индольных соединений в контексте селективного ингибирования фермента SIRT1 (сиртуин-1), являющегося членом семейства ферментов, которые удаляют ацетильные группы из лизиновых остатков в гистонах и других белках. Другой класс трициклических индольных соединений раскрыт в US 6451795 и обсуждается как полезный в лечении связанных с PBR болезненных состояний. В US 6451795 раскрыты значения IC50 для наиболее активных соединений в диапазоне от 0,2 нМ до 5,0 нМ и указано, что эти соединения полезны для предупреждения или лечения периферических невропатий и для лечения центральных нейродегенеративных заболеваний.
В Okubu et al (Bioorganic & Medicinal Chemistry 2004 12 3569-80) описаны дизайн, синтез и структура группы тетрациклических индольных соединений, а также их аффинность к PBR (низкие значения IC50 порядка примерно 0,4 нМ). В WO 2007/057705, переданной заявителю настоящего изобретения, раскрыты тетрациклические индольные производные, меченные рядом in vivo визуализирующих группировок. Предпочтительными in vivo визуализирующими группировками, раскрытыми в WO 2007/057705, являются такие группировки, которые подходят для визуализации при помощи позитронно-эмиссионной томографии (PET) или однофотонной эмиссионной томографии (SPECT), наиболее предпочтительно PET.
Кроме того, в находящейся на одновременном рассмотрении патентной заявке РСТ/ЕР2009/062827 описаны тетрациклические in vivo визуализирующие агенты, представляющие собой индольные производные, аналогичные агентам из WO 2007/057705.
Тетрациклические индольные производные, описанные в WO 2007/057705 и в находящейся в одновременном рассмотрении патентной заявке РСТ/ЕР2009/062827, обладают хорошей аффинностью в отношении PBR рецептора, и высокая доля радиоактивности в головном мозге в течение 60 минут после инъекции представляет собой родительский in vivo визуализирующий агент. Хотя эти тетрациклические индольные производные также достигают приемлемой начальной концентрации в головном мозге крысы в исследованиях биораспределения, поглощение все еще остается относительно низким и может быть улучшено. Авторы настоящего изобретения также обнаружили, что относительное удерживание в обонятельной луковице (области головного мозга, имеющей наивысшую концентрацию рецептора PBR) этих тетрацикпических индольных производных не достаточно высоко, как это требуется для визуализации in vivo. Таким образом, имеется сфера применения PBR in vivo визуализирующего агента, который сохраняет полезные свойства тетрациклических индольных in vivo визуализирующих агентов из вышеописанного уровня техники, но обладает улучшенным поглощением в головном мозге и улучшенным специфическим связыванием с рецептором PBR.
Краткое изложение сущности изобретения
В настоящем изобретении предложено новое трициклическое индольное соединение, подходящее для применения в качестве in vivo визуализирующего агента. В настоящем изобретении также предложено соединение-предшественник, полезное в синтезе in vivo визуализирующего агента по изобретению, а также способ синтеза указанного соединения-предшественника. Также предложен способ получения in vivo визуализирующего агента, включающий применение соединения-предшественника по изобретению. Кроме того предложена фармацевтическая композиция, содержащая in vivo визуализирующий агент по изобретению, а также набор, подходящий для облегчения приготовления этой фармацевтической композиции. В еще одном аспекте предложено применение in vivo визуализирующего агента для in vivo визуализации состояния, ассоциированного с аномальной экспрессией PBR. In vivo визуализирующий агент по настоящему изобретению сохраняет полезные свойства известных тетрациклических in vivo визуализирующих агентов в сочетании с улучшенным поглощением в головном мозге и специфичностью в отношении периферического бензодиазепинового рецептора.
Подробное описание изобретения
Визуализируюший агент
В одном из аспектов настоящего изобретения предложен in vivo визуализирующий агент формулы I:
где:
R1 представляет собой C1-3алкил или C1-3фторалкил;
R2 представляет собой водород, гидроксил, галогено, циано, C1-3алкил,
C1-3алкокси, C1-3фторалкил или C1-3фторалкокси;
R3 и R4 независимо представляют собой C1-3алкил, C7-10аралкил, или R3 и R4 вместе с атомом азота, к которому они присоединены, образуют азотсодержащее C1-6алифатическое кольцо, возможно содержащее 1 дополнительный гетероатом, выбранный из азота, кислорода и серы;
Y1 представляет собой О, S, SO, SO2 или CH2; и
Y2 представляет собой СН2, СН2-СН2, СН(СН3)-СН2 или СН2-СН2-СН2;
и где формула I, как она определена, содержит атом, который является радиоизотопом, подходящим для визуализации in vivo.
"In vivo визуализирующий агент" в контексте настоящего изобретения представляет собой радиоактивно меченное соединение, подходящее для визуализации in vivo. Используемый здесь термин "визуализация in vivo" относится к таким методам, которые неинвазивно позволяют получать изображения всех или части внутренностей субъекта.
Если не указано иное, термин "алкил" самостоятельно или в комбинации означает прямой или разветвленный алкильный радикал, предпочтительно содержащий от 1 до 3 атомов углерода. Примеры таких радикалов включают метил, этил и пропил.
Если не указано иное, термин "алкокси" означает алкильный радикал, как он определен выше, содержащий простую эфирную связь, а термин "эфирная связь" относится к группе -С-O-С-. Примеры подходящих алкильных эфирных радикалов включают метокси, этокси и пропокси.
Термин "галоген" или "галогено-" означает заместитель, выбранный из фтора, хлора, брома или йода. "Галогеноалкил" и "галогеноалкокси" представляют собой алкильную и алкокси группу соответственно, как они определены выше, замещенную одним или более галогенами. В случае галогеноалкильных и галогеноалкокси заместителей галоген подходящим образом заменяет водород в конце радикала, т.е. получается -алкилен-галоген или -алкоксилен-галоген. Термин "алкилен" относится к двухвалентной группе -(СН2)n-, где n равен 1-3, и термин "алкоксилен" относится к алкиленовой группе, содержащей простую эфирную связь, где простая эфирная связь является такой, как определено выше.
Термин "циано" относится к группе -CN.
Термин "гидроксил" относится к группе -ОН.
Термин "аралкил" относится к группе - алкилен-фенил, где алкилен является таким, как определено выше.
"Азот-содержащее C4-6алифатическое кольцо" представляет собой насыщенное C4-6алкильное кольцо, содержащее гетероатом азот. Примеры включают пирролидинильные, пиперидинильные и морфолинильные кольца.
Термин "содержит атом, который представляет собой радиоизотоп, подходящий для визуализации in vivo", означает, что в формуле I, как она определена выше, изотопная форма одного из атомов представляет собой радиоизотоп, подходящий для визуализации in vivo. Для того чтобы быть подходящим для визуализации in vivo, радиоизотоп является обнаруживаемым извне после введения указанному субъекту.
Если хиральный центр или другая форма изомерного центра присутствует в in vivo визуализирующем агенте по настоящему изобретению, то все формы такого изомера, включая энантиомеры и диастереоизомеры, охвачены настоящим изобретением. In vivo визуализирующие агенты по изобретению, содержащие хиральный центр, могут быть использованы в виде рацемической смеси или в виде энантиомерно-обогащенной смеси, или рацемическая смесь может быть разделена с использованием хорошо известных способов, и отдельный энантиомер может быть использован самостоятельно.
Предпочтительные визуализирующие агенты
R1 предпочтительно представляет собой метил или C2-3фторалкил и наиболее предпочтительно -этилен-F (т.е. -CH2-CH2-F).
R2 предпочтительно представляет собой водород, галогено, C1-3алкокси или C1-3фторалкокси. R2 наиболее предпочтительно представляет собой водород, галогено или C1-3алкокси и особенно наиболее предпочтительно водород, фтор или метокси. Когда R2 представляет собой заместитель, тогда он предпочтительно находится в положении 5 или 6 и наиболее предпочтительно выбран из 5-метокси, 6-метокси, 5-фтор и 6-фтор.
R3 и R4 предпочтительно независимо представляют собой метил, этил или бензил и наиболее предпочтительно оба являются этилом.
Альтернативно предпочтительно R3 и R4 вместе с атомом азота, к которому они присоединены, образуют азот-содержащее C5-6алифатическое кольцо.
Y1 предпочтительно представляет собой CH2.
Для наиболее предпочтительных in vivo визуализирующих агентов по настоящему изобретению Y2 представляет собой CH2-CH2.
Предпочтительный in vivo визуализирующий агент по изобретению подходит для визуализации с использованием однофотонной эмиссионной компьютерной томографии (SPECT) или позитронно-эмиссионной томографии (PET). Для SPECT подходящий радиоизотоп представляет собой гамма-излучающий радиоактивный галоген. Примерами гамма-излучающих радиоактивных галогенов, подходящих для применения в настоящем изобретении, являются 123I, 131I и 77Br. Предпочтительный гамма-излучающий радиоактивный галоген представляет собой 123I. Когда радиоизотоп in vivo визуализирующего агента представляет собой 123I, тогда предпочтительно, чтобы R2 представлял собой 123I. Для PET подходящий радиоизотоп представляет собой позитронно-эмиссионный радиоактивный неметалл. Примерами позитронно-эмиссионных радиоактивных неметаллов, подходящих для применения в настоящем изобретении, являются 11С, 18F и 124I. Предпочтительные позитронно-эмиссионные радиоактивные неметаллы представляют собой 11С и 18F. В случае 11C предпочтительно, чтобы R1 представлял собой 11С-метил. Когда радиоизотоп представляет собой 18F, тогда предпочтительно, чтобы R1 представлял собой C2-3[18F]фторалкил, наиболее предпочтительно -этилен-18F.
Предпочтительно, чтобы in vivo визуализирующий агент по изобретению подходил для PET визуализации, и 18F является предпочтительным радиоизотопом, подходящим для PET-визуализации. Предпочтение PET в способе по изобретению является следствием ее исключительной чувствительности и разрешающей способности, так что даже относительно небольшие изменения в поражении со временем могут быть обнаружены. PET-сканеры обычно измеряют радиоактивные концентрации в пикомолярном диапазоне. Микро-PET сканеры в настоящее время приближаются к пространственному разрешению приблизительно 1 мм, а клинические сканеры -приблизительно 4-5 мм.
Предпочтительный in vivo визуализирующий агент формулы 1 имеет формулу 1а:
где:
R2a представляет собой водород, галогено или C1-3алкокси;
R3a и R4a независимо представляют собой метил, этил или бензил, или вместе с атомом азота, к которому они присоединены, образуют пирролидинильное, пиперидинильное, азепанильное или морфолинильное кольцо;
Y2а представляет собой CH2, CH2-CH2, СН(CH3)-CH2 или CH2-CH2-CH2; и
n равен 1, 2 или 3.
В формуле Ia R3a и R4a предпочтительно оба представляют собой этил, или R3a представляет собой метил и R4a представляет собой бензил, или вместе с атомом азота, к которому они присоединены, образуют азепанильное кольцо.
R2а предпочтительно представляет собой водород, метокси или фтор.
Y2a предпочтительно представляет собой CH2-CH2 или СН(CH3)-CH2.
n предпочтительно равен 2.
В предпочтительном in vivo визуализирующем агенте формулы Ia:
R3a и R4a оба представляют собой этил, или R3a представляет собой метил и R4a представляет собой бензил, или вместе с атомом азота, к которому они присоединены, они образуют азепанил;
R2a представляет собой водород, метокси или фтор;
Y2a представляет собой CH2-CH2 или СН(CH3)-CH2; и
n равен 2.
Неограничивающими примерами in vivo визуализирующих агентов формулы Ia являются следующие:
Из приведенных выше in vivo визуализирующих агентов 1-11, in vivo визуализирующие агенты 5, 6, 7, 9, 10 и 11 являются предпочтительными, in vivo визуализирующие агенты 5 и 10 являются наиболее предпочтительными и in vivo визуализирующий агент 5 является особенно предпочтительным. Для любого in vivo визуализирующего агента по настоящему изобретению энантиомерно чистая форма является особенно предпочтительной.
Соединение-предшественник
В еще одном аспекте настоящего изобретения предложено соединение-предшественник для получения in vivo визуализирующего агента по изобретению, где указанное соединение-предшественник имеет формулу II:
где один из R11 и R12 содержит химическую группу, которая вступает во взаимодействие с подходящим источником радиоизотопа, как определено выше для in vivo визуализирующего агента по изобретению, так что in vivo визуализирующий агент по изобретению образуется при взаимодействии указанного соединения-предшественника с указанным подходящим источником указанного радиоизотопа, а другой из R11 и R12 является таким, как определено для R1 и R2, соответственно, и возможно содержит защитную группу; и
R13-14 и Y11-12 являются такими, как определено здесь для R3-4 и Y1-2, соответственно, и возможно каждый дополнительно содержит защитную группу.
"Соединение-предшественник" содержит нерадиоактивное производное радиоактивно меченного соединения, сконструированное так, что химическая реакция с удобной химической формой детектируемой метки происходит сайт-специфически; может быть проведена за минимальное количество стадий (в идеале за одну стадию); и без необходимости в значительной очистке (в идеале без дополнительной очистки), с получением желаемого in vivo визуализирующего агента. Такие соединения-предшественники являются синтетическими и легко могут быть получены с хорошей химической чистотой.
Под термином "защитная группа" подразумевают группу, которая ингибирует или подавляет нежелательные химические реакции, но которая сконструирована таким образом, чтобы быть достаточно реакционноспособной, чтобы она могла быть отщеплена от интересующей функциональной группы с получением желательного продукта в достаточно мягких условиях, которые не модифицируют остальную часть молекулы. Защитные группы хорошо известны специалистам в данной области техники и описаны в 'Protective Groups in Organic Synthesis', Theorodora W. Greene and Peter G. M. Wuts, (Third Edition, John Wiley & Sons, 1999).
Термин "подходящий источник радиоизотопа" означает радиоизотоп в химической форме, которая реакционноспособна с заместителем соединения-предшественника, так что радиоизотоп ковалентно присоединяется к соединению-предшественнику. Для каждого конкретного радиоизотопа, представленного в следующем разделе, обсуждается один или более чем один подходящий источник радиоизотопа. Специалисту в области in vivo визуализирующих агентов знакомы эти и другие источники радиоизотопов, подходящие для применения в настоящем изобретении.
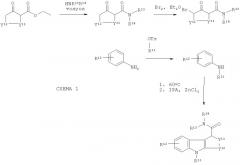
Схема 1 ниже представляет собой общую реакционную схему, которая показывает, как получить соединения, которые сами могут быть использованы в качестве соединений-предшественников или могут быть превращены в соединения-предшественники за небольшое количество дополнительных стадий. R11-14 и Y11-12 на схеме 1 являются такими, как определено выше для формулы II.
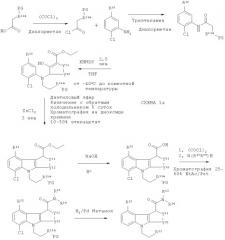
Альтернативно, когда R12 соединения-предшественника находится в верхнем положении кольца, тогда может быть использован общий путь синтеза, проиллюстрированный на схеме Ia ниже:
На схеме Ia выше -R11a-PG представляет защищенную группу R11, где R11 является таким, как подходящим образом и предпочтительно определено здесь. Когда R11 представляет собой гидрокси, тогда -R11a-PG может представлять собой, например, -O-бензил. R12-14 и Y11-12 являются такими, как подходящим образом и предпочтительно предложено для формулы II выше, при условии, что R12 не является хлоро. В этом пути синтеза хлор в нижнем положении кольца способствует прохождению циклизации только одним путем, так что образуется только один изомер. Аналогичный способ раскрыт в WO 2003/014082. Однако, когда авторы настоящего изобретения применили руководство из WO 2003/014082 для получения соединений-предшественников по настоящему изобретению, выход был низким (смотри пример 2(d)). Эта проблема была преодолена путем замены системы растворителей, используемых на стадии циклизации. В WO 2003/014082 стадию циклизации осуществляют в толуоле, в то время как авторы настоящего изобретения обнаружили, что оптимальные выходы получаются, когда вместо толуола используют диэтиловый эфир. Продукт стадии циклизации растворяется в диэтиловом эфире, в то время как не подвергшееся циклизации исходное соединение не растворяется. Таким образом, не подвергшееся циклизации исходное соединение остается с ZnCl2 в нижней части реакционного сосуда, а подвергшийся циклизации продукт переходит в диэтиловый эфир в верхней части реакционного сосуда.
Таким образом, в отдельном аспекте настоящего изобретения предложен способ получения соединения-предшественника формулы IIb:
где:
R11b является таким, как определено на схеме 1а для R11a;
R12b-14b являются такими, как определено для R12-14 формулы II, при условии, что R12b не является хлоро; и
Y11b-12b являются такими, как определено для Y11-12 формулы II;
где указанный способ включает взаимодействие соединения формулы IIc с ZnCl2:
где R12c, Y11c и Y12c являются такими, как подходящим образом и предпочтительно определено здесь для R12, Y11 и Y12 соответственно, и PGc представляет собой защитную группу;
с образованием соединения формулы IId:
где R12d, Y11d, Y12d и PGd являются такими, как определено для R12c, Y11c, Y12c и PGc соответственно;
где указанное взаимодействие осуществляют в системе растворителей, содержащей диэтиловый эфир.
Предпочтительно, указанная защитная группа PGc, PGd представляет собой - бензил. Соединение-предшественник формулы IIb представляет собой предпочтительное соединение-предшественник формулы II.
Когда радиоизотоп in vivo визуализирующего агента представляет собой 18F, тогда внесение метки 18F может быть достигнуто посредством нуклеофильного замещения уходящей группы из соединения-предшественника. Подходящие уходящие группы включают Cl, Br, I, тозилат (OTs), мезилат (OMs) и трифлат (OTf). Еще одна стратегия может заключаться в том, чтобы иметь подходящую уходящую группу вместо алкиламидной группы, представленной на соединении-предшественнике. В обоих случаях соединение-предшественник можно пометить за одну стадию путем взаимодействия с подходящим источником [18F]-фторид-иона (18F-), который обычно получают в виде водного раствора в результате ядерной реакции 18O(p,n)18F, и приводят в реакционноспособное состояние путем добавления катионного противоиона и последующего удаления воды. 18F также может быть введен путем O-алкилирования гидроксильных групп в соединении-предшественнике при помощи 18F(CH2)3-LG, где LG представляет собой уходящую группу, как определено выше. Альтернативно, радиоактивный атом фтора может быть присоединен при помощи прямой ковалентной связи к ароматическому кольцу, такому как бензольное кольцо. Для арильных систем 18F-фторидное нуклеофильное замещение из арилдиазониевой соли, арилнитросоединения или арилчетвертичной аммониевой соли являются подходящими путями получения арил-18F-производных.
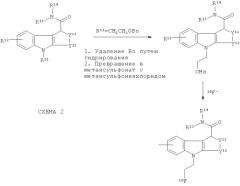
Любая из вышеприведенных схем 1 или 1а может быть продолжена с получением соединений-предшественников, подходящих для получения 18F in vivo визуализирующих агентов по изобретению, как показано на схеме 2 ниже:
Исходные соединения и промежуточные соединения имеются в продаже или известны из опубликованных научных статей, например Napper et al J Med Chem 2005; 48: 8045-54; Davies et al J Med Chem 1998; 41: 451-467.
В предпочтительном соединении-предшественнике формулы II для
получения in vivo визуализирующего агента, содержащего 18F, R11 представляет собой C1-3алкилен-LG, где LG представляет собой уходящую группу. Наиболее предпочтительное такое соединение-предшественник имеет формулу IIа:
где:
LG выбрана из мезилата, тозилата и трифлата; и R12a-14а, Y12a и m являются такими, как подходящим образом и предпочтительно определено выше для R2a-4a, Y2a и n соответственно, в формуле Ia.
Неограничивающими примерами предпочтительных соединений-предшественников формулы IIа являются следующие:
Из вышеприведенных соединений-предшественников 1-11 соединения-предшественники 5, 6, 7, 9, 10 и 11 являются предпочтительными, соединения-предшественники 5 и 10 являются наиболее предпочтительными и соединение-предшественник 5 является особенно предпочтительным.
11C-меченые PET соединения, содержащие изотопный индикатор, могут быть синтезированы путем взаимодействия соединения-предшественника с 11С-метилйодидом. Поскольку период полураспада 11С составляет только 20,4 минут, важно, чтобы промежуточный 11С-метилйодид обладал высокой специфической активностью и, следовательно, чтобы его получали с использованием реакционного процесса, который был бы настолько быстрым, насколько это возможно. Подробный обзор таких методов введения 11С-меток можно найти в Antoni et al "Aspects on the Synthesis of 11C-Labelled Compounds" in Handbook of Radiopharmaceuticals, Ed. M.J.Welch и C.S.Redvanly (2003, John Wiley and Sons).
11C-меченые in vivo визуализирующие агенты по изобретению могут быть получены путем продолжения вышеприведенной схемы 1, как показано на схеме 3 ниже:
Когда визуализирующая группировка представляет собой радиоактивный йод, тогда предпочтительные соединения-предшественники представляют собой соединения, содержащие производное, которое претерпевает электрофильное йодирование. Примерами являются металлоорганические производные, такие как триалкилстаннан (например, триметилстаннил или трибутилстаннил), или триалкилсилан (например, триметилсилил), или борорганическое соединение (например, боронатные эфиры или органотрифторбораты).
Для электрофильного радиоактивного йодирования соединение-предшественник предпочтительно содержит: активированное металлоорганическое соединение-предшественник (например, триалкилолово, триалкилсилил или борорганическое соединение). Соединения-предшественники и способы введения радиоактивного йода в органические молекулы описаны в Bolton (J. Lab. Сотр. Radiopharm. 2002; 45: 485-528). Подходящие борорганические соединения на основе боронатного эфира и их получение описаны в Kabalaka et al (Nucl. Med. Biol., 2002; 29: 841-843 и 2003; 30: 369-373). Подходящие органотрифторбораты и их получение описаны в Kabalaka et al (Nucl. Med. Biol., 2004; 31: 935-938). Предпочтительные соединения-предшественники для радиоактивного йодирования содержат металлоорганическое соединение-предшественник, наиболее предпочтительно триалкилолово.
Меченные радиоактивный йодом in vivo визуализирующие агенты по изобретению могут быть получены путем продолжения вышеприведенной схемы 1, как проиллюстрировано на приведенной ниже схеме 4:
Радиоактивное бромирование может быть осуществлено при помощи способов, аналогичных способам, описанным выше для радиоактивного йодирования. Kabalka и Varma привели обзор различных способов синтеза радиоактивных галогенированных соединений, включающих радиобромированные соединения (Tetrahedron 1989; 45(21): 6601-21).
Соединение-предшественник по изобретению в идеале предложено в стерильной апирогенной форме. Соответственно, соединение-предшественник можно использовать для изготовления фармацевтической композиции, содержащей in vivo визуализирующий агент вместе с биосовместимым носителем, подходящим для введения млекопитающему. Соединение-предшественник также подходит для включения в качестве компонента в набор или кассету для изготовления такой фармацевтической композиции. Эти аспекты более подробно обсуждаются ниже.
В еще одном предпочтительном воплощении соединение-предшественник связан с твердой фазой. Соединение-предшественник предпочтительно поставляется ковалентно присоединенным к твердой несущей матрице. Таким образом, желательный продукт образуется в растворе, в то время как исходные вещества и примеси остаются связанными с твердой фазой. В качестве примера такой системы соединения-предшественники для твердофазного электрофильного фторирования при помощи 18F-фторида описаны в WO 03/002489, и соединения-предшественники для твердофазного нуклеофильного фторирования при помощи 18F-фторида описаны в WO 03/002157.
Способ получения
В еще одном аспекте настоящего изобретения предложен способ получения in vivo визуализирующего агента по изобретению, при котором:
(1) берут соединение-предшественник по изобретению;
(2) берут подходящий источник указанного радиоизотопа, как определено здесь;
(3) приводят соединение-предшественник со стадии (1) во взаимодействие с радиоизотопом со стадии (2) с получением in vivo визуализирующего агента по изобретению.
На стадии (1) соединение-предшественник может быть получено в растворе в наборе или в кассете, подходящей для применения с аппаратом для автоматического синтеза, или альтернативно присоединено к твердому носителю, как описано выше в описании соединения-предшественника. Набор и кассета образуют дополнительные аспекты изобретения и более подробно будут обсуждаться ниже.
Стадия "взаимодействия" соединения-предшественника с радиоизотопом включает приведение двух реагирующих веществ вместе в условиях реакции, подходящих для образования желаемого in vivo визуализирующего агента с настолько высоким радиохимическим выходом (RCY), насколько это возможно. Некоторые конкретные синтетические пути получения in vivo визуализирующих агентов по настоящему изобретению представлены в нижеприведенном экспериментальном разделе.
Для способа получения по изобретению подходящие и предпочтительные воплощения in vivo визуализирующего агента, соединения-предшественника и радиоизотопа являются такими, как уже здесь предложено.
Набор и кассета
В еще одном аспекте настоящего изобретения предложен набор для получения in vivo визуализирующего агента по изобретению, где указанный набор содержит соединение-предшественник по изобретению, так, что взаимодействие со стерильным источником радиоизотопа позволяет получить желаемый in vivo визуализирующий агент с минимальным количеством манипуляций. Данные соображения особенно важны, когда радиоизотоп обладает относительно коротким периодом полураспада, и для облегчения обработки и, следовательно, уменьшенной дозы радиации для радиофармацевта. Соединение-предшественник предпочтительно представлено в наборе в лиофилизированной форме, и реакционная среда для восстановления таких наборов предпочтительно представляет собой биосовместимый носитель.
"Биосовместимый носитель" представляет собой жидкость, в частности жидкость, в которой in vivo визуализирующий агент суспендирован или растворен, так что композиция является физиологически приемлемой, т.е. может быть введена в организм млекопитающего без токсичности или чрезмерного дискомфорта. Биосовместимый носитель подходящим образом представляет собой инъецируемую жидкость-носитель, такую как стерильная апирогенная вода для инъекции; водный раствор, такой как физиологический раствор (который предпочтительно может быть сбалансирован таким образом, что конечный продукт для инъекции является или изотоническим или не гипотоническим); водный раствор одного или более веществ, регулирующих ионную силу (например, солей катионов плазмы крови с биосовместимыми противоионами), сахаров (например, глюкозы или сахарозы), сахарных спиртов (например, сорбита или маннита), гликоли (например, глицерин) или другие неионные полиольные вещества (например, полиэтиленгликоли, пропиленгликоли и т.п.). Биосовместимый носитель также может содержать биосовместимые органические растворители, такие как этанол. Такие органические растворители полезны для солюбилизации более липофильных соединений или композиций. Предпочтительно биосовместимый носитель представляет собой апирогенную воду для инъекции, изотонический физиологический раствор или водный этанольный раствор. pH биосовместимого носителя для внутривенной инъекции подходящим образом находится в диапазоне от 4,0 до 10,5.
В наборе по изобретению соединение-предшественник предпочтительно представлен в закрытом контейнере, который обеспечивает поддержание стерильности и/или радиоактивной безопасности, с возможным при