Соединения и фармацевтические композиции для лечения вирусных инфекций
Иллюстрации
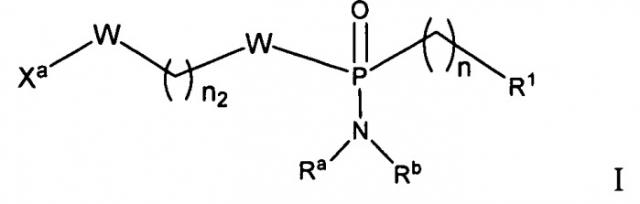
Показать всеНастоящее изобретение относится к соединениям формул:
,
где Ry представляет собой гидрокси(C1-C10)алкил; Ra и Rb независимо представляют собой водород, необязательно замещенный C1-C10 алкил, арил, арил(C1-C10)алкил или (C1-C10)циклоалкил, или Ra и Rb вместе с атомом азота образуют гетероциклическое или гетероарильное кольцо, имеющее от 3 до 7 членов; R1 выбран из рибавирина, вирамидина, валопицитабина, PSI-6130, МК-0608, резиквимода, целгосивира, ламивудина, энтекавира, телбивудина, рацивира, эмтрицитабина, клевудина, амдоксовира и валторцитабина; а также композициям на их основе для лечения гепатита B или C. Предложены новые эффективные соединения против гепатита В или С. 4 н. и 9 з.п. ф-лы, 2 ил., 28 пр.
Реферат
ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая патентная заявка устанавливает приоритет 1) предварительной заявки США № 60/877944, зарегистрированной 28 декабря 2006 года; 2) предварительной заявки США № 60/936290, зарегистрированной 18 июня 2007 года; и 3) предварительной заявки США № 60/985891, зарегистрированной 6 ноября 2007 года. Раскрытия вышеупомянутых заявок включены в настоящее изобретение в качестве ссылки во всей их полноте.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединениям, способам и фармацевтическим композициям для применения в лечении вирусных инфекций, включающих в себя вирусные инфекции гепатит C и гепатит B у организма-хозяина, который нуждается в лечении. В конкретном варианте осуществления рассматриваются нуклеозидные соединения фосфорамидатов или фосфонамидатов, которые обеспечивают концентрацию препарата в печени.
УРОВЕНЬ ТЕХНИКИ
Вирусы семейства Flaviviridae
Семейство вирусов Flaviviridae содержит по меньшей мере три разных рода: пестивирусы (pestivirus), которые вызывают болезни крупного рогатого скота и свиней, флавивирусы (flavivirus), которые являются первичной причиной таких болезней, как лихорадка денге и желтая лихорадка; и гепацивирусы (hepacivirus), единственным представителем которых является HCV. Род флавивирусов включает в себя более 68 членов, подразделяемых на группы на основе серологического родства (Calisher et al., J. Gen. Virol, 1993, 70, 37-43). Клинические симптомы различны и включают в себя лихорадку, энцефалит и геморрагическую лихорадку (Fields Virology, Editors: Fields, B.N., Knipe, D.M., and Howley, P.M., Lippincott-Raven Publishers, Philadelphia, PA, 1996, Chapter 31, 931-959). Флавивирусы, связанные с болезнями человека, вызывающие глобальную озабоченность, включают в себя вирусы геморрагической лихорадки денге (DHF), вирус желтой лихорадки, синдром шока и вирус японского энцефалита (Halstead, S.B., Rev. Infect. Dis., 1984, 6, 251-264; Halstead, S.B., Science, 239:476-481, 1988; Monath, T.P., New Eng. J. Med., 1988, 319, 641-643).
Род пестивирусов включает в себя вирус бычьей вирусной диареи (BVDV), классический вирус лихорадки свиней (CSFV, также называемый вирусом холеры свиней) и вирусом пограничной болезни овец (BDV) (Moennig, V. et al Adv. Vir. Res. 1992, 41, 53-98). Пестивирусные инфекции домашнего скота (крупного рогатого скота, свиней и овец) приносят значительные экономические потери во всем мире. Вирус BVDV вызывает вирусную диарею крупного рогатого скота и в большой степени влияет на экономику животноводства (Meyers, G. and Thiel, H.- J., Advances in Virus Research, 1996, 47, 53-118; Moennig V., et al., Adv. Vir. Res. 1992, 41, 53-98). В отличие от пестивирусов животных пестивирусы человека не были так широко изучены. Вместе с тем, серологические обследования указывают на значительное распространение пестивирусов у людей.
Pestiviruses и hepaciviruses представляют собой близко родственные группы вирусов в семействе Flaviviridae. Другие близко родственные вирусы в этом семействе включают в себя GB-вирус A, GB А-вирусоподобные агенты, GB-вирус B и GB-вирус C (также называемый G-вирусом гепатита, HGV). Группа гепацивирусов (гепатит C вирус; HCV) состоит из множества близко родственных, но генотипически различимых вирусов, инфицирующих людей. Существует около 6 генотипов и более 50 подтипов HCV. По причине сходства пестивирусов и гепацивирусов, в сочетании со слабой способностью гепацивирусов к эффективному росту в клеточной культуре, вирус бычьей вирусной диареи (BVDV) часто используют в качестве заместителя для изучения вируса HCV.
Генетическая организация пестивирусов и гепацивирусов является очень сходной. Эти плюс-нитевые РНК-вирусы обладают единственной большой открытой рамкой считывания (ORF), кодирующий все вирусные белки, необходимые для репликации вируса. Эти белки экспрессируются как полипротеины, которые со-трансляционно и пост-трансляционно процессируются как клеточными, так и вирус-кодируемыми протеиназами, для получения зрелых вирусных белков. Вирусные белки, отвечающие за репликацию вирусного генома РНК, расположены вблизи карбокси-конца. Две трети ORF называют неструктурными белками (NS). Генетическая организация и процессирование полипротеина из участка неструктурного белка ORF у пестивирусов и гепацивирусов является очень сходной. И у пестивирусов и гепацивирусов зрелые неструктурные белки (NS) состоят из p7, NS2, NS3, NS4A, NS4B, NS5A, и NS5B, в порядке последовательности от амино-конца кодирующего участка неструктурного белка к карбокси-концу ORF.
NS белки пестивирусов и гепацивирусов имеют общие области последовательностей, которые характерны для некоторых функций белка. Например, белки NS3 обеих групп вирусов имеют мотивы аминокислотной последовательности сериновых протеиназ и геликаз (Gorbalenya et al (1988) Nature 333:22; Bazan and Fletterick (1989) Virology 171:637-639; Gorbalenya et al (1989) Nucleic Acid Res. 17.3889-3897). Аналогично, белки NS5B пестивирусов и гепацивирусов имеют мотивы, характерные для РНК-направленных РНК-полимераз (Koonin, E.V. and Dolja, V.V. (1993; Crit. Rev. Biochem. Molec. Biol. 28:375-430).
Фактически, в жизненном цикле вирусов роли и функции NS белков пестивирусов и гепацивирусов являются прямо аналогичными. В обоих случаях сериновая протеиназа NS3 отвечает за весь протеолитический процессинг предшественников полипротеина, расположенных ниже от ее положения в ORF (Wiskerchen and Collett (1991) Virology 184:341-350; Bartenschlager et al (1993) J. Virol. 67:3835-3844; Eckart et al (1993) Biochem. Biophys. Res. Comm. 192:399-406; Grakoui et al (1993) J. Virol. 67:2832-2843; Grakoui et al (1993) Proc. Natl. Acad. Sci. USA 90:10583-10587; Hijikata et al (1993) J. Virol. 67:4665-4675; Tome et al (1993) J. Virol. 67:4017-4026). В обоих случаях белок NS4A действует как кофактор с сериновой протеазой NS3 (Bartenschlager et al (1994) J. Virol. 68:5045-5055; Failla et al (1994) J. Virol. 68:3753-3760; Lin et al (1994) 68:8147-8157; Xu et al (1997) J. Virol. 71:5312-5322). Белок NS3 обоих вирусов также функционирует как геликаза (Kim et al (1995) Biochem. Biophys. Res. Comm. 215: 160-166; Jin and Peterson (1995; Arch. Biochem. Biophys., 323:47-53; Warrener and Collett (1995) J. Virol. 69:1720-1726). Наконец, белки NS5B пестивирусов и гепацивирусов обладают прогнозирумым действием РНК-направленной РНК-полимеразы (Behrens et al (1996) EMBO J. 15:12-22; Lchmann et al (1997) J. Virol. 71:8416-8428; Yuan et al (1997) Biochem. Biophys. Res. Comm. 232:231-235; Hagedorn, PCT WO 97/12033; патенты США US №№ 5981247; 6248589 и 6461845, Zhong et al (1998) J. Virol. 72.9365-9369).
Вирус гепатита C
Вирус гепатита C (HCV) является основной причиной хронического заболевания печени во всем мире. (Boyer, N. et al. J. Hepatol. 32:98-112, 2000). Вирус HCV вызывает медленно развивающуюся вирусную инфекцию и является главной причиной цирроза печени и гепатоцеллюлярной карциномы (Di Besceglie, A. M. and Bacon, B.R., Scientific American, Oct.: 80-85, (1999); Boyer, N. et al. J. Hepatol. 32:98-112, 2000). Около 170 миллионов человек во всем мире инфицированы вирусом HCV. (Boyer, N. et al J. Hepatol. 32:98-112, 2000). Цирроз печени, вызываемый хроническим инфекционным гепатитом C, ежегодно в США является причиной 8000-12000 смертельных исходов, и HCV-инфекция представляет собой ведущее показание для трансплантации печени.
Известно, что HCV вызывает по меньшей мере 80% случаев посттрансфузионного гепатита и значительный процент случаев спорадического острого гепатита. Ранее доказано, что HCV также вовлечен во многие случаи "идиопатического" хронического гепатита, "криптогенного" цирроза печени, и вероятно, гепатоцеллюлярной карциномы, которые не связаны с другими вирусами гепатита, такими как вирус гепатита B (HBV). Среди здоровых людей небольшой процент, отличающийся в зависимости от географических и других эпидемиологических факторов, указывает на хроническое носительство HCV. Количество может значительно превышать цифры для HBV, хотя информация является предварительной; остается неясным число таких людей, имеющих субклиническое хроническое заболевание печени. (The Merck Manual, ch. 69, p. 901, 16th ed., (1992)).
HCV представляет собой оболочечный вирус, содержащий позитивный смысловой одноцепочечный геном РНК размером около 9,4 т.п.н. Вирусный геном состоит из 5' нетранслируемой области (UTR), длинной открытой рамки считывания, кодирующей полипротеиновый предшественник размером около 3011 аминокислот, и короткой области 3' UTR. Область 5' UTR представляет собой наиболее высококонсервативную часть генома HCV и является важной для инициации и контроля трансляции полипротеина. Трансляция генома HCV инициируется кэп-независимым механизмом, известным как внутренний вход рибосом. Этот механизм охватывает связывание рибосом с последовательностью РНК, называемой участком внутреннего входа рибосом (IRES). Недавно было выявлено, что структура псевдоузла РНК является важным структурным элементом участка IRES у вируса HCV. Вирусные структурные белки включают в себя нуклеокапсидный белок сердцевины (C) и два оболочечных гликопротеина, E1 и E2. HCV также кодирует две протеиназы: цинк-зависимую металлопротеиназу, кодирующую NS2-NS3 область, и сериновую протеиназу, кодирующую область NS3. Указанные протеиназы необходимы для расщепления некоторых областей предшественника полипротеина в зрелые пептиды. Карбоксильная половина неструктурного белка 5, а именно NS5B, содержит РНК-зависимую РНК-полимеразу. Функция остальных неструктурных белков, NS4A и NS4B, и части NS5A (амино-концевая половина неструктурного белка 5) остается неизвестной.
Современные противовирусные исследования в большой степени направлены на разработку улучшенных способов лечения хронических HCV-инфекций у людей (Di Besceglie, A.M. and Bacon, B.R., Scientific American, Oct.: 80-85, (1999)).
В свете того, что инфекция HCV достигла эпидемического уровня во всем мире, и имеет трагические последствия для инфицированного больного, существует серьезная потребность в обеспечении новых эффективных фармацевтических средств для лечения гепатита C, при этом обладающих низкой токсичностью для организма-хозяина.
Дополнительно, учитывая возрастающую угрозу других флавивирусных инфекций, остается большая потребность в обеспечении новых эффективных фармацевтических средств, обладающих низкой токсичностью для организма-хозяина.
Гепатит B
Вирусный гепатит B достиг эпидемического уровня во всем мире. После инкубационного периода продолжительностью от двух до шести месяцев, в течение которых организм не знает об инфекции, инфицирование HBV может привести к развитию острого гепатита и поражению печени, которые вызывают боль в животе, желтуху и повышение уровня содержания в крови некоторых ферментов. Вирус HBV может вызывать скоротечный гепатит, быстро прогрессирующую, часто летальную форму болезни, при которой происходит массивное разрушение долей печени. Исходом острого вирусного гепатита обычно является выздоровление больных. Вместе с тем, у некоторых больных сохраняются высокие уровни в крови вирусного антигена в течение продолжительного, или неопределенного периода, что вызывает хроническую инфекцию. Хронические инфекции могут приводить к хроническому персистирующему гепатиту. Наибольшая частота больных, инфицированных хроническим персистирующим HBV, встречается в развивающихся странах. Хронический персистирующий гепатит может вызвать истощение, цирроз печени и гепатоцеллюлярную карциному, первичный рак печени. В западных промышленно развитых странах в группы высокого риска по инфекции HBV входят лица, имеющие контакт с носителями HBV или с образцами их крови. Эпидемиология HBV фактически очень сходна с эпидемиологией синдрома приобретенного иммунодефицита, который вносит свой вклад в причины распространенности HBV-инфекции у больных СПИДом или ВИЧ-ассоциированными инфекциями. При этом HBV является более контагиозным, чем ВИЧ.
Благоприятный прогноз дает ежедневное введение α-интерферона, белка, созданного генно-инженерной технологией. Также для иммунизации пациентов против HBV разработана вакцина, полученная из человеческой сыворотки. Вакцины были получены способом генной инженерии. Вакцина проявила эффективность, но вместе с тем ее производство имеет ряд проблем, поскольку получение человеческой сыворотки от хронических носителей ограничено, и процедура очистки является продолжительной и дорогой. Дополнительно, для гарантии безопасности каждую партию вакцины, изготовленную из разной сыворотки, необходимо проверять на шимпанзе. Кроме того, вакцина не эффективна у пациентов, уже инфицированных вирусом.
Важным этапом в схеме действия пуриновых и пиримидиновых нуклеозидов против вирусных болезней, и в частности, против HBV и HCV, является их метаболическая активация клеточными киназами, для получения моно-, ди- и три-производных фосфата. Биологически активным видом многих нуклеозидов является трифосфатная форма, которая ингибирует вирусную ДНК-полимеразу, РНК-полимеразу или обратную транскриптазу, или приводит к терминации цепи.
В свете того, что инфицирование вирусами гепатита B и C достигло эпидемического уровня во всем мире и имеет тяжелейшие последствия для инфицированного больного, существует серьезная необходимость обеспечения новых эффективных фармацевтических средств для лечения людей, зараженных вирусом, при этом обладающих низкой токсичностью для организма-хозяина.
В этой связи остается потребность в эффективных способах лечения инфекций HCV и HBV.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящем изобретении рассмотрены фосфорамидатные и фосфонамидатные соединения ряда терапевтических средств, а также способы их изготовления и использования при лечении ряда патологий, включающих в себя заболевания печени. Указанные соединения можно использовать в некоторых вариантах осуществления для обеспечения концентрации терапевтического средства в печени. В одном варианте осуществления соединение представляет собой S-пивалоил-2-тиоэтилфосфорамидат, S-пивалоил-2-тиоэтилфосфонамидат, S-гидроксипивалоил-2-тиоэтилфосфорамидат или S-гидроксипивалоил-2-тиоэтилфосфонамидат.
В настоящем изобретении рассмотрены фосфорамидатные и фосфонамидатные соединения ряда терапевтических средств. Используемый в настоящем изобретении термин "фосфорамидатное или фосфонамидатное соединение терапевтического средства" включает в себя терапевтическое вещество, дериватизированное для включения в него фосфорамидатной или фосфонамидатной группы. Терапевтическое средство, например, представляет собой противовирусное средство, которое включает в себя, или было дериватизировано, чтобы включать в себя реакционно-способную группу, такую как гидроксильная группа, для присоединения фосфорамидатной или фосфонамидатной группы. Такие терапевтические средства включают в себя без ограничения нуклеозиды и аналоги нуклеозидов, включающих в себя нециклические нуклеозиды. В некоторых вариантах осуществления также рассматриваются фосфорамидаты нуклеотидов и аналогов нуклеотидов, такие как фосфорамидаты 1', 2', 3'-разветвленных и 4'-разветвленных нуклеозидов. Такие соединения можно вводить в эффективном количестве для лечения заболеваний печени, в число которых входят инфекционные болезни, такие как инфекции гепатита B и гепатита C, включающие в себя резистентные штаммы их вирусов.
В некоторых вариантах осуществления, без ограничения какой-либо теорией, возможно получение исходного лекарственного средства путем селективного метаболизма фосфорамидатного или фосфонамидатного соединения в печени, и таким образом, исходного лекарственного средства, способного к накоплению в печени организма-хозяина. Путем селективного направленного транспорта и активации соединений в печени можно уменьшать потенциальное нежелательное распространение активного соединения в желудочно-кишечном тракте. Кроме того, можно увеличивать терапевтическое количество активного соединения в участке печени, пораженном инфекцией.
В некоторых вариантах осуществления препарат 5'-монофосфата или фосфоната исходного нуклеозида (или нуклеозидного производного) создается путем метаболизма фосфорамидатного или фосфонамидатного соединения в печени, что дает возможность образования и накопления монофосфата или фосфоната в печени организма-хозяина. Таким образом, в некоторых вариантах осуществления, фосфорамидат эффективно обеспечивает устойчивый фосфат на нуклеозиде или нуклеозидном аналоге. В некоторых вариантах осуществления, когда для активации соединения необходимо его трифосфорилирование, преимущество дает устранение необходимости начального этапа фосфорилирования, и облегчение образования более зрелой формы активного трифосфата, который ингибирует фермент-мишень и может повышать общую активность нуклеозида или нуклеозидного аналога.
Без ограничения какой-либо теорией, в одном варианте осуществления рассмотрен фосфорамидат нуклеозида, такого как 2'-C-метил-рибонуклеозида, который после перорального введения селективно концентрируется в печени и метаболизируется клетками печени, с получением 5'-монофосфата, который можно энзиматически преобразовать в активную форму 5'-трифосфата, ингибирующего HCV-полимеразу. Таким образом, существует возможность уменьшить терапевтические дозы по сравнению с введением исходной нуклеозидной молекулы.
Таким образом, в некоторых вариантах осуществления, после перорального введения описываемых в настоящем изобретении фосфорамидатных и фосфонамидатных соединений, для получения терапевтического эффекта преимущество дает концентрация в клетках инфицированного участка печени указанных соединений и преобразование их в фосфат или фосфонат в клетках печени, и затем их необязательное дополнительное фосфорилирование.
Поскольку указанные способы позволяют накапливать в печени организма-хозяина фосфорамидатные или фосфонамидатные соединения, раскрытые в настоящем изобретении, указанные способы могут быть полезными, например, для лечения и/или профилактики болезней или патологии печени, таких как гепатит B или C.
В некоторых вариантах осуществления в настоящем изобретении рассматриваются соединения, полезные для профилактики и лечения флавивирусных инфекций и других связанных с ними состояний, таких как состояния с положительными анти-флавивирусными антителами и флавивирус-положительные состояния, хроническое воспаление печени, вызванное HCV, циррозом печени, фиброзом, острым гепатитом, скоротечным гепатитом, хроническим персистирующим гепатитом и истощением. Эти соединения или рецептуры можно также использовать с целью профилактики для предотвращения или замедления развития клинического проявления болезни у людей, являющихся позитивными на анти-флавивирусные антитела или флавивирус-антиген, или у людей, контактировавших с флавивирусом. В одном конкретном варианте осуществления флавивирус представляет собой вирус гепатита C. В некоторых вариантах осуществления указанное соединение используют для лечения инфекции любым вирусом, который реплицируется посредством РНК-зависимой РНК-полимеразы.
Также рассматривается способ лечения флавивирусной инфекции у организма-хозяина, включающего в себя человека, который включает в себя введение эффективного количества рассматриваемого в настоящем изобретении соединения, которое вводят единственным или в комбинации или чередовании с другим анти-флавивирусным средством, необязательно в фармацевтически приемлемом носителе.
В некоторых вариантах осуществления настоящего изобретения рассматривается способ лечения и/или профилактики инфекций гепатита B и других связанных с ним состояний, таких как состояния с положительными анти-HBV антителами и HBV-положительных состояний, хроническое воспаление печени, вызванное HBV, фиброзом, циррозом печени, острым гепатитом, скоротечным гепатитом, хроническим персистирующим гепатитом и истощением.
В некоторых вариантах осуществления можно изготавливать фосфорамидатные или фосфонамидатные соединения ряда фармацевтических средств и терапевтически применять их согласно настоящему изобретению для увеличения доставки лекарственного средства в печень. В одном варианте осуществления соединение представляет собой производное S-ацил-2-тиоэтилфосфорамидата или S-ацил-2-тиоэтилфосфонамидата, например, производное S-пивалоил-2-тиоэтилфосфорамидата или S-гидроксипивалоил-2-тиоэтилфосфонамидата.
Рассматриваемые в настоящем изобретении фосфорамидатные или фосфонамидатные соединения, а также их соли и композиции, содержащие указанные соединения, являются полезными для лечения заболеваний печени, таких как инфекции HBV и/или HCV. В одном варианте осуществления, соединение согласно настоящему изобретению представляет собой соединение формулы I:
или его фармацевтически приемлемую соль, сольват, стереоизомерную, таутомерную или полиморфную форму, в которой
Xa представляет собой
Z является O или S;
каждый из W независимо является O или S;
Ry и Ru каждый независимо представляет собой алкил, алкенил, алкинил, арил, алкиларил, циклоалкил, циклоалкенил, амино, аминоалкил, гидроксиалкил, алкокси, гетероциклил или гетероарил, все из которых необязательно замещаются;
Ra и Rb выбирают следующим образом:
i) Ra и Rb каждый независимо представляют собой водород, алкил, карбоксиалкил, гидроксиалкил, гидроксиарилалкил, ацилоксиалкил, аминокарбонилалкил, алкоксикарбонилалкил, арил, арилалкил, циклоалкил, арил, гетероарил или гетероциклил, все из которых необязательно замещаются; или
ii) Ra и Rb вместе с атомом азота, на который они замещены, образуют гетероциклическое или гетероарильное кольцо, имеющее от 3 до 7 членов;
n равен от 0 до 3;
n2 равен 1-4; и
R1 является функциональной группой, получаемой удалением водорода из гидроксигруппы противовирусного препарата.
В другом варианте осуществления
Xa представляет собой
Z является O, S, NH или NRW, при этом Rw, например, представляет собой алкил, алкил, алкенил, алкинил, арил, алкиларил, циклоалкил, циклоалкенил, амино, аминоалкил, алкокси, гетероциклил или гетероарил, все из которых необязательно замещаются;
каждый из W является O, S, NH или NRW, где Rw, например, представляет собой алкил, алкил, алкенил, алкинил, арил, алкиларил, циклоалкил, циклоалкенил, амино, аминоалкил, алкокси, гетероциклил или гетероарил, все из которых необязательно замещаются;
Ry и Ru каждый независимо представляет собой алкил, алкенил, алкинил, арил, алкиларил, циклоалкил, циклоалкенил, амино, аминоалкил, алкокси, гетероциклил или гетероарил, все из которых необязательно замещаются;
Ra и Rb выбирают следующим образом:
i) Ra и Rb каждый независимо представляют собой водород, алкил, карбоксиалкил, гидроксиалкил, гидроксиарилалкил, ацилоксиалкил, аминокарбонилалкил, алкоксикарбонилалкил, арил, алкиларил, циклоалкил, гетероарил или гетероциклил, все из которых необязательно замещаются; или
ii) Ra и Rb вместе с атомом азота, на который они замещены, образуют гетероциклическое или гетероарильное кольцо, имеющее от 3 до 7 членов;
n равен от 0 до 3;
n2 равен 1-4; и
R1 такой, как указано выше.
Специалистам в данной области техники известно, что соединения формулы I можно конструировать или изготавливать путем реакции, например, по гидроксигруппе указанного противовирусного препарата, например, посредством конденсации или дегидратирования. Для удобства, в описании настоящего изобретения, когда заместители, такие как приведенные в качестве примера R1 указаны как лекарственный препарат, специалистам в данной области техники будет очевидно, что соединение, например, формулы I, содержит производное, например, радикал противовирусного препарата. Такие производные можно изготовить, например, путем удаления водородного радикала из гидроксигруппы препарата, например, в реакции дегидратации. Если целесообразно, некоторые производные можно изготавливать модификацией фосфата или фосфоната противовирусного препарата, для получения соединения формулы I.
В некоторых вариантах осуществления формулы I R1 представляет собой нуклеозид, содержащий циклический или нециклический сахар или его аналог.
В некоторых вариантах осуществления R1 представляет собой противовирусный нуклеозидный аналог, пригодный для лечения вирусной HCV-инфекции, выбираемый из рибавирина, вирамидина, 2'-C-метилцитидина, 2'-C-метилгуанозина, валопицитабина (NM-283), МК-0608 и PSI-6130.
В некоторых вариантах осуществления R1 представляет собой противовирусный нуклеозидный аналог, пригодный для лечения вирусной HBV-инфекции, который выбирают из ламивудина (EPIVIR-HBV, Зеффикс или Гептодин), адефовира, энтекавира (Бараклуд), телбивудина (Тизека, Себиво), эмтрицитабина (FTC), клевудина (L-FMAU), виреда (Тенофовир), торцитабина, валторцитабина (моновал LdC), амдоксовира (DAPD) и RCV (Рацивир).
В некоторых вариантах осуществления R1 представляет собой ненуклеозидное противовирусное соединение, пригодное для лечения вирусной HBV-инфекции, выбираемое из резиквимода или целгосивира.
В некоторых вариантах осуществления согласно формуле I Ry представляет собой замещенный алкил, например, гидроксиалкил или аминоалкил; и Ra и Rb каждый независимо представляет собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В другом варианте осуществления Ry представляет собой ORC, -C(RC)3 или -NHRC, где каждый RC независимо представляет собой алкил, замещенный алкил, арил или замещенный арил, например, гидрокси- или амино-замещенный алкил или арил; и Ra и Rb независимо представляют собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В дополнительном варианте осуществления Ra и Rb независимо представляют собой бензил или замещенный алкил. В дополнительном варианте осуществления Ry выбирают из группы, состоящей из алкила и гидроксиалкила. В некоторых вариантах осуществления Ry является -C(CH3)2CH2OH.
В некоторых вариантах осуществления соединения, рассматриваемые в настоящем изобретении, выбирают таким образом, что R1 не является 3'-азидо-2',3'-дидезокситимидином.
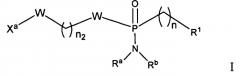
В другом варианте осуществления соединение, рассматриваемое в настоящем изобретении, является соединением формулы IIa или IIb:
или его фармацевтически приемлемой солью, сольватом, стереоизомерной, таутомерной или полиморфной формой, в котором:
Ry представляет собой алкил, алкенил, алкинил, арил, алкиларил, циклоалкил, циклоалкенил, амино, аминоалкил, гидроксиалкил, гетероциклил или гетероарил, все из которых необязательно замещаются;
Ra и Rb выбирают следующим образом:
i) Ra и Rb каждый независимо представляют собой водород, алкил, карбоксиалкил, гидроксиалкил, гидроксиарилалкил, ацилоксиалкил, аминокарбонилалкил, алкоксикарбонилалкил, арил, арилалкил, циклоалкил, арил, гетероарил или гетероциклил, все из которых необязательно замещаются; или
ii) Ra и Rb вместе с атомом азота, на который они замещены, образуют гетероциклическое или гетероарильное кольцо, имеющее от 3 до 7 членов; и
R1 является противовирусным препаратом (согласно использованию в настоящем изобретении, где R1 представляет собой противовирусный препарат, в этом варианте осуществления в него включена функциональная группа, получаемая удалением водорода из гидроксигруппы противовирусного препарата), такого как нуклеозид или нуклеозидный аналог.
В некоторых вариантах осуществления согласно формуле IIa или IIb, Ry является замещенным алкилом, например, гидроксиалкилом или аминоалкилом; и Ra и Rb каждый независимо представляет собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В другом варианте осуществления Ry представляет собой -ORC, -C(RC)3 или -NHRC, где каждый RC независимо представляет собой алкил, замещенный алкил, арил или замещенный арил, например, гидрокси- или амино-замещенный алкил или арил; и Ra и Rb независимо представляют собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В дополнительном варианте осуществления Ra и Rb независимо представляют собой бензил или замещенный алкил. В дополнительном варианте осуществления Ry выбирают из группы, состоящей из алкила и гидроксиалкила. В некоторых вариантах осуществления Ry является -C(CH3)2CH2OH.
В другом варианте осуществления соединение согласно настоящему изобретению является соединением, имеющим формулу:
,
в которых Ra, Rb и Ry таковы, как описаны в формуле I, и
в которых R2 и R3 каждый независимо представляет собой H, линейный, разветвленный или циклический алкил; ацил (включающий в себя низший ацил); СО-алкил, СО-арил, СО-алкоксиалкил, CO-арилоксиалкил, СО-замещенный арил, сложный эфир сульфоната, такой как алкил- или арилалкилсульфонил, включающий в себя метансульфонил и бензил, в котором фенильная группа необязательно замещается; алкилсульфонил, арилсульфонил, арилалкилсульфонил, липид, такой как фосфолипид; аминокислота; и аминокислотный остаток, углевод; пептид; холестерин; или другая фармацевтически приемлемая уходящая группа, которая способна дать соединение, в которых R2 и/или R3 независимо являются H, например, при введении in vivo; или R2 и R3 соединяют для образования циклической группы посредством алкильной, эфирной или карбаматной связи; и в которых каждый RL независимо представляет собой H, карбамил, линейный, разветвленный или циклический алкил; ацил (включающий в себя низший ацил); СО-алкил, СО-арил, СО-алкоксиалкил, Со-арилоксиалкил, СО-замещенный арил, сложный эфир сульфоната, такой как алкил- или арилалкилсульфонил, включающий в себя метансульфонил и бензил, в котором фенильная группа необязательно замещается; алкилсульфонил, арилсульфонил, арилалкилсульфонил, липид, такой как фосфолипид; аминокислота; аминокислотный остаток, или углевод. В некоторых вариантах осуществления согласно этому параграфу каждый из R2 и R3 является H; Ry является замещенным алкилом, например, гидроксиалкилом или аминоалкилом; и Ra и Rb каждый независимо представляет собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В другом варианте осуществления каждый из R2 и R3 является H; Ry представляет собой -ORC, -C(RC)3 или -NHRC, где каждый RC независимо представляет собой алкил, замещенный алкил, арил или замещенный арил, например, гидрокси- или амино-замещенный алкил или арил; и Ra и Rb независимо представляют собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В дополнительном варианте осуществления каждый из R2 и R3 является H; Ra и Rb независимо представляют собой бензил или замещенный алкил. В дополнительном варианте осуществления каждый из R2 и R3 является H; Ry выбирают из группы, состоящей из алкила и гидроксиалкила. В некоторых вариантах осуществления каждый из R2 и R3 является H; Ry представляет собой -C(CH3)2CH2OH. В некоторых вариантах осуществления согласно этому параграфу каждый из R2 и R3 является водородом, Ra является водородом, Rb является -СН2-С6Н5, и Ry является -C(CH3)2CH2OH.
В другом варианте осуществления соединение согласно настоящему изобретению является соединением, имеющим формулу:
в которых описание Ra, Rb и Ry приведено в формуле I. Rd выбирают из группы, состоящей из водорода, алкила и алкокси. В некоторых вариантах осуществления Rd является водородом, метилом или метокси. В некоторых вариантах осуществления согласно этому параграфу Ry является замещенным алкилом, например, гидроксиалкилом или аминоалкилом; и Ra и Rb каждый независимо представляет собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В другом варианте осуществления Ry представляет собой -ORC, -C(RC)3 или -NHRC, где каждый RC независимо представляет собой алкил, замещенный алкил, арил или замещенный арил, например, гидрокси- или амино-замещенный алкил или арил; и Ra и Rb независимо представляют собой водород, алкил, замещенный алкил, бензил или замещенный бензил, например, гидрокси- или амино-замещенный алкил или бензил. В дополнительном варианте осуществления Ra и Rb независимо являются бензилом или замещенным алкилом. В дополнительном варианте осуществления Ry выбирают из группы, состоящей из алкила и гидроксиалкила. В некоторых вариантах осуществления Ry представляет собой -C(CH3)2CH2OH. В некоторых вариантах осуществления согласно этому параграфу каждый из R2 и R3 является водородом, Ra является водородом, Rb является -СН2-С6Н5, и Ry является -C(CH3)2CH2OH. В некоторых вариантах осуществления согласно этому параграфу Ra является водородом, Rb является -СН2-С6Н5, и Ry является -C(CH3)2CH2OH.
В одном варианте осуществления нуклеозиды, которые можно дериватизировать с целью включения фосфорамидата или фосфонамидата, например, в 5'-положении, включают в себя:
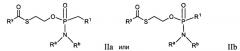
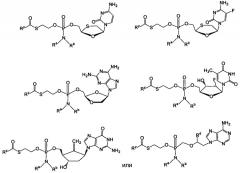
Примеры нуклеозидных соединений фосфорамидата или фосфонамидата включают в себя:
и
В одном варианте осуществления нуклеозиды, которые можно дериватизировать с целью включения фосфорамидата или фосфонамидата, например, в 5'-положении, включают в себя:
В одном варианте осуществления нуклеозидные фосфорамидатные или фосфонамидатные соединения включают в себя:
и
В одном варианте осуществления нуклеозиды, которые можно дериватизировать с целью включения фосфорамидата или фосфонамидата, например, в 5'-положении, включают в себя:
В одном варианте осуществления нуклеозидные фосфорамидатные или фосфонамидатные соединения включают в себя:
и
В одном аспекте соединения, описанные в настоящем изобретении, предоставляются или вводятся в комбинации со вторым терапевтическим средством, например, со средством, пригодным для лечения или профилактики HBV- и/или HCV-инфекций. Примеры терапевтических средств подробно описаны в нижеприведенных разделах.
В другом аспекте предоставлены фармацевтические композиции, монолитные лекарственные формы и наборы, подходящие для лечения или профилактики заболеваний, таких как HBV- и/или HCV-инфекций, которые содержат терапевтически или профилактически эффективное количество соединения, описанного в настоящем изобретении, например, соединения с формулами I, IIa или IIb, и терапевтически или профилактически эффективное количество второго препарата, например, средства, полезного для лечения или профилактики инфекций HBV и/или HCV.
В некоторых вариантах осуществления рассматривается способ лечения заболевания печени, содержащий введение человеку, нуждающемуся в таком лечении, эффективного количества фосфорамидатного или фосфонамидатного производного нуклеозида или нуклеозидного аналога, в котором необязательно производное представляет собой S-пивалоил-2-тиоэтилфосфорамидатное или S-пивалоил-2-тиоэтилфосфонамидатное производное. Производное необязательно выбирают из соединений, раскрытых в настоящем изобретении.