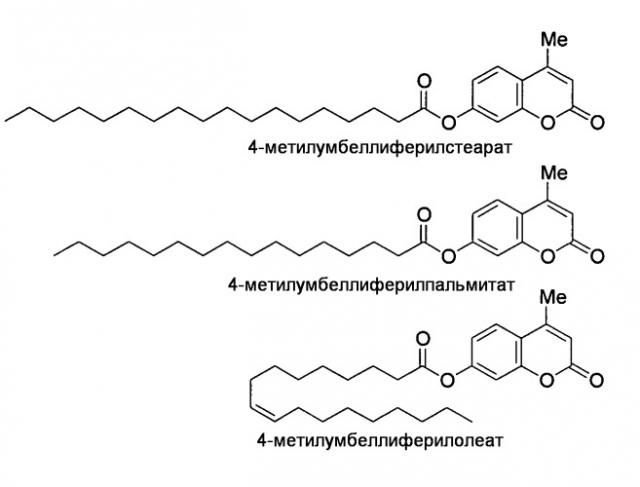
Гидролазы, кодирующие их нуклеиновые кислоты и способы их получения и применения
Иллюстрации
Показать всеИзобретение относится к области биотехнологии и представляет собой полипептиды, обладающие пальмитазной активностью. Изобретение также раскрывает способы гидролиза масел и жиров с низким содержанием насыщенных жирных кислот или с низким содержанием транс-изомеров с использованием указанных пальмитаз, способы биокаталитического синтеза липидов с использованием указанных пальмитаз, а также использование указанных пальмитаз для катализа реакции переэтерификации и способы получения триацилглицеридов (ТАГ), диацилглицеридов (ДАГ) и продуктов питания с использованием указанных реакций. Настоящее изобретение позволяет расширить ассортимент пальмитаз и использовать их для катализа реакций гидролиза. 12 н. и 44 з.п. ф-лы, 32 ил., 32 табл., 16 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА СВЯЗАННУЮ ЗАЯВКУ
По настоящей заявке испрашивается приоритет по патентной заявке США № 12/202204, поданной 29 августа 2008 года, которая, таким образом, включена в полном объеме в настоящее описание в качестве ссылки.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка подана со списком последовательностей, представленным в виде файла с именем 011631-0045-228_SeqListing.txt размером 46086 байтов, который создан 25 августа 2009 года. Список последовательностей включен в настоящую заявку в качестве ссылки в полном объеме.
ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к полипептидам, которые обладают гидролазной активностью, включая липазную, сатуразную, пальмитазную и/или стеаратазную активность, кодирующим их полинуклеотидам и способам получения и применения этих полинуклеотидов и полипептидов. Также изобретение относится к пептидам и полипептидам, например ферментам, обладающим гидролазной активностью, например липазам, сатуразам, пальмитазам и/или стеаратазам, и способам обработки жиров и масел с использованием таких пептидов и полипептидов для получения продуктов гидролиза масел, таких как животные или растительные масла с низким содержанием насыщенных жирных кислот, например соевое масло или масло канолы, продуктов такой обработки масел и продуктов, содержащих такие обработанные масла.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
В основном гидролазы, например липазы, сатуразы, пальмитазы и/или стеаратазы, используют в промышленности, включая производство напитков и продуктов питания, в качестве ингибиторов черствения для хлебобулочных изделий, а также в производстве маргарина и других пастообразных смесей с натуральными ароматизаторами масла; в системах удаления отходов; и в фармацевтической промышленности, где их используют в качестве средств, способствующих пищеварению.
Переработанные масла и жиры представляют собой основные компоненты продуктов питания, пищевые добавки и пищевые технологические добавки, а также важное возобновляемое сырье для химической промышленности. Они доступны в больших количествах в результате переработки семян масличных культур, например, рисовой мучки, кукурузы, рапса, канолы, подсолнечника, оливы, пальмы или сои. Другие источники ценных масел и жиров включают рыбу, отходы ресторанов и топленые животные жиры. Эти жиры и масла представляют собой смеси триацилглицеридов или липидов, т.е. жирные кислоты (ЖК), этерифицированные на глицериновом остове. Каждое масло или жир содержит широкий спектр липидов с различной структурой, характеризующийся содержанием ЖК и их региохимического распределения на глицериновом остове. Эти свойства отдельных липидов определяют физические свойства чистого триацилглицерида. Таким образом, содержание триацилглицерида в жире или масле в большой степени определяет физические, химические и биологические свойства масла. Ценность липидов значительно возрастает в зависимости от их чистоты. Высокой чистоты можно добиться фракционной хроматографией или дистилляцией, отделив желаемый триацилглицерид от фоновой смеси источника жира или масла. Однако это имеет высокую стоимость, а выход часто ограничен тем, что в природе триацилглицерид встречается в низкой концентрации. Кроме того, очистка продукта часто осложняется присутствием множества структурно и физически или химически схожих триацилглицеридов в масле.
Альтернативой очистки триацилглицеридов или других липидов из природного источника является синтез липидов. Продукты таких процессов называют структурированными липидами, поскольку они содержат определенный набор жирных кислот, расположенных определенным образом на глицериновом остове. Также ценность липидов значительно возрастает за счет управления содержанием и распределением жирных кислот в липиде. Устранение из триглицеридов, жиров или масел нежелательных ЖК или замена ЖК с нежелательными свойствами на жирные кислоты с более хорошими или более желательными химическими, физическими или биологическими свойствами увеличивает ценность липидов. В частности, существует потребность в липазах, которые могут отщеплять посредством гидролиза, например, избирательно отщеплять посредством гидролиза, насыщенную жирную кислоту («сатураза»), или в липазах, которые, частности, могут отщеплять посредством гидролиза, например, избирательно отщеплять посредством гидролиза, пальмитиновую кислоту («пальмитаза») или стеариновую кислоту («стеаратаза») от глицеринового остова. Липазы, такие как сатуразы, например пальмитазы и/или стеаратазы, можно использовать для осуществления такого контроля, где удаляемые, добавляемые или замещаемые ЖК представляют собой насыщенные жирные кислоты, например пальмитиновую кислоту или стеариновую кислоту.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к полипептидам, которые обладают гидролазной активностью, включая липазную активность. В одном из аспектов изобретение относится к новым классам липаз, названным «сатуразы», «пальмитазы» и «стеаратазы». Также изобретение относится к полинуклеотидам, которые кодируют полипептиды, обладающие сатуразной, например пальмитазной и/или стеаратазной, активностью, и к способам получения и применения этих полинуклеотидов и полипептидов. В одном из аспектов изобретение относится к полипептидам, например ферментам, которые обладают гидролазной активностью, например липазной, сатуразной, пальмитазной и/или стеаратазной активностью и термостабильной и/или термостабильной ферментативной (каталитической) активностью. Ферментативные активности полипептидов и пептидов по изобретению включают (содержат или состоят из) сатуразную активность или липазную активность, включая гидролиз липидов, реакции ацидолиза (например, для замещения этерифицированной жирной кислоты свободной жирной кислотой), реакции трансэтерификации (например, обмен жирными кислотами между триацилглицеридами), синтез сложных эфиров, реакции переэтерификации и активность ацилгидролаз липидов (АГЛ). В другом аспекте полипептиды по изобретению используют для синтеза энантиомерно чистых хиральных продуктов.
Полипептиды по изобретению можно использовать в различных фармацевтических, сельскохозяйственных и промышленных ситуациях, включая производство косметических средств и нутрицевтиков. Дополнительно полипептиды по изобретению можно использовать в обработке пищевых продуктов, пивоварении, добавках для ванн, производстве спирта, синтезе пептидов, энантиоселективности, изготовлении шкур в кожевенной промышленности, обработке отходов и расщеплении животных отходов, восстановлении серебра в фотопромышленности, медицинской помощи, дегуммировании шелка, разложении биопленок, превращении биомассы в этанол, биозащите, противомикробных средствах и дезинфицирующих средствах, личной гигиене и косметических средствах, биотехнологических реактивах, в повышении выхода крахмала из зерна влажного помола и в качестве фармацевтических препаратов, таких как способствующие пищеварению средства и противовоспалительные средства.
В некоторых вариантах осуществления изобретение относится к композициям (например, липазы, сатуразы, пальмитазы и/или стеаратазы) и способам получения масел с низким содержанием насыщенных жирных кислот, например масел с низким содержанием насыщенных жирных кислот, содержащих масла с низким содержанием пальмитиновой, стеариновой, миристиновой, лауриновой или масляной жирной кислоты и/или каприловой кислоты (октановой кислоты). Любое растительное масло, например, масло канолы, соевое масло или животное масло или жир, например сало, можно обработать с использованием композиции или посредством способа по изобретению. Любые пищевые продукты, съестные продукты или печеные, жареные или термически обработанные продукты (например, соусы, маринады, приправы, масла для смазывания разбрызгиванием, маргарины, пекарные масла, майонез, кулинарные масла, масла для салата, заправки, которые можно черпать ложкой и наливать, и т.п., и продукты, полученные с их использованием) могут содержать растительное масло или животный жир, которые обработаны с использованием композиции или способа по изобретению. Модифицированные растительные масла со сниженным содержанием насыщенных жирных кислот можно использовать в любых продуктах питания, съестных продуктах или печеных или термических обработанных продуктах, например в соусах, маринадах, приправах, маслах для смазывания разбрызгиванием, маргаринах, пекарных маслах, майонезе, кулинарных маслах, маслах для салата, заправках, которые можно черпать ложкой и наливать и т.п. В одном из вариантов осуществления изобретение относится к маслам, таким как растительные масла, например масло канолы или соевое масло, и продукты питания или печеные или термически обработанные продукты, включая соусы, маринады, приправы, масла для смазывания разбрызгиванием, маргарины, майонез, пекарные масла, кулинарные масла, масла для жарки, масла для салата, заправки, которые можно черпать ложкой и наливать, и т.п., где масло или продукт питания, печеный или термически обработанный продукт модифицирован с использованием фермента по изобретению. В одном из аспектов эти растительные масла, например масло канолы, касторовое масло, кокосовое масло, кориандровое масло, кукурузное масло, хлопковое масло, масло лесного ореха, конопляное масло, льняное масло, масло пенника лугового, оливковое масло, пальмовое масло, косточковое пальмовое масло, арахисовое масло, рапсовое масло, рисовое масло, сафлоровое масло, масло сасанквы, соевое масло, масло подсолнечника, талловое масло, масло цубаки, различные обладающие измененным составом жирных кислот «натуральные» масла за счет генетически модифицированных организмов (ГМО) или традиционной «селекции», такие как масла с высоким содержанием олеиновой кислоты, с низким содержанием линоленовой кислоты или с низким содержанием насыщенных жирных кислот (масло канолы с высоким содержанием олеиновой кислоты, соевое масло с низким содержанием линоленовой кислоты или масла подсолнечника с высоким содержанием стеариновой кислоты), животные жиры (сало, лярд, жир коровьего масла и куриный жир), рыбий жир (жир тихоокеанского талеихта, жир печени трески, жир хоплостета, жир сардины, жир сельди и жир менхадена) или смеси любых указанных выше компонентов и продукты питания или печеные, жареные или термически обработанные продукты содержат масла со сниженным содержанием насыщенных жирных кислот, включая масла с низким содержанием пальмитиновой кислоты, миристиновой кислоты, лауриновой кислоты, стеариновой кислоты, каприловой кислоты (октановой кислоты) и т.д., обработанные посредством использования композиции или способа по изобретению.
В одном из аспектов изобретение относится к полипептидам, например, ферментам и каталитическим антителам, которые обладают гидролазной активностью, например липазной, сатуразной, пальмитазной и/или стеаратазной активностью, включая термостабильные и термостабильные ферментативные активности, и активностями со специфичностью к жирным кислотам или избирательностью к жирным кислотам, и ферментативными активностями с высокой или низкой устойчивостью к pH, и к полинуклеотидам, кодирующим эти полипептиды, включая векторы, клетки-хозяева, трансгенные растения и животные, не относящиеся к человеку, и к способам получения и применения этих полинуклеотидов и полипептидов.
В другом аспекте изобретение относится к выделенным, синтетическим или рекомбинантным нуклеиновым кислотам, которые содержат:
(a) нуклеиновую кислоту (полинуклеотид), которая кодирует по меньшей мере один полипептид, где нуклеиновая кислота содержит последовательность, которая обладает по меньшей мере приблизительно 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более или полной (100%) идентичностью последовательностей с:
(i) SEQ ID № 1, SEQ ID № 3, SEQ ID № 5, SEQ ID № 7, SEQ ID № 9, SEQ ID № 11, SEQ ID № 13, SEQ ID № 15, SEQ ID № 17, SEQ ID № 19, SEQ ID № 22 или SEQ ID № 23, или
(ii) нуклеиновой кислотой SEQ ID № 1, которая содержит одну или несколько нуклеотидных замен (или их эквиваленты), кодирующих одну, две, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать, двадцать одну, двадцать две, двадцать три, двадцать четыре, двадцать пять или более или все аминокислотные замены (или их эквиваленты), как указано в таблице 3, таблице 4, таблице 9, таблице 10, таблице 11, таблице 16 или таблице 23,
где нуклеиновая кислота по п. (i) или (ii) кодирует по меньшей мере один полипептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, или кодирует полипептид или пептид, позволяющий создать специфическое антитело к гидролазе (например, к липазе, сатуразе, пальмитазе и/или стеаратазе) (полипептид или пептид, который выполняет функцию эпитопа или иммуногена),
(b) нуклеиновую кислоту (полинуклеотид) по п. (a), где идентичность последовательностей определяют: (a) посредством анализа с использованием алгоритма сравнения последовательностей или посредством визуального исследования, или (b) на участке длиной по меньшей мере приблизительно 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 100, 125, 150, 175, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200, 1250, 1300, 1350, 1400, 1450, 1500, 1550 или более остатков или по всей длине кДНК, транскрипта (мРНК) или гена,
(c) нуклеиновую кислоту (полипептид) по п. (a) или (b), где алгоритмом сравнения последовательностей является алгоритм BLAST версии 2.2.2, где установлены следующие настройки фильтрации blastall -p blastp -d «nr pataa» -F F, а все остальные опции имеют значения по умолчанию,
(d) нуклеиновую кислоту (полинуклеотид), кодирующую по меньшей мере один полипептид или пептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, где нуклеиновая кислота содержит последовательность, которая гибридизуется в строгих условиях с комплементарной последовательностью нуклеиновой кислоты по п. (a), (b) или (c), где строгие условия содержат стадию отмывания, которая включает отмывание в 0,2×SSC при температуре приблизительно 65°C в течение приблизительно 15 минут,
(e) нуклеиновую кислоту (полинуклеотид), кодирующую по меньшей мере один полипептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, где полипептид содержит последовательность SEQ ID № 2 или ее ферментативно активные фрагменты, которая содержит по меньшей мере одну, две, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать, двадцать одну, двадцать две, двадцать три, двадцать четыре или более или все аминокислотные замены (или их эквиваленты), как указано в таблице 3, таблице 4, таблице 9, таблице 10, таблице 11, таблице 16 или таблице 23,
(f) нуклеиновую кислоту (полинуклеотид), кодирующую по меньшей мере один полипептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, где полипептид содержит последовательность SEQ ID № 2, SEQ ID № 4, SEQ ID № 6, SEQ ID № 8, SEQ ID № 10, SEQ ID № 12, SEQ ID № 14, SEQ ID № 16, SEQ ID № 18 или SEQ ID № 20 или ее ферментативно активные фрагменты,
(g) (a) нуклеиновую кислоту (полинуклеотид) по любому из п.п. с (a) до (f), кодирующую полипептид, содержащий по меньшей мере одну консервативную аминокислотную замену и сохраняющий свою гидролазную активность, например, липазную, сатуразную, пальмитазную и/или стеаратазную активность, или, (b) нуклеиновую кислоту по п. (g)(a), где по меньшей мере одна консервативная аминокислотная замена включает замену аминокислоты на другую аминокислоту с похожими характеристиками; или консервативная замена включает: замену алифатической аминокислоты на другую алифатическую аминокислоту; замену серина на треонин или наоборот; замену кислотного остатка на другой кислотный остаток; замену остатка, несущего аминогруппу, на другой остаток, несущий аминогруппу; замену основного остатка другим основным остатком; или замену ароматического остатка другим ароматическим остатком,
(h) нуклеиновую кислоту (полинуклеотид) по любому из п.п. с (a) до (g), кодирующую полипептид, который обладает гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, но не содержит сигнальную последовательность,
(i) нуклеиновую кислоту (полинуклеотид) по любому из п.п. с (a) до (h), кодирующую полипептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, который дополнительно содержит гетерологичную последовательность,
(j) нуклеиновую кислоту (полинуклеотид) по п. (i), где гетерологичная последовательность состоит из или содержит последовательность, кодирующую: (a) гетерологичную сигнальную последовательность, (b) последовательность по п. (a), где гетерологичную сигнальную последовательность получают из гетерологичного фермента, или, (c) метку, эпитоп, таргетинг-пептид, расщепляемую последовательность, поддающийся обнаружению фрагмент или участок, или
(k) последовательность нуклеиновой кислоты (полинуклеотид), полностью (абсолютно) комплементарную последовательности по любому п.п. с (a) до (j).
В одном из аспектов выделенная, синтетическая или рекомбинантная нуклеиновая кислота кодирует полипептид или пептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, которая является термостабильной. Полипептиды и пептиды, кодируемые нуклеиновыми кислотами по изобретению, или любой полипептид или пептид по изобретению, может сохранять ферментативную или связывающую активность (например, связывание с субстратом) в условиях, которые включают температурный диапазон приблизительно от -100°C приблизительно до -80°C, приблизительно от -80°C приблизительно до -40°C, приблизительно от -40°C приблизительно до -20°C, приблизительно от -20°C приблизительно до 0°C, приблизительно от 0°C приблизительно до 5°C, приблизительно от 5°C приблизительно до 15°C, приблизительно от 15°C приблизительно до 25°C, приблизительно от 25°C приблизительно до 37°C, приблизительно от 37°C приблизительно до 45°C, приблизительно от 45°C приблизительно до 55°C, приблизительно от 55°C приблизительно до 70°C, приблизительно от 70°C приблизительно до 75°C, приблизительно от 75°C приблизительно до 85°C, приблизительно от 85°C приблизительно до 90°C, приблизительно от 90°C приблизительно до 95°C, приблизительно от 95°C приблизительно до 100°C, приблизительно от 100°C приблизительно до 105°C, 5 приблизительно 105°C приблизительно до 110°C, приблизительно от 110°C приблизительно до 120°C, или 95°C, 96°C, 97°C, 98°C, 99°C, 100°C, 101 °C, 102°C, 103°C, 104°C, 105°C, 106°C, 107°C, 108°C, 109°C, 110°C, 111°C, 112°C, 113°C, 114°C, 115°C или более. Изобретение относится к термостабильным полипептидам, которые сохраняют гидролазную активность, например, липазную, сатуразную, пальмитазную и/или стеаратазную активность, при температуре в описанных выше диапазонах, приблизительно при pH 3,0, приблизительно при pH 3,5, приблизительно при pH 4,0, приблизительно при pH 4,5, приблизительно при pH 5,0, приблизительно при pH 5,5, приблизительно при pH 6,0, приблизительно при pH 6,5, приблизительно при pH 7,0, приблизительно при pH 7,5, приблизительно при pH 8,0, приблизительно при pH 8,5, приблизительно при pH 9,0, приблизительно при pH 9,5, приблизительно при pH 10,0, приблизительно при pH 10,5, приблизительно при pH 11,0, приблизительно при pH 11,5, приблизительно при pH 12,0 или более.
В одном из аспектов полипептиды по изобретению могут быть термостабильными и могут сохранять гидролазную активность, например липазную, сатуразную, пальмитазную и/или стеаратазную активность, после воздействия температуры в диапазоне приблизительно от -100°C приблизительно до -80°C, приблизительно от -80°C приблизительно до -40°C, приблизительно от -40°C приблизительно до -20°C, приблизительно от -20°C приблизительно до 0°C, приблизительно от 0°C приблизительно до 5°C, приблизительно от 5°C приблизительно до 15°C, приблизительно от 15°C приблизительно до 25°C, приблизительно от 25°C приблизительно до 37°C, приблизительно от 37°C приблизительно до 45°C, приблизительно от 45°C приблизительно до 55°C, приблизительно от 55°C приблизительно до 70°C, приблизительно от 70°C приблизительно до 75°C, приблизительно от 75°C приблизительно до 85°C, приблизительно от 85°C приблизительно до 90°C, приблизительно от 90°C приблизительно до 95°C, приблизительно от 95°C приблизительно до 100°C, приблизительно от 100°C приблизительно до 105°C, приблизительно от 105°C приблизительно до 110°C, приблизительно от 110°C приблизительно до 120°C, или 95°C, 96°C, 97°C, 98°C, 99°C, 100°C, 101°C, 102°C, 103°C, 104°C, 105°C, 106°C, 107°C, 108°C, 109°C, 110°C, 111°C, 112°C, 113°C, 114°C, 115°C или более.
В некоторых вариантах осуществления термостабильные полипептиды сохраняют гидролазную активность, например липазную, сатуразную, пальмитазную и/или стеаратазную активность, после воздействия температуры в описанных выше диапазонах, приблизительно при pH 3,0, приблизительно при pH 3,5, приблизительно при pH 4,0, приблизительно при pH 4,5, приблизительно при pH 5,0, приблизительно при pH 5,5, приблизительно при pH 6,0, приблизительно при pH 6,5, приблизительно при pH 7,0, приблизительно при pH 7,5, приблизительно при pH 8,0, приблизительно при pH 8,5, приблизительно при pH 9,0, приблизительно при pH 9,5, приблизительно при pH 10,0, приблизительно при pH 10,5, приблизительно при pH 11,0, приблизительно при pH 11,5, приблизительно при pH 12,0 или более.
В одном из вариантов осуществления выделенные, синтетические или рекомбинантные нуклеиновые кислоты содержат последовательность, которая гибридизуется в строгих условиях с нуклеиновой кислотой по изобретению, например, с образцовой нуклеиновой кислотой по изобретению, содержащей последовательность, как указано в SEQ ID № 1, SEQ ID № 3, SEQ ID № 5, SEQ ID № 7, SEQ ID № 9, SEQ ID № 11, SEQ ID № 13, SEQ ID № 15, SEQ ID № 17, SEQ ID № 19, SEQ ID № 22 или SEQ ID № 23, или последовательность, как указано в SEQ ID № 1, которая включает замены одного, двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати или двенадцати или более или всех остатков (модификации последовательности SEQ ID № 1), изложенные в таблице 3, таблице 4, таблице 9, таблице 10, таблице 11, таблице 16 или таблице 23, или их фрагменты или подпоследовательности и последовательности, (полностью) комплементарные им. В одном из аспектов нуклеиновая кислота кодирует полипептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью. Длина нуклеиновой кислоты может составлять по меньшей мере приблизительно 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 100, 125, 150, 175, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700 или более остатков или соответствовать полной длине гена или транскрипта, содержащего SEQ ID № 1, и содержать последовательность, как указано в SEQ ID № 1, которая содержит замены одного, двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати или двенадцати или более или всех остатков (модификации аминокислотной последовательности) SEQ ID № 1, которые изложены в таблице 3, таблице 4, таблице 9, таблице 10, таблице 11, таблице 16 или таблице 23; и последовательности, (полностью) комплементарные им. В одном из аспектов строгие условия включают стадию отмывания, содержащую отмывание в 0,2×SSC при температуре приблизительно 65°C в течение приблизительно 15 минут.
В одном из вариантов осуществления зонд из нуклеиновой кислоты, например, зонд для идентификации нуклеиновой кислоты, кодирующей полипептид, обладающей гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, включает зонд, содержащий или состоящий по меньшей мере приблизительно из 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000 или более последовательных оснований последовательности по изобретению, или ее фрагментов или подпоследовательностей, где зонд позволяет идентифицировать нуклеиновую кислоту посредством связывания или гибридизации. Зонд может содержать олигонуклеотид, содержащий по меньшей мере приблизительно от 10 до 50, приблизительно от 20 до 60, приблизительно от 30 до 70, приблизительно от 40 до 80 или приблизительно от 60 до 100 последовательных оснований последовательности, содержащей последовательность по изобретению, или ее фрагменты или подпоследовательности. Зонд может содержать олигонуклеотид, содержащий по меньшей мере приблизительно от 10 до 50, приблизительно от 20 до 60, приблизительно от 30 до 70, приблизительно от 40 до 80 или приблизительно от 60 до 100 последовательных оснований последовательности нуклеиновой кислоты по изобретению, или ее подпоследовательность.
В одном из вариантов осуществления пара последовательностей праймеров для амплификации нуклеиновой кислоты, кодирующей полипептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, содержит пару праймеров, содержащую или состоящую из пары праймеров, позволяющих амплифицировать нуклеиновую кислоту, содержащую последовательность по изобретению, или ее фрагменты или подпоследовательности. Один или оба члена пары последовательностей праймеров для амплификации могут содержать олигонуклеотид, содержащий по меньшей мере приблизительно от 10 до 50 последовательных оснований из последовательности.
В одном из вариантов осуществления способы амплификации нуклеиновой кислоты, кодирующей полипептид, обладающий гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, содержат амплификацию матричной нуклеиновой кислоты с использованием пары последовательностей праймеров для амплификации, позволяющих амплифицировать последовательность нуклеиновой кислоты по изобретению, или ее фрагменты или подпоследовательности.
В одном из вариантов осуществления экспрессирующие кассеты содержат нуклеиновую кислоту по изобретению, или ее подпоследовательность. В одном из аспектов экспрессирующая кассета может содержать нуклеиновую кислоту, которая функционально связана с промоторами. Промоторы могут представлять собой промоторы вирусов, бактерий, млекопитающих или растений. В одном из аспектов промоторы растений могут представлять собой промоторы картофеля, риса, кукурузы, пшеницы, табака или ячменя. Промоторы могут представлять собой конститутивный промотор. Конститутивный промотор может содержать CaMV35S. В другом аспекте промоторы могут представлять собой индуцируемые промоторы. В одном из аспектов промоторы могут представлять собой тканеспецифичные промоторы или промоторы, регулируемые окружающей средой или регулируемые развитием. Таким образом, промоторы могут представлять собой специфические промоторы, например, семян, листьев, корней, стебля, или промоторы, индуцируемые сбрасыванием. В одном из аспектов экспрессирующая кассета может дополнительно содержать экспрессирующий вектор растения или вируса растения.
В одном из вариантов осуществления переносчики для клонирования содержат экспрессирующую кассету (например, вектор) по изобретению, или нуклеиновую кислоту по изобретению. Переносчик для клонирования может представлять собой вирусный вектор, плазмиду, фаг, фагемиду, космиду, фосмиду, бактериофаг или искусственную хромосому. Вирусный вектор может содержать аденовирусный вектор, ретровирусный вектор или аденоассоциированный вирусный вектор. Переносчик для клонирования может содержать бактериальную искусственную хромосому (BAC), плазмиду, вектор, полученный из бактериофага P1 (РАС), искусственную хромосому дрожжей (YAC) или искусственную хромосому млекопитающего (MAC).
В одном из вариантов осуществления трансформированные клетки содержат нуклеиновую кислоту по изобретению, или экспрессирующую кассету (например, вектор) по изобретению, или переносчик для клонирования по изобретению. В одном из аспектов трансформированная клетка может представлять собой бактериальную клетку, клетку млекопитающего, клетку гриба, клетку дрожжей, клетку насекомого или клетку растения. В одном из аспектов клетка растения может представлять собой клетку картофеля, пшеницы, риса, кукурузы, табака или ячменя. Трансформированная клетка может представлять собой любую клетку-хозяина, известную специалистам в данной области, включая прокариотические клетки, эукариотические клетки, такие как бактериальные клетки, клетки грибов, клетки дрожжей, клетки млекопитающих, клетки насекомых или клетки растений. Образцовые бактериальные клетки включают любые виды в пределах родов Escherichia, Bacillus, Streptomyces, Salmonella, Pseudomonas и Staphylococcus, включая, например, Escherichia coli, Lactococcus lactis, Bacillus subtilis, Bacillus cereus, Salmonella typhimurium, Pseudomonas fluorescens. Образцовые клетки грибов включают любые виды Aspergillus. Образцовые клетки дрожжей включают любые виды Pichia, Saccharomyces, Schizosaccharomyces или Schwanniomyces, включая Pichia pastoris, Saccharomyces cerevisiae или Schizosaccharomyces pombe. Образцовые клетки насекомых включают любые виды Spodoptera или Drosophila, включая Drosophila S2 и Spodoptera Sf9. Образцовые клетки животных включают линии клеток CHO, COS или меланомы Боуэса или любые линии клеток мыши или человека.
В одном из вариантов осуществления трансгенные растения содержат нуклеиновую кислоту по изобретению, или экспрессирующую кассету (например, вектор) по изобретению. Трансгенным растением может являться растение кукурузы, растение картофеля, растение помидора, растение пшеницы, растение масличной культуры, растение рапса, растение сои, растение риса, растение ячменя или растение табака.
В одном из вариантов осуществления трансгенные семена содержат нуклеиновую кислоту по изобретению, или экспрессирующую кассету (например, вектор) по изобретению. Трансгенные семена могут представлять собой рис, семена кукурузы, зерна пшеницы, семена масличных культур, семена рапса, семена сои, ядра кокосовых орехов, семена подсолнечника, семена кунжута, семена растений арахиса или табака.
В одном из вариантов осуществления выделенные, синтетические или рекомбинантные полипептиды, обладающие гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, или полипептиды, позволяющие получить специфический иммунный ответ к гидролазе, например, к липазе, сатуразе, пальмитазе и/или стеаратазе (например, эпитоп); и в альтернативных аспектах пептиды и полипептиды по изобретению содержат последовательность:
(a) которая обладает по меньшей мере приблизительно 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более или обладает 100% (полной) идентичностью последовательностей с:
(i) аминокислотной последовательностью SEQ ID № 2 или ее ферментативно активными фрагментами и содержит замены по меньшей мере одного, двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати, тринадцати, четырнадцати, пятнадцати, шестнадцати, семнадцати, восемнадцати, девятнадцати, двадцати, двадцати одного, двадцати двух, двадцати трех, двадцати четырех или более или всех аминокислотных остатков (или их эквиваленты), как указано в таблице 3, таблице 4, таблице 9, таблице 10, таблице 11, таблице 16 или таблице 23, или
(ii) аминокислотной последовательностью SEQ ID № 2, SEQ ID № 4, SEQ ID № 6, SEQ ID № 8, SEQ ID № 10, SEQ ID № 12, SEQ ID № 14, SEQ ID № 16, SEQ ID № 18, или SEQ ID № 20
где полипептид или пептид по п. (i) или (ii) обладает гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, или полипептид или пептид позволяет получить специфическое антитело к гидролазе (например, к липазе, сатуразе, пальмитазе и/или стеаратазе) (полипептид или пептид, который выполняет функцию эпитопа или иммуногена),
(b) полипептида или пептида по п. (a), где идентичность последовательностей определяют: (a) посредством анализа с использованием алгоритма сравнения последовательностей или посредством визуального исследования, или (В) на участке длиной по меньшей мере приблизительно 20, 25, 30, 35, 40, 45, 50, 55, 60, 75, 100, 150, 200, 250, 300 или более аминокислотных остатков или по всей длине полипептида или пептида или фермента и/или их ферментативно активных подпоследовательностей (фрагментов),
(c) полипептида или пептида по п. (b), где алгоритмом сравнения последовательностей является алгоритм BLAST версии 2.2.2, где установлены следующие настройки фильтрации blastall -p blastp -d «nr pataa» -F F, а все остальные опции имеют значения по умолчанию;
(d) аминокислотную последовательность, кодируемую нуклеиновой кислотой, предоставленной в настоящем документе, где полипептид обладает (i) гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, или (ii) обладает такой иммуногенной активностью, что она позволяет получить антитело, которое специфически связывается с полипептидом, содержащим последовательность по п. (a), и/или с его ферментативно активными подпоследовательностями (фрагментами);
(e) аминокислотную последовательность по любому п. с (a) до (d), включающую по меньшей мере одну замену консервативного аминокислотного остатка, но полипептид или пептид сохраняет гидролазную активность, например, липазную, сатуразную, пальмитазную и/или стеаратазную активность;
(f) аминокислотную последовательность по п. (e), где консервативная замена включает замену алифатической аминокислоты на другую алифатическую аминокислоту; замену серина на треонин или наоборот; замену кислотного остатка на другой кислотный остаток; замену остатка, несущего аминогруппу, на другой остаток, несущий аминогруппу; замену основного остатка другим основным остатком; или замену ароматического остатка другим ароматическим остатком или их сочетание,
(g) аминокислотную последовательность по п. (f), где алифатический остаток включает аланин, валин, лейцин, изолейцин или их синтетический эквивалент; кислый остаток включает аспарагиновую кислоту, глутаминовую кислоту или их синтетический эквивалент; остаток, содержащий амидную группу, включает аспарагин, глутамин или их синтетический эквивалент; основный остаток содержит лизин, аргинин, гистидин или их синтетический эквивалент; или ароматический остаток содержит фенилаланин, тирозин, триптофан или их синтетический эквивалент;
(h) полипептида по любому из п.п. с (a) до (f), обладающего гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, но не содержащего сигнальную последовательность,
(i) полипептида по любому из п.п. с (a) до (h), обладающего гидролазной активностью, например, липазной, сатуразной, пальмитазной и/или стеаратазной активностью, который дополнительно содержит гетерологичную последовательность;
(j) полипептида по п. (i), где гетерологичная последовательность содержит или состоит из: (a) гетерологичной сигнальной последовательности, (b) последовательности по п. (a), где гетерологичную сигнальную последовательность получают из гетерологичного фермента, и/или (c) метки, эпитопа, таргетинг-пептида, расщепляемой последовательности, поддающегося обнаружению фрагмента или участка; или
(m) содержат аминокислотную последовательность, кодируемую любой последовательностью нуклеиновой кислоты по изобретению.
Образцовые полипептидные или пептидные последовательности по изобретению, включают SEQ ID № 2 и ее подпоследовательности и варианты, например, длиной по меньшей мере приблизительно 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500 или более остатков или полноразмерный фермент, все содержат замены одного, двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати или двенадцати или более или всех аминокислотных остатков (модификации аминокислотной последовательности SEQ ID № 2), которые изложены в таблице 3, таблице 4, таблице 9, таблице 10, таблице 11, таблице 16 или таблице 23. Образцовые полипептидные или пептидные последовательности по изобретению, содержат последовательность, кодируемую нуклеиновой кислотой по изобретению. Образцовые полипептидные или пептидные последовательности по изобретению, включают полипептиды или пептиды, с которыми специфически связывается анти